Долгосрочная эффективность и безопасность терапии ингибитором интерлейкина-23 гуселькумабом в реальной клинической практике: данные девяти лет наблюдения
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – оценить долгосрочную эффективность терапии ингибитором ИЛ-23 гуселькумабом, влияние на показатели качества жизни у пациентов со среднетяжелым и тяжелым псориазом и удержание ответа на проводимую терапию.
Материал и методы. Проведено ретроспективное исследование 36 пациентов с диагнозом «распространенный вульгарный псориаз». Исходные показатели оценивали по индексам PASI, BSA, sPGA, визуальной аналоговой шкале зуда (ВАШ). Показатели качества жизни оценивали по шкалам DLQI и SF 36. Все пациенты получали лечение ингибитором ИЛ-23 гуселькумабом по стандартной схеме. Оценку эффективности терапии осуществляли по динамике показателей PASI, BSA, sPGA, ВАШ, DLQI и SF-36 на исходном уровне и через 12, 24, 52 и 468 недель терапии.
Результаты. Биологическая терапия гуселькумабом привела к статистически значимому улучшению всех показателей через 12 недель, и ответ сохранялся на 24, 52 и 468-й неделе для каждого пациента (р < 0,001). Продемонстрирована высокая статистическая значимость разницы между исходным уровнем и после терапии гуселькумабом по индексам PASI, BSA, sPGA, ВАШ (p < 0,001). Все пациенты с «суперответом» достигли полного очищения кожи PASI 100 к 24-й неделе терапии. Изменение показателей индекса PASI привело к статистически значимому улучшению показателей качества жизни по шкале дерматологического индекса качества жизни (ДИКЖ) (p < 0,001). По шкале SF-36 получен статистически значимый результат (p < 0,001), как по шкале физического компонента здоровья (Physical health – PH), так и по шкале психологического компонента здоровья (Mental Health – MH), до и после лечения гуселькумабом на 12, 24, 52 и 468-й неделях терапии.
Заключение. Биологическая терапия ингибитором ИЛ-23 гуселькумабом высокоэффективна для снижения тяжести заболевания и достижения высоких показателей качества жизни больных псориазом.
Цель исследования – оценить долгосрочную эффективность терапии ингибитором ИЛ-23 гуселькумабом, влияние на показатели качества жизни у пациентов со среднетяжелым и тяжелым псориазом и удержание ответа на проводимую терапию.
Материал и методы. Проведено ретроспективное исследование 36 пациентов с диагнозом «распространенный вульгарный псориаз». Исходные показатели оценивали по индексам PASI, BSA, sPGA, визуальной аналоговой шкале зуда (ВАШ). Показатели качества жизни оценивали по шкалам DLQI и SF 36. Все пациенты получали лечение ингибитором ИЛ-23 гуселькумабом по стандартной схеме. Оценку эффективности терапии осуществляли по динамике показателей PASI, BSA, sPGA, ВАШ, DLQI и SF-36 на исходном уровне и через 12, 24, 52 и 468 недель терапии.
Результаты. Биологическая терапия гуселькумабом привела к статистически значимому улучшению всех показателей через 12 недель, и ответ сохранялся на 24, 52 и 468-й неделе для каждого пациента (р < 0,001). Продемонстрирована высокая статистическая значимость разницы между исходным уровнем и после терапии гуселькумабом по индексам PASI, BSA, sPGA, ВАШ (p < 0,001). Все пациенты с «суперответом» достигли полного очищения кожи PASI 100 к 24-й неделе терапии. Изменение показателей индекса PASI привело к статистически значимому улучшению показателей качества жизни по шкале дерматологического индекса качества жизни (ДИКЖ) (p < 0,001). По шкале SF-36 получен статистически значимый результат (p < 0,001), как по шкале физического компонента здоровья (Physical health – PH), так и по шкале психологического компонента здоровья (Mental Health – MH), до и после лечения гуселькумабом на 12, 24, 52 и 468-й неделях терапии.
Заключение. Биологическая терапия ингибитором ИЛ-23 гуселькумабом высокоэффективна для снижения тяжести заболевания и достижения высоких показателей качества жизни больных псориазом.

Введение
Псориаз представляет серьезную глобальную проблему для современной медицины, что обусловлено широкой распространенностью, неуклонным ростом заболеваемости, системным характером клинических проявлений, увеличением числа тяжелых форм заболевания [1, 2]. Хроническое течение псориаза с внезапным началом и непредсказуемым течением – не только значимый аспект экономического бремени, но и причина существенных ограничений в физических, эмоциональных и социальных аспектах жизни пациентов с данным заболеванием, что влияет на их активность и профессиональную карьеру [3–5]. Заболевание поражает до 3% населения и является одним из наиболее распространенных дерматозов [6]. У 30% пациентов развиваются патологические изменения опорно-двигательного аппарата [7]. Помимо поражения суставов, для дерматоза характерен целый ряд коморбидностей, в том числе сердечно-сосудистые заболевания, сахарный диабет, неалкогольная жировая дистрофия печени, ожирение, депрессия и иммуноопосредованные заболевания, такие как болезнь Крона [8–11].
Лечение псориаза является одной из самых сложных задач в дерматологии, особенно у пациентов с коморбидными заболеваниями [12, 13]. Появление новых классов генно-инженерных биологических препаратов (ГИБП), нацеленных на специфические интерлейкины, участвующие в иммунопатогенезе псориаза, произвело переворот в терапевтическом ведении таких пациентов [14, 15]. Одними из последних одобренных ГИБП являются ингибиторы интерлейкина (ИЛ)-23 [16–18]. Гуселькумаб – это первый одобренный полностью человеческий иммуноглобулин G1 лямбда (IgG1λ), моноклональное антитело, селективно воздействующее на субъединицу p19 ИЛ-23 [19]. Эффективность и безопасность гуселькумаба освещена в клинических исследованиях VOYAGE 1, VOYAGE 2, NAVIGATE, ORION, ECLIPSE и международных публикациях реальной клинической практики [20–27].
Однако данных недостаточно, и они ограничены сокращенным периодом наблюдения. Цель исследования – оценка в реальной клинической практике эффективности и параметров безопасного применения ингибитора ИЛ-23 гуселькумаба с более длительным периодом наблюдения за пациентами со среднетяжелым и тяжелым псориазом с учетом коморбидной патологии (ожирение, сердечно-сосудистые заболевания, сахарный диабет, психические расстройства). В данном исследовании представлены данные девятилетнего наблюдения пациентов со среднетяжелым и тяжелым псориазом, получающих терапию ингибитором ИЛ-23 гуселькумабом, в реальной клинической практике и динамика показателей качества жизни.
Материал и методы
Проведено одноцентровое экспериментальное неконтролируемое исследование пациентов с распространенным бляшечным псориазом. Пациенты были включены в исследование в период с апреля 2015 г. по июнь 2024 г. и получали гуселькумаб 100 мг на 0, 4-й день и затем один раз каждые восемь недель.
Критерии включения в исследование:
- возраст от 18 лет;
- тяжелая степень тяжести псориаза (Psoriasis Area and Severity Index, PASI) > 12 баллов;
- поражение псориазом более 10% поверхности тела (Body Surfase Area, BSA);
- оценка изменений кожи врачом (Static Physician Global Assessment, sPGA) более трех баллов;
- пациенты, прошедшие тестирование по шкалам PASI, BSA, sPGA, DLQI и SF-36 с оценкой интенсивности зуда по визуальной аналоговой шкале (ВАШ) до начала и через 12, 24, 52 и 468 недель после лечения;
- добровольное желание принимать участие в исследовании; подписанное информированное согласие с общим планом обследования и лечения.
Критерии невключения:
- наличие сопутствующих соматических, а также инфекционных заболеваний в стадии декомпенсации, онкологические заболевания, наркомания, алкоголизм, гипертиреоз;
- нарушения со стороны системы кроветворения в анамнезе (клинически значимая анемия, тромбоцитопения, лейкопения, гипоплазия костного мозга);
- беременность, период лактации.
Критерии исключения:
- добровольное желание пациента завершить участие в исследовании;
- несоблюдение пациентом режима, а также назначенной схемы диагностики и терапии.
Для установления диагноза проводили клинико-анамнестическое обследование (сбор жалоб, оценивали анамнез жизни и заболевания; полное физикальное обследование; оценивали показатели жизненно важных функций, антропометрические данные – массу тела и рост, индекс массы тела (ИМТ), сопутствующие заболевания, время с момента постановки диагноза, предшествующую терапию, клинические проявления и определяли степень их тяжести c учетом индексов PASI, BSA, sPGA, NAPSI).
Индекс площади и тяжести псориаза PASI использовали для измерения площади пораженной области и оценки тяжести распространенного псориаза. Если показатель PASI < 10, поражение кожи считается легким, от 10 до 20 – умеренным, а балл, равный или превышающий 20, соответствует тяжелому поражению.
Индекс BSA (%) определяли путем измерения ладони пациента до средних фаланг пальцев, при этом каждая единица равна 1% площади тела. Значение BSA < 3 указывает на легкую степень тяжести псориаза, от 3 до 10 – на среднюю степень тяжести, а значение более 10 – на тяжелую степень тяжести.
Статическая глобальная оценка врача sPGA (фиксированная шкала, используемая врачами для оценки тяжести псориаза) предполагает оценку трех факторов (инфильтрация, шелушение, эритема). Оценка 0 указывает на отсутствие признаков псориаза, 5 – на крайне тяжелое проявление заболевания.
Оценку степени тяжести псориаза и нежелательных явлений проводили на 0, 12, 24, 52 и 468-й неделях лечения.
До назначения инъекций гуселькумаба у всех пациентов получены образцы крови и мочи для лабораторных исследований: клинический и биохимический анализ крови, серологическое исследование на ВИЧ, антикардиолипиновый тест / исследование суммарных антител IgG, IgM к антигенам Treponema pallidum, качественный тест на HbsAg, определение суммарных антител к антигенам вируса гепатита С (аnti-HCV-total), общий анализ мочи. Всем пациентам была выполнена цифровая рентгенография грудной клетки в двух проекциях с описанием, проведена внутрикожная проба с туберкулезным аллергеном (диаскинтест) / квантифероновый тест для исключения туберкулезной инфекции до назначения терапии, на 24, 52-й неделе терапии и далее в период последующего наблюдения один раз в год.
При каждом посещении на 0, 12, 24, 52, 468-й неделях оценивали рутинные анализы крови (общий клинический анализ крови с лейкоцитарной формулой и СОЭ, биохимический анализ крови: показатели трансаминаз, ГГТП, общий белок, щелочная фосфатаза, глюкоза, СРБ, липидограмма), общий анализ мочи для подтверждения безопасности ингибитора ИЛ-23 гуселькумаба.
Для измерения показателей качества жизни у больных псориазом были использованы две диагностические шкалы: дерматологический индекс качества жизни – ДИКЖ и универсальный опросник SF-36. ДИКЖ – это опросник из десяти вопросов, используемый для измерения влияния кожных заболеваний на качество жизни. Баллы ДИКЖ (DLQI) варьируются от 0 (отсутствие влияния кожных заболеваний на качество жизни) до 30 (максимальное влияние). SF-36 представляет собой опросник для оценки физического (PCS) и психического компонента (MCS) [28]. Опросник SF-36 содержит 36 вопросов, которые сгруппированы в восемь шкал: 1) физическое функционирование (Physical Functioning – PF); 2) ролевое функционирование, обусловленное физическим состоянием (Role-Physical Functioning – RP); 3) интенсивность боли (Bodily Pain – BP); 4) общее состояние здоровья (General Health – GH); 5) жизненная активность (Vitality – VT); 6) социальное функционирование (Social Functioning – SF); 7) ролевое функционирование, обусловленное эмоциональным состоянием (Role-Emotional Functioning – RE); 8) психическое здоровье (Mental Health – MH). Показатели каждой шкалы варьируют от 0 до 100 (баллы), и чем выше значение показателя, тем лучше оценка по выбранной шкале.
Все шкалы опросника объединены в два показателя – физический (первая–четвертая шкалы) и психологический (пятая–восьмая шкалы) компоненты здоровья. Клинически значимые улучшения определяются как улучшение по шкале SF-36 на ≥ 5 баллов [29–31].
На сегодняшний день наиболее часто используется усовершенствованная, вторая версия опросника SF-36, в которой были учтены замечания, высказанные исследователями в процессе пользования предыдущим вариантом опросника. Таким образом, опросник позволяет интегрально оценить влияние различных симптомов у пациентов на качество как физической, так и эмоционально-психологической активности.
Оценку качества жизни больных псориазом проводили до назначаемой терапии и на 12, 24, 52 и 468-й неделе лечения.
Оценку эффективности терапии осуществляли по динамике показателей PASI, BSA, sPGA, ВАШ, ДИКЖ и SF-36. Также были сделаны цифровые фотографии больных до начала и после окончания терапии. Размер выборки предварительно не рассчитывали.
Сбор данных, их последующую коррекцию, систематизацию исходной информации и визуализацию полученных результатов осуществляли в электронных таблицах Excel (Microsoft Office 365). Статистическую обработку результатов проводили средствами языка Python 3.11. Количественные показатели оценивали на предмет соответствия нормальному распределению, для этого использовали критерий Шапиро –Уилка. Проверка на нормальность распределения показала, что данные в исследовании не имеют нормального распределения, поэтому в дальнейшем расчеты производили методами непараметрической статистики. В качестве центра распределения была посчитана медиана, а в качестве показателей вариации – квартили (Me [Q1; Q3]). Для проверки различий между двумя сравниваемыми парными выборками был применен W-критерий Уилкоксона. Результаты качественных признаков выражены в абсолютных числах с указанием долей (%).
С целью изучения взаимосвязи между явлениями, представленными количественными данными, использовали непараметрический метод – расчет коэффициента ранговой корреляции Спирмена (r). Интерпретацию полученных значений корреляции производили по шкале Чеддока, предполагающей качественную и количественную оценку от 0,1 до 0,99. Слабая вероятность наступления рисков – от 0,1 до 0,3 балла; умеренная вероятность наступления рисков – от 0,3 до 0,5 балла; заметная вероятность наступления рисков – от 0,5 до 0,7 балла; высокая вероятность наступления рисков – от 0,7 до 0,9 балла; весьма высокая вероятность наступления рисков – от 0,9 до 0,99 балла. Коэффициент корреляции дополнен 95%-м доверительным интервалом (95%ДИ), который рассчитывали методом бутстрэп (bootstrap) при выборке 1000 экземпляров. Различия считали статистически значимыми при р < 0,05.
Результаты
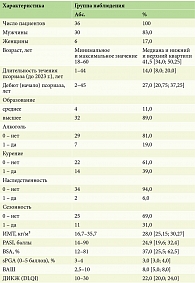
Под нашим наблюдением находились 36 пациентов (30 (83%) мужчин и 6 (17%) женщин) в трудоспособном возрасте от 18 до 60 лет, в среднем 41,5 [34,0; 50,25] лет, возраст дебюта псориаза – от 2 лет до 45 лет, в среднем 27,0 [20,75; 37,25] лет, т.е. манифестация псориаза преобладала у лиц молодого возраста, длительность заболевания варьировала от 1 года до 44 лет, в среднем 14,0 [8,0; 20,0] лет. Преобладали лица с высшим образованием – 32 (89,0%) пациента, среднее образование было у 4 (11%) пациентов; злоупотребляющие алкоголем – 7 (19%) пациентов, не употребляющие алкоголь – 29 (81,0%) пациентов; курящие – 14 (39,0%) пациентов, некурящие – 22 (61,0%) пациента; отягощенная наследственность – у 2 (6,0%) пациентов, не отягощенная наследственность – у 34 (94,0%) пациентов; сезонность выявлена у 11 (31,0%) пациентов, внесезонные обострения – у 25 (69,0%) пациентов. Основные клинико-анамнестические характеристики пациентов представлены в табл. 1.
Ожирение было диагностировано у 25 (69,0%) пациентов, ИМТ у пациентов с ожирением был в диапазоне от 30,3 до 35,7. Самый низкий балл до лечения гуселькумабом по индексу PASI составил 14, самый высокий – 90, что говорит о тяжести клинических проявлений псориаза. Баллы DLQI варьировались от 10 до 30, оценка интенсивности зуда пациентом по ВАШ – от 2,5 до максимального значения 10,0.
По клиническим формам преимущественно был представлен распространенный вульгарный псориаз у 32 (89,0%) пациентов, из них с поражением волосистой части головы – у 30 (83,0%), с псориазом лица – у 6 (17,0%) пациентов, с псориатическими поражениями в аногенитальной области (АГО) – у 6 пациентов (16,0%), псориатическая эритродермия диагностирована у 4 (11,0%) пациентов, псориатическая ониходистрофия – у 18 (50,0%) пациентов, псориатический артрит – у 19 (52,0%) пациентов (табл. 2).
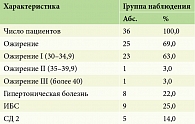
Из коморбидных патологий ожирение наблюдалось у 25 (69%) пациентов, из них ожирение I степени (ИМТ 30–34,9) – у 23 (63,0%) пациентов, ожирение II степени (ИМТ 35–39,9) – у 1 (3,0%) пациента, ожирение III степени (ИМТ более 40) – у 1 (3,0%) пациента; сердечно-сосудистые заболевания: гипертоническая болезнь (ГБ) – у 8 (22,0%) пациентов, ишемическая болезнь сердца (ИБС) – у 9 (25,0%) пациентов, сахарный диабет второго типа (СД 2) – у 5 (14,0%) пациентов (табл. 3).
Часть пациентов были бионаивными и не получали лечения препаратами генно-инженерной биологической терапии (ГИБТ) до начала терапии гуселькумабом, часть пациентов были неответчиками на терапию ингибиторами фактора некроза опухоли альфа (ФНО-α) (адалимумаб), ингибитором ИЛ-17 (иксекизумаб).
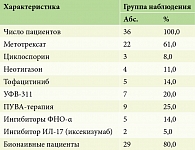
Все пациенты до назначения гуселькумаба получали стандартную базисную противовоспалительную терапию, наиболее часто назначался метотрексат – у 22 (61,0%) пациентов, циклоспорин – у 3 (8,0%) пациентов, неотигазон (ацитретин) – у 4 (11,0%) пациентов, тофацитиниб (ингибитор янус-киназ) – у 5 (14,0%) пациентов, узкополосная средневолновая терапия с длиной волны 311 нм (УФB-311) – у 7 (20,0%) пациентов, ПУВА-терапия – у 9 (25,0%) пациентов. Предшествующая терапия ГИБП была у 7 (20,0%) пациентов: лечение ингибиторами ФНО-α получали 5 (14,0%) пациентов, 2 (5,0%) пациента прекратили лечение из-за отсутствия ответа на проводимую терапию, 3 (8,0%) пациента прекратили лечение из-за ускользания ответа через 6 месяцев терапии. Предшествующая терапия ингибитором ИЛ-17 иксекизумабом не дала клинического ответа у 2 (5,0%) пациентов. Бионаивными были 29 (80,0%) пациентов, у которых терапия гуселькумабом была первой линией ГИБТ (табл. 4).
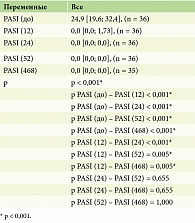
Клиническая оценка степени тяжести псориаза по индексу PASI на исходном уровне в среднем составила 24,9 [19,6; 32,4], n = 36, что соответствует тяжелому псориазу, из них у 10 (28,0%) пациентов – средняя степень тяжести (индекс PASI от 14 до 19,6 баллов), у 26 (72,0%) пациентов – тяжелая степень (индекс PASI от 20 баллов и выше).
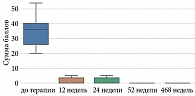
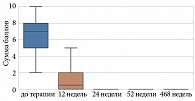
У всех пациентов наблюдалось значимое улучшение после первой инъекции гуселькумаба, 17 (47,0%) пациентов к 12-й неделе проводимой терапии достигли PASI 90, 19 (53,0%) пациентов к 12-й неделе лечения гуселькумабом достигли PASI 100. В процессе анализа по индексу PASI отмечались статистически значимые изменения на исходном уровне и на 12, 24, 52 и 468-й неделях терапии (p < 0,001) (табл. 5, рис. 1).
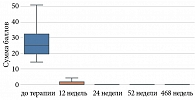
Анализ показал, что по индексу BSA отмечались статистически значимые изменения (p < 0,001) (табл. 6, рис. 2).
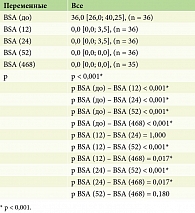
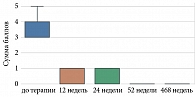
Анализ показал, что по индексу sPGA отмечались статистически значимые изменения (p < 0,001) (табл. 7, рис. 3).
На фоне терапии гуселькумабом зуд полностью прекратился к 12-й неделе у 18 (50,0%) пациентов и составил 0 по шкале ВАШ, статистически значимо снизился зуд у 18 (50,0%) пациентов и был в диапазоне от 1 до 5 по ВАШ. На 24, 52 и 468-й неделях зуд отсутствовал практически у всех пациентов, у четырех пациентов сохранялись незначительные показатели зуда от 1 до 4 по шкале ВАШ, изменения были статистически значимы (p < 0,001) (табл. 8, рис. 4).
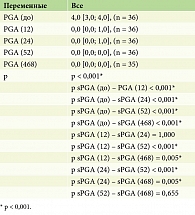
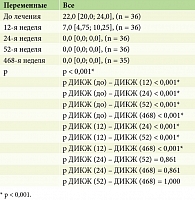
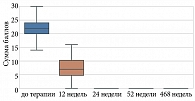
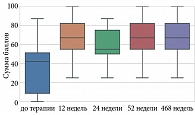
В процессе анализа по шкале ДИКЖ отмечались статистически значимые изменения (p < 0,001) (табл. 9, рис. 5).
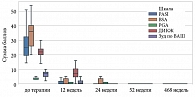
Динамика показателей оценки степени тяжести псориатического процесса по всем шкалам (PASI, BSA, sPGA), а также оценки зуда по шкале ВАШ и показателей качества жизни по опроснику ДИКЖ до лечения и на 12, 24, 52 и 468-й неделях терапии ингибитором ИЛ-23 гуселькумабом наглядно показана на рис. 6.
По показателям качества жизни достигнуты статистически значимые улучшения по всем восьми шкалам опросника SF-36 (p < 0,001).
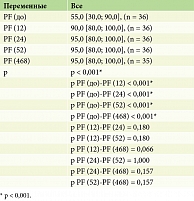
Анализ полученных результатов показал, что у пациентов с псориазом по шкале SF-36 «Физическое функционирование (Physical Functioning, PF)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 10, рис. 7).
Улучшение качества жизни человека, определяемое как достижение DLQI 0/1 и улучшение признаков на 5 и более баллов по SF-36 по сравнению с исходным уровнем, отмечалось у всех пациентов к 12-й неделе лечения гуселькумабом и сохранялось на 24, 52 и 468-й неделях наблюдения.
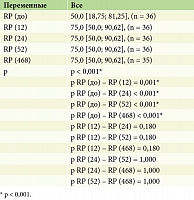
Ролевое функционирование, обусловленное физическим состоянием (Role-Physical Functioning, RP)
Анализ результатов исследования показал, что у пациентов с псориазом по шкале SF-36 «Ролевое функционирование, обусловленное физическим состоянием (Role-Physical Functioning, RP)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 11, рис. 8).
Ролевое функционирование, обусловленное эмоциональным состоянием (Role-Emotional, RE)
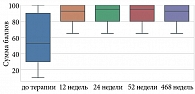
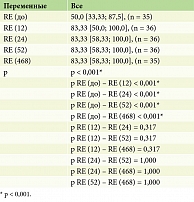
По шкале SF-36 «Ролевое функционирование, обусловленное эмоциональным состоянием (Role-Emotional, RE)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 12, рис. 9).
Интенсивность боли (Bodily pain, BP)
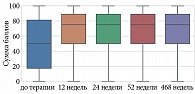
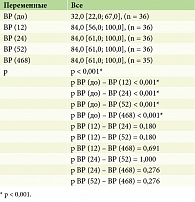
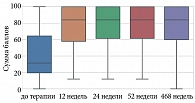
Проведенный анализ показал, что у пациентов с псориазом по шкале SF-36 «Интенсивность боли (Bodily Pain, BP)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 13, рис. 10).
Жизненная активность (Vitality, VT)
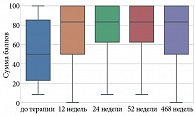
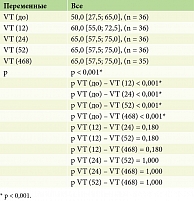
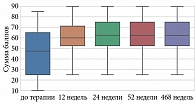
По шкале SF-36 «Жизненная активность (Vitality, VT)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 14, рис. 11).
Психическое здоровье (Mental Health, MH)
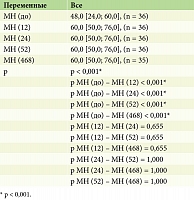
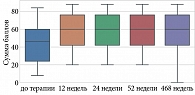
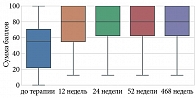
По шкале SF-36 «Психическое здоровье (Mental Health, MH)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 15, рис. 12).
Социальное функционирование (Social Functioning, SF)
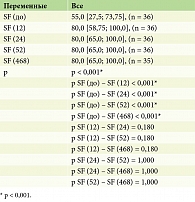
В процессе анализа у пациентов с псориазом по шкале SF-36 «Социальное функционирование (Social Functioning, SF)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 16, рис. 13).
Общее состояние здоровья (General Health, GH)
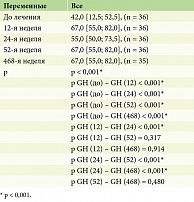
Результаты анализа показали, что у пациентов с псориазом по шкале SF-36 «Общее состояние здоровья (General Health, GH)» до и после лечения гуселькумабом отмечались статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (табл. 17, рис. 14).
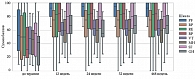
По показателям качества жизни шкалы SF-36 по всем восьми шкалам опросника (1) физическое функционирование (Physical Functioning – PF); 2) ролевое функционирование, обусловленное физическим состоянием (Role-Physical Functioning – RP); 3) интенсивность боли (Bodily Pain – BP); 4) общее состояние здоровья (General Health – GH); 5) жизненная активность (Vitality – VT); 6) социальное функционирование (Social Functioning – SF); 7) ролевое функционирование, обусловленное эмоциональным состоянием (Role-Emotional Functioning – RE); 8) психическое здоровье (Mental Health – MH)) до и после лечения гуселькумабом отмечены статистически значимые изменения (p < 0,001) на 12, 24, 52 и 468-й неделях терапии (рис. 15).
Для всех вышеперечисленных параметров исследования у больных псориазом мы получили высокую статистическую значимость разницы между исходным уровнем и после терапии гуселькумабом по индексам PASI, BSA, PGA (p < 0,001). Получено достоверно значимое снижение баллов по индексу PASI на фоне терапии гуселькумабом у всех пациентов независимо от пола, возраста, длительности псориаза, наличия коморбидного ожирения, псориатического артрита, сердечно-сосудистых заболеваний. Изменение показателей индекса PASI привело к статистически значимому улучшению показателей качества жизни по шкале ДИКЖ и по шкале SF-36 (p < 0,001). Высокие показатели улучшения качества жизни по опросникам ДИКЖ и SF-36 сохранялись в течение всего периода наблюдения.
Относительно вопроса прекращения терапии – 1 (3,0%) пациент прервал лечение гуселькумабом по причине невозможности своевременно получить препарат, в результате отмены терапии в течение года отмечено нарастание клинических проявлений псориаза, коморбидной депрессии и псориатического артрита, пациент перестал выходить из дома, заболел COVID-19 от контакта с медицинским персоналом на дому и умер. Два пациента (5,0%) перешли самостоятельно на ингибитор ИЛ-17 секукинумаб в течение трех месяцев – ответ на проводимую терапию отсутствовал (по техническим причинам не могли получить инъекции гуселькумаба), после переключения с ИЛ-17 (секукинумаб) на ИЛ-23 (гуселькумаб) ответ PASI 90 был после третьей инъекции гуселькумаба. К 24-й неделе терапии гуселькумабом у всех пациентов достигнут ответ PASI 100. На фоне проводимой терапии гуселькумабом у 1 (3,0%) пациента при плановом обследовании, по данным УЗИ, выявлено новообразование мочевого пузыря, по данным МРТ малого таза диагноз подтвержден (новообразование правых отделов мочепузырного треугольника, гиперплазия предстательной железы), по данным гистологического исследования: 1) папиллярная уротелиальная карцинома low grade без признаков инвазии, 2) фрагменты мышечной оболочки мочевого пузыря и ткани предстательной железы без опухоли, 3) фрагменты ткани предстательной железы с фокусами ацинарной аденокарциномы, сумма баллов по Gleason (3 + 3 = 6), занимает около 20% ткани. При иммуногистохимическом исследовании вокруг опухолевых желез отсутствовали базальные клетки (p63-), люминальные клетки экспрессируют P504S. Проведена операция 10.2019 г.: трансуретральная резекция (ТУР) стенки мочевого пузыря и ТУР предстательной железы. Послеоперационный период без осложнений. Проведена инфузионная, спазмолитическая, гемостатическая, антибактериальная терапия, профилактика тромбоэмболии легочной артерии. Проведена контрольная цистоскопия через три месяца с повторной консультацией онкоуролога – данных за онкопатологию не получено. На всех этапах наблюдения и проводимого лечения у онкоуролога отмены терапии гуселькумабом не потребовалось, пациент продолжал лечение по стандартной схеме – один раз в восемь недель 100 мг подкожно инъекции ингибитора ИЛ-23 гуселькумаба.
Выживаемость и безопасность препарата в исследуемой группе составила 100% (n = 36), несмотря на коморбидные состояния (ожирение, сердечно-сосудистые заболевания, сахарный диабет, тревожность и депрессия). Нежелательных явлений, в том числе опасных, с необходимостью выведения пациентов из исследования, связанных с профилем безопасности ингибитора ИЛ-23 гуселькумаба, не зарегистрировано.
Обсуждение
В последние годы с увеличением новых классов биологических препаратов, доступных для лечения псориаза, чрезвычайно важным вопросом является выбор терапии, которая может обеспечить долгосрочную эффективность и благоприятный профиль безопасности на протяжении всего периода заболевания [32, 33]. С учетом современного понимания иммунопатогенеза ключевую роль в иммунной дисрегуляции и организации провоспалительного ответа при псориазе играет регуляторный цитокин ИЛ-23 [34]. Эти знания послужили стимулом для разработки новых таргетных препаратов, направленных на блокаду ИЛ-23. Гуселькумаб – первое человеческое моноклональное антитело, являющееся ингибитором ИЛ-23 с мощным терапевтическим потенциалом для пациентов со среднетяжелым и тяжелым течением псориаза [35]. Эффективность и безопасность гуселькумаба освещена в клинических исследованиях VOYAGE 1, VOYAGE 2 и подтверждена в реальной клинической практике [35, 36]. Однако данные ограничены сокращенным периодом наблюдения.
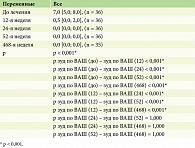
Мы провели ретроспективное одноцентровое исследование оценки долгосрочной эффективности и безопасности гуселькумаба у пациентов со среднетяжелым и тяжелым течением псориаза, в которое были включены 36 пациентов с псориазом. До лечения гуселькумабом индекс PASI составлял 24,9 [19,6; 32,4], (n = 36), BSA – 36,0 [26,0; 40,25], (n = 36), sPGA – 4,0 [3,0; 4,0], (n = 36), ВАШ – 7,0 [5,0; 8,0], (n = 36). В представленном исследовании мы подтвердили высокую эффективность гуселькумаба со статистически значимым снижением по показателям индекса PASI, BSA, sPGA и ВАШ (p < 0,001). Начиная с 12-й недели терапии 17 (47,0%) пациентов достигли PASI 90, 19 (53,0%) пациентов к 12-й неделе лечения гуселькумабом достигли PASI 100 (PASI – 0,0 [0,0; 1,73], (n = 36), BSA – 0,0 [0,0; 3,5], (n = 36), sPGA – 0,0 [0,0; 1,0], (n = 36), ВАШ – 0,5 [0,0; 2,0], (n = 36), p < 0,001). Зуд полностью прекратился к 12-й неделе у 18 (50,0%) пациентов и составил 0 по ВАШ, статистически значимо снизился зуд у 18 (50,0%) пациентов и был в диапазоне от 1 до 5 по ВАШ (p < 0,001). Клинические показатели продолжали улучшаться к 24-й неделе терапии (PASI – 0,0 [0,0; 0,0], (n = 36), BSA – 0,0 [0,0; 3,5], (n = 6), sPGA – 0,0 [0,0; 1,0], (n = 36), ВАШ – 0,0 [0,0; 0,0], (n = 36), p < 0,001). Полностью отсутствовали клинические проявления псориаза к 52-й неделе (PASI – 0,0 [0,0; 0,0], (n = 36), BSA – 0,0 [0,0; 0,0], (n = 36), sPGA – 0,0 [0,0; 0,0], (n = 36), ВАШ – 0,0 [0,0; 0,0], (n = 36), p < 0,001). Зуд отсутствовал практически у всех пациентов, у четырех пациентов сохранялись незначительные показатели зуда от 1 до 4 по ВАШ (p < 0,001). Один пациент выбыл из исследования в 2021 г. (пациент прекратил лечение самостоятельно из-за невозможности получения препарата по техническим причинам) – умер от инфекции COVID-19. Двое (5,0%) пациентов на три месяца самостоятельно перешли на лечение ингибитором ИЛ-17А секукинумабом, при переключении с ИЛ-23 на ИЛ-17А ответ на терапию отсутствовал, после переключения с ИЛ-17 (секукинумаб) на ИЛ-23 (гуселькумаб) после третьей инъекции гуселькумаба ответ был PASI 90, к 24-й неделе терапии достигнут ответ PASI 100. У 1 (3,0%) пациента при плановом обследовании была выявлена папиллярная уротелиальная карцинома low grade без признаков инвазии и аденокарцинома предстательной железы, было выполнено оперативное вмешательство без отмены терапии гуселькумабом, данных за онкопатологию при последующем наблюдении не получено.
Стойкий ответ сохранялся на протяжении всего периода наблюдения, т.е. в течение девяти лет проводимой терапии гуселькумабом, у всех включенных пациентов. Нежелательных явлений, опасных нежелательных явлений с необходимостью отмены назначения ингибитора ИЛ-23 гуселькумаба не зарегистрировано.
Эффективность гуселькумаба подтверждается в опубликованных литературных данных. Согласно данным реальной клинической практики, на фоне лечения гуселькумабом более 50% пациентов достигают полного очищения кожи в течение одного года и более [37–40].
M. Megna и соавт. в двухлетнем исследовании долгосрочной эффективности и безопасности гуселькумаба в реальных условиях у 61 пациента с псориазом получили следующие данные: на исходном уровне средние значения PASI и BSA составили 12,8 ± 8,4 и 24,5 ± 26,6 соответственно. В течение 16-й недели ответы PASI 90 и PASI 100 были достигнуты у 60,7 % и 37,7% пациентов соответственно и продолжали улучшаться до 104-й недели (PASI 90 – 73,8%, PASI 100 – 59,0%). Также было выявлено клиническое улучшение в трудно поддающихся лечению областях. Первичная и вторичная неэффективность была отмечена у 1 (1,6%) и 5 (8,2%) пациентов. Что касается безопасности, серьезных НЯ не было [41]. Согласно данным мировых регистров, 8 из 10 пациентов удерживают показатель PASI 90 в течение четырех лет терапии [42].
K. Reich и соавт. в исследованиях VOYAGE 1 и VOYAGE 2 предоставили результаты пятилетнего наблюдения терапии гуселькумабом с включением 1829 пациентов, эффективность и конечные точки качества жизни анализировали до 252-й недели, безопасность отслеживали до 264-й недели. Доля пациентов в группе гуселькумаба, достигших клинических ответов на 252-й неделе, составила 84,1 и 82,0% (≥ 90% улучшение индекса площади и тяжести псориаза (PASI)); 82,4 и 85,0% (глобальная оценка исследователя (IGA) 0 или 1); 52,7 и 53,0% (100% улучшение PASI) и 54,7 и 55,5% (IGA 0) [43]. Каждый второй пациент удерживает показатель PASI 100 в течение пяти лет терапии [44].
В нашем исследовании мы получили ответ PASI 90 у 17 (47,0%) пациентов и PASI 100 у 19 (53,0%) пациентов к 12-й неделе лечения гуселькумабом с выживаемостью терапии у 100% пациентов на протяжении всего периода наблюдения. Мы наблюдали удержание ответа «чистая кожа» в течение девяти лет терапии гуселькумабом.
Кроме того, был достигнут успех в терапии псориаза проблемных локализаций. Известно, что у значительной доли пациентов (62%) псориаз встречается в АГО, преимущественно в молодом возрасте [45–51], с выраженным зудом в области гениталий [52–54], что, в свою очередь, отрицательно влияет на качество жизни, психологическое здоровье и социальное функционирование пациента [55, 56]. В исследовании PERSIST на 28-й неделе терапии гуселькумабом у 84,3% пациентов с псориазом АГО отмечалось полное или почти полное разрешение симптомов, с улучшением показателей по индексу ДИКЖ [57]. По данным исследования GULLIVER, в реальной клинической практике покраснение в АГО значительно уменьшилось более чем у 75% пациентов, инфильтрация и шелушение – более чем у 80%, полного очищения кожи в области гениталий достигли 76% пациентов на 12-й неделе терапии гуселькумабом [58]. По нашим данным, псориатические поражения в АГО были у 6 (16,0%) пациентов (с выраженным зудом по ВАШ – от 8 до 10), а уже к 12-й неделе терапии гуселькумабом было достигнуто полное очищение кожи от псориатических проявлений в аногенитальной области (sPGA – 0,0 [0,0; 1,0]), со снижением показателей по ВАШ до 2 (0,5 [0,0; 2,0]), статистически значимом улучшении показателей качества жизни по шкалам ДИКЖ (7,0 [4,75; 10,25]) и SF-36 (p < 0,001).
Еще одной из проблемных локализаций при псориазе является зона лица. Поражение кожи лица при псориазе считают относительно редким проявлением заболевания [59], однако, по данным разных авторов, частота вовлечения кожи лица при псориазе варьирует от 17,0 до 67,7% [60]. Поражение кожи лица более характерно для пациентов молодого возраста с тяжелым распространенным поражением кожи, вовлечением ногтевых пластин и затяжным течением [61–63]. Локализация высыпаний на коже лица – в косметически и социально-значимой зоне – сопровождается значительными нарушениями качества жизни пациентов [64, 65]. В представленном исследовании псориаз с поражением в области лица был у 6 (16,0%) пациентов, течение псориаза у которых было более тяжелым, с высокими показателями нарушения качества жизни по опросникам ДИКЖ и SF-36. Разрешение псориатических элементов на коже лица коррелировало с улучшением показателей ДИКЖ и SF-36 (p < 0,001). Псориатическая ониходистрофия диагностирована у 18 (50,0%) пациентов, улучшение псориатических поражений в области ногтевых пластинок наступало медленнее по сравнению с другими проблемными локализациями, к 24-й неделе терапии гуселькумабом ногтевые пластинки отрастали здоровыми на 2/3, полностью здоровыми ногтевые пластинки отрастали к 52-й неделе терапии.
Очищение кожи у пациентов с «суперответом» сопровождалось самым высоким уровнем качества жизни, которое сохранялось на протяжении всего периода наблюдения за пациентами в течение девяти лет. Изменение показателей индекса PASI привело к статистически значимому улучшению показателей качества жизни по шкале ДИКЖ (p < 0,001) и по всем шкалам опросника SF-36 (p < 0,001) – до и после лечения гуселькумабом на 12, 24, 52 и 468-й неделях терапии. K. Schäkel и соавт. в исследовании GUIDE показали, что значительное очищение кожи у пациентов с «суперответом» позволяет достичь высокого уровня качества жизни, которое сохраняется длительное время [66–68].
В результате проведенного исследования в реальной клинической практике мы подтвердили данные других исследований о высокой и долгосрочной эффективности гуселькумаба, что является ценной поддержкой для пациентов со среднетяжелым и тяжелым течением псориаза [69]. Одной из сильных сторон ингибитора ИЛ-23 гуселькумаба является удобство применения – один раз в восемь недель в стандартной дозировке 100 мг без необходимости корректировки дозы, особенно у пациентов с коморбидным ожирением, что, в свою очередь, сохраняет приверженность к проводимой терапии и способствует соблюдению 100%-го комплаенса.
Наше исследование с участием данной категории пациентов является одним из первых с более длительным периодом наблюдения с применением ингибитора ИЛ-23 гуселькумаба. Несмотря на многообещающие результаты, возможным ограничением данного исследования может быть его недостаточная мощность. В будущем необходимо увеличить исследуемую группу пациентов, добавить группу контроля, а также группу пациентов с переключением на вторую, третью, четвертую линию ГИБП с продолжительным периодом наблюдения. Будущие исследования должны провести сравнительную оценку длительного применения ингибитора ИЛ-23 гуселькумаба и других ГИБП, а также оценить выживаемость проводимой терапии и влияние на качество жизни пациентов, в результате чего мы сможем предоставить возможность пациентам получать высокоэффективный способ контроля над заболеванием на протяжении всей жизни.
Заключение
В течение девятилетнего наблюдения мы получили убедительные данные, доказывающие устойчивую эффективность гуселькумаба с превосходным профилем безопасности у пациентов со среднетяжелым и тяжелым течением псориаза. Необходимо продолжить дальнейшие исследования долгосрочной эффективности ингибитора ИЛ-23 гуселькумаба в реальной клинической практике.
Авторы заявляют об отсутствии конфликта интересов.
I.S. Vladimirova, PhD, L.S. Kruglova, PhD, Prof
Skin and Venereal Diseases Dispensary No. 10 – Dermatology and Venereology Clinic, St. Petersburg
S.M. Kirov Military Medical Academy, St. Petersburg
Central State Medical Academy of Department of Presidential Affairs, Moscow
Corresponding author: Vladimirova Irina Sergeevna, ivladimirva@rambler.ru
Psoriasis is an autoimmune inflammatory disease with predominant involvement of the skin and musculoskeletal system, mediated by T-resident memory cells. Given the immunopathogenesis, psoriasis is a unique human problem with a sudden debut and unpredictable course. Therapy with genetically engineered biological drugs (GEBD) today allows achieving control over the disease. However, one of the main disappointments of dermatologists and patients suffering from psoriasis is the primary and secondary inefficiency of the therapy with the possible development of adverse events (AE). It is necessary to provide a highly effective and realistic treatment plan in the long term. Guselkumab is the first approved fully human immunoglobulin G1 lambda (IgG1λ), a monoclonal antibody that selectively affects the p19 subunit of interleukin (IL)-23. The efficacy and safety of guselkumab are described in the clinical trials VOYAGE 1, VOYAGE 2, NAVIGATE, ORION, ECLIPSE and international publications of real-life clinical practice. However, the data are limited by a shortened follow-up period. We present data from a nine-year follow-up of patients with psoriasis receiving guselkumab therapy in real-life clinical practice.
Purpose of the study. To evaluate the long-term efficacy of interleukin-23 inhibitor therapy (guselkumab), the impact on quality of life indicators in patients with moderate to severe psoriasis and maintenance of response to therapy.
Material and methods. A retrospective study of 36 patients diagnosed with widespread psoriasis vulgaris was conducted. Baseline indicators were assessed using the PASI, BSA, sPGA, VAS indices. Quality of life indicators were assessed using the DLQI and SF-36 scales. All patients received treatment with an interleukin-23 inhibitor (guselkumab) according to the standard regimen. Therapy efficacy was assessed by the dynamics of PASI, BSA, sPGA, VAS, DLQI, and SF-36 scores at baseline and after 12, 24, 52, and 468 weeks of therapy.
Results. Biological therapy with guselkumab resulted in a statistically significant improvement in all scores after 12 weeks, and the response was maintained at 24, 52, and 468 weeks for each patient (p<0.001). High statistical significance of the difference between baseline and after guselkumab therapy was demonstrated for PASI, BSA, sPGA, and VAS scores (p < 0.001). All patients with a "superresponse" achieved complete skin clearance PASI 100 by the 24th week of therapy. The change in PASI index values resulted in statistically significant improvement in quality of life indices according to the DLQI scale (p < 0.001). According to the SF-36 scale, statistically significant result (p < 0.001) was obtained both on the scale of physical health (PH) and on the scale of psychological health (MH) before and after treatment with guselkumab at 12, 24, 52 and 468 weeks of therapy.
Conclusion. Biological therapy with interleukin-23 inhibitor guselkumab is highly effective in reducing the severity of the disease and achieving high quality of life indices in patients with psoriasis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.