Эффективность некоторых кардиоцитопротекторов у больных артериальной гипертонией, осложненной острым ишемическим инсультом
- Аннотация
- Статья
- Ссылки





Наиболее распространенными являются ишемические инсульты (ИИ). Они становятся результатом изменений мозговых артерий и микроциркуляторного русла, формирующихся у больных АГ и церебральным атеросклерозом за многие годы клинически малосимптомного течения болезни (5, 9). Между степенью повышения как систолического артериального давления (АД), так и диастолического АД и риском инсульта установлена прямая связь во всех возрастных группах. Повышение диастолического АД на 7,5 мм рт. ст. выше нормального уровня сопровождается увеличением риска инсульта почти в 2 раза (12, 13).
АГ приводит к развитию ИИ напрямую, вызывая в перфорирующих артериях мозга липогиалиноз и фибриноидный некроз, а также через стимулирование атеросклероза прецеребральных, крупных и средних церебральных артерий и развитие сердечных заболеваний (1, 13). Повышение АД выявляется в первые дни ИИ у большинства больных, даже у тех, кто не страдал артериальной гипертонией. Поэтому с первых дней болезни возникает вопрос, снижать или не снижать АД в остром периоде ИИ. Снижение повышенного АД обосновывается опасностью геморрагической трансформации инсульта и нарастания отека мозга. С другой стороны, сохранение достаточного уровня АД диктуется необходимостью поддержания адекватного, особенно в условиях церебрального атеросклероза, перфузионного давления в зоне так называемой ишемической полутени (1, 3). Существенный дисбаланс в регуляции церебрального кровотока и трудности его коррекции обусловлены наличием дисфункции сосудистого эндотелия, нарушающей характер вазотонической реакции сосудов в ответ как на воздействие возорегулирующих систем организма, так и фармакотерапию. Поэтому адекватная терапия АГ как гипотензивными средствами, так и корректорами эндотелиальной дисфункции позволит существенно уменьшить частоту развития ИИ, снизить вероятность его осложнений и предотвратить рецидивы (2).
Особое значение при развившейся церебральной дисциркуляции имеет суточный профиль АД, так как его нарушение (недостаточное снижение или чрезмерное повышение в ночные часы), как правило, лежит в основе развития и расширения зоны инсульта, возникновения осложнений и рецидивов ИИ в остром периоде (4, 6). Внедрение в клиническую практику неинвазивного суточного мониторирования АД (СМАД) (6) позволило установить, что наиболее важными факторами, влияющими на выраженность поражения органов-мишеней и прогноз больных АГ с ИИ, по данным СМАД, являются суточная вариабельность АД и степень ночного снижения АД (6, 8).
Дисбаланс в регуляции уровней АД обусловлен не только патологическим нарушением центральной регуляции сосудистого тонуса, но и наличием дисфункции сосудистого эндотелия, сопровождающей АГ (5).Эндотелиальная дисфункция при ИИ усугубляется значительной активацией свободно-радикальных процессов, ускоряющих деградацию эндотелиального оксида азота (NO), подавляющих активность и экспрессию NO-синтазы, что уменьшает возможности регуляции сосудистого тонуса. Высокий уровень пероксидов в крови, обусловленный как исходно низким уровнем антиоксидантной защиты при АГ и атеросклерозе, так и реперфузионным синдромом при церебральной дисциркуляции, активирует свертывающую систему крови, что увеличивает вероятность тромботических осложнений при ИИ (1, 3, 5).
В этой связи для оптимизации терапии ИИ необходимо использование препаратов, корригирующих эндотелиальную дисфункцию, нормализующих работу рецепторного аппарата и оптимизирующих суточный профиль АД, а также проявляющих антиоксидантную активность, что позволит уменьшить последствия оксидантного стресса при церебральной дисциркуляции и повысить эффективность гипотензивной терапии (1).
Наибольшей эффективностью, отсутствием токсичности и минимальными побочными эффектами характеризуются производные 3-оксипиридина – Эмоксипин и Мексикор (10, 11).
Эмоксипин обладает широким спектром фармакологических свойств: способностью эффективно ингибировать свободно-радикальное окисление липидов биомембран клеток, активно реагировать и связывать перекисные радикалы липидов, стабилизировать мембраны клеток крови, уменьшать вязкость липидного слоя цитоплазматических мембран. Было отмечено церебропротекторное действие Эмоксипина при моделировании динамического нарушения мозгового кровообращения в эксперименте. Установлено положительное влияние препарата на эмоционально-волевую сферу у больных со среднетяжелыми кардиоэмболическими и лакунарными инсультами (10, 11).
Мексикор, сходный с Эмоксипином по механизму действия, обладает значительно большей антиоксидантной активностью. Он способен восстанавливать NO-продуцирующую функцию эндотелия и подавлять последствия окислительного стресса, оказывать непосредственно цитопротекторное (нейропротекторное) действие за счет оптимизации энергетического обмена в нейронах в условиях ишемии и реперфузии. В основе последнего лежит способность Мексикора ускорять окисление глюкозы, активировать менее кислородзатратный фрагмент цикла Кребса, стимулировать цитохромную цепь энергетического каскада в митохондриях, что приводит к уменьшению потребности клетки в кислороде в условиях гипоксии, восстановлению функциональной активности нейронов (7, 10, 11).
В ряде исследований было показано, что у больных АГ Мексикор в сочетании с ингибиторами АПФ ускоряет нормализацию параметров суточного профиля АД, улучшает эндотелийзависимую вазодилатацию плечевой артерии, снижает содержание липопероксидов в крови (11). Однако влияние Мексикора и Эмоксипина на профиль АД и течение острого периода ИИ остается неизученным.
Целью проведенного исследования было изучение сравнительной эффективности Мексикора и Эмоксипина в отношении их влияния на суточный профиль АД у больных АГ с ИИ в остром периоде на фоне традиционной терапии.
Было обследовано 100 больных АГ с ИИ в возрасте 65,3±2,4 года, поступивших в неврологическое отделение в первые 48 часов с момента развития инсульта. Диагноз ИИ был подтвержден данными спиральной компьютерной томографии. Пациенты были разделены на три рандомизированные группы. Критериями рандомизации служили возраст, пол и степень неврологических нарушений больных. Все больные получали традиционную терапию инсульта, включавшую цереброактивные средства (Трентал по 100 мг в/в капельно в течение первых семи дней заболевания), антиагреганты (Кардиоаспирин 300 мг/сут.) и гипотензивную терапию (Престариум по 2-4 мг/сут. и Арифон по 1,5-2,5 мг/сут.).
В первой группе традиционное лечение дополнялось Мексикором по 2,0 мл (100 мг) в первые 7 дней в/в капельно и внутрь по 0,2 г/сут. В следующие 7 дней - по 2,0 мл в/м и внутрь по 0,2 г в сутки с переходом в последующем на пероральный прием Мексикора – 0,3 г/сут. Во второй группе, помимо базовой терапии ИИ, больные получали парентерально Эмоксипин – 0,72 г/сут. в течение 3 недель.
Первую группу составили 40 человек – 18 мужчин (45%) и 22 женщины (55%), в возрасте 65,2 ± 1,3 лет. АГ II степени (по критериям ВОЗ, 2004 г.) регистрировалась у 25 больных (15 женщин и 10 мужчин), III степени отмечалась у 15 больных (9 женщин и 6 мужчин). Длительность АГ - 6,4 ± 0,3 года.
Вторую группу составили 40 человек – 20 мужчин (50%) и 20 женщин (50%), средний возраст – 63,8 ± 2,5 года. У 23 больных (13 женщин и 10 мужчин) наблюдалась АГ II степени, у 17 больных (7 женщин и 10 мужчин) – III степени. Длительность АГ – 6,6 ± 0,3 года.
Третью (контрольную) группу составили 20 больных – 11 (55%) мужчин и 9 (45%) женщин. АГ II степени наблюдалась у 13 больных, АГ III степени - у 7 больных. Длительность АГ – 7,0 ± 0,2 года.
По локализации и распространенности ИИ различий между группами выявлено не было. В первой группе ИИ локализовался в бассейне внутренних сонных артерий у 29 больных (72,5%), во второй группе – у 34 больных (85,0%), в контрольной – у 17 больных (85,0%). У 10 больных (25%) первой группы, 19 больных (47,5%) второй группы и 10 больных (25,0%) третьей группы очаг ИИ находился в средней мозговой артерии справа, слева – у 16 больных (40%) первой группы, 10 больных (25%) второй и 7 больных (35%) третьей группы. В бассейне передних мозговых артерий ИИ отмечался у 3 больных (7,5%) первой группы, 5 пациентов (12,5%) второй группы и 1 больного (5,0%) контрольной. У 11 больных (27,5%) первой группы, 6 пациентов второй и 3 больных (15%) третьей группы очаги ишемии наблюдались в вертебро-базилярном бассейне.
Суточный профиль АД оценивали путем мониторирования (СМАД), которое проводилось с помощью монитора АВРМ-02 («Meditech», Венгрия) на 1-е, 5-е, 10-е, 14-е и 21-е сутки развития инсульта с регистрацией АД каждые 15 минут днем и 30 минут ночью. При СМАД анализировали средние значения систолического (САД) и диастолического АД (ДАД) днем и ночью, вариабельность АД и суточный индекс (степень ночного снижения) САД и ДАД. При статистическом анализе была использована программа Statistica 6,0. Критерием достоверности считалось достижение уровня р < 0,05.
Достоверных различий между группами по длительности анамнеза и степени тяжести АГ выявлено не было. На фоне приема Мексикора и Эмоксипина каких-либо побочных реакций не было зарегистрировано.
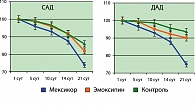
Суточная динамика уровней САД в исследуемых группах представлена в таблице 1, из которой видно, что у всех больных отмечалось снижение САД в остром периоде ИИ на фоне проводимой терапии. Обращает на себя внимание, что у больных, получавших Мексикор, САД нормализовалось на 21-е сутки ИИ, в то время как в двух других группах САД оставалось повышенным даже к концу острого периода ИИ. На 10-е сутки в группе больных, принимавших Мексикор, САД уменьшилось на 16,8% по сравнению с первыми сутками, у больных, получавших Эмоксипин, – на 10,8% (р < 0,05). У больных на фоне традиционной терапии инсульта достоверного снижения САД не наблюдалось (САД снизилось на 8,3%, р > 0,05).
На 14-е сутки отмечалось дальнейшее снижение среднесуточного САД во всех группах, но в большей степени оно было выражено в первой группе (на 21,8%). Во второй группе САД уменьшилось на 16,2% (р < 0,05). В контрольной группе эти изменения были менее выражены: САД снизилось на 9,7% по сравнению с первыми сутками развития ИИ (р > 0,05).
К концу острого периода инсульта (на 21 сутки) отмечалась нормализация цифр САД в группе пациентов, принимавших Мексикор (САД достоверно снизилось по сравнению с исходным на 24,7%). В группе больных, получавших Эмоксипин, и контрольной группе такой нормализации не регистрировалось, а снижение САД было меньше, чем в первой группе (на 18,6% и 12,3%, соответственно, по критерию χ2, р < 0,05, различия между группами достоверны).
Таким образом, Мексикор и Эмоксипин в составе комплексной терапии инсульта способствовали снижению САД в процессе гипотензивной терапии ИИ. Однако применение Мексикора у больных АГ с ИИ приводило к нормализации САД на 21-е сутки ИИ. В двух других группах окончательной нормализации САД не отмечалось на протяжении всего периода наблюдения.
Динамика уровней ДАД в группах представлена в таблице 2. У всех больных отмечалось снижение ДАД в остром периоде ИИ. У больных, получавших Мексикор, ДАД достигло нормальных значений на 10-е сутки ИИ, а во второй и третьей группах оно оставалось повышенным. На 10-е сутки в группе больных, принимавших Мексикор, ДАД уменьшилось на 14,8% и достигло нормальных значений. В то время как у больных, лечившихся эмоксипином, и в контрольной группе достоверного снижения АД не наблюдалось (ДАД снизилось на 9,3% и 6,4%, р > 0,05). На 14-е сутки отмечалось дальнейшее снижение среднесуточного показателя ДАД во всех группах, больше выраженное в первой группе (на 18,1%). Во второй группе ДАД уменьшилось на 10,1% (р < 0,05). В контрольной группе эти изменения менее выражены: ДАД снизилось на 8,4% по сравнению с первыми сутками развития ИИ (р > 0,05). К концу острого периода инсульта (на 21-е сутки) в первой группе ДАД достоверно снизилось по сравнению с исходным на 20,5%. В группе больных, получавших Эмоксипин, ДАД снизилось на 11,1%, а в контрольной группе – лишь на 9,7%.
Применение Мексикора и Эмоксипина у больных АГ с ИИ способствовали снижению ДАД за время наблюдения. Однако использование Мексикора приводило к нормализации ДАД на 10-е сутки ИИ. В двух других группах окончательной нормализации суточного профиля ДАД не отмечалось на протяжении всего острого периода инсульта.
Высокие значения вариабельности АД у больных АГ с ИИ являются фактором, увеличивающим риск развития осложнений со стороны органов-мишеней, включая головной мозг (6). В остром периоде инсульта имеет место нестабильность ауторегуляции мозгового кровотока (8) и увеличение вариабельности АД, что способствует рецидиву церебральной дисциркуляции (10) и возникновению цереброкардиального синдрома (13).
На фоне проводимой терапии во всех группах отмечалось уменьшение исходно высокой вариабельности АД в дневные часы (таблица 3), при этом в первой группе к концу острого периода вариабельность САД и ДАД уменьшилась достоверно более значительно, чем во второй и третьей группах. На 5-е и 10-е сутки показатели вариабельности САД и ДАД в трех группах достоверно не изменились. К 14-м суткам в 1-й группе больных значения вариабельности САД и ДАД в дневные часы снизились больше (на 15,3% и 12,8% соответственно, р < 0,05) по сравнению с двумя другими группами, где достоверных изменений показателя вариабельности не наблюдалось (10,1% и 4,8% – во второй группе и 7,8% и 3,4% – в третьей группе р > 0,05; различия между группами по критерию χ2 достоверны, р < 0,05, рисунок 1). Как видно из таблицы 4, в ночные часы вариабельность САД и ДАД в группе больных, принимавших Мексикор, снизилась в большей степени (на 12,4% и 12,1%), чем в двух остальных группах (на 8,1% и 7,7% – во второй и на 8,4% и 4,3% – в третьей группах, по критерию χ2 р < 0,05, межгрупповые различия достоверны, рисунок 2).
К 21-му дню ИИ в дневные часы в первой группе вариабельность САД и ДАД снизилась на 20,3% и 15,4%, а во второй группе – на 14,6% и 8,2%, а в контроле – на 10,0% и 4,1%. В ночные часы в группе больных, лечившихся Мексикором, – на 26,0% и 25,0%, в группе пациентов, получавших Эмоксипин, – на 18,0% и 9,9%, а в контрольной группе – на 14,0% и 6,4%, соответственно.
Таким образом, включение Мексикора и Эмоксипина в комплексную терапию ИИ приводило к уменьшению вариабельности АД, в особенности в ночные часы, что, безусловно, снижало риск рецидива инсульта за счет дестабилизации АД. Применение Мексикора, в отличие от Эмоксипина, в большей степени способствовало улучшению патологически повышенной вариабельности АД.
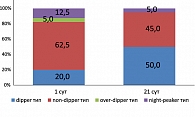
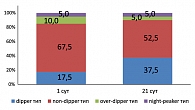
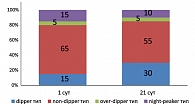
Структура суточного профиля в трех группах до начала терапии выглядела следующим образом (рисунки 3, 4, 5): нормальный («dipper») тип суточной кривой наблюдался у 8 больных (20,0%) первой, 7 больных (17,5%) второй и 3 больных (15,0%) третьей группы. non-dipper тип (снижение АД ночью менее 10%) регистрировался у 25 больных (62,5%) первой, 27 больных (67,5%) второй и 13 больных (65,0%) третьей группы. over-dipper тип (чрезмерное ночное снижение АД) – у 2 больных (5,0%) первой, 4 больных (10,0%) второй и 1 больного (5,0%) третьей группы. night-peaker тип (повышенное АД в ночное время) – у 5 больных (12,5%) первой, 2 больных (5,0%) второй, 3 больных (15,0%) третьей группы, соответственно.
В процессе лечения наблюдались изменения характера суточного профиля АД, более выраженные в группе больных, принимавших Мексикор (рисунки 3, 4, 5). Увеличилось число больных с нормальным типом суточной кривой: в первой группе – на 30,0%, во второй – на 20%, а в группе контроля – на 15,0%. Число больных, имеющих non-dipper тип суточной кривой, уменьшилось на 17,5% в первой группе, на 15,0% – во второй и на 10,0% – в контрольной группе. Количество больных, имеющих over-dipper тип, в первой группе уменьшилось на 5,0%, во второй группе – на 5,0%, а в контрольной группе динамики этого типа суточной кривой не отмечалось. Имеющих night-peaker тип – на 7,5% в первой группе и на 5,0% – в третьей группе, а во второй группе динамики этого типа кривой не наблюдалось.
Полученные результаты свидетельствуют об улучшении суточного профиля АД и снижении вероятности дестабилизации АД, уменьшении риска геморрагической трансформации инсульта, рецидива острой дисциркуляции, повышении эффективности лечения в отношении вторичной профилактики инсульта. Применение Мексикора в большей степени способствовало улучшению суточного профиля АД, чем лечение Эмоксипином.
Таким образом, Мексикор в большей степени, чем Эмоксипин, в составе комплексной терапии ИИ способствовал ускорению нормализации АД, особенно в ночное время, предотвращал его чрезмерное снижению в ранние предутренние часы, что препятствует усугублению гипоперфузии головного мозга и рецидиву инсульта (2, 7).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.