Эффективность применения пиоглитазона в лечении больных сахарным диабетом 2 типа
- Аннотация
- Статья
- Ссылки

Ключевым механизмом патогенеза СД 2 типа считается инсулинорезистентность (ИР), которая приводит не только к гипергликемии, но и провоцирует такие факторы риска развития сердечно-сосудистых заболеваний, как артериальная гипертензия и дислипидемия. В связи с этим создание и применение в терапии больных лекарственных средств, непосредственно воздействующих на ИР, является перспективным направлением в лечении данного тяжелого заболевания.
С 1996 года в лечении больных СД 2 типа используется новый класс препаратов, объединенных по механизму их действия в группу тиазолидиндионов (ТЗД) или сенситайзеров инсулина (циглитазон, росиглитазон, дарглитазон, троглитазон, пиоглитазон, энглитазон), основное действие которых направлено на повышение чувствительности периферических тканей к инсулину. Несмотря на многочисленные публикации 80-90-х годов прошлого столетия, посвященные доклиническому изучению безопасности и эффективности перечисленных соединений, в клиническую практику в дальнейшем были внедрены лишь три препарата из этой группы – троглитазон, росиглитазон и пиоглитазон. К сожалению, в последующем троглитазон был запрещен к использованию в связи с проявившейся при длительном применении гепатотоксичностью.
В настоящее время из группы ТЗД используются два препарата: пиоглитазон и росиглитазон.
Механизм действия тиазолидиндионов
Основной терапевтический эффект ТЗД при СД 2 типа заключается в снижении инсулинорезистентности за счет увеличения чувствительности периферических тканей к действию инсулина.
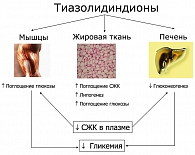
Инсулинорезистентность (ИР) появляется задолго до клинической манифестации СД 2 типа. Сниженная чувствительность жировых клеток к антилиполитическому эффекту инсулина ведет к хроническому повышению содержания свободных жирных кислот (СЖК) в плазме крови. СЖК, в свою очередь, усиливают резистентность к инсулину на уровне печени и мышечной ткани, что приводит к усилению глюконеогенеза и уменьшению захвата глюкозы этими тканями. В подобных условиях жировые клетки продуцируют избыточное количество цитокинов (фактор некроза опухоли a – ФНО-a), интерлейкин (IL-6 и резистин), которые усугубляют имеющуюся инсулинорезистентность и стимулируют атерогенез. Продукция жировыми клетками другого цитокина – адипонектина, повышающего чувствительность тканей к инсулину, снижается.
Тиазолидиндионы являются высокоафинными агонистами ядерных рецепторов, активируемых пролифератором пероксисом – PPARg (peroxisome proliferators-activated receptor), относящихся к семейству транскрипционных факторов, которые контролируют экспрессию генов, регулирующих углеводный и липидный обмен в жировой и мышечной ткани. Известно несколько изоформ PPAR: PPARa, PPARg (подтипы 1, 2) и PPARb/PPARd. PPARa, PPARg и PPARd, которые играют важную роль в регуляции адипогенеза и ИР. Ген PPARγ у ряда млекопитающих, включая человека, локализован в 3-й хромосоме (локус 3р25). Рецептор PPARg преимущественно экспрессируется в жировых клетках и моноцитах, меньше – в скелетных мышцах, печени и почках. Наиболее значимой ролью PPARg является дифференцировка клеток жировой ткани. Агонисты PPARg (ТЗД) обеспечивают формирование адипоцитов малых размеров, более чувствительных к инсулину, которые активно поглощают СЖК и регулируют преимущественное отложение жира в подкожной, а не в висцеральной жировой клетчатке (3). Кроме того, активация PPARg приводит к усилению экспрессии и транслокации на клеточную мембрану транспортеров глюкозы (GLUT-1 и GLUT-4), которые обеспечивают перенос глюкозы в клетки печени и мышц и, таким образом, снижают уровень гликемии. Под воздействием агонистов PPARg уменьшается выработка ФНО-a и увеличивается экспрессия адипонектина, что также повышает чувствительность периферических тканей к инсулину (4).
Таким образом, тиазолидиндионы, прежде всего, улучшают чувствительность тканей к инсулину, что проявляется снижением глюконеогенеза в печени, торможением липолиза в жировой ткани, снижением концентрации СЖК в крови и улучшением утилизации глюкозы в мышцах (рисунок 1).
Тиазолдиндионы не оказывают прямого стимулирующего действия на секрецию инсулина. Однако снижение гликемии и СЖК в крови на фоне приема ТЗД уменьшает глюкозо- и липотоксическое действие на b-клетки и периферические ткани и, с течением времени, приводит к улучшению секреции инсулина b-клетками (5). Исследованиями Miyazaki Y. (2002) и Wallace T.M. (2004) было доказано непосредственное положительное влияние ТЗД на функциональную активность b-клеток в виде уменьшения апоптоза и усиления их пролиферации (6, 7). В исследовании Diani A.R. (2004) было показано, что назначение пиоглитазона лабораторным животным с СД 2 типа способствовало сохранению структуры островков Лангерганса (8).
Снижение инсулинорезистентности под влиянием пиоглитазона было убедительно подтверждено в клиническом исследовании с помощью оценки модели гомеостаза НОМА (9). В работе Kawamori R. (1998) было показано улучшение периферического поглощения глюкозы тканями на фоне двенадцати недель приема пиоглитазона в дозе 30 мг/сут. по сравнению с плацебо (1,0 мг/кг × мин. vs. 0,4 мг/кг × мин, p = 0,003) (10). Исследование, проведенное Benett S.M. et al. (2004), показало, что при применении в течение 12 недель ТЗД (росиглитазона) у лиц с нарушенной толерантностью к глюкозе индекс чувствительности к инсулину увеличивался на 24,3%, в то время как на фоне применения плацебо, наоборот, снижался на 18,3% (11). В плацебо-контролируемом исследовании TRIPOD изучалось влияние троглитазона на риск развития СД 2 типа у латиноамериканских женщин с гестационным СД в анамнезе (12). Результаты работы подтвердили факт снижения в будущем относительного риска развития СД 2 типа у данной категории пациенток на 55%. Необходимо отметить, что частота развития СД 2 типа в год на фоне троглитазона составила 5,4% по сравнению с 12,1% на фоне плацебо. В открытом исследовании PIPOD, которое явилось продолжением исследования TRIPOD, назначение пиоглитазона также ассоциировалось со снижением риска развития СД 2 типа (частота вновь выявленных случаев СД 2 типа cоставила 4,6% в год) (13).
Сахароснижающий эффект пиоглитазона
Многочисленные исследования клинического применения пиоглитазона доказали его эффективность в терапии больных СД 2 типа.
Результаты многоцентровых плацебо-контролируемых исследований показали, что пиоглитазон эффективно снижает уровень гликемии как в монотерапии, так и в комбинации с другими пероральными сахароснижающими препаратами, в частности с широко применяемыми в лечении больных СД 2 типа метформином и производными сульфонилмочевины (14, 15, 16, 17).
С февраля 2008 г. другой ТЗД – розиглитазон, не рекомендован к применению в комбинации с инсулином в связи с возможным риском развития застойной сердечной недостаточности. В связи с этим современная позиция ведущих диабетологов США и Европы, отраженная в «A consensus statement of the American Diabetes Association and the European Association for the Study of Diabetes» на текущий год, является несколько неожиданной, т.к. допускает совместное использование инсулина и пиоглитазона. Очевидно, что подобное утверждение базируется на данных серьезных клинических исследований. Так, двойное слепое рандомизированное плацебо-контролируемое исследование, проведенное Matoo V. в 2005 г. с участием 289 пациентов с СД 2 типа, показало, что добавление пиоглитазона к инсулинотерапии ведет к достоверному снижению уровней гликированного гемоглобина (HbA1c) и гликемии натощак (18). Однако настораживает тот факт, что на фоне комбинированной терапии у больных достоверно чаще отмечались эпизоды гипогликемии. Кроме того, прибавка массы тела на фоне монотерапии инсулином оказалась ниже, чем при комбинации с пиоглитазоном (0,2 кг vs. 4,05 кг). В то же время комбинация пиоглитазона с инсулином сопровождалась положительной динамикой в липидном спектре крови и уровнях маркеров сердечно-сосудистого риска (ПАИ-1,СРБ). Короткая продолжительность данного исследования (6 месяцев) не позволила провести анализ сердечно-сосудистых исходов. Учитывая определенный риск развития застойной сердечной недостаточности при комбинации розиглитазона с инсулином, мы в своей практике не рискуем комбинировать последний с пиоглитазоном до получения достоверной информации о полной безопасности подобного лечения.
Влияние пиоглитазона на факторы риска развития сердечно-сосудистых заболеваний
Помимо сахароснижающего действия, ТЗД также могут оказывать положительное влияние на целый ряд факторов риска развития сердечно-сосудистых заболеваний. Особое значение имеет воздействие препаратов на липидный спектр крови. В ряде исследований, проведенных в последние годы, было показано, что пиоглитазон оказывает благоприятное воздействие на уровень липидов. Так, исследования, проведенные Goldberg R.B. (2005) и Dogrell S.A. (2008), показали, что пиоглитазон снижает уровень триглицеридов (19, 20). Кроме того, пиоглитазон способствует повышению уровня антиатерогенной фракции холестерина липопротеидов высокой плотности (ЛПВП). Эти данные согласуются с результатами исследования Proactive (PROspective pioglitAzone Clinical Trial In macroVascular Events), в котором в течение 3 лет принимали участие 5238 пациентов, страдающих СД 2 типа и имеющих макрососудистые осложнения в анамнезе. Комбинация пиоглитазона с диетой и пероральными сахароснижающими препаратами в течение 3 лет наблюдения привела к повышению на 9% уровня ЛПВП и снижению на 13% триглицеридов по сравнению с исходным. Общая смертность, риск развития нефатального инфаркта миокарда и острого нарушения мозгового кровообращения на фоне применения пиоглитазона достоверно снизились. Общая вероятность возникновения перечисленных событий у лиц, получавших пиоглитазон, уменьшилась на 16%.
Результаты исследования CHICAGO (2006) и работы, проведенной Langenfeld M.R. et al. (2005) (21), показали, что на фоне приема пиоглитазона уменьшается толщина сосудистой стенки и, таким образом, замедляется развитие атеросклероза. Экспериментальное исследование, проведенное Nesto R. (2004), указывает на улучшение процессов ремоделирования левого желудочка и восстановления после ишемии и реперфузии при применении ТЗД (22). К сожалению, влияние этих положительных морфологических изменений на отдаленные сердечно-сосудистые исходы не были изучены, что, несомненно, снижает их клиническую значимость.
Возможные побочные эффекты пиоглитазона
Во всех клинических исследованиях прием пиоглитазона, как и других ТЗД, сопровождался увеличением массы тела на 0,5-3,7 кг, особенно в первые 6 месяцев лечения. В дальнейшем вес больных стабилизировался.
Безусловно, прибавка в весе является очень нежелательным побочным эффектом любого лекарственного средства при лечении больных СД 2 типа, т.к. абсолютно подавляющее большинство пациентов имеют ожирение или избыточную массу тела. Однако важно подчеркнуть, что прием пиоглитазона сопровождается, в основном, увеличением объема подкожной жировой клетчатки, тогда как количество висцерального жира на фоне приема ТЗД снижается. Иными словами, несмотря на увеличение веса при приеме пиоглитазона, риск развития и/или прогрессирования сердечно-сосудистых заболеваний не повышается (23). Важно отметить, что степень увеличения массы тела прямо коррелирует с сопутствующей сахароснижающей терапией, т.е. прибавка в весе выше у больных, получающих комбинацию ТЗД с инсулином или препаратами сульфонилмочевины, и ниже – с метформином.
На фоне лечения пиоглитазоном у 3-15% пациентов наблюдается задержка жидкости, причины которой до конца не изучены. Так, существует точка зрения, что в результате снижения экскреции натрия и увеличения задержки жидкости происходит увеличение объема циркулирующей крови. Кроме того, ТЗД могут способствовать вазодилатации артерий с последующим увеличением объема внеклеточной жидкости (22). Именно с этим побочным эффектом ТЗД и ассоциируется застойная сердечная недостаточность. Так, в широкомасштабном исследовании PROactive частота вновь выявленных случаев застойной сердечной недостаточности на фоне терапии пиоглитазоном оказалась достоверно выше, чем при использовании плацебо (11% vs 8%, p < 0,0001). В то же время ретроспективный анализ историй болезни 23440 больных СД 2 типа, получавших монотерапию любым сахароснижающим препаратом в среднем в течение 10,2 месяцев, не подтвердил статистически достоверного увеличения частоты госпитализаций по поводу застойной сердечной недостаточности на фоне приема пиоглитазона (24).
Терапия пиоглитазоном сопровождается незначительным дозозависимым снижением уровней гемоглобина и гематокрита. Данный побочный эффект ТЗД, скорее всего, объясняется гемодилюцией вследствие задержки жидкости. Токсического воздействия на костный мозг при приеме пиоглитазона не наблюдается.
Данные относительно воздействия ТЗД на минеральную плотность кости (МПК) немногочисленны и противоречивы. В многоцентровом клиническом исследовании ADOPT, включавшем 4360 пациентов, было обнаружено повышение риска развития переломов у женщин, получавших ТЗД (росиглитазон). Повышение риска переломов наблюдали лишь при длительном приеме росиглитазона, не менее чем в течение одного года. На текущий момент времени достоверных данных относительно отрицательного воздействия ТЗД на МПК в литературе нет (25).
Важно подчеркнуть, что ни в одном из многочисленных исследований и почти десятилетнем опыте клинического использования пиоглитазона токсического действия этого препарата на печень выявлено не было. Данный факт позволяет заключить, что токсическое действие троглитазона на печень специфично только для этого тиазолидиндиона и не является классовым свойством всей группы.
Дозировка и назначение пиоглитазона
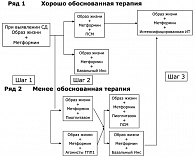
Пиоглитазон применяется для снижения инсулинорезистентности у больных с нарушенной толерантностью к глюкозе и СД 2 типа один раз в сутки в стартовой дозе 15-30 мг/сут. независимо от приема пищи. Согласно современному Консенсусу назначения сахароснижающей терапии больным СД 2 типа, препаратом первого ряда при выявлении заболевания является метформин в сочетании с изменением образа жизни («Шаг 1»).
К метформину в качестве второго «шага» последовательно добавляются производные сульфонилмочевины, или базальный инсулин, как препараты ряда наиболее обоснованной терапии на 2009 год. Пиоглитазон рекомендуется как первый препарат «второго шага» во втором ряду менее обоснованной терапии при неэффективности монотерапии метформином. При назначении комбинированной терапии с препаратами сульфонилмочевины доза пиоглитазона обычно не превышает 30 мг/сут. во избежание большей прибавки в весе. При комбинированной терапии с метформином начальная доза пиоглитазона составляет 15 мг/сут. и может быть увеличена при отсутствии побочных эффектов до 45 мг/сут. При монотерапии пиоглитазоном суточная доза может составлять 45 мг. Однако следует иметь в виду, что HbA1c > 7% через три месяца от начала сахароснижающей терапии является поводом к назначению как минимум комбинированной сахароснижающей терапии.
Эффективность пиоглитазона, как и других ТЗД, оценивается по уровню HbA1c. Адекватность дозы и эффективность других сахароснижающих препаратов, действующих на подавление глюконеогенеза или на стимуляцию секреции инсулина собственными b-клетками, можно четко определить по положительной динамике со стороны базальной или постпрандиальной гликемии. ТЗД, постепенно снижая инсулинорезистентность, не оказывают столь быстрого гипогликемизирующего эффекта, который легко оценить при домашнем самоконтроле. В связи с этим больным, получающим пиоглитазон, особенно необходим контроль HbA1c не реже одного раза в три месяца. При отсутствии достижения целевых значений гликированного (HbA1c < 7%) через 3 месяца терапии суточная доза препарата может быть увеличена на 15 мг/сут. или назначена комбинированная терапия.
Прием пиоглитазона абсолютно противопоказан во время беременности, лактации, при наличии у пациента недостаточности кровообращении (класс по NYHA I-IV) и/или нарушения функции печени. Уровень печеночных ферментов необходимо исследовать как до назначения препарата, так и в процессе терапии.
Поскольку пиоглитазон метаболизируется в печени и выводится из организма преимущественно с желчью и калом, он не так опасен для лиц с патологией почек, как метформин. Однако, учитывая задержку жидкости на фоне приема ТЗД, мы не рекомендуем назначать пиоглитазон лицам с хронической почечной недостаточностью. Злоупотребление алкоголем при лечении пиоглитазоном может способствовать развитию эпизодов гипогликемии.
Данные о безопасности и эффективности применения пиоглитазона у детей и подростков в возрасте до 18 лет отсутствуют, поэтому назначение пиоглитазона данной категории пациентов не рекомендуется.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.