Инсулин гларгин 300 ЕД/мл: новые возможности в управлении вариабельностью гликемии у больных сахарным диабетом
- Аннотация
- Статья
- Ссылки
- English
Пациенты с СД, получающие инсулин, как правило, имеют наиболее высокую ВГ, что увеличивает риск осложнений. Для решения этой проблемы разрабатываются новые препараты инсулина с оптимизированными фармакокинетическими и фармакодинамическими свойствами, в том числе аналоги инсулина пролонгированного действия. Увеличение продолжительности действия и сглаживание фармакокинетического профиля позволяют добиться равномерного сахароснижающего эффекта в течение суток с меньшим риском гипогликемии.
Создание новой формы инсулина гларгин с повышенной концентрацией действующего вещества в единице объема (300 ЕД/мл) – еще один шаг к более физиологичной инсулинотерапии. Особенности фармакокинетики и фармакодинамики гларгина 300 ЕД/мл дают основание предполагать наличие преимуществ в отношении ВГ и частоты гипогликемий. Меньшая ВГ при применении гларгина 300 ЕД/мл по сравнению с использованием гларгина 100 ЕД/мл показана в рандомизированном клиническом исследовании фазы III, а меньший риск развития гипогликемических состояний – в программе клинических исследований EDITION. Таким образом, инсулин гларгин 300 ЕД/мл открывает новые возможности в управлении СД.
Пациенты с СД, получающие инсулин, как правило, имеют наиболее высокую ВГ, что увеличивает риск осложнений. Для решения этой проблемы разрабатываются новые препараты инсулина с оптимизированными фармакокинетическими и фармакодинамическими свойствами, в том числе аналоги инсулина пролонгированного действия. Увеличение продолжительности действия и сглаживание фармакокинетического профиля позволяют добиться равномерного сахароснижающего эффекта в течение суток с меньшим риском гипогликемии.
Создание новой формы инсулина гларгин с повышенной концентрацией действующего вещества в единице объема (300 ЕД/мл) – еще один шаг к более физиологичной инсулинотерапии. Особенности фармакокинетики и фармакодинамики гларгина 300 ЕД/мл дают основание предполагать наличие преимуществ в отношении ВГ и частоты гипогликемий. Меньшая ВГ при применении гларгина 300 ЕД/мл по сравнению с использованием гларгина 100 ЕД/мл показана в рандомизированном клиническом исследовании фазы III, а меньший риск развития гипогликемических состояний – в программе клинических исследований EDITION. Таким образом, инсулин гларгин 300 ЕД/мл открывает новые возможности в управлении СД.
C 1980-х гг. основным критерием эффективности лечения сахарного диабета (СД) считался уровень гликированного гемоглобина (HbA1c), который дает представление о среднем (интегральном) уровне глюкозы за последние два-три месяца. Однако накапливались данные о том, что развитие осложнений СД обусловлено не только средним уровнем глюкозы, но и степенью изменения ее концентрации в крови, то есть вариабельностью гликемии (ВГ).
Вариабельность гликемии в норме и при сахарном диабете
В настоящее время выделяют два основных вида ВГ:
- в течение суток (флюктуация гликемии);
- межсуточная, или изо дня в день (воспроизодимость).
Суточные колебания уровня глюкозы обусловлены:
- поступлением глюкозы в кровь из желудочно-кишечного тракта после еды и последующей утилизацией глюкозы в тканях под влиянием инсулина (постпрандиальные колебания);
- физической нагрузкой;
- циркадным ритмом секреции гормонов и чувствительности к инсулину.
Межсуточные колебания гликемии менее заметны. Они могут возникать под действием цикличных эндогенных факторов (например, фазных изменений секреции половых гормонов во время менструального цикла), в результате изменения характера питания и физической активности в течение длительного периода, стресса и т.д.
У лиц с нормальной толерантностью к глюкозе ее колебания в интерстициальной жидкости, как правило, составляют 3,3–9,3 ммоль/л. До 80% значений, полученных при непрерывном мониторинге глюкозы (НМГ), находятся в диапазоне 3,3–5,5 ммоль/л, около 20% – 5,6–7,8 ммоль/л, на более высокие показатели приходится около 1% значений [1]. По другим источникам, у здоровых лиц средняя длительность колебаний с уровнем глюкозы > 7,8, > 8,9 и > 10 ммоль/л в течение суток составляет 13% (3%, 23%), 1% (0%, 6%) и 0% (0%, 1%) соответственно (данные представлены в виде медианы, 25-го и 75-го процентилей) [2].
Нарушение секреции и/или действия инсулина приводит к возрастанию не только среднего уровня глюкозы в крови, но и периода и амплитуды ее постпрандиальных колебаний. Увеличение ВГ отмечается уже на доклинических этапах СД 1 и 2 типа.
С началом сахароснижающей терапии появляется риск выхода кривой гликемии в гипогликемический диапазон.
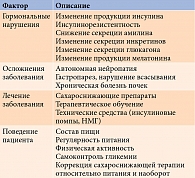
Сложные гормонально-метаболические нарушения и осложнения, развивающиеся по мере прогрессирования СД, оказывают дополнительные, подчас разнонаправленные эффекты на динамику гликемии. Большое влияние на ВГ также оказывают характер питания, физическая активность и степень вовлеченности пациента в управление заболеванием (табл. 1) [3].
Клиническое значение
Роль ВГ как предиктора сосудистых осложнений продемонстрирована при проведении субанализа данных многоцентрового проспективного исследования ADVANCE [4]. В исследовании установлена линейная связь вариабельности HbA1c и гликемии натощак с комбинацией микро- и макрососудистых осложнений (р = 0,01 и р = 0,001 соответственно), макрососудистыми осложнениями (р = 0,02 и р = 0,001 соответственно) и смертностью от всех причин (р = 0,001 и р = 0,005 соответственно) у больных СД 2 типа.
Доказательства связи между крупноволновой ВГ (уровень HbA1c) и риском осложнений получены в когорте больных СД 1 типа в исследовании DCCT. В работе анализировалась вариабельность значений HbA1c (стандартное отклонение (СО)) после стабилизации гликемии в течение шести месяцев. Длительность исследования составила девять лет. Использование показателя вариабельности HbA1c в дополнение к среднему уровню HbA1c позволило дать более точный прогноз в отношении развития микрососудистых осложнений. В частности, увеличение вариабельности HbA1c на 1% ассоциировалось с повышением риска развития ретинопатии в 2,3 раза [5].
В исследовании FinnDiane установлено, что вариабельность НbA1c влияет на риск прогрессирования нефропатии (отношение шансов (ОШ) 1,92) независимо от среднего уровня НbA1c и традиционных факторов риска [6]. Суммарная частота лазерной коагуляции сетчатки в течение пяти лет составила 19% при вариабельности HbA1c в пределах верхнего квартиля и 10% – в пределах нижнего квартиля (ОШ 1,6). Среди не получавших лазерного лечения риск развития пролиферативной диабетической ретинопатии был наибольшим у тех, кто имел вариабельность HbA1c в пределах верхнего квартиля (ОШ 1,7) [7]. Ассоциация величины СО HbA1c с сердечно-сосудистыми осложнениями сохраняла значимость после учета среднего уровня НbA1c и традиционных факторов риска [6].
В исследовании Verona Diabetes Study оценивалась связь ВГ натощак и смерти больных СД 2 типа за десятилетний период. Вариабельность (но не уровень) гликемии натощак независимо от других факторов риска оказалась связана со смертностью от сердечно-сосудистых причин (р = 0,007). Таковая при наибольших значениях вариабельности (верхняя треть диапазона) была в 2,4 раза выше, чем при наименьших [8].
Анализ данных Hong Kong Diabetes Registry выявил влияние вариабельности HbA1c на риск развития сердечно-сосудистых осложнений у больных СД 2 типа. За время наблюдения (медиана – 7,2 года) макрососудистые осложнения (ишемическая болезнь сердца, сердечная недостаточность, ишемический инсульт, макроангиопатия нижних конечностей) развились у 10% больных. Эти пациенты имели более высокие средний уровень и вариабельность HbA1c (p < 0,001) [9].
По обобщенным данным, ВГ ассоциируется с толщиной комплекса «интима – медиа» сонных артерий, коронарным атеросклерозом, содержанием липидов и фиброзированием бляшек в коронарных артериях, гипертрофией левого желудочка, риском сердечно-сосудистых катастроф в течение года после инфаркта миокарда и тяжелых желудочковых аритмий [3].
Продолжается изучение взаимосвязи между ВГ и гипогликемией. Показано, что эпизоды гипогликемии у больных СД чаще возникают в периоды повышенной ВГ [10]. По нашим данным, показатели ВГ, рассчитанные по результатам НМГ за предшествующий день, могут рассматриваться как перспективные предикторы ночной гипогликемии [11]. Перенесенная накануне гипогликемия и высокая ВГ сопряжены со снижением симпатического ответа на последующую гипогликемию [12]. Это позволяет объяснить формирование порочного круга повторяющейся гипогликемии у ряда больных СД.
Таким образом, высокая ВГ у пациентов с СД является самостоятельным фактором риска сосудистых осложнений и гипогликемии.
Вариабельность гликемии и инсулинотерапия
Пациенты с СД, получающие инсулин, как правило, имеют наиболее высокую ВГ. Разработка новых препаратов инсулина с оптимизированными фармакокинетическими и фармакодинамическими свойствами поможет решить задачу уменьшения ВГ.
Важнейшим достижением диабетологии стало появление пролонгированных аналогов инсулина, в частности гларгина, детемира. Общим трендом в совершенствовании характеристик пролонгированных аналогов инсулина является увеличение продолжительности действия и сглаживание фармакокинетического профиля для достижения более равномерного сахароснижающего эффекта на протяжении суток и уменьшения риска гипогликемии.
Результатом разработок в этом направлении стало появление новых аналогов базального инсулина, препаратов деглудек и гларгин 300 ЕД/мл.
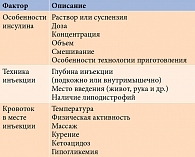
Известно, что метаболические эффекты, индуцированные одной и той же дозой инсулина, существенно различаются не только у разных, но даже у одного и то же больного в разные дни. Это обозначается как межиндивидуальная и интраиндивидуальная вариабельность действия. Разница эффектов может быть обусловлена особенностями скорости абсорбции и метаболизма инсулина (фармакокинетический аспект вариабельности), а также различием его действия на чувствительные клетки (фармакодинамический аспект). Факторы, влияющие на абсорбцию инсулина, представлены в табл. 2 [3].
Клэмп-исследования признаны классическим методом оценки вариабельности действия инсулинов. О фармакокинетической вариабельности инсулина судят по его концентрации в плазме крови, о фармакодинамической – по количеству введенной глюкозы для поддержания ее зафиксированного уровня. Показано, что высокая вариабельность кинетики и действия инсулина затрудняет подбор дозы и повышает риск гипогликемии [13].
Инсулин гларгин
Гларгин – первый и наиболее изученный длительно действующий аналог базального инсулина. Установлено, что интраиндивидуальная вариабельность суточного профиля гларгина значительно меньше, чем НПХ-инсулина.
Более плавный фармакокинетический профиль гларгина способствует снижению ВГ и риска гипогликемии [13]. Показатели ночной ВГ, в том числе высокочувствительный индекс риска гипогликемии (Low Blood Glucose Index – LBGI), у пациентов с СД 2 типа, получавших гларгин, был существенно ниже, чем у больных на терапии НПХ-инсулином [14]. В многоцентровом исследовании, включавшем больных СД 2 типа с HbA1c от 4,5 до 8,0%, оценивалось влияние перевода с НПХ-инсулина на инсулин гларгин на показатели ВГ, рассчитанные по результатам НМГ. После перевода на гларгин наблюдалось значительное увеличение площади под кривой (Area Under the Curve – AUC) гликемии, ограниченной нормальными значениями, уменьшение AUC в зоне гипергликемии, а также снижение суточных колебаний уровня глюкозы [15]. В пятилетнем исследовании с участием больных СД 2 типа суммарное количество симптоматических дневных и тяжелых гипогликемий на фоне терапии гларгином было достоверно ниже, чем на фоне терапии НПХ-инсулином (относительный риск (ОР) 0,74 и 0,64 соответственно, р < 0,05) [16].
Инсулин гларгин 300 ЕД/мл: фармакокинетические и фармакодинамические характеристики
Создание инсулина гларгин с концентрацией 300 ЕД/мл (Туджео®) стало следующим шагом в направлении физиологичной инсулинотерапии. Гларгин 300 ЕД/мл, так же как гларгин 100 ЕД/мл, биотрансформируется с образованием активных метаболитов M1 и M2. Метаболиты сохраняют свойственную гларгину активность, а их митогенный эффект не превышает таковой человеческого инсулина [13].
Сахароснижающая активность инсулина гларгин 300 ЕД/мл остается стабильной на протяжении шести- и 12-часовых интервалов в течение суток после введения. Препарат продемонстрировал низкую вариабельность показателей фармакокинетики в разные дни у одних и тех же больных (коэффициент вариации для AUC концентрации составил 17,4%) [17].
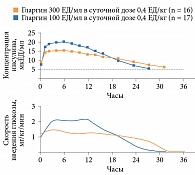
Вследствие более компактного распределения в подкожном депо гларгин 300 ЕД/мл обладает более стабильными и продолжительными фармакокинетическим и фармакодинамическим профилями по сравнению с гларгином 100 ЕД/мл (рис. 1). Гларгин 300 ЕД/мл в отличие от гларгина 100 ЕД/мл после введения в одинаковых дозах в условиях клэмпа демонстрирует более ровное и пролонгированное распределение концентрации в течение суток. У гларгина 300 ЕД/мл период полувыведения в среднем на 5,5 часа больше, чем у гларгина 100 ЕД/мл (в среднем 19,0 и 13,5 часа соответственно). Кроме того, гларгин 300 ЕД/мл обеспечивает нахождение в целевом диапазоне уровня глюкозы в последние четыре часа интервала дозирования больший процент времени [18].
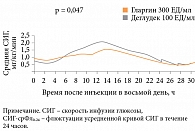
T. Bailey и соавт. сравнили фармакокинетические и фармакодинамические характеристики инсулинов гларгин 300 ЕД/мл и деглудек 100 ЕД/мл у больных СД 1 типа. Внутрисуточная вариабельность фармакодинамического эффекта (скорости инфузии глюкозы в условиях эугликемического клэмпа) оказалась ниже при введении инсулина гларгин 300 ЕД/мл в суточной дозе 0,4 ЕД/кг (р = 0,047). Фармакодинамические параметры двух инсулинов при введении в суточной дозе 0,6 ЕД/кг достоверно не различались. Длительность действия обоих инсулинов достигала 30 часов [19] (рис. 2).
Клинические преимущества
Особенности фармакокинетики и фармакодинамики гларгина 300 ЕД/мл дают основание предполагать наличие преимуществ в отношении ВГ и частоты гипогликемий.
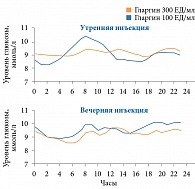
В рандомизированном клиническом исследовании фазы III сравнивалось влияние гларгинов 300 и 100 ЕД/мл на ВГ у больных СД 1 типа [20]. Пациенты получали препараты в течение 16 недель с перекрестом относительно времени введения препарата. В ходе исследования дважды проводился НМГ, продолжительность – две недели. Длительность нахождения кривой концентрации глюкозы в пределах целевого диапазона (4,4–7,8 ммоль/л) на фоне терапии гларгином 300 ЕД/мл и гларгином 100 ЕД/мл не различалась. По данным НМГ, процент времени нахождения в целевом диапазоне у пациентов, получавших гларгин 300 ЕД/мл, и больных, применявших гларгин 100 ЕД/мл, был сопоставим, однако у первых отмечен меньший процент времени нахождения в диапазоне значений менее 4,4 ммоль/л в условиях гипогликемии, а также гипергликемии более 22 ммоль/л. Подтвержденные (≤ 3,9 ммоль/л, < 3,0 ммоль/л) или тяжелые гипогликемии в ночные часы наблюдались реже при лечении гларгином 300 ЕД/мл. При этом средние изменения значений глюкозы натощак и HbA1c к 16-й неделе от исходного уровня в обеих группах были практически одинаковыми. Общая, суточная и межсуточная ВГ оказались ниже на фоне терапии гларгином 300 ЕД/мл. Необходимо также отметить, что профиль гликемии при применении Туджео® был ровнее независимо от времени введения (утром или вечером), в то время как гликемическая кривая при применении Лантуса оказалась более ровной при введении препарата в вечерние часы (рис. 3) [20].
Эффективность и частота эпизодов гипогликемии у больных СД 1 и 2 типов на фоне применения инсулина гларгин 300 ЕД/мл по сравнению с инсулином гларгин 100 ЕД/мл оценивались в программе клинических исследований EDITION.
Титрация дозы инсулина проводилась до достижения целевого уровня глюкозы плазмы натощак (4,4–5,6 ммоль/л) по данным самоконтроля. При оценке эффективности главной вторичной точкой была доля участников, перенесших хотя бы один эпизод подтвержденной (≤ 3,9 ммоль/л) или ночной (00:00–05:59) тяжелой гипогликемии с девятой недели по шестой месяц наблюдения. Дополнительной вторичной точкой стало количество эпизодов гипогликемии в расчете на одного пациента в год.
В исследовании EDITION-4 сравнивался риск гипогликемии у больных СД 1 типа на фоне лечения гларгином 300 ЕД/мл и гларгином 100 ЕД/мл [21, 22]. Уменьшение частоты эпизодов ночной гипогликемии в группе гларгина 300 ЕД/мл было зафиксировано в первые восемь недель терапии (ОР 0,82 при 95%-ном доверительном интервале (ДИ) 0,70–0,96). К концу исследования (через 12 месяцев) суточная доза препарата у получавших гларгин 300 ЕД/мл была несколько выше (0,47 по сравнению с 0,40 ЕД/кг). Несмотря на это, различия в частоте гипогликемий между группами отсутствовали.
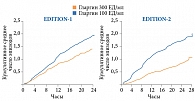
В исследованиях EDITION-1 и -2 зафиксировано меньшее количество пациентов, перенесших как минимум один эпизод подтвержденной или тяжелой ночной гипогликемии, на фоне лечения гларгином 300 ЕД/мл в режиме базис-болюсной инсулинотерапии (EDITION-1) или базальной инсулинотерапии (EDITION-2) – на 21 и 23% соответственно (р = 0,0045 и р = 0,038) [23, 24]. Частота ночной подтвержденной или тяжелой гипогликемии за весь период наблюдения в EDITION-1 была ниже на 25% (OP 0,75 (95% ДИ 0,58–0,95)), в EDITION-2 – на 48% (OP 0,52 (95% ДИ 0,35–0,77)) (рис. 4). Частота подтвержденной или тяжелой гипогликемии в любое время суток при введении гларгина 300 ЕД/мл была несколько ниже в EDITION-2 (ОР 0,77 (95% ДИ 0,63–0,96)) и не различалась в EDITION-1 (ОР 0,95 (95% ДИ 0,8–1,13)). При этом уменьшение риска ночной гипогликемии в EDITION-1 и -2 произошло несмотря на то, что суточная доза инсулина к концу исследований оказалась в среднем на 10% больше у больных, получавших гларгин 300 ЕД/мл, чем у применявших гларгин 100 ЕД/мл.
В программе клинических исследований EDITION продемонстрирована возможность адаптации времени введения гларгина 300 ЕД/мл с учетом особенностей образа жизни пациента. У 13,9% участников EDITION-1 и 18,7% – EDITION-2 интервалы между инъекциями выходили за рамки трехчасового отклонения от среднего 24-часового интервала (гибкая схема дозирования). Частота эпизодов подтвержденной или тяжелой гипогликемии в любое время суток и ночью была аналогичной при фиксированной и гибкой схемах дозирования.
Таким образом, применение гларгина 300 ЕД/мл позволяет адаптировать время введения.
В исследовании EDITION-3 сравнивались эффективность и безопасность гларгина 300 ЕД/мл и гларгина 100 ЕД/мл у больных СД 2 типа, ранее не получавших инсулинотерапии [25]. При сопоставимом снижении уровня HbA1c в течение 12 месяцев в группе гларгина 300 ЕД/мл зафиксирована меньшая доля больных, перенесших как минимум один эпизод подтвержденной (≤ 3 ммоль/л) или тяжелой гипогликемии в любое время суток (ОР 0,66 (95% ДИ 0,50–0,88)).
Заключение
Появление инсулина гларгин 300 ЕД/мл (Туджео®) открывает новые возможности в управлении гликемией при СД. Благодаря ровному и пролонгированному распределению концентрации обеспечивается равномерное сахароснижающее действие препарата и, как следствие, снижение ВГ и риска развития гипогликемии.
V.V. Klimontov
Research Institute of Clinical and Experimental Lymphology – Branch of the Institute of Cytology and Genetics, Siberian Branch of Russian Academy of Sciences
The Institute of Medicine and Psychology, Novosibirsk National Research State University
Contact person: Vadim Klimontov, klimontov@mail.ru
In recent years, as criterion of diabetes mellitus (DM) treatment efficiency has been considered the glycemic variability (GV). In several clinical researches (ADVANCE, DCCT, FinnDiane, Verona Diabetes Study, etc.) the relationship between GV and micro- and macrovascular complications have been demonstrated.
Patients with diabetes using insulin tend to have the highest GV, which increases the risk of complications. To solve this problem new insulin preparations were developed with optimized pharmacokinetic and pharmacodynamic properties, including insulin analogs of prolonged action. The increase in duration of action and smooth pharmacokinetic profile allows achieving even hypoglemic effect during the day with the less risk of hypoglycemia.
Creation of the new form of insulin glargine with increasing concentration of the active substance per unit of volume (300 U/ml) – the step towards more physiological insulin therapy. Features of pharmacokinetics and pharmacodynamics of glargine 300 U/ml allow suggesting the presence of benefits in terms of GV and frequency of hypoglycemia. Smaller GV when using glargine of 300 U/ml compared with the use of glargine of 100 U/ml are was observed in a randomized clinical study of phase II and the smaller risk of hypoglycemic states in a program of clinical researches EDITION. Thus, insulin glargine of 300 U/ml opens new possibilities in the diabetes management.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.