Кардиоренальное метаболическое здоровье*
- Аннотация
- Статья
- Ссылки
- English
Кардиоренальное метаболическое здоровье отражает взаимодействие метаболических факторов риска, хронической болезни почек и сердечно-сосудистой системы и оказывает абсолютное влияние на заболеваемость и смертность.
Ввиду «плохого» кардиоренального метаболического здоровья, особенно среди лиц с неблагоприятными социальными детерминантами (условиями жизни), существует необходимость в понимании термина «кардиоренальный метаболический синдром», определении его стадий, а также в обсуждении возможностей профилактики и лечения на каждой стадии. Крайне важно также уделить внимание социальным детерминантам здоровья в моделях оказания помощи и уменьшить разделение помощи путем упрощения подходов к междисциплинарной модели, ориентированной на пациента.
Кардиоренальное метаболическое здоровье отражает взаимодействие метаболических факторов риска, хронической болезни почек и сердечно-сосудистой системы и оказывает абсолютное влияние на заболеваемость и смертность.
Ввиду «плохого» кардиоренального метаболического здоровья, особенно среди лиц с неблагоприятными социальными детерминантами (условиями жизни), существует необходимость в понимании термина «кардиоренальный метаболический синдром», определении его стадий, а также в обсуждении возможностей профилактики и лечения на каждой стадии. Крайне важно также уделить внимание социальным детерминантам здоровья в моделях оказания помощи и уменьшить разделение помощи путем упрощения подходов к междисциплинарной модели, ориентированной на пациента.



Определение
Кардиоренальное метаболическое здоровье представляет собой патофизиологическое взаимодействие между метаболическими факторами риска, такими как ожирение и сахарный диабет (СД), хронической болезнью почек (ХБП) и сердечно-сосудистой патологией. На сегодняшний день хорошо описана двунаправленная связь между дисфункцией сердечно-сосудистой системы и почек, известная как кардиоренальный синдром, при котором дисфункция одного из органов обусловливает дисфункцию другого. Столь же широко распространено понимание кардиометаболического синдрома [1]. Избыточная и дисфункциональная жировая ткань (особенно висцеральное ожирение и другие эктопические жировые отложения) может вызывать воспаление, резистентность к инсулину, появление метаболических факторов риска и множества системных последствий, включая повышенный риск сердечно-сосудистых заболеваний (ССЗ) [2]. Хотя эти синдромы достаточно известны, растет понимание того, что метаболические нарушения играют ключевую патофизиологическую роль в двунаправленных взаимодействиях сердечно-сосудистой системы и почек. Кроме того, дисфункция почек все чаще признается ключевым медиатором связи между метаболическими факторами риска и ССЗ, особенно сердечной недостаточностью (СН) [3, 4]. Таким образом, вместо того чтобы рассматривать кардиоренальный синдром и кардиометаболические заболевания как отдельные процессы, становится все более очевидным, что необходимо рассматривать их пересечения как более обширную концепцию CArdioREnal and MEtabolic (CaReMe).
Определение кардиоренального метаболического синдрома поможет выявить лиц с высоким риском заболеваемости и смертности и инициировать профилактические стратегии до повреждения органов-мишеней. Кроме того, единое определение CaReMe-синдрома будет способствовать лучшему взаимодействию между научными организациями и общественностью, что позволит улучшить прогностические исходы.
В результате обширного обсуждения и научного подкрепления в данной статье было сформулировано определение кардиоренального метаболического синдрома, рекомендованное к дальнейшему применению. Кардиоренальный метаболический синдром – системное заболевание, характеризующееся патофизиологическими взаимодействиями между метаболическими факторами риска, ХБП и сердечно-сосудистой патологией, приводящими к полиорганной дисфункции и высокой частоте неблагоприятных сердечно-сосудистых исходов. К группе кардиоренального метаболического синдрома относят как лиц с риском сердечно-сосудистых заболеваний из-за наличия метаболических факторов риска, ХБП или их обоих, так и лиц с существующими сердечно-сосудистыми заболеваниями, которые потенциально связаны с метаболическими факторами риска/ХБП или осложняют их. На повышенную вероятность развития синдрома и его неблагоприятных последствий дополнительно влияют неблагоприятные социальные детерминанты здоровья.
Стадийность
Кардиоренальный метаболический синдром – прогрессирующее состояние, которое начинается в раннем возрасте с биологических, социальных и экологических воздействий или воздействий, приводящих к накоплению избыточной и дисфункциональной жировой ткани [5, 6], с развитием в последующем воспаления, окислительного стресса и резистентности к инсулину. Избыточная и дисфункциональная жировая ткань часто приводит к формированию метаболических факторов риска (например, артериальной гипертензии (АГ), гипертриглицеридемии, метаболическому синдрому, СД 2 типа) и ХБП [7]. Со временем эти заболевания могут приводить к развитию субклинического коронарного атеросклероза в виде кальцификации коронарных артерий, субклинических нарушений структуры и функции миокарда, а также прогрессирующему снижению функции почек, что предрасполагает к высокому риску клинических сердечно-сосудистых заболеваний, почечной недостаточности, инвалидизации и смерти. Поэтому важно определить объем профилактических мероприятий на ранних стадиях развития синдрома, когда клинические проявления отсутствуют.
Концепция стадирования CaReMe-синдрома отражает его прогрессирующую патофизиологию, важность раннего выявления изменений, связанных с ним, для поддержки мер по профилактике и подчеркивает поэтапное увеличение абсолютного риска сердечно-сосудистых заболеваний, связанного с более поздними стадиями, при которых усиленная терапия будет приводить к наибольшей конечной клинической пользе.
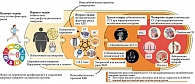
Выделяют четыре стадии кардиоренального метаболического синдрома (рис. 1).
Нулевая стадия – отсутствие факторов риска кардио-ренального метаболического синдрома при нормальном индексе массы тела (ИМТ) и окружности талии, нормогликемии, нормотензии, нормальном липидном профиле и отсутствии признаков ХБП или субклинических/клинических сердечно-сосудистых заболеваний.
Первая стадия – наличие избыточного веса/ожирения, абдоминального ожирения или дисфункции жировой ткани и других метаболических факторов риска или ХБП, таких как ИМТ ≥ 25 кг/м2 (или ≥ 23 кг/м2 у азиатов), окружность талии ≥ 88/102 см у женщин/мужчин (или ≥ 80/90 см у женщин/мужчин азиатского происхождения), уровень глюкозы в крови натощак ≥ 100–124 мг/дл (5,55–6,88 ммоль/л) или гликированного гемоглобина (HbA1c) – от 5,7 до 6,4%.
К лицам с первой стадией также относят женщин с гестационным диабетом в анамнезе, которые находятся в зоне риска развития диабета и должны наблюдаться на предмет возникновения нарушения толерантности к глюкозе после беременности [8].
Вторая стадия – наличие метаболических факторов риска, таких как гипертриглицеридемия ≥ 135 мг/дл (1,526 ммоль/л), артериальная гипертензия первой и второй стадий, метаболический синдром, сахарный диабет, ХБП умеренного и высокого риска или то и другое вместе.
Третья стадия – субклинические сердечно-сосудистые заболевания и ХБП, субклиническое атеросклеротическое заболевание сердца или субклиническая СН в сочетании с избыточным/дисфункциональным ожирением, другими метаболическими факторами риска или ХБП.
Субклиническое атеросклеротическое заболевание сердца диагностируется по коронарному кальцинозу (субклинический атеросклероз – по результатам коронарографии/КТ-ангиографии). Субклиническая сердечная недостаточность определяется по повышенным уровням сердечных биомаркеров (NT-proBNP ≥ 125 пг/мл, высокочувствительный тропонин T ≥ 14 нг/л для женщин и ≥ 22 нг/л для мужчин, высокочувствительный тропонин I ≥ 10 нг/л для женщин и ≥ 12 нг/л для мужчин) или по эхокардиографическим параметрам, комбинация двух параметров указывает на самый высокий риск развития СН.
Выделяют следующие эквиваленты риска субклинических сердечно-сосудистых заболеваний:
- ХБП очень высокого риска (ХБП четвертой или пятой стадии или очень высокий риск по классификации KDIGO);
- высокий прогнозируемый десятилетний риск сердечно-сосудистых заболеваний.
Четвертая стадия – клинические сердечно-сосудистые заболевания (ишемическая болезнь сердца (ИБС), сердечная недостаточность, инсульт, заболевание периферических артерий, фибрилляция предсердий (ФП)) на фоне избыточного/дисфункционального ожирения, других факторов риска кардио-ренального метаболического синдрома или ХБП. В зависимости от отсутствия/наличия почечной недостаточности выделяют две подстадии – 4а и 4b.
Факторы, повышающие риск
Помимо патофизиологических процессов, обусловливающих стадирование кардиоренального метаболического синдрома, существуют дополнительные факторы, которые увеличивают вероятность его прогрессирования:
- хронические воспалительные состояния (например, псориаз, ревматоидный артрит, волчанка, ВИЧ/СПИД);
- принадлежность к определенной демографической группе (например, лица южноазиатского происхождения, более низкого социально-экономического статуса);
- высокая нагрузка неблагоприятных социальных детерминант здоровья;
- расстройства психического здоровья (например, депрессия и тревога);
- нарушения сна (например, синдром обструктивного апноэ во сне);
- гендерные факторы риска (кроме гестационного диабета первой стадии):
- преждевременная менопауза в анамнезе (возраст < 40 лет);
- неблагоприятные исходы беременности в анамнезе (например, гипертонические нарушения беременности, преждевременные роды, малый гестационный возраст);
- синдром поликистозных яичников;
- эректильная дисфункция;
- повышение уровня С-реактивного белка (≥ 2,0 мг/л);
- семейный анамнез почечной недостаточности, семейный анамнез диабета.
Скрининг
Особое внимание уделяется выявлению лиц на доклинической фазе с целью ранней профилактики и предотвращения прогрессирования кардиоренального метаболического синдрома, возникновения клинических проявлений сердечно-сосудистых заболеваний и почечной недостаточности. Скрининговые программы должны быть высокоточными, легко воспроизводимыми и доступными на любом уровне оказания медицинской помощи. Важно также, чтобы результаты скрининга напрямую влияли на дальнейшую тактику профилактики и лечения.
В рамках CaReMe-концепции проводят скрининг биологических факторов, а также социальных детерминант здоровья. Биологические факторы включают в себя скрининг метаболических факторов риска и оценку функции почек, а также мероприятия, направленные на выявление субклинического атеросклероза и дисфункции сердца. Скрининг на социальные детерминанты здоровья предусматривает установление ограничений на пути к здоровому образу жизни, самообслуживанию, доступу к медицинской помощи, а также к профилактике и лечению клинически значимых заболеваний.
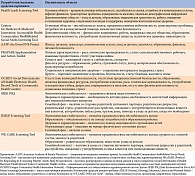
Сердечно-сосудистые заболевания развиваются от зачатия до позднего взросления, а воздействие факторов риска начинается еще до зачатия. Внутриутробное материнское ожирение и гипертензия влияют на кардиометаболические факторы риска у ребенка посредством геномного импринтинга. Наличие факторов риска в юности также связано с ранними сердечно-сосудистыми нарушениями, которые часто проявляются уже в зрелом возрасте. Тем не менее существуют противоречивые рекомендации крупных профессиональных сообществ относительно целесообразности скрининга факторов риска в юности. Именно поэтому мероприятия скрининга подразделяют на две группы: для лиц моложе 21 года и для лиц старше этого возраста (табл. 1). Различные подходы к скринингу для каждой группы пациентов способствуют более раннему и лучшему выявлению доклинических признаков кардиоренального метаболического синдрома.
Особое внимание уделяется скринингу социальных детерминант здоровья. Экономические, социальные, экологические и психосоциальные факторы, влияющие на состояние здоровья на протяжении всей жизни, играют важную роль в кардиоренальном метаболическом здоровье. Кроме того, неблагоприятные социальные детерминанты напрямую влияют на сердечно-сосудистое здоровье, на уровень смертности от сердечно-сосудистых заболеваний и общей смертности. В США хорошо развит скрининг социальных детерминант здоровья, оценивающий различные области (табл. 2).
Прогнозирование риска
Предотвращению сердечно-сосудистых событий будет способствовать разработка нового алгоритма прогнозирования риска возникновения кардиоренального метаболического синдрома [9].
С учетом роста заболеваемости и смертности, связанных с ССЗ и ХБП, первым шагом является создание и оценка моделей прогнозирования риска, способных количественно определить абсолютный риск развития любого сердечно-сосудистого события и его составных частей (атеросклеротических заболеваний сердца и СН).
Действующие руководства рекомендуют использовать многопараметрические уравнения прогнозирования риска для предотвращения как атеросклеротических болезней сердца, так и сердечной недостаточности. В совместных рекомендациях Американской кардиологической ассоциации (American Heart Association – AHA) и Американского колледжа кардиологов (American College of Cardiology – ACC) 2019 г. по первичной профилактике ССЗ предусмотрен класс рекомендаций 1, уровень доказательности B-NR (нерандомизированное исследование) для расчета десятилетнего риска развития атеросклеротических болезней сердца. В совместные рекомендации Американского колледжа кардиологов/Американской кардиологической ассоциации/Американского общества сердечной недостаточности 2022 г. впервые был включен класс рекомендаций 2a, уровень доказательности B-NR для рассмотрения валидированных многопараметрических показателей с целью оценки риска развития СН [10].
Факторы риска как для атеросклеротических болезней сердца, так и для СН схожие, при наличии нескольких факторов риска абсолютный риск неблагоприятных исходов считается более высоким. Однако необходим единый многопараметрический метод, позволяющий количественно оценить вероятность сердечно-сосудистого события и его составляющих (атеросклеротических заболеваний сердца и СН), который будет точным, обобщающим различные группы населения и хорошо валидированным. Идеальное уравнение прогнозирования риска ССЗ должно быть получено и проверено на выборке, которая в полной мере отражает современную популяцию с ее расовым, этническим, социально-экономическим и географическим разнообразием, включать в себя предикторы кардио-ренального метаболического синдрома, случаи атеросклеротических сердечно-сосудистых заболеваний (АССЗ) и СН в качестве исходов, охватывать широкий возрастной диапазон и быть актуально на протяжении всей жизни.
Акцент на взаимосвязи между здоровьем почек и здоровьем сердечно-сосудистой системы
Здоровье почек неразрывно связано со здоровьем сердечно-сосудистой системы, причем риск развития ССЗ у лиц с нарушенной функцией почек повышается прямолинейно в зависимости от тяжести нарушения. Поэтому прогнозирование снижения функции почек или почечной недостаточности имеет большое значение для сердечно-сосудистой системы. Кроме того, наличие препаратов, предотвращающих снижение функции почек, таких как ингибиторы ангиотензинпревращающего фермента (АПФ)/блокаторы рецепторов ангиотензина II (БРА), ингибиторы натрий-глюкозного контранспортера 2 (НГЛТ-2) и нестероидные антагонисты минералокортикоидов (АМКР), подчеркивает важность стратегий, основанных на оценке риска, в которых приоритет отдается здоровью как почек, так и сердечно-сосудистой системы.
Подход к профилактике и лечению
Подходы к профилактике и лечению на разных стадиях CaReMe-синдрома были разработаны научно-консультативной группой кардиоренального метаболического здоровья после тщательного анализа литературы и основных клинических рекомендаций.
Алгоритмы для нулевой – третьей стадий кардио-ренального метаболического синдрома направлены на профилактику событий, связанных с ХБП (рис. 2), для четвертой стадии – на лечение ХБП в контексте факторов синдрома (рис. 3). При этом на всех стадиях междисциплинарная помощь и коррекция социальных детерминант здоровья являются главными отправными точками профилактики и лечения (см. рис. 2 и 3).
Кроме того, предлагается создать междисциплинарную группу по лечению кардиоренального метаболического синдрома, которая совместно с врачами первичного звена будет разрабатывать протоколированные рекомендации по уходу за пациентами с двумя и более совместно протекающими заболеваниями в рамках CaReMe-синдрома для поддержания целостного подхода к обеспечению качественного и своевременного доступа к лечению. Междисциплинарная команда будет поддерживаться координатором, а также включать представителей первичной медицинской помощи, кардиологов, нефрологов, эндокринологов, фармации и сестринского дела, навигаторов по уходу, социальных работников или работников здравоохранения на уровне общества.
Определены потенциальные пороговые значения для направления пациента на консультацию к узкому специалисту:
- нефрологу – при повышенном риске по KDIGO: стадии 3a (A3, особенно если нет реакции на ингибиторы АПФ/БРА), 3b (A2/A3), 4 и 5;
- эндокринологу – при СД с плохим гликемическим контролем (HbA1c > 9%) или микрососудистых заболеваниях и/или повреждениях органов-мишеней;
- кардиологу – при наличии сердечно-сосудистых заболеваний, можно рассмотреть необходимость консультации при наличии субклинического ССЗ высокого риска, например заметно повышенный показатель коронарного кальция (≥ 300 у взрослых непожилого возраста (мужчины < 65 лет или женщины < 75 лет) и/или множественные факторы риска кардиоренального метаболического синдрома или уровень коронарного кальция ≥ 1000) или сочетание повышенного уровня сердечного биомаркера и наличие отклонений по данным эхокардиографии.
Нулевая стадия: отсутствие факторов
Целью ухода за пациентами на нулевой стадии кардиоренального метаболического синдрома является поддержание нормальных антропометрических показателей, нормогликемии, нормотензии и нормального липидного профиля для минимизации риска развития ХБП или ССЗ. Концепция AHA Life's Essential 8 представляет собой основу для достижения, поддержания и наблюдения за состоянием сердечно-сосудистого здоровья населения. Среди всех показателей сердечно-сосудистого здоровья профилактика ожирения является основным направлением первичной профилактики кардиоренального метаболического синдрома в связи с его ролью в развитии СД 2 типа, артериальной гипертензии и гипертриглицеридемии. Продвижение здорового питания и регулярной физической активности имеет основополагающее значение для предотвращения чрезмерного увеличения веса в детстве [11]. Для поддержания здорового образа жизни и предотвращения формирования факторов риска кардио-ренального метаболического синдрома необходимо [12, 13]:
- оптимизировать кардиоренальное метаболическое здоровье матери (даже до беременности), чтобы снизить вероятность развития кардиоренального метаболического синдрома у потомства;
- обеспечивать надлежащее санитарное просвещение;
- осуществлять изменение образа жизни и использовать ресурсы для предотвращения возникновения факторов риска кардиоренального метаболического синдрома у более молодых групп населения.
Первая стадия: избыточное или дисфункциональное ожирение
На первой стадии кардиоренального метаболического синдрома целью лечения является устранение избыточного или дисфункционального ожирения для предотвращения формирования метаболических факторов риска. Рекомендовано измерять не только ИМТ, но и окружность талии. Наличие абдоминального ожирения (окружность талии ≥ 88 см у женщин и ≥ 102 см у мужчин, ≥ 80 и 90 см для азиатского населения соответственно [14]) определяет основную группу для предотвращения ожирения. Независимо от ИМТ нарушение толерантности к глюкозе или предиабет являются основанием для первоочередного проведения мероприятий по изменению образа жизни, снижению массы тела с привлечением при необходимости междисциплинарной команды. Важно стремиться к снижению массы тела не менее чем на 5%. При этом большее снижение будет приводить к более благоприятным результатам. Фармакотерапия и бариатрическая хирургия являются вспомогательными методами у лиц с ИМТ ≥ 30 и 40 кг/м2 соответственно и у тех, кто не может достичь целевого снижения веса с помощью модификации образа жизни. При сохраняющемся/прогрессирующем нарушении толерантности к глюкозе, несмотря на модификацию образа жизни, может быть рассмотрен вопрос о применении метформина для предотвращения прогрессирования сахарного диабета.
Вторая стадия: метаболические факторы риска и заболевания почек
Целью лечения на второй стадии является комплексное устранение метаболических факторов риска и ХБП с целью предотвращения прогрессирования ССЗ до субклинических и клинических форм.
Метаболический синдром, гипертриглицеридемия и артериальная гипертензия. Достижение оптимального снижения сердечно-сосудистого риска при метаболическом синдроме (МС) обеспечивается изменением образа жизни с последующей фармакотерапией неконтролируемого артериального давления (АД), повышенного уровня глюкозы в крови и липидов. У лиц с промежуточным риском развития атеросклеротических болезней сердца метаболический синдром является дополнительным фактором риска, что обусловливает использование статинов [15].
Гипертриглицеридемия повышает риск развития атеросклеротических болезней сердца и часто связана с метаболическим синдромом и инсулинорезистентностью. Таким образом, после исключения вторичных причин первой линией терапии является модификация образа жизни. При остаточной гипертриглицеридемии у лиц с промежуточным или более высоким предполагаемым риском атеросклеротических заболеваний сердца рекомендуется терапия статинами для снижения риска и умеренного снижения уровня триглицеридов (10–30%). Лицам с уровнем триглицеридов ≥ 500 мг/дл и повышенным риском развития панкреатита рекомендуется терапия фибратами, при этом фенофибрат предпочтителен при совместном приеме со статинами из-за меньшего количества побочных эффектов. Для лиц с уровнем триглицеридов от 135 до 499 мг/дл при наличии диабета и дополнительных факторов риска можно рассматривать возможность назначения икозапента этила для снижения риска возникновения атеросклеротических ССЗ.
Лечение артериальной гипертонии должно проводиться в соответствии с установленными рекомендациями, предусматривающими изменение образа жизни, соблюдение сбалансированной диеты с низким содержанием соли и применение фармакотерапии при необходимости [16]. Целевым уровнем АД для пациентов с диабетом и без него является уровень < 130/80 мм рт. ст. Ингибитор ренин-ангиотензин-альдостероновой системы (РААС) должен быть частью схемы лечения гипертензии у больных диабетом с альбуминурией и пациентов с ХБП для дополнительной нефропротекции.
Сахарный диабет. Подходы к профилактике сердечно-сосудистых заболеваний при СД 2 типа включают изменение образа жизни, достижение целевого уровня HbA1c, АД и холестерина, а также использование препаратов, снижающих риск развития сердечно-сосудистых заболеваний, включая сахароснижающие, гиполипидемические препараты и антиагреганты [17]. Рекомендовано достижение целевых значений: HbA1c < 7% для небеременных взрослых без значительной гипогликемии, АД < 130/80 мм рт. ст. Поскольку у большинства лиц с диабетом отмечается промежуточный риск возникновения АССЗ, показана терапия статинами средней и высокой интенсивности с возможностью добавления эзетимиба для лиц с высоким прогнозируемым риском таковых с целью снижения уровня липопротеинов низкой плотности (ЛПНП) на ≥ 50%. Ингибитор НГЛТ-2 или агонист рецепторов глюкагоноподобного пептида 1 (ГПП-1) показаны для снижения риска ССЗ у лиц с высоким прогнозируемым риском или отдельными сопутствующими заболеваниями. Ингибиторы НГЛТ-2 предпочтительны для пациентов с ХБП с учетом их нефропротективного эффекта, а также с учетом влияния на показатели госпитализации по поводу СН и развитие серьезных неблагоприятных сердечно-сосудистых событий [18]. Агонисты рецепторов ГПП-1 предпочтительны при ожирении второй степени и выше (ИМТ ≥ 35 кг/м2), уровне HbA1c ≥ 9% или проведении терапии высокими дозами инсулина, учитывая их влияние на вес, резистентность к инсулину и снижение основных неблагоприятных сердечно-сосудистых событий (MACE). Использование метформина с ингибитором НГЛТ-2 или агонистом рецепторов ГПП-1 целесообразно у пациентов с уровнем HbA1c ≥ 7,5% для достижения целевых показателей гликемии с минимальными побочными эффектами и ввиду большей доступности.
Хроническая болезнь почек. Устранение основных факторов риска сердечно-сосудистых заболеваний остается главной задачей для пациентов с хронической болезнью почек. При артериальной гипертензии, особенно на фоне протеинурии, которая признана независимым фактором риска развития сердечно-сосудистых заболеваний (особенно при СН), препаратами первой линии являются ингибиторы АПФ/БРА. Терапия ингибиторами НГЛТ-2 должна проводиться для всех пациентов с ХБП (с умеренным или повышенным риском по KDIGO) независимо от статуса диабета для нефропротекции, снижения частоты госпитализаций по поводу СН и сердечно-сосудистой смерти [18]. Она может быть безопасно инициирована у пациентов с расчетной скоростью клубочковой фильтрации (рСКФ) ≥ 20 мл/мин/1,73 м2. У лиц с диабетической нефропатией и протеинурией, принимающих ингибиторы АПФ/БРА, можно рассмотреть возможность назначения финренона для уменьшения риска развития неблагоприятных сердечно-сосудистых и почечных событий [19]. Вероятно, финренон можно начинать принимать на фоне терапии ингибиторами НГЛТ-2 у пациентов с рСКФ > 25 мл/мин/1,73 м2 и уровнем калия < 5 ммоль/л, хотя окончательные данные об одновременном применении этих препаратов еще не получены. Для лечения гиперлипидемии ХБП является фактором риска, обусловливающим назначение статинов пациентам с промежуточным риском. Терапию статинами и эзетимибом можно рассматривать как средство снижения риска первичного серьезного атеросклеротического события у лиц с ХБП, особенно у не находящихся на диализе [20, 21].
Третья стадия: субклинические сердечно-сосудистые заболевания и эквиваленты риска кардиоренального метаболического синдрома
Целью лечения третьей стадии кардиоренального метаболического синдрома является усиление профилактических мер у пациентов с субклиническими сердечно-сосудистыми заболеваниями, ХБП очень высокого риска или высоким прогнозируемым риском сердечно-сосудистых заболеваний для предотвращения прогрессирования клинических ССЗ и почечной недостаточности.
Субклинические атеросклеротические заболевания сердца. Наличие субклинического атеросклероза связано с повышенным риском в общей популяции [22] и среди лиц с различными факторами риска возникновения CaReMе-синдрома, включая ХБП [23, 24] и СД [25], что должно обусловливать назначение статинов в высоких дозах. Наличие и высокий уровень коронарного кальция (как абсолютный балл ≥ 100, так и повышенный перцентиль выявления молодых пациентов с атеросклерозом) могут быть показанием для назначения помимо статинов еще аспирина, ингибитора пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9), икозапента этила при гипертриглицеридемии, антигипертензивных препаратов и агонистов рецепторов ГПП-1 в разных подгруппах пациентов с кардиоренальным метаболическим синдромом [26]. В рекомендациях ACC/AHA 2018 г. указывается на необходимость рассмотреть возможность терапии статинами для всех пациентов с диабетом в возрасте от 40 до 75 лет, даже при наличии нулевого показателя коронарного кальция [27].
Субклиническая сердечная недостаточность. В соответствии с действующими рекомендациями по сердечной недостаточности субклиническая СН определяется как наличие аномальной структуры или сердечной функции при визуализации сердца или повышение сердечных биомаркеров (NT-proBNP, высокочувствительного сердечного тропонина или их обоих). Субклиническая СН связана с повышенным абсолютным риском ее прогрессирования до клинической формы [28]. В дополнение к контролю сердечно-сосудистых факторов риска и сопутствующих заболеваний лицам с бессимптомной систолической дисфункцией левого желудочка рекомендуется лечение ингибиторами АПФ/БРА и β-блокаторами для замедления прогрессирования СН. Использование ингибиторов НГЛТ-2 у пациентов с СД 2 типа снижает вероятность госпитализаций по поводу СН и сердечно-сосудистой смерти [29].
Эквиваленты риска кардиоренального метаболического синдрома. Лица с очень высоким риском возникновения ХБП, согласно KDIGO, или высоким прогнозируемым риском развития ССЗ также относятся к популяции с третьей стадией кардиоренального метаболического синдрома. Пороговое значение высокого риска предстоит определить после разработки новых алгоритмов прогнозирования. В связи с высоким абсолютным риском ССЗ в данной подгруппе также должна проводиться усиленная профилактическая терапия в отсутствие противопоказаний. При этом конкретное лечение должно назначаться с учетом профилей риска ССЗ. Кроме того, у пациентов с СД 2 типа, высоким прогнозируемым риском или несколькими неконтролируемыми факторами риска CaReMe-синдрома может быть рассмотрена возможность применения комбинированной терапии ингибиторами НГЛТ-2 и агонистами рецепторов ГПП-1 для большего снижения абсолютного риска развития ССЗ.
Четвертая стадия: сердечно-сосудистые заболевания при кардиоренальном метаболическом синдроме с или без почечной недостаточности
На четвертой стадии кардиоренального метаболического синдрома проводятся оптимизация лечения и вторичная профилактика у пациентов с сердечно-сосудистыми заболеваниями и сопутствующими метаболическими факторами, ХБП или ими обоими. Всем лицам с АССЗ показано применение аспирина или ингибиторов P2Y12 в дополнение к высокоинтенсивной терапии статинами с рассмотрением возможности назначения дополнительных препаратов, снижающих уровень ЛПНП, таких как эзетимиб и ингибитор PCSK9, в зависимости от наличия высокого риска атеросклеротических заболеваний сердца и пороговых значений ЛПНП. Препараты не из группы статинов, снижающие уровень ЛПНП, такие как ингибитор PCSK9, бемпедоевая кислота и инклизиран, могут быть рассмотрены как альтернатива при непереносимости первых. Медикаментозная терапия также показана всем пациентам с СН, при этом акцент делается на четыре основных класса препаратов: β-блокаторы, ингибиторы рецепторов ангиотензина/неприлизина, антагонисты минералокортикоидных рецепторов и ингибиторы НГЛТ-2 для лиц с сердечной недостаточностью с низкой фракцией выброса (СНнФВ).
Ожирение, метаболический синдром и сердечно-сосудистые заболевания. У лиц с четвертой стадией кардиоренального метаболического синдрома необходимо не реже одного раза в год измерять ИМТ и окружность талии. При наличии ожирения и абдоминального ожирения снижение веса является первоочередной задачей. Умеренное снижение массы тела (5–10%) направлено на улучшение контроля метаболических факторов риска у пациентов с сердечно-сосудистыми заболеваниями, а также на улучшение функционального статуса и качества жизни пациентов с СН [30]. Усиленное снижение веса (> 10%) нацелено на потенциальное улучшение сердечно-сосудистых исходов у лиц с сердечно-сосудистыми заболеваниями [31, 32]. Прежде всего следует уделять внимание модификации образа жизни, включающей изменение пищевого поведения, умеренное ограничение потребляемых калорий и регулярную физическую активность. Снижение веса должно поддерживаться многопрофильной командой с использованием дополнительных подходов фармакотерапии (при ИМТ ≥ 27 кг/м2) и метаболической хирургии (при ИМТ ≥ 35 кг/м2) для дальнейшего снижения веса и кардиометаболического риска.
Среди фармакотерапевтических средств приоритетными должны быть инкретины – агонисты рецепторов ГПП-1, ГПП-1/глюкозозависимого инсулинотропного полипептида/глюкагона, поскольку они способствуют снижению массы тела и улучшают контроль метаболических факторов риска. Кроме того, первые данные клинического исследования SELECT свидетельствуют о том, что высокие дозы агонистов рецепторов ГПП-1 снижают частоту сердечно-сосудистых событий у пациентов с ожирением и ССЗ.
Наличие МС и гипертриглицеридемии должно послужить основанием дальнейшего усиления модификации образа жизни. Выраженная гипертриглицеридемия (≥ 500 мг/дл) является показанием для терапии фибратами (фенофибратом в сочетании со статинами). При умеренной гипертриглицеридемии (135–499 мг/дл) следует рассмотреть возможность применения икозапента этила. При АГ целевой уровень АД составляет < 130/80 мм рт. ст. при модификации образа жизни и фармакотерапии. У лиц с хронической болезнью почек или диабетом и резистентной артериальной гипертензией особые фармакологические рекомендации включают применение ингибиторов АПФ/БРА и АМКР. У темнокожих пациентов с СНнФВ при стойкой неконтролируемой артериальной гипертензии после использования четырех основных классов терапии приоритетными должны быть гидралазин/изосорбид.
Сахарный диабет и сердечно-сосудистые заболевания. У пациентов с СД и ССЗ основополагающее значение имеют модификация образа жизни, контроль факторов риска с помощью препаратов по мере необходимости, а также более интенсивные гипохолестериновая и сахароснижающая терапии. Многие пациенты с СД и АССЗ относятся к группе очень высокого риска. Для них при уровне ЛПНП ≥ 70 мг/дл (1,810 ммоль/л) на фоне максимально переносимой терапии статинами может быть рассмотрено назначение терапии эзетимибом, ингибитором PCSK9 или другим препаратом для усиленного снижения показателя [15, 33]. Пациентам с диабетом и АССЗ показан ингибитор НГЛТ-2 или агонист рецепторов ГПП-1 для снижения риска MACE и сердечно-сосудистой смерти. При этом использование ингибитора НГЛТ-2 рекомендовано лицам с ХБП или сопутствующей СН, а агониста рецепторов ГПП-1 – лицам с ИМТ ≥ 35 кг/м2, уровнем HbA1c ≥ 9% или получающим высокие дозы инсулина [17]. Показания к совместному применению обоих классов препаратов пока не определены, но могут быть рассмотрены для лиц с высоким риском развития атеросклеротических ССЗ или с атеросклеротическим заболеванием сердца и комбинацией вышеупомянутых сопутствующих заболеваний. Согласно современным рекомендациям, ингибиторы дипептидилпептидазы 4 (ДПП-4) и тиазолидиндионы противопоказаны при СН и должны быть отменены. Использование метформина в сочетании с другими сахароснижающими препаратами, особенно ингибиторами НГЛТ-2, позволяет достичь целевой гликемии с минимальными побочными эффектами и рекомендуется пациентам с уровнем HbA1c > 7,5% или получающим инсулин, лицам с рСКФ ≥ 30 мл/мин/1,73 м2 и без нестабильной или декомпенсированной СН.
Хроническая болезнь почек и атеросклеротические сердечно-сосудистые заболевания. У пациентов с сопутствующим атеросклеротическим ССЗ и ХБП проводится терапия статинами в средних и высоких дозах [34]. Препараты, которые сохраняют функцию почек и снижают смертность от сердечно-сосудистых заболеваний, такие как ингибиторы НГЛТ-2, должны быть назначены вне зависимости от статуса диабета [35]. При недостижении индивидуальных целевых показателей глюкозы в крови при применении метформина и ингибитора НГЛТ-2 или непереносимости этих препаратов рекомендован прием агониста рецепторов ГПП-1 длительного действия [18]. Можно рассматривать возможность применения финренона для снижения неблагоприятных сердечно-сосудистых и почечных событий у лиц с диабетом и ХБП, которые уже получают максимально переносимые дозы ингибитора ренин-ангиотензиновой системы [19] с или без ингибитора НГЛТ-2.
Хроническая болезнь почек и сердечная недостаточность. Учитывая ограниченные выборки пациентов, включенных в ранее проведенные исследования, основные рекомендации по СН содержат менее подробные данные о терапии, особенно ингибиторами РААС, при сочетании СН с ХБП четвертой и пятой стадий, диализом и трансплантацией.
Ингибиторы НГЛТ-2 показаны всем пациентам с ХБП и СН независимо от фракции выброса (ФВ), статуса диабета и исходного альбумин-креатининового соотношения в моче [36, 37]. Инициация терапии возможна при рСКФ 20 мл/мин/1,73 м2 и может продолжаться до момента проведения заместительной почечной терапии. При СНнФВ ангиотензиновых рецепторов и неприлизина ингибитор (АРНИ) предпочтительнее ингибиторов АПФ/БРА с обсуждением возможности снижения дозы препарата (24/26 мг два раза в день) при рСКФ < 30 мл/мин/1,73 м2. Применение АРНИ также связано с более медленным снижением функции почек и меньшим числом неблагоприятных почечных событий, что обеспечивает дополнительные преимущества в контроле АД при разных показателях СКФ [38–40]. Ингибиторы АПФ/БРА можно продолжать принимать пациентам с рСКФ < 30 мл/мин/1,73 м2 и СНнФВ при частом контроле уровня калия. Титрация дозы может осуществляться в соответствии с рекомендациями KDIGO с тщательным мониторингом уремических симптомов и учетом сроков и необходимости заместительной почечной терапии [34]. Использование таких препаратов, как АРНИ/ингибиторы АПФ/БРА и АМКР, может быть ограничено наличием ХБП из-за опасения ухудшения функции почек и гиперкалиемии [41]. Одновременное применение препаратов, связывающих калий, и ингибиторов НГЛТ-2 или АРНИ может быть ассоциировано с более низкой частотой гиперкалиемии и, следовательно, может быть рассмотрено для оптимизации терапии. Колебания уровня креатинина на фоне использования диуретической терапии в значительной степени обусловлены ожидаемыми и предполагаемыми изменениями гломерулярной гемодинамики, поэтому не должны служить поводом для немедленного ее прекращения [42].
Фибрилляция предсердий. Некоторые факторы риска кардиоренального метаболического синдрома, включая артериальную гипертензию, ожирение, ХБП и дислипидемию [43], связаны с большей вероятностью развития и тяжестью ФП, поэтому рекомендован комплексный контроль факторов риска у таких пациентов [33]. Кроме того, факторы риска кардио-ренального метаболического синдрома при СД и артериальной гипертензии повышают риск инсульта при фибрилляции предсердий, что обусловливает использование антикоагулянтов в целях профилактики. При наличии показаний к антикоагулянтной терапии последние рекомендации поддерживают использование двойных пероральных антикоагулянтов или варфарина у пациентов с кардиоренальным метаболическим синдромом, включая лиц с тяжелым ожирением или ХБП. Однако при прогрессировании заболевания почек требуется коррекция дозы прямых пероральных антикоагулянтов. Для улучшения течения ФП рекомендованы снижение веса, регулярная физическая активность и улучшение кардиореспираторной работоспособности. Лечение синдрома обструктивного апноэ сна, который тесно связан с ожирением, может помочь снизить тяжесть фибрилляции предсердий [43].
Почечная недостаточность. Риск сердечно-сосудистых заболеваний непропорционально повышен у пациентов с почечной недостаточностью, находящихся на поддерживающем диализе, при этом в данной популяции СН и атеросклеротические ССЗ представляют два основных фенотипа [44]. Несмотря на ограниченное количество высококачественных данных, позволяющих определить оптимальные методы лечения СН и атеросклеротических ССЗ при почечной недостаточности, некоторые виды терапии продемонстрировали положительный эффект, особенно в отношении исходов, связанных с СН. Большое внимание следует уделить частым сеансам диализа для снижения гипертрофии левого желудочка/индекса массы левого желудочка и госпитализаций по поводу СН, а также для улучшения качества жизни [45–47]. При использовании таких классов лекарств, как β-адреноблокаторы или ингибиторы АПФ, необходимо учитывать их диализируемость и синхронизацию с циклом диализа [48]. Роль рутинного начала приема статинов у находящихся на диализе без известного атеросклеротического ССЗ ограничена, однако продолжение их приема, начатого до диализа, вполне обоснованно [35]. И наконец, учитывая высокий уровень легочной гипертензии и правожелудочковой недостаточности, характерный для почечной недостаточности и процесса заместительной почечной терапии, рекомендуется ранний мультидисциплинарный подход с привлечением ведущих специалистов по СН [49].
Регресс стадий
В рамках кардиоренального метаболического синдрома возможны как его прогрессирование, так и регресс. Наиболее надежно это достигается путем целенаправленного снижения веса и существенного изменения образа жизни, что ассоциируется с уменьшением объема жировой ткани и улучшением толерантности к глюкозе (первая стадия) [50, 51], ремиссией диабета [50], артериальной гипертензии [52], гиперлипидемии [51] и метаболического синдрома, а также с улучшением функции почек (вторая стадия) [53] и обращением вспять неблагоприятного ремоделирования сердца (третья стадия) [54]. Поэтому рекомендуется уделять особое внимание способам улучшения состояния здоровья лиц, находящихся на более поздних стадиях кардиоренального метаболического синдрома.
Пробелы в исследованиях
Кардиоренальный метаболический синдром является распространенным, смертельно опасным и излечимым. Однако многочисленные пробелы в знаниях обусловливают необходимость проведения целенаправленных исследований в ключевых областях. В отношении развития концепции CaReMe существует неполное представление о половых различиях, генетических основах и применении генетического тестирования, механизмах развития дисфункции сосудов, миокарда и почек, а также о факторах риска на уровне окружающей среды и общества. Механизмы, связывающие факторы риска кардиоренального метаболического синдрома с ССЗ и ХБП как по отдельности, так и в совокупности, также остаются неясными. Стратегии применения комбинированной терапии, а также научно обоснованные подходы к ее началу, мониторингу (например, частота контроля альбумин-креатининового соотношения и цели по его снижению) и поддержанию имеют важное значение и представляют собой области будущих исследований.
Заключение
Кардиоренальное метаболическое здоровье отражает сложную связь между метаболическими факторами риска, ХБП и сердечно-сосудистой системой. «Плохое» кардиоренальное метаболическое здоровье имеет серьезные последствия для неблагоприятных клинических исходов, особенно сердечно-сосудистой заболеваемости и преждевременной смерти. Тем не менее существует все больше методов лечения и стратегий здравоохранения, которые имеют большой потенциал для улучшения результатов лечения пациентов с кардиоренальным метаболическим синдромом. Разработка четкого определения и стадирования синдрома, совершенствование алгоритмов прогнозирования риска, а также разъяснение подходов к профилактике и лечению ССЗ у пациентов с кардиоренальным метаболическим синдромом обеспечат основу для улучшения кардиоренального метаболического здоровья населения и связанных с ним исходов.
* В журнале «Эффективная фармакотерапия» опубликован расширенный реферат статьи Ndumele C.E., Rangaswami J., Chow Sh.L., et al. Cardiovascular-kidney-metabolic health: a presidential advisory from the American Heart Association, подготовленный д.м.н., заведующей лабораторией возрастных метаболических и эндокринных нарушений Российского геронтологического научно-клинического центра ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, заведующей отделением эндокринологии консультативно-диагностического центра, руководителем клиники остеопороза Е.Н. Дудинской. Оригинальная статья размещена в Circulation. 2023; 148 (20): 1606–1635.
E.N. Dudinskaya, MD, PhD
Russian Gerontology Research and Clinical Centre of N.I. Pirogov Russian National Research Medical University
Contact person: Ekaterina N. Dudinskaya, Dudinskaya_en@rgnkc.ru
Until recently, the issues of the connection between the ‘heart – kidney’ axis and the metabolic syndrome were not covered in detail. Cardiorenal, cardiometabolic and metabolic syndromes stood apart from each other. However, the high incidence of morbidity and mortality, in particular from cardiovascular causes, raises many questions, the answers to which have not been fully found.
Сardiorenal metabolic health reflects the interaction of metabolic risk factors, chronic kidney disease and the cardiovascular system and has an absolute impact on morbidity and mortality.
Due to the ‘poor’ cardiorenal metabolic health, especially among people with unfavorable social determinants (living conditions), there is a need to understand the term ‘cardiorenal metabolic syndrome’, to determine its stages, as well as to discuss the possibilities of prevention and treatment at each stage. It is also crucial to pay attention to the social determinants of health in care delivery models and reduce the separation of care by way of simplifying approaches to the interdisciplinary patient-centered model.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.