Комбинированная терапия препаратами йода и левотироксина в лечении эутиреоидного зоба
- Аннотация
- Статья
- Ссылки


Патогенез и патоморфоз эутиреоидного зоба
Современные подходы к лечению и профилактике зоба базируются на представлениях о его патогенезе. В настоящее время общепринято, что основной причиной эутиреоидного зоба является дефицит йода. Так, в эндемичных регионах с дефицитом йода связано около 90–95% случаев увеличения ЩЖ, а у детей – до 99%.
Первое научное обоснование взаимосвязи зоба и дефицита йода было сделано ученым из США Дэвидом Марином (Marine; 1880–1976). В 1917 году Марин провел исследование, в котором продемонстрировал эффективность йодной профилактики среди девочек-подростков, проживающих в штате Огайо, в результате которой распространенность зоба уменьшилась с 20% до 5% [25, 26]. Наряду с этим Марин впервые обнаружил зависимость между объемом ЩЖ и содержанием в ней йода, а также описал гистологические изменения, характерные для эндемическо- го зоба.
Каковы непосредственные механизмы формирования йододефицитного зоба, в то время было не понятно. В дальнейшем, после описания регуляции ЩЖ гипоталамо-гипофизарной систе-мой, а именно отрицательной обратной связи между продукцией ТТГ и Т4, в экспериментах на животных было показано, что искусственно смоделированный абсолютный йодный дефицит приводит к повышению уровня ТТГ (гипотиреозу) и образованию зоба; кроме того, к формированию зоба приводило экзогенное введение ТТГ [5]. Таким образом, была выдвинута теория, согласно которой ТТГ не только стимулирует продукцию тиреоидных гормонов, но и обуславливает увеличение ЩЖ. В дальнейшем выяснилось, что у лиц, проживающих в регионе с умеренным дефицитом йода, уровень ТТГ не превышал или даже оказывался ниже такового у лиц, не испытывающих йодный дефицит [15]. Тогда патогенез зоба при дефиците йода стали объяснять так называемым «повышением чувствительности ЩЖ к эффектам ТТГ в условиях йодного дефицита» или «сенсибилизацией тиреоцитов к ТТГ» [5]. До конца 80‑х годов эта концепция абсолютно доминировала и обуславливала основной и доминирующий подход к лечению зоба – супрессивную терапию, направленную на подавление эндогенной продукции ТТГ препаратами L-Т4. Поскольку до этого времени контролируемые исследования, изучавшие эффективность такой терапии, не проводились, на протяжении многих десятилетий целесообразность монотерапии L-T4 как метода лечения зоба практически не подвергалась сомнению. Но уже первые рандомизированные исследования показали, что использование для лечения йододефицитного зоба препаратов йода было сопоставимо по эффективности с супрессивной терапией L-Т4 (таблица 1). В дальнейшем были продемонстрированы существенные преимущества комбинированной терапии йодом и L-T4. Было отмечено, что препараты йода, как в виде монотерапии, так и в виде комбинации, обуславливали значительно более стойкую нормализацию объема ЩЖ [16].
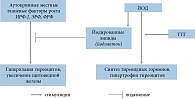
Кроме того, эту концепцию подтвердили результаты экспериментальных исследований in vitro и in vivo, в которых были получены новые данные об ауторегуляции ЩЖ йодом и аутокринными ростовыми факторами (АРФ). По современным представлениям повышение продукции ТТГ или повышение к нему чувствительности тиреоцитов в патогенезе йододефицитного зоба имеет второстепенное значение (рис. 1). Основная роль в этом плане отводится АРФ, в частности, инсулиноподобному ростовому фактору 1‑го типа (ИРФ-I), эпидермальному ростовому фактору (ЭРФ) и фактору роста фибробластов (ФРФ), которые в условиях снижения содержания йода в ЩЖ оказывают мощное стимулирующее воздействие на пролиферацию тиреоцитов. Основным физиологическим блокатором продукции АРФ является йод, связанный с непредельными жирными кислотами (йодлактоны). В экспериментальных работах было показано, что аутокринная продукция тиреоцитами ИРФ-I может быть полностью блокирована йодом [18]. Более того, рост изолированных интактных фолликулов ЩЖ, содержащих достаточное количество йода, не удается простимулировать добавлением ТТГ [13], а при блокаде рецепторов ИРФ-I специфическими антителами, ТТГ не способен оказать трофические эффекты на тиреоциты [24]. Приведенные факты отчетливо указывают на то, что сам ТТГ не является основным и прямым стимулятором пролиферации тиреоцитов, а при йодном дефиците этот эффект опосредован АРФ. Таким образом, подавление продукции ТТГ экзогенно вводимым L-T4 не предотвращает гиперпластические процессы в ЩЖ, хотя достаточно эффективно блокирует гипертрофию тиреоцитов, что и лежит в основе эффективности L-T4 в лечении зоба.
Клиническое значение эутиреоидного зоба
Эутиреоидный зоб классифицируется на основании макроскопических изменений ЩЖ, которые наиболее точно можно охарактеризовать при УЗИ ЩЖ, рассчитав ее объем и оценив размер узловых образований. Выделяют диффузный зоб (объем ЩЖ более 18 мл у женщин и менее 25 мл у мужчин), а также узловой, многоузловой и смешанный зоб. Диагностика эутиреоидного зоба подразумевает использование до-статочно простых методов, доступных для широкой клинической практики. Наиболее просто обстоит дело с диффузным зобом, для диагностики которого достаточно определения уровня ТТГ и УЗИ ЩЖ; определение АТ-ТПО может помочь в дифференциальной диагностике с АИТ. При обнаружении в ЩЖ узловых образований дополнительно проводится пункционная биопсия для исключения опухоли ЩЖ и сцинтиграфия для исключения функциональной автономии, что может существенным образом отразиться на подходах к лечению. Прежде чем обсуждать лечение эутиреоидного зоба, необходимо четко представлять, какое патологическое значение он имеет, то есть какую опасность он несет для пациента. По современным представлениям, патологическое значение эутиреоидного зоба исчерпывается следующим:
- риск (небольшой) значительного увеличения ЩЖ со сдавлением окружающих органов и формированием косметического дефекта;
- риск прогрессирования процесса в соответствии с этапами естественного течения йододефицитного зоба (формирование узлового и многоузлового зоба);
- риск развития функциональной автономии ЩЖ и тиреотоксикоза в отдаленном будущем;
- значительное повышение затрат на диагностику и лечение отдаленных последствий зоба (пункционная биопсия, оперативное вмешательство, терапия радиоактивным йодом), при том, что лечение диффузного эутиреоидного зоба значительно дешевле.
С позиций общей патологии ДЭЗ можно расценить как компенсаторную гипертрофию и гиперплазию ЩЖ, направленную на обеспечение организма тиреоидными гормонами в условиях дефицита йода. Это обеспечение в условиях йодного дефицита происходит ценой хронической гиперстимуляции ЩЖ. Последняя запускает цепь последовательных гиперпластических процессов и соматических мутаций в тиреоцитах, итогом которых является формирование функциональной автономии ЩЖ. Отдельные клетки ЩЖ оказываются более чувствительными к стимуляции АРФ, в результате чего получают преимущественный рост. Так формируется узловой и многоузловой эутиреоидный зоб. Далее, в отдельных активно делящихся тиреоцитах, начинают запаздывать репаративные процессы, в результате чего накапливаются мутации, среди которых наибольшее значение имеют так называемые активирующие. Дочерние клетки, несущие активирующие мутации, приобретают способность автономно, то есть вне регулирующих эффектов ТТГ, продуцировать тиреоидные гормоны. Среди активирующих мутаций тиреоцитов в настоящее время наиболее известна мутация рецептора ТТГ, приводящая к его стойкой активации даже в отсутствии лиганда, а также мутация a-субъединицы Gs-белка каскада ТТГ-цАМФ, которая также стабилизирует его в активном состоянии. Конечным этапом естественного морфогенеза йододефицитного зоба является узловой и многоузловой токсический зоб. Этот процесс занимает многие десятилетия; отсюда следствие: узловой и многоузловой токсический зоб наиболее часто встречается у лиц пожилого возраста. В связи с этим одной из наиболее серьезных проблем легкого и умеренного йодного дефицита является высокая заболеваемость многоузловым и узловым токсическим зобом в старшей возрастной группе [23].
Консервативное лечение эутиреоидного зоба
На сегодняшний день разработано три варианта консервативной терапии эутиреоидного зоба: монотерапия препаратами йода, супрессивная терапия L-T4 и комбинированная терапия йодом и L-T4. Как уже можно было заключить из сказанного, супрессивная монотерапия L-Т4, по современным патогенетическим представлениям, не является лечением выбора при диффузном эутиреоидном зобе. Другими словами, препараты йода всегда должны быть частью комплексной терапии эндемического эутиреоидного зоба. Основные преимущества и недостатки трех обсуждаемых методов лечения представлены в таблице 2.
На первом этапе лечения детям и подросткам, как правило, целесообразно назначение монотерапии йодидом калия в дозе 100–200 мкг в день. В контролируемых клинических исследованиях (таблица 1) было показано, что на фоне терапии йодом за первые 6 месяцев объем ЩЖ может уменьшиться примерно на 30%. Основными преимуществами монотерапии препаратами йода являются ее этиотропный характер (направлена на причину зоба), безопасность, отсутствие необходимости в подборе дозы и в проведении частых гормональных исследований. К относительным недостаткам монотерапии йодом можно отнести то, что эффект развивается медленнее, чем при назначении терапии, в которую входит L-T4. Кроме того, эффективность монотерапии йодом обратно пропорциональна возрасту, то есть у взрослых она менее эффективна, чем у детей. Кроме того, как будет сказано ниже, монотерапия йодом недостаточно эффективна для профилактики послеоперационного рецидива зоба.
Основным преимуществом монотерапии L-T4 является ее эффективность и быстрота редукции объема ЩЖ за счет подавления гипертрофии тиреоцитов, в то время как основным недостатком – высокая вероятность рецидива зоба после отмены препарата. Это связано с тем, что на фоне назначения одного только L-T4 происходит уменьшение интратиреоидного содержания йода. В связи с этим отмена препарата сопровождается достаточно быстрым увеличением объема ЩЖ до исходного. Так, в часто цитируемом исследовании D. Einenkel (1992) [7] у подростков 13–15 лет изучались все три варианта лечения диффузного эутиреоидного зоба. Уменьшение объема ЩЖ спустя 6 месяцев произошло во всех трех группах: на фоне приема 100 мкг L-T4 – с 14,1 ± 4,2 мл до 8,3 ± 2,6 мл, на фоне приема 150 мкг йода – с 18,5 ± 6,2 мл до 8,8 ± 2,7 мл, а на фоне комбинации 100 мкг йода и 50 мкг L-T4 – c 17,2 ± 3,1 мл до 8,3 ± 2,0 мл. Спустя три месяца после прекращения лечения увеличение объема ЩЖ (до 11,3 ± 2,5 мл) произошло только в группе монотерапии L-T4. Кроме того, на фоне терапии йодом и комбинации йода и L-T4 произошло снижение показателей серой шкалы по данным УЗИ, что соответствует уменьшению размера фолликулов и содержания в них коллоида. К таким же результатам приходит схожее по дизайну рандомизированное исследование G. Hintze (1989) [16], в которое вошли 166 пациентов с зобом.
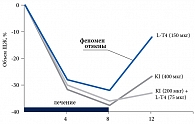
Феномен «отмены» демонстрирует и более позднее исследование группы G. Hintze (1992) [17], которое также изучает три основных метода лечения зоба (рис. 2). Как это показано на рисунке, после отмены монотерапии L-T4 объем ЩЖ быстро возвращается к исходному, чего не происходит на фоне терапии, которая подразумевала назначение йода – в виде монотерапии или в комбинации с L-T4.
Другим недостатком терапии L-T4 является возможность развития медикаментозного тиреотоксикоза при передозировке. В связи с этим она требует контрольных определений уровня ТТГ, то есть дозу L-T4 необходимо подбирать индивидуально. Целью терапии, в которую входит L-T4, является поддержание низконормального уровня ТТГ (0,3–0,7 мЕд/л), что у взрослых, как правило, требует назначения около 50–100 мкг L-Т4.
Комбинированная терапия препаратами йода и левотироксина
Хорошо себя зарекомендовавшей в клинических исследованиях альтернативой монотерапии L-Т4 и монотерапии препаратами йода является их комбинированное назначение. Когда речь идет о комбинации L-T4 с каким-либо препаратом или веществом, всегда, в первую очередь, возникает вопрос, не меняет ли это вещество биодоступность L-T4. В отношении йода на этот вопрос можно ответить отрицательно: йодид калия, который входит в фиксированные комбинации с L-T4, не изменяет биодоступность L-T4, как это было показано в исследовании G. Foerster (1998) и ряде других работ [11].
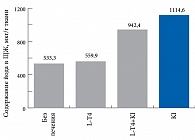
Вопреки представлениям о том, что назначение L-Т4 с подавлением продукции ТТГ приводит к снижению захвата йода ЩЖ, то есть один компонент терапии как бы мешает другому, на практике эти компоненты оказывают синергичное действие на конечный результат – редукцию зоба. Концепция конкуренции йода и L-Т4 на уровне тиреоцита не получила подтверждения и в экспериментальных работах, изучавших интратиреоидное содержание йода на фоне различных вариантов терапии (рис. 3). Так, по данным H. D. Röher (1986) [28], интратиреоидное содержание йода на фоне комбинированной терапии существенно не отличается от такового на фоне монотерапии препаратами йода. По данным B. Saller (1991), комбинированная терапия 100 мкг йода и 100 мкг L-T4 не приводит к изменению интратиреоидного содержания йода по данным флюоресцентной сцинтиграфии. При этом следует заметить, что назначение в контрольной группе 500 мкг йода в день привело к увеличению содержания йода в ЩЖ, но перевод в дальнейшем этих пациентов на указанную комбинированную терапию привел к большей редукции объема ЩЖ, чем на фоне монотерапии такой большой дозой йода [30]. Тем не менее избыточное подавление продукции ТТГ большими дозами L-T4, вероятно, не оправдано, тем более что, по данным M. Grussendorf (1996) [14], корреляция между уровнем супрессии ТТГ и степенью редукции зоба практически отсутствует. В этом исследовании при сравнении монотерапии L-T4 (n = 45), с комбинацией L-T4 и 150 мкг йодида калия (n = 49) выяснилось, что на фоне лечения в обеих группах произошло сопоставимое уменьшение объема ЩЖ (16,8% и 18,5% соответственно), тем не менее, на фоне комбинированной терапии существенно чаще, чем при монотерапии L-T4, происходило снижение уровня ТТГ. Кроме того, на фоне монотерапии L-T4 происходило постепенное повышение уровня ТТГ по мере лечения. Это свидетельствует, во‑первых, о постепенном снижении эффективности монотерапии L-T4 по мере увеличения длительности лечения, а во‑вторых, о том, что добавление к терапии йода снижает потребность в L-T4. В качестве комбинированной терапии в этом исследовании назначалась фиксированная комбинация в одной таблетке 75–150 мкг L-T4 и 150 мкг йода.
О синергичности эффектов йода и L-T4 при назначении их в комбинации свидетельствуют результаты исследования P. Pfannenstiel (1988), в котором было показано, что на фоне комбинированной терапии происходит значимо больший регресс объема ЩЖ (-30,3%), чем на фоне монотерапии L-T4 (-25,2%), при этом указанные различия появлялись уже через 3 месяца от начала лечения и сохранялись через 6 и 9 месяцев [27].
Таким образом, комбинированная терапия препаратами йода и L-T4 обладает при лечении зоба наибольшей эффективностью. Судя по всему, это связано с тем, что на ее фоне происходит воздействие сразу на два ключевых патогенетических механизма формирования зоба: йод оказывает антипролиферативный эффект, который опосредован снижением продукции тканевых факторов роста и подавлением гиперплазии тиреоцитов, в то время как L-T4 подавляет продукцию ТТГ, предотвращая его гипертрофические эффекты на тиреоциты.
Важно заметить, что эффект комбинированной терапии проявляется независимо от супрессии ТТГ, то есть на ее фоне нет необходимости добиваться поддержания у пациента потенциально небезопасного субклинического тиреотоксикоза. В рандомизированном исследовании M. Kreissl (2001) [23] проводилось сравнение двух вариантов комбинированной терапии. 44 пациента (по 22 в каждой группе) с диффузным эути-
реоидным зобом получали фиксированную комбинацию 100 мкг L-T4 и 100 мкг йодида калия или 75 мкг L-T4 и 150 мкг йодида калия. Контрольные исследования, включая оценку интратиреоидного содаржания йода, проводились через 3 и через 6 месяцев от начала терапии. В итоге были продемонстрированы одинаковая эффективность двух вариантов лечения в плане редукции зоба (рис. 4) и отсутствие различий между ними по интратиреоидному содержанию йода. Единственное отличие состояло в большей частоте подавления ТТГ на фоне комбинации 100 мкг L-T4 и 100 мкг йода. Автор делает вывод о том, что комбинация с меньшим содержанием L-T4 более предпочтительна, поскольку столь же эффективна, но более безопасна для пациентов, так как реже сопровождается медикаментозным тиреотоксикозом. Такие же выводы позволило сделать схожее по дизайну более позднее исследование L. A. Hotze (2002) [19], сравнивавшее две фиксированные комбинации йода и L-T4 (100 + 100 и 150 + 75 мкг соответственно): отличий по степени редукции зоба между двумя препаратами выявлено не было.
Аналогичные данные были получены в рандомизированном исследовании B. Klemenz (1998) [20]. В нем 105 пациентам с эутиреоидным зобом назначалась либо комбинация 150 мкг йода с индивидуально адаптированной дозой L-T4, или фиксированная комбинация 100 мкг йода и 100 мкг L-T4. В обеих группах объем ЩЖ спустя 12 недель лечения снизился примерно на 24%. Суммируя результаты исследования, авторы делают вывод, что подбор дозы L-T4 в рамках комбинированной терапии исходя из расчета около 1,4 мкг на 1 кг веса часто приводит к передозировке, нередко с полным подавлением уровня ТТГ. В связи с этим было рекомендовано исходить из расчета 1,0 мкг на 1 кг веса, то есть назначать относительно меньшие дозы L-T4. Схожее исследование той же группы авторов (Foerster G., et al., 1998) опять же не выявило существенных различий фиксированной комбинации 100 мкг L-T4 и 100 мкг йода по сравнению с йодом (150 мкг) и различными дозами L-T4 (75, 100 и 150 мкг), которые назначались в виде двух отдельных препаратов [10]. На мой взгляд, в ситуации, когда есть возможность выбора нескольких лекарственных форм, которые в одной таблетке комбинируют йод с разными дозами L-T4, этот вопрос не является принципиальным. Более того, логично предположить, что, когда речь идет об отдельных пациентах (а не о больших группах в рамках исследования), возможность индивидуального выбора гормонального компонента комбинированной терапии зоба в зависимости от веса пациента и, отчасти, от исходного уровня ТТГ позволяет значительно снизить риск передозировки.
Таким образом, комбинированная терапия препаратами йода и L-T4 на сегодняшний день является наиболее эффективным и относительно безопасным методом лечения эутиреоидного зоба. Это связано с тем, что она направлена сразу на два патогенетических механизма его формирования, не сопровождается феноменом отмены (рецидивом зоба) и ее эффективное ведение не требует назначения больших доз L-T4, приводящих к подавлению уровня ТТГ ниже нормы, что несет риск осложнений медикаментозного тиреотоксикоза.
Существуют два варианта назначения комбинации йода и L-T4. Первый вариант подразумевает исходное назначение монотерапии препаратами йода, а при отсутствии эффекта – добавление к йоду L-T4. Такая схема больше всего подходит для лечения зоба у детей, поскольку именно у них можно ожидать достаточной эффективности монотерапии йодом.
Второй вариант подразумевает назначение комбинации йода и L-T4 уже на первом этапе лечения. Это наиболее рациональный подход для лечения диффузного эутиреоидного зоба у взрослых пациентов [32], в связи c тем, что монотерапия йодом в этом случае значительно менее эффективна. Подбор дозы осуществляется по гормональному компоненту, то есть по L-T4. Его доза должна быть такой, чтобы уровень ТТГ поддерживался в низконормальном диапазоне (0,3–0,7 мЕд/л), но не был подавлен. Доза йода обычно выбирается исходя из суточной потребности в этом микроэлементе (100–200 мкг в день).
Комбинированная терапия может назначаться в виде двух разных препаратов, но наиболее просто и удобно для пациента ее назначение в виде одной таблетки с необходимой фиксированной комбинацией йода и L-T4. На фармацевтическом рынке многих европейских стран представлено достаточно много препаратов, содержащих сочетание различных доз L-Т4 с йодом, что позволяет индивидуализировать комбинированную терапию и, таким образом, сделать ее максимально безопасной. На отечественном фармацевтическом рынке недавно появился новый комбинированный препарат «ЙОДОКОМБ». Он представлен двумя вариантами сочетания йода и L-T4 – «Йодокомб-50», содержащий 50 мкг L-T4 и 150 мкг йода, и «Йодокомб-75», содержащий 75 мкг L-T4 и 150 мкг йода. Удобство использования двух дозировок «Йодокомба» заключается в возможности индивидуальной титрации дозы L-Т4 (по уровню ТТГ) в составе комбинированного препарата от 50 до 150 мкг в день, что предопределяет эффективность и безопасность лечения.
Послеоперационная профилактика узлового зоба
Общая тенденция хирургии ЩЖ в последние десятилетия заключается в том, что если хирургическая операция на ЩЖ по поводу эутиреоидного зоба вообще предпринимается, то удаляется большая часть органа, после чего пациент получает заместительную терапию L-T4. То есть, с одной стороны, речь идет о значительных ограничениях в показаниях к оперативному лечению, а с другой – к тому, что в тех ситуациях, когда операция действительно показана, чаще всего наиболее рациональным оказывается проведение тиреоидэктомии. Наряду с этим отсутствие в нашей стране единых подходов к оперативному лечению заболеваний ЩЖ приводит к тому, что эндокринологи сталкиваются с пациентами, в отношении которых в одинаковых клинических ситуациях предпринимаются совершенно разные по объему операции. Чаще всего приходится сталкиваться с пациентами, которым была предпринята частичная резекция ЩЖ с оставлением того или иного объема тиреоидной ткани (тиреоидный остаток). Субтотальная или частичная резекция ЩЖ являются самыми частыми объемами хирургических вмешательств на ЩЖ в нашей стране.
Разбирая принципы профилактики послеоперационного рецидива узлового зоба после частичных резекций ЩЖ, прежде всего следует отметить, что такая профилактика необходима. На это указывает тот факт, что риск послеоперационного рецидива узлового зоба после частичных резекций ЩЖ достаточно высок и варьирует от 20 до 80% [12, 21]. Поскольку рецидив узлового зоба в тиреоидном остатке обусловлен активной пролиферацией тиреоцитов, то, исходя из сказанного выше о патогенезе йододефицитного зоба, можно предположить, что эффективным в плане предотвращения его рецидива может быть назначение препаратов йода. И действительно, в рандомизированном исследовании С. Carella (2002) [6], в которое вошли 139 пациентов после резекции ЩЖ, было показано, что в том случае, когда терапия L-T4 дополнялась йодом, спустя 12 месяцев у пациентов определялся меньший объем тиреоидного остатка, чем у получавших монотерапию L-T4. Суммируя полученные данные, авторы делают выводы о том, что добавление к терапии йода улучшает результаты послеоперационной терапии L-T4, причем у пациентов как с большим, так и с малым объемом тиреоидного остатка. На фоне монотерапии L-T4 удовлетворительных результатов в этой работе удалось достичь только у пациентов с подавленным уровнем ТТГ, тогда как эффективность комбинированной терапии и в этой ситуации зависела от уровня ТТГ. Это опять же указывает на то, что комбинированная терапия не требует поддержания у пациента подавленного ТТГ, без потери своей эффективности.
В рандомизированном исследовании J. Feldkamp (1997) [9], в котором 107 пациентов наблюдались после резекции ЩЖ на протяжении 52 недель, было показано, что рецидивы могли возникать как на фоне монотерапии L-T4, так и на фоне комбинированной терапии L-T4 с йодом, но в последнем случае происходило существенно большее снижение уровня тиреоглобулина, который в данном случае можно рассматривать как маркер гиперстимуляции тиреоцитов, а его высокий уровень – как предиктор рецидива зоба.
Как уже неоднократно указыва-лось, гиперпластические процес-сы в ЩЖ, наиболее вероятно, развиваются по независимым от ТТГ механизмам. И действительно, по данным M. Rotondi (2000) [29], вероятность рецидива узлового зоба после резекции ЩЖ мало зависела от поддерживавшегося уровня ТТГ на фоне различных (супрессивных, заместительных) доз L-T4. По данным этого исследования, вероятность рецидива преимущественно зависела от объема тиреоидного остатка. Таким образом, монотерапия L-T4 в различных доза (даже супрессивных) не снижает вероятность рецидива узлового зоба, независимо от достигаемого на ее фоне уровня ТТГ.
Преимущества комбинированной терапии в плане профилактики послеоперационного рецидива зоба были продемонстрированы и в проспективном исследовании P. M. Schumm-Draeger (2003) [31], в котором пациенты получали комбинацию 150 мкг йода и 75 мкг L-T4. Полученные данные позволили сделать авторам следующие выводы:
у пациентов с большим тиреоидным остатком, который обеспечивал эутиреоидное состояние, на фоне комбинированной терапии происходило более выраженное уменьшение объема остаточной ткани ЩЖ, чем на фоне монотерапии йодом (200 мкг);
у пациентов с послеоперационным гипотиреозом на фоне комбинированной терапии также происходил более выраженный регресс объема остаточной тиреоидной ткани, чем на фоне монотерапии L-T4.
Последний момент требует более детального обсуждения. Действительно, после резекции ЩЖ, несмотря на сохранение тиреоидного остатка того или иного объема, у многих пациентов развивается послеоперационный гипотиреоз. В ситуации, когда была предпринята тиреоидэктомия, гипотиреоз развивается в 100% случаев, и при этом у пациента отсутствует тиреоидный остаток и все наблюдение подразумевает оценку уровня ТТГ на фоне заместительной терапии L-T4. В случае резекции ЩЖ, помимо необходимости компенсации гипотиреоза L-T4, у пациента нужно периодически контролировать состояние оставшейся части ЩЖ при помощи УЗИ, поскольку развитие послеоперационного гипотиреоза не исключает возможность рецидива узлового зоба в тиреоидном остатке. В такой ситуации опять же наиболее рационально назначение комбинированной терапии L-T4 и йодом. В этой ситуации L-T4 будет компенсировать послеоперационный гипотиреоз, а йод будет способствовать профилактике рецидива зоба. Как и в случае лечения зоба, в этой ситуации на фоне комбинированной терапии уровень ТТГ рекомендуется поддерживать в низконормальном диапазоне.
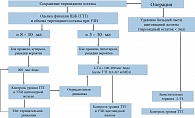
Таким образом, на сегодняшний день алгоритм лечения и профилактики послеоперационного рецидива узлового зоба во многом исходит из объема оставшейся тиреоидной ткани, который оценивается при помощи УЗИ [8]. В нашей модификации он представлен на рис. 5. Наиболее прост этот алгоритм в ситуации, когда пациенту предпринята тиреоидэктомия (предельно субтотальная резекция), которая приводит к развитию гипотиреоза, при этом рецидив узлового зоба невозможен. В этом случае пациенту назначается L-T4 под контролем уровня ТТГ, а в других методах исследования необходимости нет.
Если объем тиреоидного остатка достаточно велик, чтобы поддерживать эутиреоидное состояние (обычно около 10 мл), пациенту может быть назначена монотерапия препаратами йода в дозе около 200 мкг в день. Хотя, в соответствии с процитированной выше работой, комбинированная терапия L-T4 и йодом имеет определенные преимущества и в этой ситуации. В том случае, если на фоне монотерапии йодом, по мере наблюдения, со временем выявляется повышение уровня ТТГ (развивается субклинический гипотиреоз) или при УЗИ выявляется прогрессирующее увеличение размера ЩЖ (рецидив зоба), лечение дополняется L-T4 с целью поддержания уровня ТТГ в интервале 0,3–0,7 мМЕ/л.
В том случае, если у пациента после операции развивается гипотиреоз (даже субклинический с небольшим повышением уровня ТТГ) и при этом ЩЖ удалена не полностью (тиреоидный остаток около 3–10 мл), ему рекомендуется назначение комбинированной терапии препаратами йода и L-T4. В данном случае L-Т4 назначается для заместительной терапии L-T4, а йод, подавляя пролиферативные процессы в тиреоидном остатке, обеспечивает профилактику рецидива узлового зоба. Комбинированная терапия подразумевает назначение либо отдельно двух препаратов, либо, что значительно более удобно для пациента, фиксированных комбинаций йода и L-T4 в одной таблетке.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.