Лефлуномид – модификатор течения и исходов ревматоидного артрита
- Аннотация
- Статья
- Ссылки
- English
Ревматоидный артрит (РА) относится к самым частым аутоиммунным заболеваниям. Он является основной нозологической формой воспалительных заболеваний суставов. Этиология РА до сих пор не установлена. Для заболевания характерны прогрессирующая деструкция синовиальных суставов и дегенерация хрящей и костей, повреждение связок и сухожилий, системное воспалительное поражение внутренних органов. У больных РА снижаются функциональные возможности и качество жизни. Кроме того, заболевание становится причиной преждевременной смерти [1, 2].
Распространенность РА в разных регионах мира различна – от 0,5 до 2%. В два-три раза чаще им страдают женщины. Пик развития приходится на возрастную категорию от 35 до 55 лет.
По данным эпидемиологического исследования, в России 0,6% больных РА [3].
Патогенез РА мультифакториальный, клинические проявления разнообразны. Необходимо отметить, что РА является идеальной моделью для изучения эволюции и исходов аутоиммунных заболеваний человека, а также для апробации основных групп лекарственных препаратов – от нестероидных противовоспалительных препаратов (НПВП) и глюкокортикостероидов (ГКС) до иммуносупрессоров цитотоксического действия и генно-инженерных биологических препаратов (ГИБП).
Согласно Федеральным клиническим рекомендациям за 2013 г. основная цель фармакотерапии РА – достижение ремиссии (или низкой активности) заболевания (степень рекомендаций A), а также снижение риска коморбидных заболеваний (степень рекомендаций С).
Основное место в лечении РА занимает медикаментозная терапия, включая НПВП, простые анальгетики, ГКС, синтетические базисные противовоспалительные препараты (БПВП) и средства таргетной терапии, в частности ГИБП (степень рекомендаций А).
Теоретическим обоснованием применения при РА болезнь-модифицирующих или базисных противовоспалительных препаратов являются результаты многочисленных исследований, свидетельствующие об иммунном воспалении как основе тканевых изменений. При РА отмечается синтез различных аутоантител, прежде всего ревматоидных факторов и антител к циклическому цитруллинированному пептиду. Необходимость применения БПВП обусловлена и хроническим прогрессирующим течением РА.
К БПВП, которые применяют при РА, относятся цитостатические иммуносупрессоры (метотрексат, циклоспорин А и др.), лефлуномид, сульфасалазин, производные хинолина, препараты золота, микофенолата мофетил, моноклональные антитела к цитокинам и их рецепторам, а также тофацитиниб и апремиласт. Такой широкий спектр препаратов, обладающих патогенетическим действием, обусловлен необходимостью активного воздействия на различные звенья патогенеза.
Терапия заболевания должна проводиться всем пациентам и назначаться как можно раньше – в течение трех – шести месяцев с момента появления симптомов [4] (степень доказательности А).
Так, результаты многочисленных контролируемых исследований показали, что эффективность БПВП тем выше, чем раньше начато лечение.
Кроме того, терапия РА должна быть многолетней и непрерывной. Ее целесообразно продолжать даже при снижении активности заболевания и достижении ремиссии.
Выполнение этих рекомендаций по базовой противовоспалительной терапии позволяет снизить общую стоимость медицинского обслуживания пациентов с РА.
Среди БПВП достойное место занимает оригинальный лефлуномид (препарат Арава), специально созданный для лечения РА. Это единственный БПВП, внедренный в ревматологическую практику за последние 25 лет. Терапевтическое воздействие лефлуномида связано с его активным метаболитом А77 1726 – терифлуномидом. Метаболит ингибирует митохондриальный фермент дегидрооротат дегидрогеназу, который играет важную роль в биосинтезе пиримидина de novo. Пиримидин необходим для синтеза РНК и ДНК в пролиферирующих клетках. При его дефиците происходит угнетение клеточного цикла.
Главной мишенью терифлуномида являются активированные Т-лимфоциты, однако он воздействует и на метаболизм макрофагов и моноцитов. Лефлуномид блокирует стимулирующее воздействие провоспалительных цитокинов, включая фактор некроза опухоли α (ФНО-α), интерлейкины 1 и 10, интерферон γ, на пролиферацию клона Т-лимфоцитов в завершающей фазе клеточного цикла. В связи с этим препарат можно рассматривать в качестве иммуномодулирующего агента, не обладающего цитотоксическим эффектом.
Среди биологических эффектов лефлуномида при РА выделяют [5]:
-
ингибицию пролиферации активированных Т-лимфоцитов;
-
блокаду стимулирующего воздействия цитокинов на пролиферацию Т-лимфоцитов;
-
ингибицию синтеза пиримидина;
-
подавление активности дегидрооротат дегидрогеназы;
-
воздействие на экспрессию HLA-DR-позитивных Т-лимфоцитов;
-
модуляцию экспрессии провоспалительных цитокинов Т-клетками и нейтрофилами;
-
торможение хемотаксиса нейтрофилов;
-
супрессию синтеза иммуноглобулина В-лимфоцитами;
-
блокаду экспрессии молекул клеточной адгезии;
-
ингибицию активации ядерного фактора каппа-би;
-
снижение синтеза матриксных металлопротеиназ;
-
снижение экспрессии кислородных радикалов;
-
торможение синтеза р53 – регулятора негативного клеточного цикла.
Фармакокинетика лефлуномида имеет ряд особенностей. Она линейна, учитывая насыщающую и поддерживающую дозы. Суточная потребность в препарате не зависит от приема пищи, возраста и пола пациента. При одновременном применении лефлуномида и НПВП нежелательные явления препаратов не увеличиваются. При комбинации лефлуномида и метотрексата их фармакокинетика не изменяется, как и при комбинации с преднизолоном или циклоспорином.
Помимо РА лефлуномид применяется при псориатическом артрите, анкилозирующем спондилите, воспалительных заболеваниях кишечника, болезни Шегрена, гранулематозе Вегенера, рассеянном склерозе, злокачественной миастении, нефропатии [6–8]. При псориатическом артрите эффективность лефлуномида была подтверждена PsARC (Psoriatic Arthritis Response Criteria) [8]. Так, к концу шестого месяца терапии PsARC в основной группе составил 58,9%, в контрольной – 29,7%. По окончании лечения число болезненных суставов в основной группе оказалось в три раза меньше, чем в контрольной, припухших – в 1,6 раза меньше.
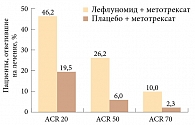
Лефлуномид статистически достоверно превосходил плацебо по числу больных, достигших ответа на терапию по критериям ACR 20 (American College of Rheumatology). В основной группе таких больных было в 1,5 раза больше, чем в контрольной.
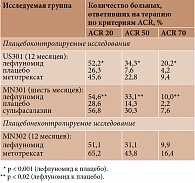
Эффективность лефлуномида в лечении РА продемонстрирована в трех исследованиях [9, 10]. В плацебоконтролируемое исследование US301 были включены 482 пациента с активным РА длительностью не менее шести месяцев. Участники получали лефлуномид 20 мг/день (n = 182), или метотрексат с возрастающей дозой от 7,5 до 15 мг/нед (n = 182), или плацебо (n = 118). Длительность терапии составила 52 недели. В исследовании MN301 (длительность – шесть месяцев) участвовали 358 пациентов с активным РА, получавшие или лефлуномид 20 мг/день (n = 133), или сульфасалазин 2,0 г/день (n = 133), или плацебо (n = 92). Плацебонеконтролируемое исследование MN303 – продленная фаза исследования MN301. Цель – сравнить эффективность лефлуномида и сульфасалазина. Количество участников – 999. В него вошли больные активным РА, получавшие лефлуномид в дозе 20 мг/день (n = 501) либо метотрексат (с увеличением дозы от 7,5 до 15 мг/нед) (n = 498). Продолжительность лечения – 52 недели. Результаты исследований приведены в таблице.
Количество больных с улучшением РА по критериям ACR 20 на фоне терапии статистически достоверно было выше в группе лефлуномида, чем в группе плацебо: 52,2 против 26,3% и 54,6 против 28,6% в исследованиях US301 и MN301 соответственно. По указанному показателю эффективность терапии была стабильной и составляла через шесть месяцев 41% случаев, через 12 месяцев – 49%. Более высокий ответ на терапию лефлуномидом зарегистрирован и по критериям АCR 50 и 70. Так, в исследовании US301 у больных, принимавших лефлуномид, ответ на терапию по ACR 50 зафиксирован в 34,3% случаев, по АСR 70 – 20,2% (против 7,6 и 4,2% случаев среди получавших плацебо).
Интересно, что статистически значимый эффект лефлуномида по критерию ACR 20 у участников исследования US301 отмечался уже через месяц терапии (38% случаев в группе лефлуномида и 20% случаев в группе плацебо). На третьем – шестом месяце он достигал максимума (50–55 и 26–30% соответственно) и практически не изменялся в течение следующих шести месяцев.
Был сделан вывод: достоверных различий в эффективности лечения как между лефлуномидом и метотрексатом, так и между лефлуномидом и сульфасалазином не выявлено. Необходимо отметить, что таковая не оценивалась в зависимости от длительности РА.
Н.В. Чичасова и Е.Л. Насонов ретроспективно, по данным контролируемых исследований, выделили группу больных РА. Длительность заболевания – до двух лет. Оказалось, что через шесть месяцев ответ на терапию по критериям АСR наблюдался у 45,5% больных, получавших лефлуномид, и у 38,8% больных, получавших сульфасалазин [4].
В другом исследовании через 12 месяцев от начала лечения ответ по критериям АСR 50 был зарегистрирован у 34,8% пациентов в группе лефлуномида и у 23,3% – в группе метотрексата. Был зафиксирован очень высокий процент ответа на лечение лефлуномидом – 94 [11].
В открытом исследовании, проведенном в Научно-исследовательском институте ревматологии, показано, что терапия лефлуномидом в качестве препарата первой линии у больных ранним РА (длительность менее шести месяцев) способствовала быстрому развитию клинического эффекта и достижению клинической ремиссии более чем у 40% больных. Последняя сохранялась у большинства пациентов при продолжении лечения [12].
В рандомизированном многоцентровом исследовании (999 больных активным РА) после года терапии ответ на терапию по критериям АСR 20 достоверно чаще регистрировался у больных, получавших метотрексат. Однако через два года различия по данному показателю между группой метотрексата и группой лефлуномида отсутствовали. При лечении лефлуномидом достоверное улучшение по указанным критериям было достигнуто быстрее и наблюдалось в среднем через 74 дня от начала терапии, а при лечении метотрексатом – только через 101 день.
По итогам двухлетнего наблюдения изменение основных клинических показателей воспалительной активности на фоне лечения метотрексатом и лефлуномидом существенно не различалась.
Динамика рентгенологических проявлений в обеих группах была аналогичной.
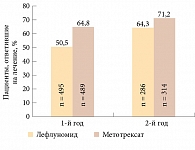
В то же время при оценке двухлетней терапии активного РА лефлуномидом, плацебо и метотрексатом установлено, что доля больных, ответивших на терапию по критериям АСR 20, при лечении лефлуномидом составила 79%, метотрексатом – 67% [13].
В другом исследовании по оценке эффективности двух основных БПВП, применяющихся при РА, показано, что метотрексат эффективнее лефлуномида (рис. 1) [10]. При сравнительной оценке терапии лефлуномидом и сульфасалазином установлено, что лефлуномид значительно превосходит сульфасалазин по таким параметрам, как функциональный индекс оценки здоровья HAQ (Health Assessment Questionnaire), общая оценка врачом и пациентом и число ответивших на терапию по критериям АCR.
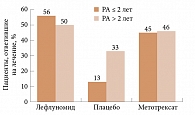
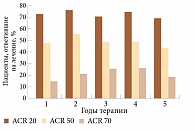
Таким образом, лефлуномид снижает воспалительную активность как при раннем, так и позднем РА (рис. 2). Его эффект устойчив в течение длительного времени – минимум пять лет [14]. При этом не надо увеличивать суточную дозу препарата. Эффективность лефлуномида, как правило, не связана с исходной активностью заболевания, наличием ревматоидного фактора, стадией заболевания. Различия по критериям АСR 20 и 50 на первом и пятом годах терапии практически не наблюдаются. Однако больных, ответивших на терапию по критериям АСR 70 к концу пятого года, оказалось больше, чем в конце первого года лечения (рис. 3).
Таким образом, согласно результатам рандомизированных контролируемых исследований лефлуномид следует рассматривать как высокоэффективный препарат. В результате его применения положительная динамика отмечается более чем у 90% больных РА и гораздо раньше, чем при лечении метотрексатом или сульфасалазином [7]. Так, к концу первого месяца терапии такой ответ наблюдается у каждого третьего пациента, четвертого месяца – у двух третей пациентов. При этом к концу первого года приема лефлуномида клиническая ремиссия фиксируется у каждого третьего больного.
Эффективность лечения РА лефлуномидом в целом сопоставима с эффективностью лечения сульфасалазином и метотрексатом. Лефлуномид превосходит другие БПВП (метотрексат, сульфасалазин, плаквенил) в отношении влияния на качество жизни. Препарат может применяться в комбинации с метотрексатом и ГИБП.
Влияет ли лефлуномид на рентгенологическое прогрессирование РА?
По сравнению с плацебо лефлуномид существенно замедляет рентгенологическое прогрессирование, оцениваемое по приросту эрозий и сужению суставной щели [15]. Достоверных различий влияния лефлуномида или метотрексата на рентгенологическое прогрессирование не получено, однако результаты длительной терапии показали преимущество лефлуномида над сульфасалазином.
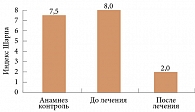
Анализ рентгенологического прогрессирования, оцениваемого по методу Шарпа, показал замедление прироста эрозий и сужения суставной щели у больных РА за 12 и 36 месяцев лечения лефлуномидом, а также обратимость костной эрозии [7].
Оценка рентгенологического прогрессирования РА в долгосрочном исследовании у 128 больных, получавших лефлуномид более двух лет, проведена D. van der Heijde и соавт. [5]. Средняя длительность заболевания составляла 5,1 года, лечения – 4,3 года. К началу терапии у 12% больных эрозии зафиксированы не были, у 72% – наблюдался медленный тип рентгенологического прогрессирования РА, у 16% – быстрый. По окончании терапии прогрессирование РА остановлено у 33% больных, что свидетель-ствовало о положительном влиянии лефлуномида на структурные изменения опорно-двигательного аппарата и супрессию заболевания (рис. 4).
Комбинированная терапия лефлуномидом и метотрексатом, лефлуномидом и инфликсимабом очень эффективна, хорошо переносится и может быть рекомендована пациентам, не ответившим на монотерапию БПВП, или при быстром прогрессировании костной деструкции (рис. 5).
Мониторинг больных при комбинированной терапии должен быть тщательным, так как возможно увеличение частоты побочных реакций. При использовании комбинации лефлуномида и ингибиторов ФНО-α не рекомендуются насыщенные дозы лефлуномида (100 мг/сут в течение трех дней), а также одновременноe назначение лефлуномида и ингибитора ФНО-α. При риске развития побочных эффектов или назначении лефлуномида на фоне терапии ингибиторами ФНО-α начальная доза должна составлять 10 мг/сут и увеличиваться до 20 мг/сут в течение двух-трех месяцев [5].
Установлено, что сочетание ритуксимаба и лефлуномида достоверно более эффективно в отношении развития хорошего ответа на лечение по критериям EULAR (European League Against Rheumatism), чем его сочетание с метотрексатом и монотерапия лефлуномидом [16].
Важной составляющей анализа БПВП является оценка их переносимости и безопасности. Переносимость лефлуномида характеризуется как удовлетворительная. По данным исследования TOPAS, на фоне его приема чаще всего наблюдаются такие нежелательные явления, как диарея (13%), гриппоподобный синдром (12,5%), повышение уровня аланинаминотрансферазы (12,5%), головная боль (11,5%), тошнота (9,4%), кожная сыпь (7,3%), повышенная утомляемость/сонливость (6,3%) [17]. В редких случаях отмечались боль в конечностях, мышечная слабость, алопеция легкой степени, фоточувствительность, незначительное повышение артериального давления, транзиторная лейкопения.
Наиболее серьезное осложнение терапии лефлуномидом – повышение печеночных аминотрансфераз и в первую очередь аланинаминотрансферазы. Гиперферментемия чаще всего характеризовалась незначительным увеличением значений аминотрансфераз. Однако у некоторых больных они превышали нормальные значения в три раза и более. Необходимо отметить, что у всех больных нормализация печеночных аминотрансфераз происходила без дополнительных лечебных мероприятий.
Данные о переносимости лефлуномида обобщены в материалах международной конференции «Practical Management of Rheumatoid Arthritis Patients Treated with Leflunomide» (2004 г.) [18]. По мнению экспертов, практически все нежелательные реакции развиваются в первые три месяца лечения. В дальнейшем при использовании той же самой дозы препарата, как правило, не возобновляются.
Диарея у большинства больных разрешается самостоятельно. Полагают, что она является результатом воздействия лефлуномида на клеточный цикл эпителия желудочно-кишечного тракта.
Алопеция – характерный признак интоксикации лефлуномидом – выражена слабо или умеренно и имеет преходящий характер.
Как и при назначении других БПВП, нарушение функции печени развивается в первые три-четыре месяца терапии. Учитывая гепатотоксичность лефлуномида, рекомендуется определять печеночные энзимы каждые две недели в первые шесть месяцев терапии, далее – один раз в два месяца.
При появлении кожных реакций, таких как сыпь или зуд, следует уменьшить суточную дозу препарата или временно отменить его.
Синдром Стивенса – Джонсона (некротический эпидермолиз) встречается крайне редко.
Поскольку при использовании лефлуномида возможно развитие артериальной гипертензии, необходимо проводить мониторинг артериального давления, особенно у больных с гипертонической болезнью. Из гематологических цитопений первостепенное значение имеет нейтропения. При развитии умеренной или выраженной нейтропении лечение лефлуномидом прекращают.
Многие среднетяжелые и тяжелые нежелательные реакции являются дозозависимыми. Их можно избежать, своевременно скорректировав суточную дозу. В частности, не всегда следует назначать насыщающую дозу препарата, поскольку это мало отражается на быстроте развития терапевтического эффекта. В ряде случаев допустимо снижение суточной дозы лефлуномида до 10 мг/сут на протяжении длительного периода.
При развитии выраженных нежелательных реакций необходимо проводить дезинтоксикационную терапию. Наиболее эффективен холестирамин – по 8 г дважды в день. Следует отметить, что спектр нежелательных явлений при многолетнем применении лефлуномида имеет тенденцию к снижению.
Преимущество лефлуномида перед метотрексатом – лучшая переносимость. Так, при применении метотрексата побочные эффекты наблюдаются чаще, носят более серьезный характер и могут привести к летальному исходу. К таковым относятся оральный синдром, мукозит, эпиляция, гематологические девиации, определяющие цитотоксическую болезнь (по интерпретации А.И. Воробьева), токсические явления со стороны центральной нервной системы, остеопатия, аллергические проявления и эндокринные расстройства, а также токсический гепатит, фиброз и цирроз печени.
Таким образом, лефлуномид при РА обладает высокой эффективностью, сравнимой с другими БПВП. При этом заболевании он применяется в качестве монотерапии или в комбинации с другими базисными препаратами, например с метотрексатом или сульфасалазином, а также с биологическими препаратами. Лефлуномид характеризуется не только симптом-модифицирующим, но и структурно-модифицирующим действием. Его целесообразно назначать как на поздних, так и на ранних стадиях РА. Особенностью лефлуномида является устойчивый терапевтический эффект в случае длительного применения (месяцы и годы).
В национальном руководстве по ревматологии за 2008 г. отмечено, что по эффективности лефлуномид не уступает метотрексату и превосходит метотрексат и сульфасалазин по влиянию на качество жизни и быстроте развития лечебного ответа. Согласно рекомендациям ACR, принятым в 2008 г., начинать лечение РА следует с монотерапии метотрексатом или лефлуномидом, независимо от продолжительности, степени активности и наличия признаков неблагоприятного прогноза, в то время как алгоритм лечения РА, разработанный ЕULAR, рекомендует начинать терапию с монотерапии метотрексатом независимо от продолжительности и воспалительной активности и только при его непереносимости в качестве первого БПВП следует использовать лефлуномид [19, 20].
Лефлуномид эффективен в комбинации с метотрексатом и сульфасалазином при недостаточном эффекте монотерапии БПВП, а также с ГИБП. Подчеркивается, что основным показанием к применению лефлуномида являются недостаточная эффективность, плохая переносимость или наличие противопоказаний для назначения метотрексата, в том числе на ранних стадиях РА. Пациентам c ранним РА, имеющим факторы риска неблагоприятного прогноза, высокую активностью заболевания и резистентным к монотерапии метотрексатом, целесообразно назначение комбинированной терапии метотрексатом с другими БПВП – сульфасалазином и гидроксихлорохином и в первую очередь с лефлуномидом.
V.V. Badokin
Russian Medical Academy for Postgraduate Education
Contact person: Vladimir Vasilyevich Badokin, vbadokin@yandex.ru
Rheumatoid arthritis (RA) is the main nosological entity of joint inflammatory diseases. The results of numerous studies evidencing about immune inflammation underlying tissue changes served as a theoretical justification for using RA-modifying or anti-inflammatory drugs. A need for applying them was due to chronic progressive course of the disease as well. Here we consider issues regarding efficacy and safety of leflunomide during RA.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.