По данным разных авторов, заболеваемость экземой варьирует от 6 до 15 на 1000 населения и составляет 30–40% от общего числа кожных заболеваний. Экзему регистрируют с одинаковой частотой во всех странах мира у представителей всех рас вне зависимости от пола [1, 3]. Этиология и патогенез экзематозного процесса сложны и до настоящего времени окончательно не изучены. Большинство авторов считают, что заболевание развивается в результате комплексного воздействия нейроаллергических, эндокринных, обменных и экзогенных факторов. Среди эндогенных факторов следует отметить генетически обусловленную способность реагирования иммунной, нервной, эндокринной систем, наличие очагов хронической инфекции и патологии желудочно-кишечного тракта. Экзогенными раздражителями могут быть химические и биологические агенты, бактериальные аллергены, физические факторы, медикаменты, пищевые продукты, косметические средства и др. [4, 5].
Общепринятой классификации экземы не существует. В России на основании клинических проявлений и особенностей течения наиболее часто выделяют следующие варианты экземы [5]:
- истинная;
- микробная (нумулярная, паратравматическая, варикозная, сикозиформная, экзема сосков);
- себорейная;
- тилотическая;
- профессиональная;
- детская.
В зависимости от длительности заболевания выделяют острую (до 3 мес.), подострую (3–6 мес.) и хроническую (более 6 мес.) экзему.
Для экземы характерно формирование аллергической реакции по типу гиперчувствительности замедленного типа (ГЗТ). Антиген является гаптеном (неполным антигеном), и дальнейшее развитие аллергической реакции происходит после связывания его с белком-носителем. Иммунный ответ может быть направлен не только против гаптена, но и против белка-носителя. Презентация антигена Т-лимфоцитам осуществляется клетками Лангерганса, с последующей дифференцировкой лимфоцитов в направлении Th1-фенотипа. В результате запуска многокомпонентного иммунологического каскада выделяются провоспалительные и противовоспалительные цитокины и другие биологически активные вещества, под действием которых и формируются общие и местные клинические проявления [5, 6].
При микробной экземе развивается сенсибилизация к бактериальным, вирусным и грибковым антигенам. Нередко одной из причин развития заболевания может быть сочетанная бактериальная и грибковая флора. Согласно отечественным данным, у больных, страдающих экземой, при исследовании соскобов с элементов сыпи в 80% случаев высевается S. aureus, в 14% – S. haemolyticus, в 40,7% – нелипофильные дрожжевые грибы, преимущественно рода Candida [7].
Известно, что неповрежденная кожа выполняет защитную функцию и в норме непроницаема для микроорганизмов. Местные механизмы защиты формируются некоторыми физиологическими и структурными особенностями кожи, например плотным сцеплением роговых чешуек, кислым рН, жирными кислотами кожного сала, синтезом в эпидермисе некоторых интерлейкинов, а также микрофлорой, которая формирует микробиоценоз кожи. В норме микробиоценоз кожи представлен резидентной (S. aureus, Micrococcus spp. и др.) и транзиторной (патогенные и условно-патогенные микроорганизмы) микрофлорой, которая находится в состоянии биологического равновесия и антагонистическом взаимодействии, что обеспечивает защитную функцию. Длительное неконтролируемое воздействие агрессивных физико-химических факторов, помимо прямого повреждения кожи, вызывает нарушения качественного и количественного состава ее микробиоценоза, что усугубляет патологический процесс. Изменение структуры рогового слоя приводит к повышению проницаемости кожи для грибов и бактерий [8]. Микробные аллергены обладают выраженной антигенной активностью, вызывают и поддерживают иммунное воспаление. Все звенья патогенеза экземы находятся в тесной взаимосвязи, реализуя сложный механизм развития заболевания [9].
Необходимыми условиями, способствующими развитию вторичной инфекции, являются экссудация на поверхность кожи белков плазмы крови; нарушение целостности кожного покрова вследствие зуда и расчесываний, открывающее «входные ворота» для инфекции; изменение уровня рН на поверхности кожи и липидного состава рогового слоя, а также нарушение местного иммунного ответа. При атопическом дерматите и экземе наличие дополнительного источника аминокислот, содержащихся в лимфе, может явиться значимым стимулирующим фактором, способствующим повышенной колонизации кожи нелипофильными дрожжевыми грибами. Данному процессу способствует и длительное использование наружных глюкокортикоидных средств, а также локализация дерматоза в кожных складках и на стопах.
Клинические проявления экземы имеют патогномоничный признак – «точечное» (везикулярное) мокнутие на фоне отека, эритемы, наличия серозно-гнойных корочек. При длительном хроническом течении заболевания возможно формирование участков инфильтрации и лихенификации кожи.
Выбор метода лечения экземы определяется степенью тяжести и распространенностью патологического процесса. Важный этап терапии – выявление причин развития заболевания и устранение провоцирующих факторов. В комплексной терапии, как правило, используются антигистаминные, десенсибилизирующие препараты, в тяжелых случаях – глюкокортикостероидные средства. Иногда требуется назначение системной антибактериальной и противогрибковой терапии.
В комплексном лечении микробной экземы большую роль играет наружная терапия, которая должна быть адекватна остроте заболевания, тяжести состояния и возрасту пациента, выраженности клинических проявлений и локализации патологического процесса. Для быстрого купирования воспалительных явлений и снятия зуда в очагах микробной экземы, значительно облегчающего состояние больного, традиционно используются глюкокортикоидные препараты для местного применения. Кроме того, согласно исследованиям зарубежных авторов, блокирование медиаторов воспаления на раннем этапе воспалительного процесса уменьшает стимуляцию меланоцитов, ответственных за формирование длительно сохраняющейся поствоспалительной гиперпигментации кожи в очагах поражения, вызывающей у больных беспокойство и эстетическую неудовлетворенность проведенным лечением [10].
С целью одновременного воздействия на несколько звеньев патогенеза заболевания и для устранения действия различных инфекционных факторов в терапии микробной экземы чаще всего используют комбинированные глюкокортикостероидные препараты местного воздействия: 2-компонентные (с антибиотиками или противогрибковыми средствами), а также 3-компонентные (преимущественно с гентамицином и клотримазолом). В состав большинства таких лекарственных средств входит бетаметазон – фторированный глюкокортикостероид (ГКС), относящийся к препаратам высокой активности (3-й класс). Для таких препаратов существуют определенные ограничения к применению – их нельзя использовать длительно, а также у беременных и у женщин в период лактации, нежелательно применять у детей, на область лица, наружных гениталий и в складки кожи, на обширные участки кожного покрова. Целесообразность применения столь сильных ГКС в составе комбинированных препаратов вызывает большие сомнения, причем с точки зрения не только безопасности, но и эффективности лечения. Нужно учитывать, что активные ГКС вызывают избыточную иммуносупрессию в очаге воспаления, повышающую шансы инфекционного агента на выживание. Кроме того, в случае бактериальной и/или грибковой инфекции наибольшее значение имеет не противовоспалительная активность глюкокортикостероида, входящего в состав комбинированного средства для наружной терапии, а эффективность его антибактериальных/антимикотических компонентов [11]. Так, использование средств, в состав которых входят клотримазол и/или гентамицин, не всегда целесообразно в связи с часто встречающейся в последние годы устойчивостью патогенных агентов. Нерациональный выбор препарата способствует дальнейшему распространению инфекции, прогрессированию процесса и повышению резистентности микроорганизмов к лекарственным средствам.
В качестве безопасной альтернативы для наружного лечения микробной экземы у взрослых и детей целесообразно применение препарата Пимафукорт, в состав которого входит «эталон безопасности» среди ГКС – гидрокортизон, а также натамицин и неомицина сульфат.
Гидрокортизон – мягкий ГКС 1-го класса активности, применяемый в дерматологии с 1952 г., по безопасности во много раз превосходящий бетаметазон, за счет чего возможно применение Пимафукорта у новорожденных, беременных женщин, на участках с тонкой кожей и в кожных складках, а также, при необходимости, в течение достаточно длительного времени. Препарат обладает противовоспалительным, сосудосуживающим и противозудным действием, устраняет сенсибилизацию к бактериальным и грибковым антигенам без излишней иммуносупрессии, о чем свидетельствует его микробиологическая эффективность. Особенно актуально применение гидрокортизонсодержащих препаратов для наружного лечения при острых процессах в соответствии с базовым принципом наружной терапии дерматозов: чем острее протекает процесс, тем более мягким должно быть воздействие.
Натамицин относится к противогрибковым средствам из группы полиеновых макролидов, обладает фунгицидным действием за счет необратимого связывания с эргостеролом клеточной мембраны гриба, вызывая ее деструкцию и лизис, высокоактивен преимущественно в отношении дрожжевых и дрожжеподобных грибов, а также проявляет активность в отношении ряда дерматофитов и других патогенных грибов (Aspergillus, Fusarium и др.). Стабильность фунгицидного действия натамицина сохраняется в широком диапазоне рН кожи – от 4,5 до 9,0. Преимуществом натамицина перед другими противогрибковыми средствами, в первую очередь перед азолами, является отсутствие резистентности к препарату штаммов грибов рода Candida (albicans и, что особенно важно, non-albicans) [12], высокая активность даже в низкой концентрации, отсутствие токсического и эмбриопатогенного действия и аллергогенных свойств. Натамицин не всасывается с поверхности кожных покровов и слизистых оболочек в кровоток, в связи с чем препарат не оказывает системного действия [13].
Неомицин – антибиотик широкого спектра действия из группы аминогликозидов. Неомицин продуцируется Actinomyces fradiae, активен в отношении как грамположительных (Staphylococcus spp., Enterococcus spp.), так и грамотрицательных (Klebsiella spp., Proteus spp.,
Escherichia coli и др.) бактерий. Важным преимуществом неомицина является его активность в отношении гентамицин-резистентных штаммов, что особенно актуально, поскольку из-за широкого и зачастую необоснованного применения гентамицина в России в настоящее время сформировалась вторичная резистентность к нему основных патогенных микроорганизмов. Чувствительность к гентамицину метициллин-резистентных стафилококков (MRSA), выделенных у пациентов с атопическим дерматитом, составила всего 56% [14]. Многие гентамицин-резистентные патогенные штаммы ингибируются неомицином, несмотря на наличие некоторой перекрестной устойчивости, поскольку она является неполной.
Основными показаниями к применению Пимафукорта являются дерматозы, осложненные вторичной бактериальной и/или грибковой инфекцией (атопический дерматит, экзема), а также себорейный дерматит, пеленочный дерматит, баланопостит. При этом возможно использование данного препарата для эмпирической терапии поражений кожи, протекающих на фоне выраженного воспаления и вызванных смешанной или неидентифицированной флорой. Препарат выпускается в двух лекарственных формах – крем и мазь, что позволяет использовать его как при острой и подострой стадиях заболевания (крем), так и на участки с выраженной инфильтрацией и лихенизацией кожных покровов при хронической стадии заболевания (мазь).
Исследованиями современных авторов доказана более высокая эффективность и безопасность Пимафукорта при лечении хронических дерматозов, осложненных вторичной инфекцией, по сравнению с использованием комбинации других средств (мазь Травокорт в сочетании с гентамициновой мазью, крем Кандид Б), часто назначаемых специалистами. Клиническая эффективность препарата Пимафукорт в терапии различных инфицированных дерматозов достигает 80–100%, приближаясь к 100% в лечении микробной экземы [11, 15, 16].
Целью собственных наблюдений, которые проводились на базе Нижегородского научно-исследовательского кожно-венерологического института (НИКВИ) и поликлиники № 3 Приволжского окружного медицинского центра Н. Новгорода и включали 30 больных обоего пола в возрасте от 6 месяцев до 72 лет, страдающих различными формами микробной экземы, была оценка эффективности и безопасности применения препарата Пимафукорт в комплексном лечении данной патологии. Все больные получали традиционную терапию (антигистаминные и гипосенсибилизирующие средства; энтеросорбенты, физиотерапевтическое лечение и седативные препараты по показаниям); для наружного лечения применяли крем Пимафукорт при острой и подострой стадиях процесса или мазь Пимафукорт при хроническом течении заболевания 2 раза в день. Препарат наносили тонким слоем на патологические очаги в течение 7–20 дней до полного регресса клинических проявлений заболевания.
Практически сразу после начала лечения (на 2–3-й день) все пациенты отмечали значительное уменьшение зуда, отечности и прекращение мокнутия в очагах воспаления, распространение патологического процесса останавливалось. К 7–10-му дню полностью регрессировали проявления пиодермии в очагах, уменьшалась выраженность эритемы. К моменту завершения терапии у большинства больных (83,3%) был отмечен полный регресс высыпаний, в остальных случаях (в основном при хроническом течении заболевания) было отмечено значительное улучшение. Ни в одном случае не было необходимости в дополнительном назначении системной антибактериальной и/или противогрибковой терапии. Переносимость лечения во всех случаях была хорошей, побочных эффектов на фоне применения препарата Пимафукорт зарегистрировано не было.
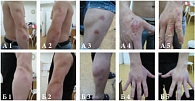
На рис. 1 представлены проявления микробной экземы до и после лечения кремом Пимафукорт в комплексной терапии у больного А., возраст 23 года, в течение 2 лет страдавшего распространенной микробной экземой и поступившего в стационар НИКВИ через 2 недели после обострения заболевания.
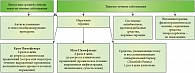
Предлагаемый нами алгоритм ведения пациентов с микробной экземой представлен на рис. 2. Таким образом, можно сделать вывод о высокой эффективности и безопасности применения препарата Пимафукорт для наружной терапии различных форм микробной экземы (нумулярной, паратравматической, варикозной).