Опыт применения дутастерида перед трансуретральной резекцией простаты больших размеров
- Аннотация
- Статья
- Ссылки



Длительное использование медикаментозной симптоматической терапии привело к увеличению удельного веса пациентов с доброкачественной гиперплазией простаты больших размеров, когда размеры предстательной железы превышают 80 кубических сантиметров. В течение нескольких десятилетий трансуретральная резекция (ТУР) простаты остается стандартом хирургического лечения ДГП (1). Этот метод сочетает в себе достаточный радикализм и эффективность, характерные для открытого оперативного вмешательства, обладает рядом преимуществ, среди которых меньшая инвазивность, возможность повторения без повышения риска для больного, более легкий послеоперационный период и др.
Обладая высокой клинической эффективностью, ТУР простаты имеет определенные осложнения, уровень которых хорошо изучен и остается достаточно стабильным (5, 6, 8). Смертность после выполнения этого оперативного вмешательства за последние 30 лет значительно снизилась и на сегодняшний день, по нашим данным, не превышает 0,25% (1).
Наиболее серьезным интаоперационным осложнением ТУР остается массивное кровотечение, требующее проведения гемотрансфузии (2). По данным Mebust и соавт., подобная необходимость возникает у 2,5% пациентов (8), а Horinger и соавт. отмечают частоту гемотрансфузий для восполнения интаоперационной кровопотери после ТУР простаты до 4,2% (5). По данным сводной статистики, потребность в подобной терапии остается достаточно высокой и сохраняется на уровне 7,2%, что безусловно говорит об актуальности и значимости проблемы (6). Особенно велик риск кровотечения при выполнении трансуретральной резекции простаты больших размеров (1).
Финастерид являлся первым ингибитором 5 альфа-редуктазы второго типа, и после его внедрения в клиническую практику были отмечены эффекты снижения интраоперационной кровопотери при ТУР простаты (2, 3, 10). Дутастерид является новым, более мощным препаратом – ингибитором 5 альфа-редуктазы обоих типов (7, 9), что позволило нам применить препарат у пациентов с ДГП больших размеров (более 80 куб.см.) с целью улучшения результатов оперативного лечения больных с ДГП путем профилактики развития интра- и послеоперационных геморрагических осложнений перед выполнением трансуретральной резекции простаты. Для достижения вышеуказанной цели нами были поставлены следующие задачи: изучить уровень интра- и послеоперационных геморрагических осложнений в группах больных, которым перед операцией назначался дутастерид, а также в контрольной группе пациентов, которые не принимали дутастерид; изучить особенности трансуретральной резекции простаты и послеоперационного периода у больных после приема дутастерида и у больных, не принимавших дутастерид, и на основании полученных данных определить сроки приема дутастерида до операции и группу больных, у которых следует ожидать наибольшего эффекта от вышеуказанной терапии.
Пациенты и методы
С января 2005 года по сентябрь 2006 года в НИИ урологии Росздрава и московской ГКУБ № 47 было отобрано 70 мужчин в возрасте от 67 до 82 лет (в среднем 74 года) с ДГП больших размеров (более 80 см3), у которых при обследовании были выявлены показания к операции, и методом лечения была выбрана ТУР простаты. Всем пациентам проводилось предварительное амбулаторное обследование, включающее в себя сбор жалоб и их оценку по шкале I-PSS, выяснение анамнеза заболевания, пальцевого ректального исследования, инструментального обследования, состоящего из трансректального ультразвукового исследования простаты, ультразвукового исследования мочевого пузыря с определением остаточной мочи, ультразвукового исследования почек, урофлоуметрии и лабораторного обследования, включавшего в себя общий анализ крови и мочи, биохимический анализ крови с определением креатинина, мочевины, коагулограмму, анализ крови на простатспецифический антиген, микробиологическое исследование мочи. Перед включением в исследование все пациенты дали информированное согласие. Критериями исключения были выявление коагулопатии, подозрение на рак простаты (повышенный показатель ПСА, изменения при ректальном исследовании и трансректальном ультразвуковом исследовании), а также указание в анамнезе на терапию ингибиторами 5 альфа-редуктазы. После включения в исследование больные были рандомизированы на две группы по 35 пациентов. Первая группа больных принимала до операции ежедневно дутастерид (Аводарт, GSK, Великобритания) в дозе 0,5 мг (в среднем 38 дней), а также альфа-адреноблокатор тамсулозин (Омник или Омник-Окас, «Астеллас», Япония) в дозе 0,4 мг для профилактики острой задержки мочеиспускания. Вторая группа (контрольная) принимала только альфа-адреноблокатор.
В течение месяца по различным причинам из исследования было исключено 3 пациента в первой группе и 2 пациента в контрольной группе. В таблице 1 приведены основные характеристики двух групп.
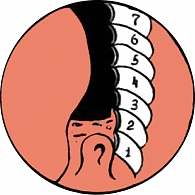
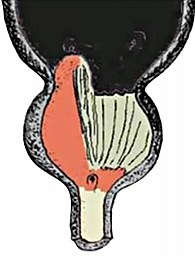
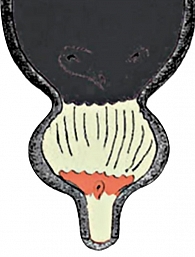
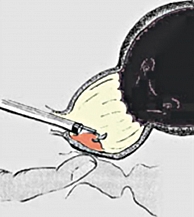
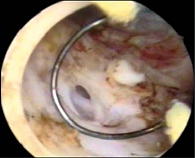
Всем пациентам выполнена трансуретральная резекция предстательной железы по методике Вarnes (рисунки 1 – 6).
Нами изучались такие показатели, как время электрорезекции, объем ирригационной жидкости, концентрация гемоглобина в промывной жидкости, уровень гемоглобина до и после операции, в дальнейшем по специальной формуле производилась оценка интраоперационной кровопотери. Кроме того, определялось количество резецированной ткани и всем больным производился этаноловый тест для исключения синдрома водной интоксикации.
Мы производили определение концентрации гемоглобина в промывной жидкости, с последующим расчетом кровопотери исходя из известных показателей концентрации гемоглобина крови перед операцией и объема использованного ирригационного раствора. Образец промывной жидкости (10 мл) забирали после окончания операции и направляли в биохимическую лабораторию. Определение концентрации гемоглобина в промывной жидкости выполняли гемоглобинцианидным методом (метод Drapkin), после чего цианметгемоглобин определялся на приборе ФП 901 с использованием наборов фирмы Labsystems (Финляндия). Чувствительность метода позволяет регистрировать концентрацию гемоглобина в представленном материале вне зависимости от его разведения трансформирующим раствором. Для выполнения расчета концентрации гемоглобина в промывной жидкости использовали следующую формулу:
Еоп
С hb в растворе = Ест ´ С ´ К ´ 0,01,
где С hb в растворе – концентрация гемоглобина в промывной жидкости (г/л); Еоп – оптическая плотность опытной пробы; Ест – оптическая плотность стандартного раствора; С – концентрация гемоглобинцианида в стандартном растворе (мг/л); К – коэффициент разведения крови.
Определение объема интраоперационной кровопотери производили с учетом концентрации гемоглобина в промывной жидкости, объема использованной промывной жидкости и концентрации гемоглобина в крови:
С hb в растворе ´ Vраствора
Vкр = C hb крови
где Vкр – объем интраоперационной кровопотери (литров); С hb в растворе – концентрация гемоглобина в промывной жидкости (г/л); Vраствора – объем использованной при операции промывной жидкости (литров); C hb крови – концентрация гемоглобина в крови пациента перед операцией (г/л).
После вмешательства по уретре устанавливали трехходовой катетер Foley № 20-22F, раздували баллон на 50-80 мл и натягивали катетер на 2 часа. Если при снятии натяжения отмечали усиление примеси крови в промывной жидкости, натяжение катетера возобновлялось на сутки.
Все операции произведены одним урологом с использованием резектоскопа с постоянным промыванием диаметром № 28 F фирмы Karl Storz (Германия). Помимо вышеуказанных характеристик обращали внимание на вид слизистой простатического отдела уретры и шейки мочевого пузыря, кровоточивость слизистой при проведении инструмента в мочевой пузырь, четкость эндоскопической картины операционного поля. В раннем послеоперационном периоде обращали внимание на сроки натяжения уретрального катетера, сроки промывания мочевого пузыря, необходимость гемотрансфузии, фиксировались случаи наступления послеоперационных геморрагических осложнений – тампонады мочевого пузыря и количество повторных эндоскопических вмешательств, направленных на ликвидацию тампонады мочевого пузыря. Полученные данные были обработаны с определением достоверности различий с помощью критерия Фишера.
В таблице 2 приведены основные результаты изучаемых показателей в обеих группах.
Помимо изучения вышеуказанных показателей, нами произведено сравнение скорости удаления тканей, что составило 1,48 см3/мин. в основной группе и 1,08 см3/мин. в контрольной группе (p < 0,01). Также произведено сравнение кровопотери во времени и по отношению к количеству удаленной ткани в обеих группах. В группе пациентов, которые применяли дутастерид, средняя скорость кровопотери составила 1,51 мл/минуту и в контрольной группе – 1,75 мл/мин. (p < 0,01). Средняя скорость кровопотери по отношению к 1 грамму удаленной ткани составила в основной группе 1,02 мл/г и 1,63 мл/г в контрольной группе (p < 0,01). Статистически достоверные отличия были получены в количестве интраоперационной кровопотери, длительности функционирования системы орошения мочевого пузыря, продолжительности послеоперационного койко-дня и количестве случаев послеоперационной тампонады мочевого пузыря. Кроме того, в группе пациентов, принимавших дутастерид перед операцией, не было отмечено случаев развития синдрома водной интоксикации организма, в послеоперационном периоде не было отмечено случаев развития тампонады мочевого пузыря и необходимости в гемотрансфузии.
Широкое использование медикаментозной терапии и, в частности альфа-адреноблокаторов, как препаратов первой линии в консервативной терапии больных с ДГП привело к увеличению доли больных с большими (более 80 кубических сантиметров) размерами предстательной железы при обращении к урологу (9). Трансуретральная резекция предстательной железы, являясь «золотым стандартом» оперативного лечения данного заболевания, имеет определенные ограничения и осложнения (1). Так при превышении времени резекции в 60 минут значительно повышается уровень развития таких осложнений, как синдром водной интоксикации и кровотечение (5, 8). С увеличением объема резецируемой ткани прямо пропорционально возрастает риск развития интраоперационных осложнений – кровотечения, повреждения устьев мочеточников, перфорации простаты и развития синдрома водной интоксикации организма. Накопление опыта эндоскопических операций на предстательной железе, появление новых генераторов, резектоскопов с ротационным внутренним тубусом, усовершенствование системы постоянной ирригации позволило расширить показания к трансуретральной резекции у пациентов с размерами предстательной железы более 80 см3. Однако частота геморрагических осложнений трансуретральной резекции предстательной железы у данной группы пациентов остается высокой и данное обстоятельство послужило поводом к развитию малоинвазивных оперативных вмешательств – гольмиевая лазерная энуклеация простаты, лазерная трансуретральная вапоризация и др. (6).
Влияние ингибитора 5 альфа-редуктазы второго типа финастерида на кровоснабжение предстательной железы отражено в нескольких публикациях (2-4, 10). Были получены данные о том, что назначение финастерида на 3 месяца перед планируемой операцией на предстательной железе позволяет уменьшить объем интраоперационной кровопотери (10). Внедрение в клиническую практику нового препарата ингибитора 5 альфа-редуктазы обоих типов – дутастерида позволило нам применить данный лекарственный препарат в комплексной подготовке пациентов с большими размерами доброкачественной гиперплазии предстательной железы перед планируемой трансуретральной резекцией. Основанием для подобного выбора явились данные о том, что дутастерид приводит к снижению концентрации дигидротестостерона на 93% по сравнению с финастеридом (70%) (7, 9). Учитывая более мощный эффект дутастерида, нами был выбран срок в 1 месяц до получения клинического эффекта.
Терапия дутастеридом переносилась пациентами хорошо и не было отмечено наступления побочных эффектов. Дутастерид ингибирует 5 альфа-редуктазу обоих типов, приводит практически к полному исчезновению в предстательной железе дигидротестостерона, что в свою очередь приводит к резкому снижению выработки эндотелиального фактора роста сосудов и ослаблению васкуляризации предстательной железы. Данное обстоятельство становится очевидным в начале операции, когда отчетливо видно снижение очерченности подслизистого сосудистого рисунка и практически полностью отсутствует контактное кровотечение из вен долей простаты при проведении инструмента в мочевой пузырь. Особенностями трансуретральной резекции предстательной железы после приема дутастерида является более четкая эндоскопическая видимость, которая является профилактикой повреждения таких анатомических структур, как устье мочеточника, наружный сфинктер мочевого пузыря, а также помогает избежать перфорации мочевого пузыря и предстательной железы, является профилактикой развития синдрома водной интоксикации организма. При удалении ткани были отмечены некоторые особенности: меньшая плотность сосудов в поле зрения инструмента, при этом на фоне хорошей эндоскопической видимости лучше видны крупные артериальные стволы, требующие немедленной коагуляции; практически отсутствует диффузная кровоточивость тканей, которая затрудняет и замедляет ход операции. Подтверждением вышеуказанных данных является большая скорость удаления ткани 1,48 см3/мин. в группе больных, принимавших дутастерид, против 1,08 см3/мин. в группе больных, принимавших плацебо. Также обращает на себя внимание статистически достоверно меньшая интраоперационная кровопотеря у больных после приема дутастерида. Одним из лучших доказательств обеднения кровотока в предстательной железе является показатель соотношения объема кровопотери по отношению к массе рецизированной ткани, который составил 1,02 и 1,63 мл/см3, то есть плотность сосудов в предстательной железе после приема дутастерида снизилась на 60%. Данный факт позволил нам расширить показания к трансуретральной резекции у больных с ДГП и улучшить качество оказываемой помощи пациентам за счет снижения в первую очередь частоты развития осложнений.
После окончания резекции тканей на фоне приема дутастерида снизилась продолжительность финишной коагуляции операционного поля и количество пациентов, которым необходимо натяжение уретрального катетера на 24 часа, уменьшились сроки послеоперационного орошения мочевого пузыря, что приводит к более быстрому удалению уретрального катетера и снижению сроков госпитализации.
В группе пациентов, принимавших дутастерид, нами не было отмечено случаев послеоперационного кровотечения, которые бы требовали проведения гемотрансфузии, только в одном случае была отмечена тампонада мочевого пузыря, которая была ликвидирована консервативными мероприятиями.
Выраженные интеркуррентные заболевания у пациентов, прием аспирина в качестве антиагреганта после интервенционных кардиохирургических вмешательств в сочетании с большими размерами ДГП делают проблему профилактики развития геморрагических осложнений после трансуретральной резекции простаты наиболее актуальной. Применение дутастерида в течение 1 месяца перед планируемой трансуретральной резекцией простаты позволяет эффективно и безопасно выполнить данную операцию у больных с большими размерами ДГП.
Заключение
Наш первый опыт применения дутастерида для профилактики геморрагических осложнений при трансуретральной резекции простаты при ДГП больших размеров показал высокую клиническую эффективность и безопасность его применения.
Нами доказано, что использование дутастерида (Аводарт, GSK, Великобритания) в дозировке 0,5 мг в течение 1 месяца перед планируемой трансуретральной резекции предстательной железы по поводу ДГП позволяет статистически достоверно уменьшить время операции, объем кровопотери, облегчить течение послеоперационного периода за счет меньших сроков натяжения уретрального катетера и функционирования промывной системы, уменьшить сроки госпитализации.
После получения результатов данного исследования мы считаем необходимым назначать дутастерид в течение месяца перед планируемой трансуретральной резекцией предстательной железы пациентам не только с большими (более 80 см3) но и с гораздо меньшими объемами (30-80 см3) предстательной железы. Однако, для более полной оценки клинической эффективности необходимы дальнейшее накопление опыта применения дутастерида перед планируемым оперативным эндоскопическим вмешательством в урологической практике у пациентов с различными объемами предстательной железы, дальнейшее изучение отдаленных результатов и выполнение ряда рандомизированных исследований в этом направлении.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.