Опыт применения гуселькумаба при псориазе и коморбидной депрессии
- Аннотация
- Статья
- Ссылки
- English
Псориаз – хроническое воспалительное иммуноопосредованное заболевание с ярко выраженной генетической предрасположенностью [1], которое тесно связано с сопутствующими психическими заболеваниями, такими как депрессия и тревожные расстройства [2, 3]. Распространенность псориаза во всем мире составляет около 2%, но варьирует в зависимости от региона, с более низкими показателями в азиатской и некоторых африканских популяциях и до 11% в европеоидной и скандинавской популяциях [4–7]. У 30% пациентов развиваются патологические изменения опорно-двигательного аппарата [8]. Помимо поражения суставов, для дерматоза характерны целый ряд коморбидностей, в том числе метаболический синдром, сердечно-сосудистые заболевания [9], сахарный диабет, неалкогольная жировая дистрофия печени, ожирение, воспалительные заболевания кишечника [10–12]. Психические расстройства при псориазе стали предметом активного изучения последние годы.
Депрессия является частым сопутствующим заболеванием псориаза [13]. Скрининг пациентов с псориазом, обращающихся за помощью в дерматологические клиники, показал, что уровень распространенности клинической депрессии составляет примерно 12–13% по кодам Международной классификации болезней (МКБ) [14, 15]. Однако в зависимости от методологии скрининга депрессивные симптомы обнаруживаются у 28–55% пациентов с псориазом [15, 16]. Тревожные расстройства преобладают у 7–48% больных псориазом [16, 17]. Стало очевидным, что одним из факторов, способствующих их формированию, является общность звеньев патогенеза дерматоза и коморбидных психических расстройств, особенно депрессии [17, 18]. Цитокиновая гипотеза подтверждает эту связь. Многие исследования показали, что уровни некоторых цитокинов, участвующих в патогенезе псориаза, прежде всего интерлейкина (ИЛ) 6, в плазме и центральной нервной системе (ЦНС) повышены и могут способствовать развитию психических заболеваний. У больных псориазом хроническое и системное воспаление, опосредованное цитокинами, может индуцировать биохимические и физиологические изменения в ЦНС, ведущие к депрессии. Однако природа этого механизма не до конца изучена [18]. У пациентов с псориазом вероятность развития депрессии в 1,5 раза выше, чем у пациентов без псориаза (отношение шансов 1,57; 95%-ный доверительный интервал (95% ДИ) 1,40–1,76). У пациентов с псориазом суицидальные мысли встречаются в два раза чаще, чем у остальных людей, – 17,3 и 8,2% соответственно (p < 0,001). Кроме того, среди пациентов, страдающих псориазом, по сравнению с остальными выше показатель самоубийств [17, 18]. У пациентов с псориазом по сравнению с общей популяцией наблюдается более высокая частота сексуальной дисфункции: 53,7 и 17,5% соответственно (p < 0,001). У пациентов с псориазом и депрессией уровень сексуальной дисфункции оказывается выше, чем у пациентов с псориазом, но без депрессии [18].
Важно отметить, что у больных псориазом не всегда очевидны депрессивные проявления, в то время как их наличие во многом определяет прогноз, течение заболевания и выбор терапии. Для диагностики и наблюдения за развитием депрессивных расстройств у больного псориазом в динамике и их регрессом на фоне проводимой терапии нами были использованы шкалы и опросники, рассмотренные в настоящей статье.
Госпитальная шкала тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS) разработана A.S. Zigmond и R.P. Snaith в 1983 г., относится к опросникам для самозаполнения, предназначена для выявления клинически значимой тревоги и депрессии у амбулаторных пациентов. Для интерпретации необходимо суммировать баллы по каждой подшкале (Д и Т) в отдельности: 0–7 баллов – норма (отсутствие достоверно выраженных симптомов тревоги и депрессии), 8–10 баллов – субклинически выраженная тревога/депрессия, 11 баллов и выше – клинически выраженная тревога/депрессия [19].
Шкала депрессии Гамильтона (Hamilton Rating Scalefor Depression, HDRS) используется для количественной оценки состояния пациентов с депрессивными расстройствами до, во время и после лечения (в динамике). Применяется и в клинических испытаниях и является стандартом для определения эффективности медикаментозных средств в лечении депрессивных расстройств. Суммарный балл высчитывают по 17 первым пунктам, четыре последних пункта шкалы (с 18 по 21) используются для оценки дополнительных симптомов депрессии и определения подтипов депрессивного расстройства. Чем выше балл, тем тяжелее депрессивное расстройство [20].
Шкала Монтгомери – Асберга (Montgomery – Asberg Depression Rating Scale, MADRS) основана на шкале оценки психопатологии – стандартной скрининговой шкале для общего выявления основных типов психопатологических расстройств. В шкале выделены 17 пунктов, ассоциированных с расстройствами депрессивного спектра, которые были валидизированы на конвергентную и дискриминативную значимость, в результате чего отобрали 10 наиболее чувствительных утверждений. Данные 10 вопросов оцениваются от 0 до 6 баллов. Чем тяжелее состояние пациента, тем больший балл ему присваивается. Общая оценка тяжести депрессивных расстройств по шкале варьирует от 0 до 60 баллов и снижается при улучшении состояния [21].
Опросник депрессии Бека (Beck's Depression Inventory, BDI) включает 21 категорию симптомов и жалоб. Каждая категория состоит из четырех-пяти утверждений, соответствующих специфическим проявлениям депрессии. Эти утверждения ранжированы по мере увеличения удельного вклада симптома в общую степень тяжести депрессии. В зависимости от степени выраженности симптома каждому пункту присвоены значения от 0 до 3 баллов. Показатель по каждой категории рассчитывается следующим образом: каждый пункт шкалы оценивается от 0 до 3 баллов в соответствии с нарастанием тяжести симптома. Суммарный балл варьирует от 0 до 62 и снижается по мере улучшения состояния [22].
Опросник о состоянии здоровья пациента (The Patient Health Questionnaire, PHQ-9) в популяционной группе используется в качестве инструмента скрининга и диагностики расстройств психического здоровья, депрессии, тревоги, злоупотребления алкоголем, нарушения пищевого поведения, соматоформных расстройств. Состоит из девяти пунктов с вариацией из четырех возможных ответов на каждый пункт. Каждый ответ оценивается от 0 до 3 баллов, на основе которых определяется выраженность депрессии. Если пациент набирает минимальное количество баллов (0–4), то депрессия является минимально выраженной, если максимум (20–27) – депрессия крайне тяжелая. PHQ существует на более чем 20 языках. Как исходная анкета о состоянии здоровья пациента, так и более поздние варианты являются общедоступными; для использования или копирования мер не требуется никаких сборов или разрешений [23, 24].
Колумбийская суицидальная шкала (Columbia Suicide Severity Rating Scale, C-SSRS) – клиническая шкала, применяемая для оценки тяжести суицида и суицидального риска. Создана коллективом авторов: K. Posner, M.A. Oquendo, M. Gould, B. Stanley и M. Davies в 2007 г. Шкала состоит из четырех модулей: суицидальные идеи, интенсивность суицидальных идей, суицидальное поведение, реальная/потенциальная опасность суицидальных попыток. Оценка тяжести суицидальных идей 3 балла и выше свидетельствует о серьезном риске суицида. Оценка 5 баллов, а также любые выявленные суицидальные действия означают наличие крайне высокого риска и абсолютной необходимости ургентных терапевтических мероприятий и госпитализации. Раздел «интенсивность суицидальных идей» позволяет более точно оценить тяжесть состояния, а также спрогнозировать его динамику. Здесь очень важны пункты, отражающие способность контроля, наличие сдерживающих факторов и оснований для совершения суицида. Безусловным достоинством шкалы является возможность ретроспективной оценки прежних эпизодов, связанных с повышенным риском суицида. Это очень важно с практической точки зрения, поскольку дает дополнительную возможность моделировать развитие актуальной ситуации у больного. Но, пожалуй, самое важное практическое значение Колумбийской шкалы заключается в том, что она, по сути, является своеобразной дорожной картой для обследования и оценки суицидального пациента [25].
Известно, что лечение среднетяжелых и тяжелых форм псориаза требует назначения системной генно-инженерной биологической терапии. Однако данных об эффектах тех или иных системных биологических препаратов, применяемых при псориазе и коморбидной депрессии, недостаточно. Было обнаружено, что психические показатели SF-36 улучшились после лечения устекинумабом [26] и бродалумабом по сравнению с плацебо (исследование фазы II) [27] и секукинумабом по сравнению с эфирами фумаровой кислоты (исследование PRIME) [28]. Клинические исследования псориаза, посвященные изучению различных терапевтических средств, показали улучшение течения депрессии при противовоспалительной терапии [29–33]. Однако данные в этой области относительно скудны, так как лишь немногие опорные исследования на сегодняшний день использовали психометрические шкалы для оценки качества жизни в целом и депрессивных симптомов в частности.
Представляем пациента с тяжелым течением псориаза, сопутствующей тяжелой депрессией и успешным применением ингибитора ИЛ-23 без назначения антидепрессантов.
Клинический случай
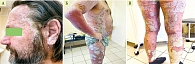
Пациент 46 лет с диагнозом «распространенный бляшечный псориаз, тяжелое непрерывно-рецидивирующее течение» обратился на консультацию с жалобами на распространенные высыпания, в том числе с поражением кожи лица, ушных раковин, заушных областей, кистей – так называемых косметически значимых локализаций, сопровождающиеся выраженным зудом, подавленностью, сниженным настроением, нарушение сна.
Болен с 2001 г. на протяжении 22 лет. Впервые высыпания на коже волосистой части головы, туловища, верхних и нижних конечностей отметил в возрасте 24 лет. Получал амбулаторное и стационарное лечение дезинтоксикационными препаратами, гепатопротекторами, топическими глюкокортикостероидами, ПУВА-терапию с незначительным эффектом. В 2015 г. диагностирован псориатический артрит. Лечение не назначалось. Самостоятельно использовал наружные глюкокортикостероидные препараты, с незначительным эффектом. Кожный процесс неуклонно прогрессировал. С 2017 г. пациент неоднократно был госпитализирован, получал лечение дезинтоксикационными препаратами, ПУВА-терапию, наружное лечение, с незначительным эффектом. В связи с неэффективностью проводимого лечения, появлением депрессивной симптоматики пациент самостоятельно отказался от получения медицинской помощи и проведения какой-либо терапии. На фоне усугубления психического состояния, нарастания симптомов депрессии, прогрессирования псориатического процесса пациент бросил работу, перестал общаться с близкими, изолировался от семьи. В феврале 2020 г. по настоянию жены обратился на прием в кожно-венерологический диспансер (КВД) № 10, где было рекомендовано системное лечение биологическими препаратами. Из-за боязни побочных эффектов, неэффективности предшествующей терапии пациент от лечения отказался. Через 10 дней был госпитализирован в городской КВД, где ему был назначен метотрексат в дозе 20 мг в неделю – три инъекции, далее в дозе 15 мг в неделю, который получал на протяжении трех месяцев, с незначительным эффектом. Из-за плохой переносимости пациент самостоятельно отменил терапию метотрексатом, далее лечение не проводил.
В марте 2020 г. отметил рецидив высыпаний, которые постепенно распространялись на протяжении полугода. Помимо поражения туловища и конечностей, папулы и бляшки впервые возникли на коже лица, в связи с чем пациент самостоятельно использовал топический бетаметазон в комбинации с салициловой кислотой, топические ингибиторы кальциневрина, с незначительным эффектом.
При обращении к дерматовенерологу отмечено удовлетворительное состояние, сознание ясное, фон настроения снижен, речь замедленная, мимика печальная, проговаривает идеи малоценности, мышление замедленное по темпу, память, интеллект без нарушений, внимание ослаблено, критика к состоянию достаточная, масса тела 102,7 кг, рост 180 см, окружность талии 124 см, индекс массы тела 31. Кожный процесс носил распространенный характер, захватывал кожу лица в области лба, височных, заушных областей, шеи, волосистой части головы, туловища, разгибательных поверхностей верхних и нижних конечностей. Поражение кожи было представлено псориатическими бляшками ярко-красного цвета с выраженной инфильтрацией, шелушением на поверхности (рис. 1). PASI (Psoriasis Areaand Severity Index) на момент обращения составил 32,4 балла, BSA (Body Surfase Area) – 40%, sPGA (Static Physician Global Assessment) – 4 балла, интенсивность зуда по визуальной аналоговой шкале (ВАШ) – 8/10 баллов, дерматологический индекс качества жизни (DLQI) – 30 баллов. Для диагностики депрессии использовали диагностические шкалы депрессии: госпитальная шкала тревоги и депрессии (HADS) – 10/17 – субклинически выраженная депрессия/клинически выраженная тревога; шкала депрессии Гамильтона (HDRS) – 28 баллов – депрессивное расстройство тяжелой степени; шкала депрессии Монтгомери – Асберга (MADRS) – 30 баллов – умеренный депрессивный эпизод; шкала депрессии Бека (BDI) – 32 балла – явно выраженная депрессивная симптоматика, не исключена эндогенность; PHQ-9 – опросник здоровья пациента – 21 балл – крайне тяжелая депрессия; Колумбийская суицидальная шкала (C-SSRS) – неинформативна/неприменима (пациент отказался отвечать на вопросы анкеты). Лабораторные данные: общий клинический анализ крови – в пределах нормы, в биохимическом анализе крови: общий холестерин – 7,2 ммоль/л (5,2), триглицериды – 3,19 (1,7) ммоль/л, липопротеины низкой плотности (ЛПНП) – 4,54 ммоль/л (< 3,37), коэффициент атерогенности – 4,92 ммоль/л (< 4), С-реактивный белок (СРБ) – 29,6 (< 5), аланинаминотрансфераза (АЛТ) – 71 ед/л (1–42), аспартатаминотрансфераза (АСТ) – 50 ед/л (1–38), гамма-глютамилтранспептидаза (ГГТП) – 120 ед/л (1–38).
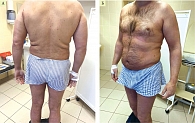
В связи с тяжестью процесса пациенту назначен ингибитор ИЛ-23 гуселькумаб по стандартной схеме. К четвертой неделе лечения отмечено значительное уменьшение интенсивности зуда – до 2 баллов по ВАШ, снижение PASI до 10,2, BSA – до 20%, sPGA – до 2 баллов (легкое), улучшение качества жизни пациента по DLQI – 7 баллов. Полное очищение кожных покровов было достигнуто к восьмой неделе терапии (рис. 2). Лабораторные данные: общий клинический анализ крови – в пределах нормы, в биохимическом анализе крови: общий холестерин – 5,1 ммоль/л (5,2), триглицериды – 1,71 (1,7) ммоль/л, ЛПНП – 2,89 ммоль/л (< 3,37), коэффициент атерогенности – 3,74 ммоль/л (< 4), СРБ – 4,7, АЛТ – 28 ед/л (1–42), АСТ – 31 ед/л (1–38), ГГТП – 37 ед/л (1–38).
Пациент получает лечение гуселькумабом по настоящее время. Достигнута полная ремиссия кожного процесса, PASI – 100%. Отмечается отсутствие симптомов депрессии по шкалам: госпитальная шкала тревоги и депрессии (HADS) – 5/7 – отсутствие достоверно выраженных симптомов тревоги и депрессии; шкала депрессии Гамильтона (HDRS) – 7 баллов – норма; шкала депрессии Монтгомери – Асберга (MADRS) – 15 баллов – отсутствие депрессивного эпизода; шкала депрессии Бека (BDI) – 9 баллов – отсутствие депрессивных симптомов; PHQ-9 – опросник здоровья пациента – 3 балла – минимальная депрессия; Колумбийская суицидальная шкала (C-SSRS) – неинформативна/неприменима (пациент отказался отвечать на вопросы анкеты).
На фоне лечения гуселькумабом симптомы депрессии к восьмой неделе терапии отсутствовали по всем диагностическим шкалам без назначения системных антидепрессантов.
Обсуждение
Психические заболевания при псориазе, одном из наиболее распространенных дерматозов, в последние годы наблюдаются часто. Так, A. Armstrongetal в крупнейшем исследовании (Clear About Psoriasis), включившем 8338 пациентов со среднетяжелым и тяжелым псориазом из 31 страны мира, получили следующие данные: 38% больных псориазом страдают психическими заболеваниями, ассоциированными с псориазом, 25% имеют тревожные нарушения, 24% – депрессию, 16% избегают общества [34]. В данном исследовании оценивали удовлетворенность лечением: 56% были удовлетворены, 24% были не уверены и 20% были недовольны. Была очевидна корреляция между удовлетворенностью лечением и наличием чистой/почти чистой кожи. Большинство пациентов не знали, что чистая/почти чистая кожа – реалистичная цель лечения: 56% не согласились с утверждением, что в будущем можно добиться чистой/почти чистой кожи. Также пациентов, которые уже достигли чистой/почти чистой кожи с помощью текущего лечения, попросили ретроспективно сообщить, считали ли они, что цель лечения достижима, до фактического ее достижения: 53% не верили, что чистая/почти чистая кожа возможна, пока не испытали это на себе. Среди пациентов, которые сами сообщили о чистой/почти чистой коже, почти три четверти начали текущую эффективную терапию в течение более чем одного года после постановки диагноза, а 28% назначали текущую терапию в течение более чем пяти лет после постановки диагноза [34], что наблюдалось у представленного нами пациента.
Чтобы проследить подход к воспалению, возможно, стоит изучить псориатический артрит [35]. Пациенты с псориазом и псориатическим артритом характеризуются дополнительной физической инвалидностью, и в среднем показатели коморбидной депрессии у них значительно выше [36], чем у пациентов без этого заболевания (p = 0,002), что наблюдалось у представленного нами пациента. Это согласуется с мнением о том, что периферические воспалительные процессы представляют собой основной связующий механизм между псориазом и депрессией. Аргумент о том, что наложение псориаза и депрессии связано с системным воспалением, лежащим в основе обоих состояний, подразумевает, что по мере того, как психические симптомы и симптомы псориаза улучшаются на фоне терапии, уменьшается и воспалительная нагрузка. В некоторых исследованиях изучали развитие воспалительных маркеров при биологической терапии псориаза. Одним из маркеров, который неоднократно оценивали и уровень которого снижался в ходе лечения, является СРБ [37, 38]. Показатель СРБ у представленного пациента был 29,66 мг/л до назначения гуселькумаба, на восьмой неделе терапии снизился до 4,7 мг/л.
Важным симптомом псориаза является зуд. Степень его выраженности у пациентов с псориазом коррелирует с тяжестью депрессии (p = 0,034). У представленного нами пациента интенсивность зуда по ВАШ составляла 8/10 баллов, что подтверждает данные исследований [38].
Другие коморбидные заболевания при псориазе могут служить неблагоприятным прогностическим фактором развития депрессии. Возможным кандидатом может быть ожирение, поскольку оно является фактором риска возникновения псориаза, усугубляет существующий псориаз [39, 40] и само по себе связано с системным воспалением [41], а также с депрессией [42]. Ожирение характеризуется высоким уровнем ключевых цитокинов патогенеза псориаза – ИЛ-17 и ИЛ-23 [43, 44] и является негативным предиктором эффективности терапии псориаза [45]. В ходе анализа данных, полученных при наблюдении за 19 372 пациентами с различными иммуноопосредованными воспалительными заболеваниями, включая псориаз и псориатический артрит, установлено, что вероятность неэффективности терапии у пациентов с ожирением достигает 60% (относительный риск 1,60; ДИ 95% 1,39–1,83) [46]. У представленного нами пациента диагностировано ожирение первой степени (индекс массы тела 31), что, в свою очередь, усугубило течение и псориаза, и депрессии. Однако ответ на проводимую терапию ингибитором ИЛ-23 гуселькумабом был достаточно высоким.
Клинические исследования псориаза, посвященные изучению различных терапевтических средств, показали улучшение течения депрессии при системной противовоспалительной терапии. Однако данные в этой области относительно скудны, так как лишь в немногих опорных исследованиях на сегодняшний день использовали психометрические шкалы для оценки качества жизни в целом и депрессивных симптомов в частности [47, 48]. Исследования с использованием дерматологического индекса качества жизни (DLQI) последовательно показали, что системная терапия, особенно биологическими агентами, в целом превосходит плацебо в улучшении качества жизни, связанного с кожей. Эти данные свидетельствуют об улучшении психологического самочувствия на фоне терапии; однако у одной трети пациентов с положительным результатом скрининга на депрессию или тревогу были обнаружены невысокие баллы по DLQI, что иллюстрирует недостаточность DLQI как единственного инструмента скрининга [48].
Одним из распространенных инструментов для оценки симптомов тревоги и депрессии в клиническом контексте является госпитальная шкала тревоги и депрессии (HADS). Эту шкалу использовали, например, в исследованиях PHOENIX, AMAGINE-1 [49], VOYAGE [50], в которых сообщалось о значительном улучшении симптомов тревоги и депрессии на фоне лечения устекинумабом, бродалумабом и гуселькумабом соответственно по сравнению с группами плацебо. Еще одним хорошо известным методом оценки депрессивных симптомов является шкала депрессии Бека (BDI). Эту шкалу использовали в двух более ранних исследованиях по оценке эффективности этанерцепта [51, 52] и отмечали улучшение показателей BDI в течение курса лечения [53]. Кроме того, противовоспалительное лечение продемонстрировало антидепрессивный эффект у пациентов с воспалительными заболеваниями. В нашей работе мы расширили перечень инструментов для оценки симптомов депрессии, используя шесть шкал опросников депрессии. В результате по всем депрессивным шкалам зафиксированы максимальные показатели депрессии, за исключением Колумбийской суицидальной шкалы (C-SSRS), которая оказалась в нашем случае неинформативна/неприменима, так как пациент отказался отвечать на вопросы анкеты.
Стоит отметить, что широкий скрининг пациентов с псориазом на наличие психических расстройств и проблем с психическим здоровьем в целом еще не получил должного развития [54]. Одной из причин, препятствующих скринингу пациентов с псориазом на сопутствующие психологические расстройства, может быть то, что направление к психиатру часто затруднено и связано с длительным ожиданием; следовательно, некоторые дерматологи могут не узнать, что их пациенты нуждаются в психологической помощи. Другим фактором, объясняющим отсутствие скрининга в клинической практике, может быть отсутствие установленного инструмента скрининга для оценки сопутствующих психических заболеваний, который последовательно рекомендуется. Инструментом для дерматологической практики, рекомендованным, по крайней мере, Немецкой национальной конференцией по здравоохранению при псориазе, является тест с двумя вопросами (PHQ-2) [55–57]. Если пациенты отвечают «да» на оба вопроса, показано направление к лечащему врачу или, предпочтительно, к психиатру или психотерапевту для клинического выявления формальных диагностических критериев. Однако, насколько нам известно, этот инструмент скрининга не использовали ни в одном из исследований лечения.
При назначении системной биологической терапии дерматолог должен учитывать, что назначать блокаторы рецепторов ИЛ-17 и низкомолекулярного апремиласта пациентам с депрессией и/или суицидальными мыслями (в анамнезе) требуется с осторожностью [58].
В представленном клиническом случае у пациента на фоне применения системной биологической терапии ингибитором ИЛ-23 (гуселькумабом) отмечено полное разрешение высыпаний и отсутствие депрессивной симптоматики. Выбор препарата из группы ингибиторов ИЛ-23 в данном случае был обусловлен ранее полученными данными по эффективности применения гуселькумаба у больных псориазом. Улучшение показателей по всем депрессивным шкалам, используемым в исследовании, у пациента было ассоциировано с разрешением псориатических высыпаний на коже лица, туловища и конечностей.
Заключение
Представленный клинический случай подтверждает высокую эффективность (достижение стойкой ремиссии) и безопасность применения гуселькумаба, что существенно меняет качество жизни в положительную сторону. Важно отметить, что у больных псориазом не всегда очевидны депрессивные проявления, в то время как многие из них осознают прогноз, течение заболевания и выбор терапии. Тревожно-депрессивные расстройства усугубляют тяжесть течения псориаза, степень социальной и трудовой дезадаптации пациента. Будущие исследования должны будут способствовать консенсусу по конкретным инструментам скрининга для обеспечения сопоставимости между исследованиями и клинической практикой. Установление комплексного скрининга на психическую коморбидность необходимо в дерматологической практике. С учетом такого большого количества сопутствующих психических заболеваний интегративное ведение пациентов с псориазом в дерматологической практике имеет важное значение. Препарат гуселькумаб (ингибитор ИЛ-23) показал высокую эффективность при тяжелом течении псориаза с сопутствующей депрессией с достижением полного очищения от псориатического процесса к восьмой неделе терапии и полного устранения симптомов депрессии без дополнительного назначения антидепрессантов.
Авторы заявляют об отсутствии конфликта интересов.
I.S. Vladimirova, PhD, A.Yu. Bermas
Saint Petersburg State University
Military Medical Academy named after S.M. Kirov, Saint Petersburg
Dermatovenerologic Dispensary No. 10 – Clinic of Dermatology and Venereology, Saint Petersburg
Contact person: Irina S. Vladimirova, ivladimirva@rambler.ru
Mental disorders in psoriasis have become the subject of active study in recent years. The prevalence of comorbid depression among patients with psoriasis is quite high, in cases of more severe psoriasis even higher. It was previously believed that stigmatizing experiences were primarily responsible for this association. However, evidence is now accumulating that overlapping biological mechanisms contribute to the close association between psoriasis and depression. Elevated levels of pro-inflammatory cytokines are present in psoriasis and depression, indicating that inflammation may represent a pathophysiological link between both diseases. It is important to note that in patients with psoriasis, depressive manifestations are not always obvious, while they determine a lot in the prognosis, course of the disease, and in the choice of therapy. Treatment with systemic biologics is aimed at reversing the clinical manifestations, but they may also play an important role in reducing concomitant depressive symptoms in patients with psoriasis. We present a patient with severe psoriasis and comorbid depression, against which the patient refused therapy. In the course of monitoring the patient, questionnaire scales were used to diagnose depression. In the article, we discuss the impact of depression on the course of psoriasis and the choice of effective therapy. A description of the observation of a patient with severe psoriasis, comorbid depression and the effectiveness of guselcumab (an IL-23 inhibitor) in this matter is presented.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.