Оценка эффективности и безопасности применения севеламера карбоната для лечения гиперфосфатемии у больных, получающих гемодиализ. Результаты проспективного открытого многоцентрового исследования
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – определить среднюю суточную дозу севеламера карбоната, необходимую для достижения целевого уровня сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль, в условиях реальной клинической практики у пациентов с хронической болезнью почек (ХБП), находящихся на гемодиализе.
Материал и методы. В двух российских нефрологических центрах проводили проспективное открытое несравнительное локальное многоцентровое исследование, которое состояло из четырех периодов: двухнедельный скрининговый период, двухнедельный период отмывки, 12-недельный период титрации дозы препарата и 12-недельный период терапии (период активного контроля). Начальную дозу севеламера карбоната определяли в соответствии с исходным уровнем фосфора в сыворотке крови: 2,4 г в сутки для больных с уровнем фосфора 1,78–2,42 ммоль/л (5,5–7,5 мг/дл) и 4,8 г в сутки при уровне фосфора > 2,42 ммоль/л (> 7,5 мг/дл). Дозу севеламера карбоната в течение периода лечения титровали в зависимости от уровня фосфора в сыворотке с параллельным контролем у больных уровней кальция и паратгормона (ПТГ). Нежелательные явления (НЯ) оценивали с момента получения информированного согласия и до окончания исследования.
Результаты. В исследование были рандомизированы 94 пациента (52 пациента с начальным уровнем фосфора 1,78–2,42 ммоль/л и 42 пациента с уровнем фосфора > 2,42 ммоль/л). Из 94 рандомизированных пациентов исследование завершили 86 (91,5%) человек. Средний уровень фосфора в сыворотке последовательно снижался у всех пациентов с 2,43 ± 0,65 до 1,67 ± 0,47 ммоль/л (p < 0,0001). В группе пациентов с максимальным уровнем фосфора до 2,42 ммоль/л средний уровень фосфора снизился с 1,92 ± 0,23 до 1,62 ± 0,31 ммоль/л (p < 0,0001). У пациентов с высоким уровнем фосфора (более 2,42 ммоль/л) средний уровень фосфора снизился с 3,05 ± 0,33 до 1,72 ± 0,44 ммоль/л (p < 0,0001). Средняя суточная доза севеламера карбоната в двух группах пациентов составила 5,63 ± 1,98 г. К концу исследования статистически достоверно снизился уровень скорр.Са с 2,27 ± 0,12 до 2,04 ± 0,11 ммоль/л (р < 0,001), уровень ПТГ не изменился. Все связанные с приемом исследуемого препарата НЯ были ожидаемы на основании ранее проведенных исследований и проявлялись в виде желудочно-кишечных нарушений (тошнота и запор).
Заключение. Применение севеламера карбоната позволило достоверно снизить уровень фосфора у всех пациентов, получающих гемодиализ, а у большинства пациентов были достигнуты целевые уровни фосфора в крови. Данные результаты свидетельствуют о том, что применение севеламера карбоната эффективно и безопасно у пациентов с ХБП и гиперфосфатемией.
Цель исследования – определить среднюю суточную дозу севеламера карбоната, необходимую для достижения целевого уровня сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль, в условиях реальной клинической практики у пациентов с хронической болезнью почек (ХБП), находящихся на гемодиализе.
Материал и методы. В двух российских нефрологических центрах проводили проспективное открытое несравнительное локальное многоцентровое исследование, которое состояло из четырех периодов: двухнедельный скрининговый период, двухнедельный период отмывки, 12-недельный период титрации дозы препарата и 12-недельный период терапии (период активного контроля). Начальную дозу севеламера карбоната определяли в соответствии с исходным уровнем фосфора в сыворотке крови: 2,4 г в сутки для больных с уровнем фосфора 1,78–2,42 ммоль/л (5,5–7,5 мг/дл) и 4,8 г в сутки при уровне фосфора > 2,42 ммоль/л (> 7,5 мг/дл). Дозу севеламера карбоната в течение периода лечения титровали в зависимости от уровня фосфора в сыворотке с параллельным контролем у больных уровней кальция и паратгормона (ПТГ). Нежелательные явления (НЯ) оценивали с момента получения информированного согласия и до окончания исследования.
Результаты. В исследование были рандомизированы 94 пациента (52 пациента с начальным уровнем фосфора 1,78–2,42 ммоль/л и 42 пациента с уровнем фосфора > 2,42 ммоль/л). Из 94 рандомизированных пациентов исследование завершили 86 (91,5%) человек. Средний уровень фосфора в сыворотке последовательно снижался у всех пациентов с 2,43 ± 0,65 до 1,67 ± 0,47 ммоль/л (p < 0,0001). В группе пациентов с максимальным уровнем фосфора до 2,42 ммоль/л средний уровень фосфора снизился с 1,92 ± 0,23 до 1,62 ± 0,31 ммоль/л (p < 0,0001). У пациентов с высоким уровнем фосфора (более 2,42 ммоль/л) средний уровень фосфора снизился с 3,05 ± 0,33 до 1,72 ± 0,44 ммоль/л (p < 0,0001). Средняя суточная доза севеламера карбоната в двух группах пациентов составила 5,63 ± 1,98 г. К концу исследования статистически достоверно снизился уровень скорр.Са с 2,27 ± 0,12 до 2,04 ± 0,11 ммоль/л (р < 0,001), уровень ПТГ не изменился. Все связанные с приемом исследуемого препарата НЯ были ожидаемы на основании ранее проведенных исследований и проявлялись в виде желудочно-кишечных нарушений (тошнота и запор).
Заключение. Применение севеламера карбоната позволило достоверно снизить уровень фосфора у всех пациентов, получающих гемодиализ, а у большинства пациентов были достигнуты целевые уровни фосфора в крови. Данные результаты свидетельствуют о том, что применение севеламера карбоната эффективно и безопасно у пациентов с ХБП и гиперфосфатемией.
Введение
Основной причиной летальности как в общей популяции, так и у больных с хронической болезнью почек (ХБП) являются сердечно-сосудистые заболевания, которые ассоциируются с гиперфосфатемией. У больных ХБП при нарушении функции почек происходит снижение экскреции фосфора, которое стимулирует рост уровня FGF-23 и паратгормона (ПТГ). У больных ХБП развивается симптокомплекс минеральных и костных нарушений. Фосфат-биндеры, применяемые для снижения уровня фосфора, снижают всасывание фосфора в кишечнике и уровень фосфора в крови. В проспективных обсервационных исследованиях (DOPPS и COSMOS) показано, что применение фосфат-биндеров способствует снижению как общей смертности, так и смертности от сердечно-сосудистых заболеваний [1, 2]. Применение фосфат-биндеров, содержащих Са и свободных от Са, с одинаковой эффективностью снижает уровень фосфора при адекватной дозировке. Метаанализ 11 рандомизированных исследований (4622 пациента) по применению фосфат-биндеров показал 22%-ное снижение общей летальности у пациентов, применявших свободный от Са фосфат-биндер, по сравнению с больными, получавшими Са-содержащие фосфат-биндеры [3]. Фосфат-биндеры, не содержащие Са, снижают не только уровень фосфора, но и уровень FGF-23, что непосредственно приводит к гипертрофии миокарда и увеличению смертности [4]. Международные рекомендации предлагают ограничить дозу фосфатсвязывающих препаратов на основе кальция [5]. Севеламер – наиболее часто используемый фосфат-биндер у больных с ХБП. Севеламер (свободный от Са фосфат-биндер) – катионный полимер смолы, молекулярный вес 1,016 Da – предотвращает абсорбцию Р, связываясь с ним в желудочно-кишечном тракте [6, 7]. Севеламер имеет клинически предпочтительный профиль безопасности в сравнении с другими фосфат-биндерами на основе кальция, он не всасывается и, следовательно, не способствует появлению катион-индуцированной токсичности [8]. Имеются две солевые формы севеламера – гидрохлоридная и карбонатная. Карбонат севеламера лучше переносится больными, чем севеламера гидрохлорид, так как не способствует развитию метаболического ацидоза [9, 10]. С учетом противоречивых данных об эффективности севеламера карбоната требуется уточнение необходимой дозы препарата для достижения целевых уровней фосфора в крови [11].
Цель исследования – определение средней суточной дозы севеламера карбоната, необходимой для достижения целевого уровня сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль, в условиях реальной клинической практики у пациентов с ХБП, находящихся на гемодиализе.
Материал и методы
Исследование было проведено в двух диализных центрах России (Городская клиническая больница им. С.П. Боткина и Медицинский центр «Диалог»). Каждый пациент, включенный в исследование, подписывал информированное согласие на участие.
Критерии включения в исследование:
- пациенты мужского и женского пола в возрасте от 18 до 85 лет включительно на момент подписания формы информированного согласия;
- пациенты, находящиеся на гемодиализе по поводу хронической почечной недостаточности (с анурией или без анурии) на протяжении более трех месяцев до визита 0;
- прием пероральных фосфатсвязывающих препаратов в течение как минимум первого месяца до визита 0;
- соблюдение стабильной диеты;
- готовность пациента не принимать фосфатсвязывающие препараты на основе алюминия, магния, кальция или лантана вне зависимости от приема препаратов кальция на протяжении двух недель (период отмывки с визита 1 по визит 2);
- концентрация фосфата крови ≥ 1,0 и ≤ 4,0 ммоль/л и iPTH ≤ 1000 пг/мл на момент визита 0;
- концентрация фосфата крови после двух недель отмывки (визит 2) ≥ 1,78 ммоль/л;
- наличие подписанной формы информированного согласия на участие в клиническом исследовании;
- готовность и возможность принимать постоянную дозу витамина D (или его аналогов) и цинакальцета (этилкальцетида) в течение периода лечения, если это применимо;
- пациенты, подписавшие информированное согласие;
- пациенты, не участвовавшие в каких-либо других исследованиях изучаемых препаратов в течение 30 дней до включения в данное исследование;
- наличие соответствующего уровня понимания и готовность принимать рекомендованную дозу фосфат-биндера, сотрудничество при проведении всех визитов и процедур в соответствии с требованиями персонала исследовательского центра.
Критерии исключения из исследования:
- гиперчувствительность к севеламера карбонату или любому другому компоненту препарата;
- гипофосфатемия;
- кишечная непроходимость;
- непереносимость лактозы, дефицит лактозы, глюкозо-галактозная мальабсорбция;
- заболевания, требующие постоянного приема гормональных препаратов;
- участие в других клинических исследованиях;
- паратиреоидэктомия в течение шести месяцев до посещения скрининга (визит 0);
- активное симптоматическое желудочно-кишечное кровотечение или воспалительное заболевание кишечника;
- уровни сывороточного фосфора > 10,0 мг/дл (3,2 ммоль/л), задокументированные во всех трех ежемесячных анализах (выполняемых обычно в отделении диализа) за три месяца до скринингового посещения (визит 0);
- история злокачественных новообразований за последние пять лет;
- психическое расстройство, которое мешает пациенту соблюдать протокол исследования;
- запланированная операция или госпитализация во время испытания (разрешена операция по амбулаторному доступу по расписанию);
- любое другое заболевание, которое делает завершение исследования маловероятным или невозможным или которое может помешать оптимальному участию в исследовании или создать значительный риск для пациента;
- неспособность сотрудничать с персоналом или история несоблюдения рекомендаций.
Дизайн и план исследования
Проведено региональное двухцентровое проспективное открытое несравнительное исследование подбора необходимой дозы севеламера карбоната (Селамерекс, Сотекс, Россия) для достижения эффекта снижения уровня фосфора в параллельных группах пациентов с ХБП и гиперфосфатемией, получающих гемодиализ.
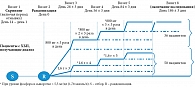
Исследование состояло из четырех периодов: двухнедельный скрининговый период, двухнедельный период вымывания (предусмотренный для пациентов, получающих на момент включения в исследование фосфатсвязывающие препараты), 12-недельный период титрации дозы препарата и 12-недельный период лечения. Севеламера карбонат в таблетках по 800 мг назначали от трех раз в сутки и чаще вместе с пищей. Начальную дозу севеламера карбоната определяли в соответствии с исходным уровнем фосфора в сыворотке крови: 2,4 г в сутки для больных с уровнем фосфора 1,78–2,42 ммоль/л (5,5–7,5 мг/дл) и 4,8 г в сутки при уровне фосфора > 2,42 ммоль/л (> 7,5 мг/дл). Дозу Селамерекса в течение периода лечения титровали в зависимости от уровня фосфора в сыворотке с повышением суточной дозы на 1,6–2,4 г (на 2–3 таблетки) на каждом запланированном визите (день 28, день 56 и день 84), если уровень фосфора в сыворотке был выше чем 5,5 мг/дл (1,78 ммоль/л). Если при измерении уровня фосфора в сыворотке во время запланированного визита полученные значения были < 1,78 ммоль/л (< 5,5 мг/дл), то дозу севеламера не изменяли до следующего визита. Максимально возможная суточная доза 14,4 г была выбрана в соответствии с результатами предшествующих исследований. В день 186 забирали последние образцы крови для определения уровня фосфора в сыворотке. Нежелательные явления (НЯ) оценивали с момента получения информированного согласия и до окончания исследования (день 186). Любые серьезные нежелательные явления (СНЯ), произошедшие в течение 30 дней после завершения исследования или прекращения участия в исследовании, также регистрировали.
Дизайн исследования представлен на рисунке.
Цели исследования
Первичная цель – определить среднюю суточную дозу севеламера карбоната, необходимую для достижения целевого уровня сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль, в условиях реальной клинической практики у пациентов с ХБП, находящихся на гемодиализе.
Вторичной целью была оценка безопасности на основании нежелательных явлений за весь период исследования.
Изучаемые препараты: севеламера карбонат 800 мг, таблетки во флаконах, по 180 таблеток в одном флаконе (Селемарекс, Сотекс, Россия). Данное исследование являлось открытым, и название лекарства не маскировалось. Препарат назначали перорально три раза в день со дня 0 до дня 186, дозу определяли по уровню фосфора.
Критерии эффективности
Первичная конечная точка: первичной целью было достижение целевого уровня сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль к концу периода лечения с определением необходимой средней суточной дозы севеламера карбоната.
Вторичная конечная точка: безопасность оценивали по нежелательным явлениям, изменению значений лабораторных параметров и основных показателей состояния организма с исходного уровня (день 0) до дня 186 (окончание исследования).
Статистические методы
Для обобщения непрерывных переменных рассчитывали число пациентов, среднее, стандартное отклонение, минимум, максимум и медиану. Для обобщения категорийных переменных рассчитывали число и процент для каждого вида лечения. Показатели описательной статистики были представлены для демографических данных и первичных характеристик всех пациентов и каждой группы лечения; показателей безопасности, включая нежелательные явления, лабораторные показатели, артериальное давление и жизненно важные показатели.
Изменение среднего уровня фосфора от исходного значения до визита 8 (день 186) анализировали и обобщали как непрерывную переменную. Для обработки статистических данных использовали программу SPSS 20 (IBM, США).
Результаты
Исследование продолжалось с июля 2020 г. до декабря 2021 г. В исследование были включены 94 пациента с ХБП, находящихся на гемодиализе, из которых у 52 больных (первая группа) уровень фосфора был 1,78–2,42 ммоль/л, у 42 больных (вторая группа) уровень фосфора был выше 2,42 ммоль/л.
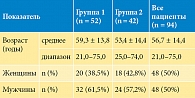
При включении в исследование средний уровень фосфора составил 2,43 ± 0,65 ммоль/л, средний возраст – 56,7 ± 14,4 года. Демографические данные представлены в табл. 1.
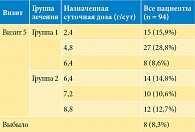
В соответствии с протоколом исследования 52 (55,3%) пациента изначально получали лечение севеламера карбонатом в дозе 2,4 г/сут и 42 (44,7%) пациента получали севеламера карбонат в дозе 4,8 г/сут. В первой группе на визите 3 34 (65,47%) пациента продолжили прием исследуемого препарата в суточной дозе 2,4 г, 18 (24,0%) пациентам потребовалось увеличение суточной дозы до 4,8 г. Во второй группе суточная доза севеламера карбоната у 21 пациента осталась прежней – 4,8 г/сут, а 21 пациенту пришлось увеличить дозу до 7,2 г/сут. В первой группе на визите 4 15 (28,9%) больных продолжили прием севеламера карбоната в дозе 2,4 г/сут, 27 (51,9%) больных получали севеламера карбонат в дозе 4,8 г/сут, 8 (14,8%) больных – в дозе 6,4 г/сут. Во второй группе на визите 4 у 14 пациентов доза севеламера карбоната составила 6,4 г/сут, у 11 пациентов – 7,2 г/сут, еще у 11 пациентов – 8,8 г/сут. На визите 5 изменения дозировки севеламера карбоната не потребовалось, больные продолжили прием в той же дозе (табл. 2).
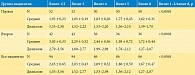
Таким образом, минимальное количество Селамерекса – 2,4 г/сут (три таблетки) – принимали только 15 из 94 (15,9%) пациентов, у остальных пациентов доза Селамерекса была выше и в среднем составила 5,6 ± 1,98 г/сут. Динамика изменений уровня фосфора за время исследования представлена в табл. 3.
У всех больных наблюдалось достоверное снижение уровня сывороточного фосфора. Целевой уровень сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль/л к концу лечения был достигнут у 75 (87,2%) пациентов. У 11 (12,7%) пациентов, не достигших целевого уровня фосфора, средний уровень фосфора к концу исследования составил 1,85 ± 0,23 ммоль/л.
К концу исследования в обеих группах статистически значимо снизился уровень скорр.Са с 2,27 ± 0,12 до 2,04 ± 0,11 ммоль/л (р < 0,001), уровень ПТГ не изменился.
Безопасность
Из 94 пациентов, включенных в анализ безопасности, у 7 (7,4%) пациентов было отмечено 10 возникших в период лечения НЯ, включая два СНЯ у 2 (2,1%) пациентов и восемь НЯ у 5 (5,3%) пациентов, которые не отвечали критериям серьезности.
Все СНЯ были расценены исследователями как не связанные с приемом севеламера карбоната. Трое (3,2%) больных отказались от дальнейшего участия в исследовании, и один пациент умер. Летальный исход явился результатом развития СНЯ (сердечно-сосудистой недостаточности). Один пациент отказался от участия в исследовании без определенной причины, двое пациентов – на фоне развития НЯ. Все связанные с приемом исследуемого препарата НЯ, возникшие в период лечения, проявлялись в виде желудочно-кишечных нарушений (тошнота и запор). Все случаи досрочного прекращения участия в исследовании были результатом желания пациентов, а не медицинских показаний безопасности по мнению исследователей.
Обсуждение
Гиперфосфатемия ассоциируется с плохими результатами лечения у больных ХБП и ухудшает выживаемость в общей популяции. Контроль фосфора в пределах нормальных значений является одной из главных задач в лечении больных с почечной недостаточностью. Применение диеты и эффективного диализа у больных, получающих заместительную почечную терапию, в большинстве случаев не позволяет контролировать уровень фосфора, поэтому назначение фосфат-биндеров, снижающих уровень фосфора в крови, играет важную роль [12, 13]. Применение недорогих кальцийсодержащих фосфат-биндеров ассоциируется с гиперкальциемией, развитием адинамической болезни кости, сосудистой и внекостной кальцификацией [14]. Средние дозы карбоната кальция и ацетата кальция в рандомизированных контролируемых исследованиях для контроля гиперфосфатемии колебались от 1,2 до 2,3 г элементарного кальция. Такие дозы способствуют положительному балансу кальция и развитию гиперкальциемии. В настоящее время в мире доступны не содержащие кальций фосфат-биндеры: севеламер, лантана карбонат, соли алюминия, магния и железа. Каждый из этих препаратов может эффективно снижать уровень фосфора, но только при использовании в адекватных дозировках, при строгой титрации и комплаентности пациентов. Вследствие разной фосфатсвязывающей способности медикаментов количество таблеток назначаемых препаратов может различаться, однако до последнего времени оно остается очень высоким. Так, в США среднее потребление фосфат-биндера составляет 7,4 ± 4,7 таблеток в сутки [15]. Y.W. Chiu и соавт. [16] сообщили о среднем ежедневном потреблении таблеток у диализных пациентов (n = 233), равном 19, при этом некоторым пациентам назначали более 25 (в среднем 11 ± 4) таблеток в день, а фосфатсвязывающие вещества составили около 50% дневной дозы таблеток. Увеличение количества принимаемых таблеток приводит к низкой приверженности пациентов лечению.
Результаты нашего исследования применения севеламера карбоната показали его эффективность в снижении уровня фосфора в крови. У всех больных, принимавших участие в исследовании, наблюдалось достоверное снижение уровня сывороточного фосфора. Целевой уровень сывороточного фосфора ≥ 1,13 и ≤ 1,78 ммоль/л к концу лечения достигнут у 75 (87,2%) пациентов. Из 86 завершивших участие в исследовании пациентов 80 (93,0%) имели хорошую приверженность лечению.
Уровень фосфора в сыворотке последовательно снижался у пациентов первой группы с максимальным уровнем фосфора до 2,42 ммоль/л со среднего уровня 1,92 ± 0,23 ммоль/л на визите 1/2 до 1,62 ± 0,31 ммоль/л на визите 8 (p < 0,0001). Во второй группе пациентов с уровнем фосфора < 2,42 ммоль/л средний уровень фосфора снизился с показателей 3,05 ± 0,33 ммоль/л на визите 1/2 до 1,72 ± 0,44 ммоль/л на визите 8 (p < 0,0001). При этом достоверное снижение уровня фосфора отмечалось как в группе с исходно высоким уровнем фосфора, так и в группе с исходно более низким уровнем фосфора < 2,42 ммоль/л (p < 0,0001). В двух исследуемых группах исходно средний уровень фосфора составил 2,43 ± 0,65 ммоль/л, к концу исследования он достоверно снизился до 1,67 ± 0,47ммоль/л (p < 0,0001). Хорошие результаты лечения были достигнуты за счет строгого отбора пациентов по критерию сотрудничества, выполнения рекомендаций. Минимальную дозу Селамерекса 2,4 г/сут (три таблетки) принимали 15 (15,9%) из 94 пациентов, у остальных больных доза Селамерекса была выше и в среднем составила 5,6 ± 1,98 г/сут.
Кроме того, было выявлено достоверное снижение уровня кальция в обеих группах (2,27 ± 0,12 до 2,04 ± 0,11 ммоль/л, р < 0,001). Данный эффект севеламера также отмечен и в недавнем метаанализе J. Phannajit и соавт. [17]. В этом же метаанализе было зафиксировано снижение общей летальности и числа госпитализаций вследствие применения севеламера по сравнению с другими фосфат-биндерами, что, на наш взгляд, могло быть обусловлено снижением кальция. Так, в работе H.K. Sawires и соавт. [18] была отмечена обратная связь между уровнем кальция и белком Клото, а повышение уровня белка Клото всегда способствует снижению летальности [19]. Известно и благоприятное влияние севеламера на уровень липидов в крови, однако наше исследование не было посвящено этому аспекту. Требуются дополнительные исследования по изучению влияния севеламера на уровни белка Клото, FGF-23, уточнение их взаимосвязи с эффективной дозой лекарства.
В целом севеламера карбонат обладал благоприятным профилем безопасности при применении у пациентов с ХБП. Частота развития связанных с приемом исследуемого препарата НЯ, согласно данным, полученным в проведенных ранее исследованиях, была ожидаемо невысокой и сводилась к проявлениям со стороны желудочно-кишечного тракта (запор, тошнота). Ни одно из возникших в ходе исследования СНЯ не было связано с приемом исследуемого препарата. Один летальный исход на фоне развития серьезных нежелательных явлений также не был связан с приемом севеламера карбоната.
Заключение
Данное исследование продемонстрировало эффективность севеламера карбоната для снижения уровня фосфора при его должной титрации. Целевой уровень сывороточного фосфора к концу лечения достигнут у 87,2% больных при средней дозировке препарата 5,6 ± 1,98 г/сут. Профиль безопасности был сопоставимым с результатами предшествующих исследований и укладывался в рамки известного профиля безопасности севеламера карбоната. В группе пациентов с изначально высоким уровнем фосфора эффект достигался благодаря назначению более девяти таблеток в сутки (7,2 г), что диктует необходимость использования других форм препарата (в виде порошка с большим содержанием препарата) у этой категории больных.
E.V. Shutov, PhD, Prof., I.V. Svechka, E.E. Lukina, S.M. Keroglyan, G.V. Kotlyarova, K.M. Lysenko
S.P. Botkin City Clinical Hospital
Russian Medical Academy of Continuous Professional Education
‘Dialog’ Medical Center
Contact person: Evgeny V. Shutov, shutov_e_v@mail.ru
Sevelamer carbonate is a non-intestinal, calcium-free phosphate binder. Sevelamer carbonate controls hyperphosphatemia in dialysis and non-dialysis patients with renal insufficiency, without the concomitant risk of hypercalcemia. The phosphate-binding ability of this drug is clearly dose-dependent, and its lack of effectiveness in some patients may be associated with receiving it in an insufficient dose. Our study aimed to determine the average daily dose of sevelamer carbonate required to achieve a target serum phosphorus level of ≥ 1.13 and ≤ 1.78 mmol in real clinical practice in patients with chronic kidney disease (CKD) on hemodialysis.
Material and methods. The study was a prospective, open-label, non-comparative, local, multicenter study conducted at 2 nephrology centers in the Russian Federation. The study consisted of 4 periods: a 2-week screening period, a 2-week washout period, a 12-week dose titration period, and a 12-week therapy period (active control period). The initial dose of sevelamer carbonate was determined in accordance with the initial level of phosphorus in the blood serum: 2.4 g per day for patients with a phosphorus level of 1.78–2.42 mmol/l (5.5–7.5 mg/dl), and 4.8 g per day for patients with a phosphorus level > 2.42 mmol/l (> 7.5 mg/dl). The dose of sevelamer carbonate during the treatment period was titrated according to serum phosphorus levels. In patients, the levels of Ca and PTH were also monitored. Adverse events (AEs) were assessed from the time the informed consent was obtained until the end of the study.
Results. 94 patients were randomized to the study (52 patients with baseline P 1.78–2.42 mmol/l and 42 patients with P > 2.42 mmol/l). Of the 94 randomized patients, 86 (91,5%) completed the study. Serum phosphorus levels consistently decreased in all patients from a mean level of 2.43 ± 0.65 to 1.67 ± 0.47 mmol/l (p < 0.0001). In the group of patients with a maximum P level of up to 2.42 mmol/l, the average phosphorus level decreased from 1.92 ± 0.23 to 1.62 ± 0.31 mmol/l (p < 0.0001). In patients with high P levels (more than 2.42 mmol/l), the mean phosphorus level decreased from 3.05 ± 0.33 to 1.72 ± 0.44 mmol/l (p < 0.0001). The average daily dose of sevelamer carbonate in 2 groups of patients was 5.63 ± 1.98 g, by the end of the study. The level of adjusted Ca decreased statistically significantly from 2.27 ± 0.12 to 2.04 ± 0.11 mmol/l (p < 0.001), the PTH level did not change. All study drug-related adverse events included gastrointestinal manifestations (nausea and constipation) and were expected based on previous studies.
Conclusions. The use of sevelamer carbonate allowed to significantly reduce the level of phosphorus in all patients receiving hemodialysis, and in most patients the target levels of phosphorus in the blood were achieved. These results indicate that the use of sevelamer carbonate is effective and safe in patients with CKD and hyperphosphatemia.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.