Патогенетическое и клиническое значение тизанидина в терапии анкилозирующего спондилита
- Аннотация
- Статья
- Ссылки
- English
Анкилозирующий спондилоартрит (АС) является основной формой воспалительных заболеваний позвоночника и занимает господствующее положение среди других спондилоартритов. АС характеризуется хроническим прогрессирующим течением и приводит к анкилозированию илеосакральных и межпозвонковых суставов, обызвествлению спинальных связок и ограничению подвижности позвоночника, как следствие, происходит ранняя инвалидизация больных.
Спектр патологических изменений при АС не ограничивается только заинтересованностью осевого скелета. Для АС характерны артриты периферических суставов (асимметричный олигоартрит), прежде всего тазобедренных, коленных, голеностопных и плечевых суставов, что наблюдается у каждого третьего больного. Одно из наиболее типичных проявлений всех спондилоартритов – энтезиты – обнаруживается у 25–40% больных АС, при этом чаще всего в патологический процесс вовлекаются ахиллово сухожилие, плантарная фасция, соединение рукоятки с телом грудины, лобковый симфиз, область прикрепления связок к остистым отросткам, вертелы бедренной кости, надколенники, ключицы и пяточные кости (место прикрепления ахиллова сухожилия и подошвенного апоневроза) [1]. Нередко встречается остеопороз позвоночника, который приводит к его переломам у больных молодого возраста [2]. Системные проявления характеризуются поражением сердца (аортит, формирование органических пороков сердца (в 1–10% случаев), нарушение ритма и сердечной проводимости, а также относительно высокий риск развития атеросклероза венечных и других сосудов), легких (рестриктивная и обструктивная дыхательная недостаточность, апикальный фиброз легких), почек (IgA-нефропатия, АА-амилоидоз), глаз (у 25–30% больных развивается острый передний увеит с острой болью, снижением остроты зрения, последующим формированием синехий и глаукомы) [3].
АС обычно начинается в молодом возрасте, а его развитие после 45 лет наблюдается крайне редко. Средний возраст дебюта этой болезни приходится на 24 года [4]. Это заболевание чаще встречается у мужчин. Считается, что хотя АС нередко страдают и женщины, но у них заболевание обычно протекает более доброкачественно и не приводит к выраженной деформации позвоночника. Некоторые авторы, напротив, не находят существенного различия в клинических проявлениях и течении этого заболевания в зависимости от половой принадлежности больных. Если учитывать все случаи АС, включая его латентное течение, то соотношение мужчин и женщин составляет 2:1 или 3:1. Распространенность АС ассоциируется с частотой встречаемости антигена НLA-B27 среди населения и варьирует в широких пределах – от 0,15% в Финляндии до 1,4% в Норвегии. В некоторых регионах этот показатель еще выше (2,5% среди взрослого населения эскимосов Аляски), но в среднем составляет 1:200 взрослого населения, или 0,05% [5].
Рассматривая различные аспекты диагностики и лечения спондилоартритов, в первую очередь следует отметить их позднюю выявляемость, что затрудняет своевременное проведение адекватной патогенетической терапии. Согласно данным зарубежных авторов, достоверный диагноз АС устанавливается у мужчин в среднем через 8,4 года, а у женщин – только через 9,8 года после появления первых симптомов заболевания [4]. Отечественными исследователями получены аналогичные показатели [6]. Поздняя диагностика АС обусловлена низким уровнем осведомленности врачей первичного звена об особенностях клинических проявлений и клинической гетерогенности АС и других спондилоартритов.
Первостепенное значение в диагностике АС имеют общепринятые диагностические критерии, но должны учитываться и другие характерные проявления. При диагностировании АС следует иметь в виду такие факторы, как возможность его субклинического течения, постепенное начало заболевания у лиц молодого возраста, высокая заболеваемость мужчин, асимметричный моно- или олигоартрит средних и крупных суставов нижних конечностей, болезненность при пальпации пояснично-крестцовых суставов, ощущение скованности в пояснице, ранние признаки двустороннего сакроилеита (рентгенографические или по данным магнитно-резонансной томографии). Неправильная диагностика во многом связана с поздним появлением характерных рентгенологических изменений в крестцово-подвздошных суставах и позвоночнике и с трудностями в их интерпретации. Кроме того, зачастую неправильно интерпретируются симптоматика опорно-двигательного аппарата или системные проявления, а также воспалительная боль в позвоночнике – один из наиболее информативных симптомокомплексов этого заболевания. С введением магнитно-резонансной томографии появилась возможность ранней диагностики АС, до появления его рентгенологических стигматов, и прежде всего сакроилеита.
Для заболеваний группы спондилоартритов характерны общность морфологических изменений, ассоциация с HLA-B27 и схожесть ответа на лекарственные препараты. Так, при всех спондилоартритах наблюдается более высокая эффективность локальной терапии глюкокортикостероидами по сравнению с системным применением и низкая эффективность пульс-терапии сверхвысокими дозами метилпреднизолона. При АС отмечается неэффективность метотрексата, как и других иммунодепрессантов, лишь при псориатическом артрите наблюдается симптоматический эффект метотрексата без его активного влияния на рентгенологическое прогрессирование артрита и спондилита.
Чем объясняются вышеприведенные особенности? Прежде всего они связаны с заинтересованностью энтезисов. В настоящее время энтезис рассматривается как самостоятельный орган с особенностями патоморфологии и иммунологии и высокой метаболической активностью. При АС, как и при других спондилоартритах, первичным и основным плацдармом патологического процесса являются энтезисы и кость с развитием энтезита и остита, а синовит рассматривается как следствие распространения патологического процесса на синовиальную оболочку, то есть является вторичным по отношению к пораженным энтезисам [7]. Показано, что уже на ранней стадии развития энтезита имеются макрофагальные и воспалительные инфильтраты с большим количеством Т-лимфоцитов, которые локализуются в близлежащем волокнистом хряще и, в меньшей степени, в кости. При АС наблюдаются энтезиты как на периферии, так и в позвоночнике, причем кокситы и формирование синдесмофитов можно рассматривать как частный вариант распространенной энтезопатии.
Особенности патоморфологических изменений при АС определяют ответ больных на лекарственные препараты. Можно сказать, что при этом заболевании отсутствуют базисные противовоспалительные препараты, за исключением сульфасалазина, который оказывает слабовыраженное положительное действие на артрит периферических суставов, но не на воспалительный процесс в позвоночнике. В этой связи особенно большое значение приобретают симптоматические средства, прежде всего нестероидные противовоспалительные препараты (НПВП). НПВП при АС не только уменьшают боль в позвоночнике и суставах и снижают воспалительную активность, но и тормозят рентгенологическое прогрессирование в осевом скелете [8, 9]. В проспективном исследовании изучалось влияние длительной терапии НПВП на динамику рентгенологических изменений у 215 больных, которые принимали целекоксиб по 200 мг/сут в течение 52 недель. Оказалось, что у больных, принимавших целекоксиб регулярно, рентгенологическая динамика в позвоночнике была выражена в 4 раза меньше по сравнению с группой больных, принимающих НПВП по своему усмотрению. В другом исследовании у 150 больных АС рентгенологическое прогрессирование (по индексу mSASSS – modified Stoke Ankylosing Spondylitis Spine Score) оказалось почти в 4 раза меньше в группе непрерывного приема НПВП по сравнению с группой приема НПВП по требованию, при этом препарат принимали 2 года. Эти данные представляют большой интерес и позволяют рассматривать НПВП как средства патогенетического действия при АС, но не при ревматоидном артрите или каких-либо других заболеваниях опорно-двигательного аппарата.
АС характеризуется выраженной гетерогенностью и многообразием течения. Однако в клинической картине доминируют два основных проявления – боль воспалительного типа и ригидность. Согласно критериям ASAS (Assessment of SpondyloArthritis international Society – Международное общество по спондилоартритам), боль воспалительного типа в спине характеризуется постепенным началом, развитием до 40-летнего возраста, уменьшением после физической нагрузки, отсутствием улучшения в покое и болями в ночные часы [10]. Динамика воспалительной боли в позвоночнике является одним из критериев ответа на проводимую терапию и критерием ремиссии этого заболевания.
Причинами болевого синдрома при АС являются воспалительные изменения в периферических, корневых и крестцово-подвздошных суставах, а также в межпозвонковых суставах, телах позвонков, связках позвоночника, межпозвонковых дисках (дисцит). Как известно, все структуры позвоночного столба, за исключением костной ткани, содержат нервные окончания. Свободные нервные окончания, выполняющие функцию болевых рецепторов, выявлены в капсулах межпозвонковых суставов, задней продольной и межостистой связках, периосте позвонков, стенках артериол и вен, сосудах паравертебральных мышц, наружной трети фиброзного кольца межпозвоночных дисков. Деформация позвоночника при АС приводит к сдавлению и, как следствие, к болям [5].
Дорсалгии при этом заболевании могут быть проявлением вертеброгенного корешкового синдрома (радикулопатия) или рефлекторных болевых синдромов. Возможны и другие причины развития дорсалгии при АС, например спондилолистез, остеопороз или несостоятельность структур, обеспечивающих вертикальное положение тела. Причинами стеноза позвоночного канала при АС могут быть задние остеофиты, грыжи межпозвонковых дисков, вторичный артроз межпозвонковых (фасеточных) суставов, явления спондилеза.
Не меньшее значение, чем боль, имеет и такое клиническое проявление АС, как ригидность (скованность). В начале заболевания этот симптом определяется только в пояснице, а в дальнейшем распространяется на весь осевой скелет. Ригидность обычно наблюдается в ранние утренние часы, но у некоторых больных с высокой активностью воспалительного процесса она сохраняется на протяжении всего дня. Наличие воспалительного процесса в позвоночнике вызывает рефлекторное напряжение мышц спины, что, в свою очередь, приводит к изменению осанки и деформации позвоночника (нивелируется физиологический лордоз в поясничном отделе позвоночника, подчеркивается кифоз грудного отдела и развивается гиперлордоз шейного отдела). В далеко зашедших случаях формируется характерная для больных АС «поза просителя», определяются положительный симптом Форестье, высокие значения теста Томайера и значительные нарушения функциональной способности позвоночника. Деформация позвоночника поддерживается не только структурными изменениями в суставах позвоночника, его связках и непосредственно в телах позвонков, но и гипертонусом мышц спины.
Выраженность и длительность ригидности адекватно отображают активность воспалительного процесса при АС, причем в большей степени, чем такие общепринятые лабораторные тесты, как СОЭ и С-реактивный белок, а ее динамика, как и динамика боли, имеет большое значение в оценке эффективности проводимой терапии. Анализ этих двух основных симптомов важен для оценки воспалительной активности АС, так как при этом заболевании нет адекватных лабораторных тестов ее определения, а значения реактантов острой фазы далеко не всегда совпадают с выраженностью тканевых изменений. В настоящее время основным инструментом для оценки активности АС принят индекс BASDAI (Bath Ankylosing Spondylitis Disease Activity Index), в который включено 6 пунктов, 5 из них касаются выраженности боли, а также выраженности и продолжительности утренней ригидности. Интенсивность и длительность ригидности обычно соответствуют интенсивности болей в суставах и позвоночнике, подчеркивая их единый генез.
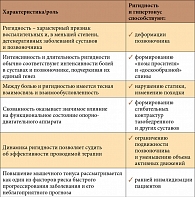
При АС нередко имеют место рефлекторные (мышечно-тонические) синдромы, которые обусловлены раздражением рецепторов в ответ на изменения в дисках, связках и суставах позвоночника. Импульсы от рецепторов достигают двигательных нейронов спинного мозга, что сопровождается повышением тонуса соответствующих мышц. Одним из симптомов такой дисфункции является симптом «вожжей», обусловленный спазмом длинных мышц спины. Спазмированные мышцы приводят к ограничению подвижности определенного сегмента позвоночника, а также становятся вторичным источником боли, запуская порочный круг «боль – мышечный спазм – боль» и способствуя формированию миофасциального синдрома. Следует отметить, что в генезе развития контрактур и фиброза мышц также принимает участие гипертонус поперечно-полосатой мускулатуры. Некоторые авторы рассматривают повышение мышечного тонуса как один из факторов риска быстрого прогрессирования функциональной недостаточности позвоночника при этом заболевании. О значении мышечно-тонического компонента при АС свидетельствуют хорошие результаты эпидуральной анестезии, которая приводит к существенному увеличению объема движений в позвоночнике даже у безнадежных в функциональном отношении больных. Подчеркнем: выраженная и длительная ригидность рассматривается как фактор риска неблагоприятного течения АС, а также как фактор, способствующий хронизации боли. Значение ригидности и повышенного мышечного тонуса при АС и взаимосвязь этих симптомов с болевым синдромом показаны в таблице.
Для купирования ригидности или существенного уменьшения ее интенсивности и длительности используют миорелаксанты. Кроме того, они снижают мышечный гипертонус и уменьшают тоническое напряжение мышц, что способствует уменьшению боли и увеличению объема движений в суставах и позвоночнике. У больных АС наблюдается и рефлекторное напряжение мышц, которое, в свою очередь, еще в большей мере способствует ограничению подвижности позвоночника, вызванного прежде всего структурными изменениями. В этих случаях применение миорелаксантов увеличивает амплитуду движений в позвоночнике и периферических суставах, что и делает их назначение целесообразным. Отметим, что рефлекторное напряжение мышц создает неблагоприятные условия для кровоснабжения тканей, что способствует усугублению метаболических расстройств.
Особое место среди миорелаксантов занимает тизанидин – эффективный препарат для лечения мышечно-тонических синдромов и миофасциального болевого синдрома, спастичности различного генеза [11]. Тизанидин относится к миорелаксантам центрального действия и является агонистом a2-адренергических рецепторов. Препарат реализует свой эффект на спинальном и супраспинальном уровнях. Тизанидин снижает мышечный тонус за счет стимулирующего действия на моноаминергетические ядра ствола головного мозга. Это приводит к угнетению полисинаптических рефлексов спинного мозга, ответственных за гипертонус мышц, и подавлению передачи возбуждения через них, что вызывает снижение повышенного тонуса сгибательной и разгибательной мускулатуры и уменьшение болезненных мышечных спазмов [12].
Особенностью этого препарата является сочетание миорелаксирующего и анальгетического эффектов, при этом уменьшение выраженности боли обусловлено не только расслаблением мышц, но и непосредственным центральным анальгетическим действием [13]. Предполагают, что в его основе лежит непрямое антиноцицептивное действие, осуществляемое через неопиоидную нейрональную систему. Привыкания к анальгетическому действию препарата при длительном применении не развивается. Тизанидин также обладает противовоспалительной активностью и потенцирует действие НПВП [14].
Тизанидин применяется внутрь по 2–4 мг. Суточная доза подбирается индивидуально, при этом всегда следует начинать лечение с небольших доз. При АС, как правило, применяется не больше 4 мг/сут. При выраженной утренней скованности целесообразно назначение дополнительно 2 или 4 мг на ночь. Более яркий терапевтический эффект наблюдается при одновременном назначении миорелаксантов с НПВП, тем более что такая сочетанная терапия снижает риск развития нежелательных явлений на фоне приема НПВП. Возраст и пол больных, а также прием пищи не влияют на фармакокинетику тизанидина.
Тизанидин снижает мышечный тонус, уменьшая лишь его тонический компонент, что способствует сохранению, а в ряде случаев и повышению мышечной силы. Это выгодно отличает его от толперизона и баклофена, которые не обладают этими свойствами. Благодаря такой особенности и отчетливому обезболивающему действию тизанидин повышает повседневную активность больных и улучшает качество их жизни. При внезапной отмене препарата может произойти некоторое усиление мышечного тонуса, следовательно, необходима постепенная отмена. Синдром «рикошета» наблюдается и при быстрой отмене некоторых других миорелаксантов.
Интересным представляется гастропротективное действие тизанидина, что связано с его адренергической активностью [15]. Это тем более важно, что больные АС практически постоянно принимают НПВП и у них часто развивается медикаментозная гастропатия и энтеропатия, повышение артериального давления и другая кардиальная симптоматика, гастро- и нефротоксичность. Установлено, что тизанидин улучшает переносимость НПВП, в частности диклофенака, и усиливает их обезболивающее действие. Применение пироксикама, дифлунизала и диклофенака в комбинации с тизанидином (4 мг/сут), назначавшихся в течение 10–12 дней, показало значительное уменьшение боли и улучшение подвижности позвоночника в группе приема диклофенака и тизанидина. При этом показатели опросника Освестри, рекомендованного ВОЗ для больных с болями в спине, улучшились на 25%, а выраженность боли по визуальной аналоговой шкале (ВАШ) уменьшилась с 56 до 34 мм. Переносимость диклофенака и тизанидина при их сочетанном применении была хорошей [16].
Доказательства гастропротективного действия тизанидина получены и в многоцентровом рандомизированном клиническом исследовании, в котором участвовали 405 больных. Гастропатия была выявлена у 12% пациентов, получавших комбинацию диклофенака и тизанидина, а в группе больных, которые принимали диклофенак и плацебо, – у 32% [17]. В многоцентровом двойном слепом исследовании у пациентов с болью в нижней части спины комбинация тизанидина с ибупрофеном достоверно превосходила по эффективности комбинацию плацебо с ибупрофеном и монотерапию ибупрофеном [18].
Тизанидин в малых дозах редко приводит к нежелательным реакциям. Помимо сонливости, заторможенности и снижения концентрации внимания, может наблюдаться головокружение, сонливость, сухость во рту, повышенная утомляемость, явления кишечной диспепсии и крайне редко – повышение печеночных аминотрансфераз. На фоне приема тизанидина возможно умеренное снижение артериального давления, к тому же препарат способен потенцировать гипотензивные препараты. Снижение артериального давления наблюдается и у больных, принимающих одновременно c тизанидином ингибиторы CYP1A, например ципрофлоксацин. Возможны расстройства сна, бессонница, брадикардия, нарушения ритма сердца, удлинение интервала QT. Но в целом препарат характеризуется хорошей переносимостью как при краткосрочном, так и при длительном применении, а имеющие место нежелательные явления носят преходящий характер и не приводят к его отмене. В отличие от других миорелаксантов тизанидин не вызывает мышечной слабости, что является его большим преимуществом, и в целом обладает лучшей переносимостью [14].
Таким образом, назначение тизанидина при АС способствует быстрому регрессу боли и ригидности как в позвоночнике, так и в периферических суставах, улучшению подвижности позвоночника, существенному снижению вероятности развития контрактур и мышечных атрофий. Снижение рефлекторного мышечного напряжения улучшает двигательные функции и облегчает проведение реабилитационных мероприятий.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.