Патогенетическое обоснование реабилитации репродуктивного здоровья женщин после прерывания беременности в поздние сроки
- Аннотация
- Статья
- Ссылки
- English
Актуальность
Проблема абортов в современных демографических условиях в Российской Федерации занимает особое место. Распространенность и динамика абортов, уровень материнской смертности после искусственного прерывания беременности – это показатели, по которым оценивается эффективность государственных мер по охране репродуктивного здоровья и здоровья населения в целом [1–4]. Для нашей страны характерен низкий уровень рождаемости, на фоне которого имеет место значительное число абортов с последующими нарушениями репродуктивной функции. В этой связи важно выработать организационную систему реабилитации репродуктивного здоровья женщин после прерывания беременности, в том числе на поздних сроках, и принять эффективные меры, направленные на сохранение и улучшение репродуктивного потенциала нации [2, 5–7].
По региональным данным, 16% женщин, перенесших аборт за последние пять лет, нуждались в лечении осложнений, среди которых значительное место занимают воспалительные процессы в репродуктивных органах (50%), нарушения менструального цикла (15% у первобеременных и 40,5% у повторнобеременных) [3, 8–10].
Проведенный анализ литературы по данной проблеме дает основание утверждать, что большинство российских авторов отмечают отрицательные последствия аборта. Среди них следует выделить нарушение репродуктивной системы женщины и развитие гормонально обусловленных заболеваний, нарушение менструального цикла, травматическую истмико-цервикальную недостаточность с последующим невынашиванием беременности, воспалительные заболевания женских половых органов, вторичное бесплодие [6, 7, 11].
В то же время остаются медицинские и социальные показания, при которых прерывание беременности во втором триместре является осознанно необходимым [12, 13]. Система организации пренатального скрининга позволяет выявлять на ранних этапах гестации наличие врожденных пороков развития у плода, несовместимых с жизнью. Пилотные проекты, реализованные в четырех регионах Российской Федерации, показали хорошие результаты по снижению перинатальной и младенческой смертности в стране. Так, в Московской области, принимающей участие в пилотном проекте, младенческая смертность за последние пять лет снизилась с 7,5 до 7,0 на 1000 родившихся живыми.
При искусственном прерывании беременности во втором триместре по сравнению с первым триместром риск для здоровья женщины повышается в три-четыре раза [7, 9, 14]. Частота осложнений (ранних, отсроченных и отдаленных) пропорционально возрастает по мере увеличения срока беременности. Индуцированное прерывание беременности после 14-й недели беременности связано с резким увеличением частоты осложнений и стоимости последующей медицинской помощи [8, 12]. В России, например, на долю поздних абортов приходится до 2/3 всех осложнений и 50% всех связанных с абортами случаев материнской смертности [7, 11].
Цель исследования
Сравнительная оценка восстановления менструальной функции у женщин после прерывания беременности различными способами.
Материал и методы исследования
Для определения влияния на менструальную функцию различных методов прерывания беременности в поздние сроки было проведено обследование 75 пациенток. Они были разделены на две группы в зависимости от способа прерывания беременности: путем амниоинфузии гипертонического раствора хлорида натрия (n = 50) или простагландинов (n = 25).
Медицинскими показаниями для прерывания беременности являлись врожденные пороки развития плода, несовместимые с жизнью: сердца и сосудов (14,7%), центральной нервной системы (19,6%), желудочно-кишечного тракта (21,5%), множественные пороки (39,7%), болезнь Дауна (4,5%). Диагноз «врожденные пороки развития плода» подтвержден медико-генетическим консилиумом на основании результатов ультразвукового и инвазивных методов исследования.
Обследование пациенток проводилось с помощью общеклинических, ультразвукового, генетических, радиоиммунологического, бактериологического методов. При исследовании эндометрия использовались гистологический и иммуногистохимический методы.
Результаты исследования и их обсуждение
Наиболее важными клиническими маркерами восстановления менструального цикла являются своевременное начало и характер первой (после прерывания беременности) менструации (табл. 1). У 96% женщин первой группы первая менструация наступила через 60–90 дней. В среднем период времени от момента индуцированного выкидыша до первой менструации составил 78,2 ± 5,6 дня, причем у большинства женщин (52%) менструации были скудными, что свидетельствовало о неполноценности восстановления эндометрия. После амниоинфузии простагландинов средняя продолжительность времени до наступления первой менструации составила 46,2 ± 3,8 дня. Ни у одной пациентки после применения этого метода прерывания беременности не отмечено своевременного восстановления менструального цикла.
Для сравнительной оценки влияния различных методов прерывания беременности в поздние сроки на гормональную функцию проведено исследование сывороточного содержания гонадотропных и стероидных гормонов на 22–24-й день после индуцированного аборта.
После прерывания беременности методом амниоинфузии гипертонического раствора у 29 (58%) женщин отмечалось увеличение уровня пролактина (до 1020,6 ± 92,5 мМЕ/л), у семи (14%) – повышение уровня лютеинизирующего гормона (8,4 ± 1,2 мМЕ/л), у пяти (10%) – низкие значения фолликулостимулирующего гормона (1,1 ± 0,4 мМЕ/л); у 21 (42,0%) – сниженные уровни прогестерона (14,3 ± 2,1 нмоль/л); у 16 (32%) – одновременное снижение сывороточного содержания эстрадиола (218,6 ± 21,6 пмоль/л).
После прерывания беременности методом амниоинфузии простагландинов изменения гормональной функции яичников характеризовались прежде всего увеличением продукции пролактина до 970,6 ± 44,6 мМЕ/л у девяти (36%) женщин, снижением прогестерона до 13,2 ± 4,2 нмоль/л – у 16 (48%) женщин, эстрадиола до 324,6 ± 32,4 пмоль/л – у десяти (40%) женщин; повышением уровня лютеинизирующего гормона (10,8 ± 1,3 мМЕ/л) в сочетании с нормальными значениями фолликулостимулирующего гормона (4,5 ± 1,6 мМЕ/л) – у четырех (16%) женщин.
Таким образом, изменения гормонального статуса пациенток после прерывания беременности в поздние сроки характеризовались в основном увеличением пролактина, снижением уровней эстрадиола и прогестерона. Максимально эти изменения были выражены после прерывания беременности методом амниоинфузии с применением гипертонического раствора.
Результаты определения содержания гонадотропных и стероидных гормонов в сыворотке крови пациенток на 22–24-й день первого после прерывания беременности менструального цикла показали, что после амниоинфузии гипертонического раствора у 12 (24%) женщин сохранялась гипопродукция эстрадиола (368 ± 24 пмоль/л) и прогестерона (15,6 ± 1,8 нмоль/л). После амниоинфузии простагландинов эти изменения наблюдались у четырех (16,0%) пациенток.
Полноценность восстановления менструальной функции оценивали также по данным УЗИ. После применения амниоинфузий гипертонического раствора для прерывания беременности в поздние сроки лишь у 15 (30%) пациенток была овуляция и полноценная лютеиновая фаза цикла. У 26 (52%) пациенток при УЗИ на 22–24-й день цикла выявлена недостаточность лютеиновой фазы, на которую указывали маленькие размеры желтого тела и нарушение кровотока в яичниковой артерии. У девяти (18%) женщин были ановуляторные циклы, о чем свидетельствовали отсутствие желтого тела и выраженный спазм яичниковых артерий.
После применения амниоинфузий простагландинов восстановление овуляторного менструального цикла отмечено у 12 (48%) из 25 пациенток, недостаточность лютеиновой фазы – у 11 (44%), ановуляция – у двух (8%) пациенток (табл. 2).
Для оценки темпов восстановления эндометрия у 30 пациенток первой группы использованы пайпель-биопсии, проводимые на 22–24-й день после искусственного позднего медицинского аборта, индуцированного методом амниоинфузии гипертонического раствора.
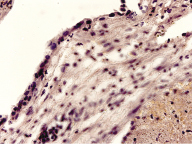
Во всех исследованных пайпель-биоптатах спустя три недели после прерывания беременности методом амниоинфузии гипертонического раствора преобладали инфицированные тромбы, некротизированные фрагменты децидуальной ткани, обрывки желез и сгустки крови. У 18 (72%) женщин в составе биоптатов выявлены небольшие фрагменты новообразованного эндометрия в виде отдельных пластов маточного эпителия. Подобный тип покровного эпителия матки характерен для начального этапа эпителизации (рис. 1). У остальных 12 (28%) женщин в фрагментах эндометрия покровный маточный эпителий отсутствовал, что отражает неполную эпителизацию внутренней поверхности матки.
Дополнительные иммуногистохимические методы исследования биоптатов подтвердили морфофункциональную несостоятельность новообразованного рецепторного аппарата в фрагментах эндометрия. Так, выявлена лишь умеренная иммуноэкспрессия рецепторов к эстрогену в ядрах эпителиоцитов желез и стромальных клеток, рецепторы к прогестерону не выявлялись в биоптатах женщин данной группы. Вместе с тем в тех пайпель-биоптатах, где обнаруживался сохранный маточный эпителий и отдельные железы, присутствовал интенсивный васкулогенез, что демонстративно представлено иммуногистохимически с помощью маркера эндотелия CD34 (табл. 3).
Следовательно, на 22–24-е сутки после медицинского аборта путем интраамниального введения 20%-ного раствора хлорида натрия эндометрий соответствовал лишь ранней стадии пролиферации, то есть пятому-шестому дню нормального цикла.
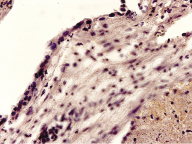
У 20 пациенток второй группы в пайпель-биоптатах эндометрия покровный маточный эпителий был неравномерной толщины, порой представлял собой конгломерат ядер эпителиоцитов. Иными словами, бывшая раневая поверхность после аборта полностью эпителизирована, но в отдельных участках маточный эпителий не завершил полностью свою дифференцировку (рис. 2).
Параллельно с развитием эндометриальных желез формировалась капиллярная сеть стромы, их количество увеличивалось, появлялись первые соединительные веточки. Однако явно отставало образование рецепторов, в частности к эстрогену, которые были выражены в эпителиоцитах отдельных желез, маточного эпителия и редко определялись в ядрах стромальных клеток. На таком же уровне была снижена экспрессия рецепторов к прогестерону в ядрах эпителиоцитов желез и стромальных клеток.
Следует подчеркнуть, что восстановление эндометрия после аборта, вызванного Энзапростом Ф, происходило на три – пять дней быстрее, чем при интраамниальном введении 20%-ного раствора хлорида натрия, поскольку маточным эпителием полностью закрывается бывшая раневая поверхность матки. Однако маточный эпителий не достигал еще окончательной дифференцировки. В такой же степени отставало формирование желез, несмотря на достаточную пролиферативную активность ядер их эпителиоцитов. Обнаружена также существенная недостаточность рецепторов к эстрогену, особенно в ядрах стромальных клеток, которая должна отразиться на темпах образования рецепторов к прогестерону, столь необходимых для полноценного развития эндометрия в целом.
Иными словами, на 22–24-й день после аборта, вызванного Энзопростом Ф, в биоптатах фиксировалась неполная картина развития эндометрия, которая соответствовала лишь восьмому – десятому дням нормального менструального цикла.
Результаты проведенного исследования свидетельствуют о необходимости проведения реабилитации репродуктивной функции женщин после прерывания беременности в поздние сроки. С учетом степени тяжести нарушения гормональной функции яичников и повреждения эндометрия предпринят дифференцированный подход к назначению гормональных препаратов.
Пациенткам с ановуляторными циклами и недостаточностью лютеиновой фазы в первой группе назначали монофазные низкодозированные комбинированные оральные контрацептивы в течение шести месяцев, затем микронизированный прогестерон (Утрожестан 200–400 мг/сут в зависимости от сывороточного содержания прогестерона) для коррекции лютеиновой фазы цикла (с 16-го по 25-й дни цикла) в течение трех месяцев. Такая же схема гормональной реабилитации применялась у двух (8%) пациенток второй группы с ановуляторными циклами. Пациенткам с недостаточностью лютеиновой фазы во второй группе назначали только Утрожестан во вторую фазу цикла в течение трех месяцев. Вследствие абсолютной идентичности химической структуры Утрожестана и эндогенного прогестерона препарат полноценно восполнял дефицит последнего, что подтверждалось результатами лабораторных исследований.
На фоне приема Утрожестана сывороточное содержание прогестерона на 22–24-й день менструального цикла у всех пациенток находилось в пределах нормальных референсных значений (41,3 ± 3,6 нмоль/л). Столь выраженный компенсаторный эффект Утрожестана обусловлен его высокой биодоступностью вследствие микронизации. Комплаентность и сродство к рецепторам прогестерона обеспечивают его клиническую эффективность, а именно адекватную секреторную трансформацию эндометрия и регуляцию менструального цикла. Кроме того, Утрожестан не обладает побочными эффектами, присущими ряду синетических гестагенов (анаболическим, андрогенным).
Наблюдение пациенток первой и второй групп в течение года после проведения гормональной реабилитации показало, что нарушения менструальной функции отмечались у трех (6%) пациенток первой группы и одной (4%) пациентки второй группы, которые имели предшествующие последней беременности гормонально обусловленные заболевания (миому матки, эндометриоз, дисфункцию яичников).
Заключение
Прерывание беременности в поздние сроки методом амниоинфузий вызывает серьезные нарушения менструального цикла вследствие тяжелых структурных изменений в эндометрии и нарушений гормональной функции яичников, максимально выраженные при использовании гипертонического раствора. Гормональная реабилитация с использованием микронизированного прогестерона позволяет нормализовать эти нарушения и сохранить репродуктивное здоровье женщин.
Pathogenetic justification for rehabilitation of women’s reproductive health after late termination of pregnancy
T.N. Melnik1, 2, G.V. Tamazyan3, A.P. Milovanov4, O.F. Serova2, 5, L.V. Sedaya2, 5, N.V. Shutikova2, 5
1 Lyubertsy district hospital № 3
2 Federal medical biophysical center named after A.I. Burnazyan
3 Moscow regional research clinical institute named after M.F. Vladimirsky
4 Research institute of human morphology of the Russian academy of medical sciences
5 Moscow district perinatal center
Contact person: Olga Fyodorovna Serova, olga-serova@yandex.ru
Late termination of pregnancy induced by amnioinfusions results in structural changes in endometrium. During the performed study it was found that after Enzaprost-F-induced abortion endometrium was restored by three-five days earlier compared to intraamnial application of 20%-sodium chloride solution.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.