Применение таргетной терапии у пациентов с бронхиальной астмой и полипозным риносинуситом
- Аннотация
- Статья
- Ссылки
- English
Введение
Бронхиальная астма (БА) – одно из самых распространенных заболеваний бронхолегочной системы, в основе которого лежит хроническое воспаление. Терапевтические подходы к лечению данной патологии на протяжении последних десятилетий претерпели существенные изменения, касающиеся как синтеза новых молекул, так и формы доставки лекарственных средств. Тяжелая БА, диагностируемая, по данным разных источников, в 5–10% случаев всей популяции больных БА [1, 2], является наиболее трудной и затратной для лечения формой заболевания. При этом стандартная базисная терапия не всегда способствует контролю БА [1–3]. Понимание гетерогенности БА, вариантов течения и ответа на лечение привело к изучению и впоследствии выделению так называемых фенотипов и эндотипов БА [1, 4]. В настоящее время особый интерес представляют два эндотипа БА – Т2 и не-Т2 [5, 6] с различными типами воспаления с вовлечением разных типов Т-хелперов и интерлейкинов (ИЛ) [6]. Существенно расширились знания о патогенезе Т2-опосредованных заболеваний. К ним кроме БА относят полипозный риносинусит, атопический дерматит, аллергический ринит, экзему, крапивницу, которые характеризуются эозинофильным типом воспаления [5]. Нередко такие заболевания встречаются у одного пациента, снижают качество его жизни и утяжеляют течение друг друга [5, 6].
Как известно, ведущими участниками Т2-воспаления являются ИЛ-4 и ИЛ-13, которые в основном секретируются CD4+-Th2-клетками и врожденными лимфоидными клетками 2-го типа (ILC2) [4–6]. Кроме общих механизмов воздействия ИЛ-4 и ИЛ-13 на миграцию эозинофилов в тканях организма, ИЛ-4 влияет на запуск гуморальных и аллергических реакций. В то же время ИЛ-13 оказывает влияние на функциональные и структурные изменения в бронхиальном дереве, включая сокращение и пролиферацию гладкомышечных клеток, гиперплазию бокаловидных клеток, гиперпродукцию слизи и субэпителиальный фиброз [1, 6]. Результаты ряда исследований показали, что ИЛ-4 и ИЛ-13 играют ключевую роль и в формировании полипов при хроническом полипозном риносинусите (ХПРС), который нередко сочетается с БА и может предшествовать ей [7, 8]. К формированию полипов приводят такие последствия Т2-воспаления, как воспаление и отек тканей, пропотевание плазмы, подавление деградации фибрина с его избыточным отложением, развитие отека и ремоделирование тканей придаточных пазух носа (ППН) [8, 9].
Применение моноклонального антитела дупилумаб
Понимание механизмов Т2-воспаления и роли значимых ИЛ способствовало созданию человеческого моноклонального антитела, ингибирующего эффекты ИЛ-4 и ИЛ-13, – дупилумаба. Дупилумаб был зарегистрирован в России в 2019 г. под названием Дупиксент [10]. Эффект препарата реализуется за счет его связывания с IL-4Rα-субъединицей и блокады передачи сигналов ИЛ-4/ИЛ-13 [10]. Препарат характеризуется большой доказательной базой, разрешен к использованию при ряде других Т2-опосредованных заболеваний [5, 10]. В 2021 г. он был включен в федеральные клинические рекомендации по БА [3].
В Астраханской области дупилумаб начали применять с 2020 г. В настоящее время лечение получают десять пациентов в возрасте 20–60 лет, шесть из них с тяжелой БА, четыре – с сочетанием БА среднетяжелого течения и ХПРС. Отметим, что ХПРС тяжелого течения стал чаще диагностироваться у молодых пациентов.
С ноября 2022 г. по май 2023 г. лечение дупилумабом получают четыре пациента со среднетяжелой БА и тяжелым ХПРС, по поводу которого в первую очередь и был назначен препарат. Возраст пациентов – 20, 24, 48 (женщины) и 60 (мужчина) лет. У всех имеются признаки эозинофильного воспаления с эозинофилией крови более 600 клеток/мкл, непереносимость нестероидных противовоспалительных препаратов, прогрессирующий рост полипов в носу и ППН, приведший к отсутствию носового дыхания и обоняния. Во всех случаях ранее проводились оперативные вмешательства на ППН, в двух случаях четырехкратно с очень кратковременным эффектом. У двух пациенток разрастание полипозных масс привело к деформации мягких тканей лица с наличием экзофтальма в одном случае. Показатели функции внешнего дыхания (ФВД) в пределах нормы. На момент назначения дупилумаба пациенты постоянно принимали базисную терапию ингаляционными глюкокортикостероидами (ИГКС) и длительно действующими бронхолитиками, что соответствует 3–4-й ступени лечения БА, и интраназальные ГКС (ИнГКС). На фоне приема ИнГКС в двух случаях отмечались сухость в носу и кровоточивость. В связи с этим препараты были отменены. Дупилумаб во всех случаях назначали коллегиально после проведения необходимого обследования, инъекции выполнялись на базе Александро-Мариинской областной клинической больницы (Астрахань). Первоначально при инициации вводили нагрузочную дозу 600 мг подкожно, далее 300 мг каждые две недели. Эффект от лечения дупилумабом пациенты отмечали уже после первой инъекции, через два-три месяца он усиливался. У всех значительно уменьшилась заложенность носа, восстановились носовое дыхание и обоняние, у двух пациенток исчезла деформация мягких тканей лица, существенно уменьшилась потребность в применении короткодействующих бронхолитиков, сократился объем базисной терапии, две пациентки полностью отказалась от ингаляций будесонида/формотерола, приступы удушья их не беспокоят.
Клинический случай
Пациентка Б. 24 лет обратилась за консультацией к аллергологу перед предстоящим оперативным лечением по поводу ХПРС. За четыре года перед обращением ей диагностировали аллергический ринит, по поводу которого она принимала мометазона фуроат. После перенесенной новой коронавирусной инфекции впервые появились признаки бронхообструкции, а в 2021 г. диагностирована БА. Пациентка принимала базисную терапию – беклометазон + формотерол 100/6 мкг две ингаляции в сутки. В 2022 г. диагностирован ХПРС, проведены двусторонняя гайморотомия, резекция носовых раковин, а через шесть месяцев пункция с промыванием ППН и антибактериальной терапией. В 2023 г. пациентка отметила значительное ухудшение носового дыхания, полное отсутствие обоняния и деформацию левой носогубной складки на лице. При обследовании в 2022–2023 гг. в анализах крови уровень эозинофилов – 620 и 640 кл/мкл, иммуноглобулин E – 466 МЕ/мл. Компьютерная томография (КТ) ППН от 28 февраля 2023 г.: хронический ринопансинусит с продуктивным компонентом. Спирографические показатели в норме.
Учитывая неконтролируемый рост полипов (прогрессирующий рост полипозной ткани, в том числе с деструкцией медиальной стенки и распространением в носовой ход и клетки решетчатого лабиринта), наличие БА аллергической формы с эозинофильным фенотипом, среднетяжелого персистирующего течения, не контролируемой коллегиально (аллерголог, пульмонолог, лор-врач), специалисты приняли решение об инициации терапии дупилумабом.
Введена нагрузочная доза препарата – 600 мг подкожно и далее 300 мг через две недели, всего три инъекции. После начала таргетной терапии отмечалось значительное улучшение состояния, прежде всего в виде восстановления носового дыхания, обоняния, уменьшения заложенности носа, исчезновения деформации левой носогубной складки на лице, сокращения потребности в ИнГКС, отсутствия приступов удушья. В крови в динамике после трех инъекций дупилумаба – эозинофилы – 600 кл/мкл (для препарата характерно медленное снижение уровня эозинофилов). При оценке контроля БА по АСТ до начала лечения – 15 баллов, на фоне лечения – 25 баллов.
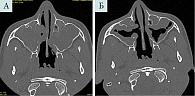
КТ ППН от 10 мая 2023 г. (через полтора месяца после инициации терапии дупилумабом): отчетливая положительная динамика (рисунок). До начала лечения пневматизация ППН была снижена за счет тотального выполнения пазух полипозными массами (А), с уменьшением их объема и улучшением пневматизации ППН на фоне таргетной терапии (Б). Приступов удушья во время данной терапии пациентка не отмечала, базисную терапию БА сократила вдвое. Лечение дупилумабом продолжается, согласно инструкции, каждые две недели.
Заключение
Представленный клинический случай демонстрирует высокую эффективность современной таргетной терапии, в частности дупилумабом. Препарат расширяет возможности лечения БА в сочетании с ХПРС, избавляя пациентов от повторных неэффективных оперативных вмешательств на ППН и существенно улучшая качество их жизни.
T.R. Kasyanova, MD, PhD, Prof., Zh.M. Kenesarieva, Ye.A. Kovaleva, Ye.M. Lipchanskaya, E.V. Churyukina, PhD, V.M. Skripkina
Astrakhan State Medical University
Alexander-Mariinsky Regional Clinical Hospital, Astrakhan
Rostov State Medical University
Kuban State Medical University
Contact person: Tatyana R. Kasyanova, kasyanova.tatjana@yandex.ru
Currently, therapeutic approaches to the treatment of asthma are expanding, The heterogeneity of аsthma contributed to the isolation of endotypes (T2 and non-T2), which are based on different types of inflammation and the participation of different interleukins. T2 inflammation, which is currently the most studied, occurs in addition to аsthma in chronic polypous rhinosinusitis (CPRS), while both diseases can occur in the same patient, aggravating the course of each other.
In both cases, there is an eosinophilic nature of inflammation, and interleukins (IL) 4 and 13 play a key role in this, affecting the launch of humoral and allergic reactions, as well as functional, structural changes in the bronchial tree and the formation of polyps in CPRS. Understanding the mechanisms of T2 inflammation and the role of IL-4 and IL-13 has led to the creation of targeted therapy drugs, in which specific biological targets are affected. To inhibit the effects of IL-4 and IL-13, a human monoclonal antibody called dupilumab (Dupixent) was created, which was registered in Russia in 2019, and in 2021 included in the Federal Clinical Guidelines for аsthma. The effect of the drug is realized by binding it to the IL-4Rα subunit and blockade of IL-4/IL-13 signaling. Dupilumab can be used not only in severe аsthma, but also in moderate course of the disease, and has shown its effectiveness especially in the combination of аsthma with CPRS with high blood eosinophilia. The article presents a clinical case of the use of dupilumab in a 24-year-old patient with a combination of moderate-to-severe аsthma and CPRS.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.