Рак печени: состояние проблемы и современные возможности противоопухолевой лекарственной терапии
- Аннотация
- Статья
- Ссылки
- English



Злокачественные новообразования (ЗНО) занимают второе место после сердечно-сосудистых заболеваний среди причин смерти в Российской Федерации (РФ). Заболеваемость, инвалидизация и смертность вследствие онкологических заболеваний имеют не только медицинское, но и огромное социально-экономическое значение. Изучение влияния тактики лечения на эпидемиологические показатели ЗНО является важным инструментом в планировании и реализации специализированной помощи населению [1].
В Сибирском федеральном округе (СФО) за период с 2018 по 2022 г. было зарегистрировано 384 707 впервые установленных случаев ЗНО, из них 180 172 (46,8%) – у мужчин, 204 535 (53,2%) – у женщин. Также за этот период выявлено 6989 случаев ЗНО печени и внутрипеченочных желчных протоков: 4173 (59,7%) – у мужчин и 2816 (40,3%) –
у женщин.
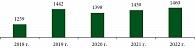
Прирост впервые выявленных случаев ЗНО печени и внутрипеченочных желчных протоков за 5 лет составляет 16,0% (увеличение числа случаев с 1259 до 1460).
Средний ежегодный прирост числа впервые выявленных случаев составляет 4,0%. При этом на фоне ограничений, связанных с распространением новой коронавирусной инфекции (COVID-19) и снижением числа лиц, прошедших профилактические осмотры и диспансеризацию в 2020 г., наблюдалось снижение числа выявленных случаев рака печени (рис. 1).
В 2022 г. в структуре общей заболеваемости ЗНО в СФО рак печени и внутрипеченочных желчных протоков находится на 16-м месте среди обоих полов – 1,9%. Лидирующие позиции занимают ЗНО молочной железы (12,0%), ЗНО кожи (кроме меланомы) (11,3%), ЗНО трахеи, бронхов и легкого (10,7%). В структуре заболеваемости у мужского населения округа ЗНО печени и внутрипеченочных желчных протоков занимают 11-е место (2,3%), в структуре заболеваемости у женского населения – 15-е место (1,5%) (рис. 2). В Республике Тыва, например, ЗНО печени и внутрипеченочных желчных протоков находятся на 5-м месте (6,3%) среди обоих полов, в Красноярском крае – на 14-м (2,3%), в Иркутской области – на 15-м (2,2%), в Новосибирской области – на 16-м месте (1,5%).
В России ЗНО печени и внутрипеченочных желчных протоков занимают 16-е место в общей структуре заболеваемости ЗНО – 1,2% [2].
Заболеваемость ЗНО печени и внутрипеченочных желчных протоков в 2022 г. по сравнению с 2018 г. в СФО выросла на 45,7% (с 6,0 на 100 тыс. населения в 2018 г. до 8,7 на 100 тыс. населения в 2022 г.). На протяжении всего анализируемого периода заболеваемость остается выше, чем в целом по России. При этом максимальный показатель заболеваемости отмечается в 2022 г., до этого наиболее высокий показатель был в 2019 г. Схожая ситуация наблюдается во всех регионах СФО (рис. 3).
Заболеваемость ЗНО печени и внутрипеченочных желчных протоков в СФО среди женского населения в 2022 г. составила 6,8 случая на 100 тыс. женского населения, по сравнению с 2018 г. показатель увеличился на 25,9% (5,4 случая на 100 тыс. женского населения в 2018 г.). Показатель заболеваемости среди мужского населения за тот же период увеличился на 14,7% (с 9,5 случая на 100 тыс. мужского населения в 2018 г. до 10,9 случая на 100 тыс. мужского населения в 2022 г.) (рис. 4).
В целом заболеваемость среди мужского населения выше, чем среди женского, максимальное расхождение в исследуемом периоде наблюдалось в 2021 г. и составляло 81,9% (6,1 случая на 100 тыс. женского населения и 11,1 случая на 100 тыс. мужского населения).
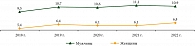
Средний возраст заболевших среди обоих полов в Российской Федерации в 2022 г. по сравнению с 2018 г. снизился с 66,9 до 66,7 года. Средний возраст заболевших женщин выше, чем мужчин. Так, среди женского населения средний возраст заболевания увеличился с 70,0 до 70,4 года, а у мужчин, наоборот, снизился с 64,6 до 64,2 года.
Максимальное число впервые выявленных случаев заболеваний ЗНО печени и внутрипеченочных желчных протоков в РФ диагностируется в возрастных группах 65–69 лет – 1738 (17,7%) случаев, 60–64 года – 1600 (16,3%), 70–74 года – 1588 (16,2%) случаев. Наиболее активный рост числа заболевших отмечается в возрастных группах 75–79 лет – на 63,5%, 35–39 лет – на 43,1%. Снижение числа заболевших произошло в возрастные периоды 70–74 года – на 30,9% и 45–49 лет – на 23,9% (рис. 5) [2–5].
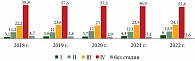
Стоит отметить, что наибольшее значение при лечении ЗНО имеет стадия заболевания. Благоприятный прогноз характерен для ранних стадий. При этом выявление рака печени и внутрипеченочных желчных протоков на ранних стадиях, несмотря на их рост, остается низким. Так, выявление ЗНО печени и внутрипеченочных желчных протоков на I–II стадиях за период 2018–2022 гг. в целом по РФ увеличилось на 29,4% (с 14,3% в 2018 г. до 18,5% в 2022 г.), в том числе на I стадии – на 93,5%, на II стадии – на 11,6%, а показатель запущенности при ЗНО печени и внутрипеченочных желчных протоков в 2022 г. по сравнению с 2018 г. снизился на 1,4% (с 81,0% в 2018 г. до 79,9% в 2022 г.) в основном за счет снижения случаев, выявленных на IV стадии опухолевого процесса, – на 5,1% (с 58,8% в 2018 г. до 55,8% в 2022 г.).
Также необходимо отметить, что за период 2018–2022 гг. произошло снижение доли случаев, стадия злокачественного процесса которых не была установлена, на 65,9% (с 4,7 до 1,6%) (рис. 6). В СФО выявление ЗНО печени и внутрипеченочных желчных протоков на ранних стадиях составляет 16,7%, что на 43,6% выше показателя 2018 г. (11,6%). При этом число случаев ЗНО, выявленных на IV стадии, практически не изменилось: 2018 г. – 58,1%, 2022 г. – 58,3%. Но отмечается положительная динамика уменьшения доли образований с неустановленной стадией с 4,2 до 1,7% [2–5].
На конец 2022 г. число пациентов с ЗНО печени и внутрипеченочных желчных протоков, состоящих под диспансерным наблюдением, в СФО составило 975 человек, показатель распространенности – 5,8 на 100 тыс. населения. Наибольший показатель отмечается в Новосибирской области – 7,7, Республике Тыва – 6,6, Иркутской области – 6,5 на 100 тыс. населения (РФ – 6,4 на 100 тыс. населения). В сравнении с 2018 г. данный показатель по СФО не изменился (2018 г. – 5,8 на 100 тыс. населения), но при этом изменилось ранжирование внутри округа: наибольший показатель отмечался в Республике Тыва – 14,4, в Кемеровской области – 10,8 на 100 тыс. населения [2–5].
Доля лиц с ЗНО печени и внутрипеченочных желчных протоков, состоящих на учете 5 лет и более, в целом по СФО составляет 31,3%, что ниже, чем в среднем по РФ – 35,2%. При этом в субъектах СФО данный показатель варьировал от 13,6% в Республике Тыва до 37,5% в Омской области. Индекс накопления контингента в СФО вырос по сравнению с 2018 г. с 1,2 до 7,2 [2–5].
Доля больных, умерших в течение первого года после установления диагноза, из взятых на учет в предыдущем году с раком печени и внутрипеченочных желчных протоков составила 67,3% (2018 г. – 69,4%), что выше среднероссийского показателя – 63,7% (65,6%) [2, 5].
Стоит отметить, что на ряд эпидемиологических данных (доля лиц с ЗНО, состоящих на учете 5 лет и более; доля больных, умерших в течение первого года после установления диагноза; число пациентов, состоящих под диспансерным наблюдением) влияют показатели, связанные с лечением онкологических пациентов. Так, в СФО в 2022 г. 12,8% от числа впервые выявленных пациентов с ЗНО печени и внутрипеченочных желчных протоков закончили радикальное лечение (РФ – 12,3%), в Республике Алтай – 50,0%, в Красноярском крае – 36,1%, в Республике Хакасия – 22,2%. В сравнении с 2018 г. в 2022 г. отмечается изменение структуры использованных методов лечения пациентов. Так, в 2018 г. на долю хирургических методов лечения приходилось 42,6%, комбинированного лечения – 57,4; тогда как в 2022 г. – 73,3 и 26,7% соответственно (РФ, 2018 г. – 56,0 и 44,%; 2022 г. – 57,7 и 42,3%) [2–4].
Приведенные данные свидетельствуют о необходимости применения современных методов лечения рака печени. В отношении специализированного лечения стоит отметить, что в последние годы не отмечалось существенных изменений в хирургических и радиотерапевтических подходах. Основные достижения в лечении заболеваний связаны с противоопухолевой лекарственной терапией.
Согласно ведущим международным и российским рекомендациям по раку печени, в качестве предпочтительной первой линии системной терапии у пациентов с гепатоцеллюлярной карциномой (ГЦК) рекомендуется комбинация ингибитора PD-L1 атезолизумаба и моноклонального антитела к VEGF бевацизумаба. В качестве альтернативы при наличии противопоказаний к назначению иммунотерапии в первой линии лечения ГЦК могут быть назначены мультикиназные ингибиторы – сорафениб или ленватиниб [6–9]. Комбинация двойной иммунотерапии дурвалумабом (ингибитор PD-L1) и тремелимумабом (антитело против CTLA-4) также вошла в рекомендации NCCN и RUSSCO 2023, но при непрямом сравнении медиана общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и частоты объективных ответов при двойной иммунотерапии уступает аналогичным показателям эффективности комбинации атезолизумаб + бевацизумаб [10, 11].
Клиническое исследование IMbrave150 – это исследование III фазы, направленное на демонстрацию превосходства комбинации атезолизумаб + бевацизумаб над терапией сорафенибом у пациентов с неоперабельной ГЦК [11]. Особенностью исследования IMbrave150 было включение пациентов с неблагоприятным прогнозом: с макроваскулярной инвазией главного ствола или ветви воротной вены (Vp4), с инвазией желчных протоков, с ≥ 50% поражением печени, тромбозами печеночной и нижней полой вен [12]. Такая сложная когорта пациентов обычно исключается из других исследований ГЦК III фазы.
Исследование IMbrave150 доказало, что применение комбинации атезолизумаб + бевацизумаб у пациентов с нерезектабельной ГЦК имело большую эффективность, чем применение мультикиназного ингибитора сорафениба. Медиана ОВ была значимо выше и составила 19,2 месяца (95% доверительный интервал (ДИ) 17,0–23,7) в группе комбинации атезолизумаб + бевацизумаб и 13,4 месяца (95% ДИ 11,4–16,9) в группе сорафениба (отношение рисков (ОР) 0,66; 95% ДИ 0,52–0,85; p < 0,001). Показатели ОВ через 12 и 18 месяцев составили 67 и 52% соответственно в группе комбинации атезолизумаб + бевацизумаб и 56 и 40% в группе сорафениба. Преимущество комбинации наблюдалось также и в отношении медианы ВБП, которая статистически и клинически значимо была выше в группе атезолизумаба и бевацизумаба, чем в группе сорафениба: 6,9 месяца (95% ДИ 5,7–8,6) по сравнению с 4,3 месяца (95% ДИ 4,0–5,6) (ОР 0,59; 95% ДИ 0,47–0,76; р < 0 ,001) [10]. При этом в когорте пациентов без неблагоприятного прогноза комбинация атезолизумаб + бевацизумаб показала медиану ОВ в 22,8 месяца (95% ДИ 19,1–24,9) против 15,7 месяца (95% ДИ 13,2–19,0) на сорафенибе (ОР 0,68; 95% ДИ 0,52–0,91), а медиану ВБП – 7,2 месяца (95% ДИ 6,5–9,6) против 4,4 месяца (95% ДИ 4,0–5,8) соответственно [12]. Кроме того, использование комбинации препаратов показало ту же частоту нежелательных явлений 3-й и 4-й степени, что и применение сорафениба, несмотря на большую длительность терапии комбинацией атезолизумаб + бевацизумаб по сравнению с сорафенибом (8,4 месяца – средняя длительность терапии атезолизумабом, 7,0 месяцев – бевацизумабом, против 2,8 месяца – сорафенибом) [13].
После успеха IMbrave150 стало очевидно, что комбинация атезолизумаб + бевацизумаб является наиболее эффективной и предпочтительной опцией первой линии терапии для лечения пациентов с неоперабельной ГЦК.
Последующие анализы исследования IMbrave150, метаанализы рандомизированных клинических исследований терапии ГЦК и исследования реальной практики показали, что комбинация атезолизумаб + бевацизумаб эффективна при терапии ГЦК [14–18].
Результаты представленных данных подтверждаются собственными наблюдениями в лечении ЗНО печени. Приводим клинический случай из нашей практики.
Клинический случай
Мужчина 68 лет направлен в Иркутский онкологический диспансер в октябре 2018 г. с подозрением на объемное образование печени. В результате комплексного обследования установлен диагноз: гепатоцеллюлярный рак правой доли печени Т2N0M0, II стадия.
Хронический вирусный гепатит С, генотип 1, фаза репликации, высокая степень вирусемии с нормальной ферментативной активностью, METAVIR F2.
Ишемическая болезнь сердца (ИБС). Стабильная стенокардия I функционального класса (ФК). Артериальная гипертензия III стадии, 1-й степени, риск 4-й (ИБС, мужской пол, возраст). Хроническая сердечная недостаточность I ФК.
05.12.2018 выполнена масляная химиоэмболизация правой доли печени.
С декабря 2018 г. по март 2019 г. проведен 12-недельный курс лечения вирусного гепатита комбинацией препаратов софосбувир и велпатасвир. При контрольном ПЦР-исследовании от 18.03.2019 РНК вируса не обнаружено.
16.05.2019 пациенту выполнена правосторонняя гемигепатэктомия.
25.05.2019 проведено гистологическое исследование операционного материала: желчный пузырь 80 × 30 × 30 мм, не вскрыт, сероза гладкая, в просвете густая темная желчь, стенка 2 мм, слизистая бархатистая. При микроскопии гистологическое строение сохранено. Правая доля печени 150 × 140 × 80 мм; на разрезе, ближе к нижней поверхности округлый, четко ограниченный опухолевый узел 40 × 45 × 40 мм, интимно рядом с ним второй очаг 10 × 5 × 5 мм, опухолевый узел тесно прилежит к вене. При микроскопии определяется ГЦК G2 с преобладанием трабекулярного строения, инвазией за пределы псевдокапсулы опухоли, наличием сосудистой инвазии. Удалена в пределах здоровых тканей. Сохранная паренхима печени с умеренной лимфо-лейкоцитарной инфильтрацией, очагово проникающей в дольки, очаговый слабый фиброз портальных трактов. Рак правой доли печени (ГЦК) 8170/3 G2, pT2 N0 LV1 Pn0 R0 (7-е издание, 2009 г.).
После радикальной операции установлен диагноз: гепатоцеллюлярный рак правой доли печени рТ2N0M0G2, II стадия, III клиническая группа. Пациент оставлен под динамическим диспансерным наблюдением, адъювантного лечения не проводилось.
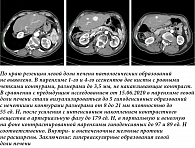
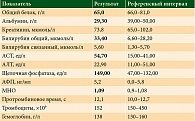
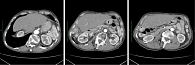
В январе 2021 г. при плановом контрольном обследовании на фоне клинического благополучия, по данным мультиспиральной компьютерной томографии (МСКТ) с контрастированием, выявлены множественные очаговые образования в левой доле печени (рис. 7), под ультразвуковым контролем выполнена пункционная биопсия одного из очагов в 3-м сегменте, получена цитологическая картина гепатоцеллюлярного рака. Состояние пациента расценено как удовлетворительное, ECOG 1, признаков портальной гипертензии нет, лабораторно компенсирован (табл.), оценка по Child – Pugh A (6 баллов). В феврале 2021 г. пациенту была назначена комбинация атезолизумаб 1200 мг один раз в три недели в/в + бевацизумаб 15 мг/кг один раз в три недели. В соответствии с критериями mRECIST, был достигнут частичный ответ (рис. 8) на фоне проводимой терапии.
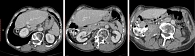
Данное лечение продолжалось до марта 2023 г., когда произошел ишемический инсульт, больной был госпитализирован в неврологическое отделение по месту жительства, выполнены МСКТ, магнитно-резонансная томография головного мозга, проведена соответствующая терапия с положительной динамикой, противоопухолевое лечение атезолизумабом и бевацизумабом было прервано. У пациента сохранялся выраженный правосторонний гемипарез, и на контрольное обследование он смог явиться лишь в октябре 2023 г., по результатам которого клинически и рентгенологически сохранялся достигнутый частичный ответ. При мультидисциплинарном обсуждении принято решение продолжить активное динамическое наблюдение. Очередное обследование проведено в январе 2024 г. (рис. 9), сохраняется рентгенологический частичный ответ при удовлетворительных клинико-лабораторных показателях. Пациент ведет привычный образ жизни.
Таким образом, внедрение в повседневную практику современной противоопухолевой лекарственной терапии существенным образом изменило результаты лечения рака печени. На примере представленных данных показано, что лекарственная терапия стала неотъемлемым стандартом лечения, что в свою очередь приводит к снижению показателей смертности и увеличению продолжительности жизни у данной категории пациентов.
R.A. Zukov, PhD, I.P. Safontsev, PhD, K.D. Permyakova, D.M. Ponomarenko, PhD, D.Yu. Yukalchuk
A.I. Kryzhanovsky Krasnoyarsk Regional Clinical Oncology Dispensary
V.F. Voino-Yasenetsky Krasnoyarsk State Medical University
Irkutsk State Medical University
Irkutsk State Medical Academy of Postgraduate Education
Irkutsk Regional Oncology Center
Contact person: Ruslan А. Zukov, priem@onkolog24.ru
The development and implementation of new methods for the diagnosis and treatment of malignant neoplasms, improving their effectiveness and safety are one of the most urgent tasks of modern oncology. Currently, antitumor drug therapy makes a great contribution to the treatment of this pathology, and one of the most striking examples of this approach is the treatment of liver cancer. The article presents epidemiological data on the prevalence, indicators of the state of oncological care for liver cancer in Russia and the Siberian Federal District, as well as modern approaches to antitumor drug therapy of this disease.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.