Роль иммуномодулирующей терапии в комплексном лечении хронического простатита: результаты сравнительного плацебо-контролируемого исследования препарата Генферон®
- Аннотация
- Статья
- Ссылки


Социальная значимость хронического простатита обусловлена преимущественным развитием данного заболевания у мужчин трудоспособного возраста, а также негативным влиянием на репродуктивное здоровье. Снижение фертильности, сексуальная дисфункция, синдром хронической тазовой боли и расстройства мочеиспускания не только в значительной степени снижают уровень жизни больных хроническим простатитом, но и влекут за собой развитие невротических и депрессивных расстройств, которые нередко требуют проведения дополнительной медикаментозной терапии (2).
До настоящего времени не существует единого мнения об этиологии и патогенетических механизмах развития хронического простатита. Известно, что пусковым моментом в реализации воспалительного процесса в предстательной железе наиболее часто становится инфекционный фактор (10, 11). Специфические свойства отдельных возбудителей (способность к образованию L-форм, своеобразной мимикрии, длительной персистенции и т. п.), а также частое отсутствие адекватного иммунологического ответа служат причиной упорного течения и хронизации воспалительных изменений в предстательной железе. В то же время фактором, предрасполагающим к развитию хронического простатита, являются анатомические особенности предстательной железы: плотное строение долек, узкие выводные протоки, затрудняющие дренаж, легкое возникновение венозного стаза и т.п. (8).
Отечественные исследования свидетельствуют о формировании существенных иммунологических нарушений у больных хроническим простатитом. Так, достаточно часто у пациентов определяется снижение абсолютного и относительного количества Т-лимфоцитов, натуральных киллеров, истощение системы комплемента, низкий уровень интерферона-альфа и -гамма, декомпенсация функции фагоцитарной активности иммунокомпетентных клеток, снижение концентрации sIgA и повышение содержания провоспалительных цитокинов в секрете предстательной железы (ИЛ-6, ИЛ-8) (1, 3, 9).
Устойчивость ряда возбудителей к традиционным методам лечения хронического бактериального простатита и достоверное угнетение клеточного звена иммунитета диктуют необходимость расширения терапевтического алгоритма при хроническом простатите с введением в него современных иммунотропных препаратов.
Для оценки терапевтических эффектов топической интерферонотерапии хронического бактериального простатита нами было проведено сравнительное рандомизированное двойное слепое плацебо-контролируемое исследование эффективности и безопасности препарата Генферон®(ЗАО «Биокад», Россия). Исследовательскими базами являлись ФГУ НИИ Урологии Росмедтехнологий, кафедра урологии и оперативной нефрологии ГОУ ВПО РГМУ Росздрава, Урологический центр НУЗ ЦКБ №1 ОАО «РЖД» и кафедра урологии ВГМА на базе Дорожной больницы Юго-Восточной железной дороги г. Воронеж.
Целями данного клинического исследования являлись оценка эффективности препарата Генферон® в комплексной терапии хронического бактериального простатита и оценка динамики иммунологических показателей на фоне применения иммуномодулирующей терапии.
Препарат Генферон® (ЗАО «Биокад», Россия) представляет собой суппозитории для ректального и вагинального введения, активными компонентами которых являются рекомбинантный человеческий интерферон альфа2b, таурин и анестезин.
Интерферон-альфа (ИФН-a) обладает широким спектром иммунобиологической активности: он способен ингибировать практически любую стадию размножения вируса, включая процесс проникновения в клетку, транскрипцию, созревание, сборку и высвобождение патогена из клетки (4). ИФН-a увеличивает фагоцитарную активность иммунокомпетентных клеток (макрофагов, моноцитов, нейтрофилов), натуральных киллеров, повышает количество и киллерный потенциал Т-клеток, стимулирует дифференцировку В-лимфоцитов и продукцию ими специфических антител, способствует повышению уровня секреторного IgA и оказывает ряд других положительных иммуномодулирующих эффектов.
Помимо этого, препараты экзогенного ИФН-a потенцируют действие противомикробных лекарственных средств, что позволяет повысить эффективность этиотропной терапии ряда заболеваний, вызванных трудно поддающимися стандартному лечению микроорганизмами (микоплазмами, уреаплазмами, хламидиями) (5).
Таурин – это незаменимая серосодержащая аминокислота, метаболит цистеина. Оказывает выраженное противовоспалительное антиоксидантное, метаболическое и регенеративное воздействие. Сочетание таурина и ИФН-a в составе одной лекарственной формы увеличивает биологическую активность последнего и обеспечивает более широкий спектр действия препарата по сравнению с другими суппозиторными формами ИФН-a.
Анестезин (бензокаин) – местный анестетик, способствующий устранению основных алгических симптомов, характерных для хронического простатита (боль в промежности, яичках, нижней части живота и др.). Не оказывает системного воздействия.
В настоящее время накоплен обширный опыт применения препарата Генферон® в терапии различных инфекционно-воспалительных заболеваний, а именно хронических воспалительных заболеваний органов малого таза у женщин, урогенитальных инфекций вирусной и бактериальной этиологии, профилактике инфекционных осложнений после спонтанного аборта, при аногенитальном кондиломатозе, цервикальной неоплазии и др. Имеющиеся научные данные свидетельствуют о высоком терапевтическом потенциале и широком профиле безопасности препарата Генферон®, что послужило предпосылкой для изучения его эффектов в рамках нашего клинического исследования.
Материалы и методы
Продолжительность наблюдения составила 4 месяца, в течение которых было проведено 3 визита. В рамках визитов всем пациентам выполнялось комплексное клинико-лабораторное обследование, включавшее тщательный клинический осмотр, бактериологическое и микроскопическое исследование секрета предстательной железы (СПЖ), бактериологическое исследование трех порций мочи, а также оценку субъективных симптомов хронического простатита по шкале Национального института здоровья США NIH-CHSI (NIH – Chronic Prostatitis Symptom Index). Пациентам, наблюдавшимся на базе НИИ Урологии и кафедры урологии ВГМА, было выполнено дополнительное иммунологическое обследование (определен уровень интерферонов-альфа и -гамма, функциональной активности нейтрофилов, уровня иммуноглобулинов IgA, G и М), клинический анализ крови и общий анализ мочи, а также ТРУЗИ предстательной железы.
После проведения скринингового визита, а также предусмотренных протоколом лабораторно-инструментальных исследований, оценки соответствия критериям включения/невключения и подписания информированного согласия больные рандомизировались в 2 равнозначные группы: основную и группу сравнения. Пациенты основной группы в дополнение к стандартной антибактериальной терапии (ципрофлоксацин в табл. 500 мг 2 р./сут. в течение 10 дней) получали суппозитории Генферон® ректально в дозе 1 000 000 МЕ 2 р./сут. в течение 10 дней. Пациенты группы сравнения также параллельно стандартной антибактериальной терапии получали плацебо, внешне не отличимое от активного препарата.
В течение всего исследования регистрировались нежелательные явления, произошедшие в период приема исследуемого препарата.
Через 3 месяца после начала терапии с пациентом устанавливался телефонный контакт, во время которого исследователем определялась выраженность симптомов хронического простатита по шкале NIH-CHSI.
Данные по эффективности и безопасности исследуемой терапии, полученные в рамках клинического исследования, анализировались при помощи методов описательной, параметрической и непараметрической статистики.
Результаты и их обсуждение
В исследование были включены 160 человек в возрасте от 19 до 55 лет (медиана 37,2 года, нижний и верхний процентили – 29,0 и 48,0 лет соответственно). Возраст большинства пациентов на момент включения в исследование составил 40-49 лет (59 человек – 36,8%).
Практически все включенные в исследование больные имели отягощенный соматический и урологический анамнез. Так, приблизительно треть мужчин перенесли оперативное вмешательство по поводу варикоцеле, более чем в половине случаев у больных диагностировался хронический очаг инфекции (хр. тонзиллит, хр. бронхит, хр. отит, хр. вирусный гепатит и т.п.), у части пациентов в анамнезе имелись перенесенные урогенитальные инфекции (гонорея, хламидиоз, уреаплазмоз).
Выраженность симптомов хронического простатита оценивалась по шкале NIH-CHSI. На скрининговом визите суммарный балл, в среднем, составил 23 балла. В ходе лечения выраженность симптомов хронического простатита уменьшилась у пациентов обеих групп: так, уже на втором визите она снизилась вдвое, а к третьему, в среднем, составляла 4,65 ± 2,53 балла в основной группе и 5,70 ± 2,63 балла в группе сравнения. Полученные результаты свидетельствуют о том, что у пациентов, получавших препарат Генферон®, отмечалось более выраженное снижение суммарного балла по шкале NIH-CHSI.
По данным бактериологического исследования СПЖ, проведенного до начала лечения, у большинства больных были выделены E. coli, E. faecalis, St. haemolyticus и St. epidermidis. У 10% больных в СПЖ определялось более одного возбудителя. Чаще всего микробная ассоциация была представлена сочетанием энтеробактерий, несколько реже – St. agalactiae и C. albicans, St. agalactiae и E. coli, St. epidermidis и E. coli. Проведенная терапия позволила добиться эрадикации возбудителя в 60-70% случаев в обеих группах, при этом в основной группе санация СПЖ наступала чаще, чем в группе сравнения.
Если при включении в исследование средний уровень лейкоцитов в СПЖ в обеих группах не различался и составлял 40-50 клеток в поле зрения (р > 0,05), то к моменту окончания лечения нами были выявлены статистически значимые различия между группами. Так, у 45% пациентов основной группы лейкоциты в СПЖ не определялись, у остальных их количество не превышало 10 клеток в поле зрения, в то время как в группе сравнения количество лейкоцитов 15 и более клеток в поле зрения сохранялось у 10% больных (р < 0,05). Это позволяет предположить, что препарат Генферон®, по сравнению со стандартной терапией, способствует наступлению более выраженного противовоспалительного эффекта.
Иммунологическое исследование, проведенное до начала лечения и сразу после его окончания, включало в себя определение уровня интерферонов-альфа и -гамма, функциональной активности нейтрофилов, уровня иммуноглобулинов IgA, G и М.
Функциональная активность нейтрофилов определялась с помощью НСТ-спонтанного и НСТ-стимулированного теста. До начала лечения, по данным НСТ-спонтанного теста, показатели функциональной активности нейтрофилов в группах не имели различий и равнялись 6,94 ± 0,59% в основной группе и 6,9 ± 0,67% в группе сравнения (нормальное значение – 9,8 ± 0,9%). На 18-й день от начала лечения у пациентов, получавших препарат Генферон®, показатель НСТ-теста составил 13,03 ± 0,88%, тогда как в группе сравнения подобной динамики выявлено не было (р < 0,05).
Аналогичные результаты были получены и при анализе параметров НСТ-стимулированного теста, который позволяет оценить способность нейтрофилов к завершенному фагоцитозу. Установлено, что по завершении терапии уровень функциональной активности в основной группе повысился до нормы, а в группе сравнения, напротив, регистрировалась отрицательная динамика данного показателя (таблица 1).
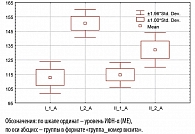
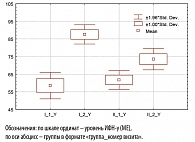
Концентрации интерферонов-альфа и -гамма также оценивались до и после лечения. Результаты проведенного исследования свидетельствуют о том, что если до начала терапии в обеих группах уровень интерферонов-альфа и -гамма был значительно ниже нормы, то к моменту окончания лечения в основной группе наблюдалась более выраженная положительная динамика, а концентрация ИФН-a достигла нормальных значений (таблица 2, рисунки 1, 2). Различия между группами в динамике прироста анализируемых показателей статистически достоверны (р < 0,05).
Уровень секреторного иммуноглобулина А (sIgA) в секрете предстательной железы определяли до и после лечения. При включении в обеих группах концентрация данного иммуноглобулина была существенно ниже нормы. По окончании курса терапии в основной группе было зарегистрировано приблизительно двукратное повышение уровня sIgA, в группе сравнения уровень sIgA повысился в 1,5 раза.
До начала лечения концентрация IgG и IgM в крови была повышена у пациентов обеих групп. При повторном исследовании, проведенном на 18 ± 1 день от начала терапии, у всех больных отмечалось снижение уровня иммуноглобулинов, при этом в большей степени подобная динамика проявлялась у пациентов, получивших комплексную терапию с использованием препарата Генферон®. Описанные изменения свидетельствуют об уменьшении интенсивности воспалительного процесса, а также о нормализирующем влиянии интерферонотерапии на гуморальный иммунитет больных, страдающих хроническим простатитом.
Исследуемая терапия характеризовалась хорошей переносимостью. Так, за все время исследования не было зарегистрировано ни одного случая развития аллергических реакций или других нежелательных побочных явлений. Кроме того, проведенные общеклинические исследования образцов крови и мочи не выявили каких-либо патологических изменений со стороны кроветворных органов и почек. Эти данные свидетельствуют о безопасности применения препарата Генферон® в комплексной терапии хронического простатита.
Оценка эффективности терапии
На 108 ± 5 день от начала лечения нами была проведена комплексная оценка эффективности, основанная на данных клинического наблюдения и лабораторных исследований.
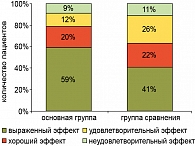
Были использованы следующие критерии эффективности: выраженный эффект – снижение показателя на 50% и более, хороший эффект – снижение показателя на 25-49%, удовлетворительный – уменьшение показателя менее чем на 25%, отсутствие динамики или ухудшение состояния расценивалось как неудовлетворительный эффект.
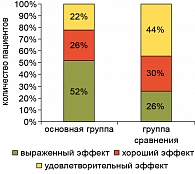
По данным клинического наблюдения, хороший и выраженный эффект был достигнут у 78% пациентов, получавших иммуномодулирующую терапию, в то время как в группе сравнения они регистрировались у 56% больных (рисунок 3).
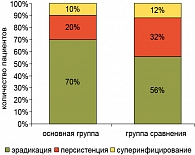
Согласно результатам бактериологического исследования СПЖ, проведенного после окончания курса терапии, эрадикация патогенной и условно-патогенной флоры в основной группе регистрировалась чаще, чем в группе сравнения. У пациентов, получавших комплексную терапию с использованием препарата Генферон®, персистенция возбудителей и суперинфицирование наблюдалось реже (в 20% и 10% случаев соответственно). Данные бактериологического исследования СПЖ, проведенного сразу после окончания терапии, представлены на рисунке 4.
Комплексный анализ данных позволяет сделать вывод о том, что выраженный и хороший терапевтический эффект зарегистрирован у 79% пациентов основной группы, что превышает аналогичный показатель в группе сравнения (63%) (рисунок 5).
Выводы
Проведенное нами исследование позволило определить ряд закономерностей, характеризующих особенности течения хронического простатита бактериальной этиологии.
Так, у большинства больных были выявлены существенные иммунологические нарушения: снижение фагоцитарной активности нейтрофилов, их способности к завершенному фагоцитозу и выработке кислородзависимых бактерицидных факторов, снижение уровня интерферонов-альфа и -гамма, секреторного иммуноглобулина А, повышение уровня иммуноглобулинов G и M. Подобный иммунологический дисбаланс играет важную роль в поддержании хронического воспалительного процесса в предстательной железе и требует обязательной лечебной коррекции.
Установлено, что включение препарата Генферон® в стандартный алгоритм терапии пациентов, страдающих хроническим простатитом, оказывает выраженное иммуномодулирующее действие, а также способствует повышению эффективности лечебных мероприятий и не сопровождается развитием местных или системных побочных реакций.
Полученные нами результаты позволяют рекомендовать использование препарата Генферон® в комплексной терапии хронического простатита по следующей схеме – по 1 суппозиторию в дозе 1 000 000 МЕ ректально 2 раза в сутки в течение 10 дней.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.