Современные подходы к лечению тромботических осложнений в онкологии
- Аннотация
- Статья
- Ссылки
![Таблица 1. Клинические исследования длительного применения антикоагулянтов для профилактики рецидивирующего тромбоза вен у онкологических больных [22]](/upload/resize_cache/iblock/a50/195_350_1/frgmin2.jpg)

Что же лежит в основе высокой тромбофилии при опухолевых заболеваниях? Возможно, на этот вопрос нет единого ответа, и конкретные механизмы активации могут меняться при различных неоплазиях. В качестве первопричин запуска прокоагулянтного звена гемостаза могут выступать тканевой фактор (высоко экспрессирован на клетках рака поджелудочной железы, печени, некоторых лейкозов) [3], опухолевая цистеиновая протеиназа (часто продуцируется клетками рака толстой кишки, рака молочной железы, меланомы) [4], муциновые микровезикулы (выделяются клетками рака яичников, рака поджелудочной железы, рака толстой кишки) [5]. Тромбоциты при опухолях могут активироваться как под воздействием сформировавшегося тромбина, так и при взаимодействии с измененным в процессе контакта с провоспалительными цитокинами (ФНО, интерферон–γ) сосудистым эндотелием [6]. К перечисленным факторам тромбофилии могут добавляться воздействия общего характера, связанные с наличием опухоли в организме – местный сосудистый стаз при прорастании или сдавлении сосудов, обезвоживание, гиподинамия. При лабораторных коагулологических исследованиях пациенты с неоплазиями и без клинических проявлений тромбоза часто имеют повышенный уровень активированных форм факторов VIII и XII, а также маркеров коагуляции (фрагменты протромбина 1+2, тромбин-антитромбин комплекс, продукты деградации фибрина/фибриногена) и активации тромбоцитов (PF4). Эти изменения чрезвычайно распространены и, по некоторым данным, встречаются у 90% онкологических больных [7].
Прогрессии тромбоза способствует цитостатическая и гормональная терапия, повреждающая как опухолевые клетки с выходом прокоагулянтных субстанций в кровоток, так и эндотелий сосудов. Повреждение эндотелия, характерное для антрациклинов, сопровождается снижением выработки тромбомодулина, простоциклина, тканевого активатора плазминогена и высвобождением субэндотелиальных структур (коллаген, эластин), активирующих тромбоциты и белки свертывания [8, 9]. В значительной мере увеличивают риск тромбоза оперативные вмешательства и постоянные сосудистые катетеры. Все эти состояния сопровождаются тромбозами и тромбоэмболиями, значимо повышающими летальность пациентов в группах наибольшего риска.
В крупном ретроспективном исследовании в США, включившем в анализ 8 млн пациентов, госпитализированных с различными диагнозами, рак являлся наиболее частой причиной тромбозов. Среди видов опухоли первые три места занимали рак яичников, опухоли ЦНС и рак поджелудочной железы. По некоторым данным, наличие венозной тромботической болезни (тромбозы глубоких вен голени / тромбоэмболии легочной артерии) у больных с распространенными опухолями повышает риск смерти в течение полугода на 60% в сравнении с пациентами сходной распространенности рака, но не имеющими тромботических осложнений [10]. Наличие маркеров активации свертывания в крови онкологических больных является отрицательным фактором прогноза даже в отсутствие тромбоза [11].
Отдельная проблема тромботической болезни – это материальные затраты, связанные с необходимостью госпитализации больных и проведения интенсивной, порой дорогостоящей противотромботической терапии. В одно из европейских исследований были включены данные 529 онкологических больных, у которых развились тромбозы и которые наблюдались в последующем на протяжении нескольких лет. Были подсчитаны затраты, связанные с госпитализацией по поводу тромбозов или их осложнений, включая осложнения антикоагулянтной терапии. Средняя стоимость госпитализации составила 20 065 долл. США. Авторы делают вывод о серьезности медицинских последствий тромботической болезни и высокой стоимости лечения ее осложнений, а также о необходимости разработки более эффективных методов предотвращения и лечения тромбозов/эмболий у пациентов с опухолевыми заболеваниями.
Лечение тромбозов/тромбоэмболий у больных с неоплазиями
Больные с опухолевыми заболеваниями и развившимися тромбозами/тромбоэмболиями имеют крайне высокий риск прогрессирования (развитие дополнительных тромбов и тромбоэмболий) или рецидивов этих осложнений на протяжении 6–12 месяцев, поэтому им показана длительная антикоагулянтная терапия.
В соответствии с рекомендациями АССР на первом этапе, как правило, применяют прямые антикоагулянты (гепарины, фондапаринукс) в течение 5–10 дней с переходом на антивитамины К (АВК), перорально.
Нефракционированные гепарины (НФГ), низкомолекулярные гепарины (НМГ) или фондапаринукс назначаются по возможности немедленно после установки диагноза тромбоза. НФГ назначают в виде постоянной инфузии (80 ЕД/кг болюсно и затем 18 ЕД/кг/час) под контролем активированного частичного тромбопластинового времени (АЧТВ), которое должно быть выше нормы в 1,5–2,5 раза [12]. Низкомолекулярные гепарины не требуют постоянного лабораторного контроля (за исключением подсчета числа тромбоцитов раз в 10 дней, как и для НФГ) и вводятся 1–2 (далтепарин и эноксапарин) или 2 (надропарин) раза в день. Удобство назначения при сопоставимой эффективности и безопасности приводит к постепенному вытеснению нефракционированных гепаринов низкомолекулярными. НФГ могут иметь преимущество у больных с почечной недостаточностью (в связи с почечным клиренсом низкомолекулярных гепаринов), а также в тех случаях, когда высокий риск кровотечений может потребовать немедленной остановки антикоагулянтной терапии. В то же время опасность кумуляции НМГ, по крайней мере в отношении далтепарина, невелика, что показано в исследовании Дукетиса [13] и при соответствующем контроле препарат может быть использован при почечной недостаточности. У 120 пациентов в критическом состоянии с клиренсом креатинина менее 30 мл/мин при применении далтепарина в дозе 5000 МЕ не получено доказательств биоаккумуляции препарата на основании серийного измерения уровня анти-Ха активности.
Назначение АВК начинают с первого дня применения гепаринов и до достижения уровня гипокоагуляции 2,0–3,0 МНО (международное нормализованное отношение, INR) гепарины отменяют при условии, что они вводились как минимум 5 дней.
Эта методика хорошо зарекомендовала себя у больных, не имеющих опухолей с высоким риском ретромбозов, например, после ортопедических операций на тазобедренном суставе. В то же время больные с неоплазиями представляют собой особую группу с точки зрения эффективности и токсичности стандартных методов лечения и профилактики тромботических осложнений. Общая эффективность противотромботической профилактики у них, как правило, ниже, а частота геморрагических осложнений выше, чем у больных в общей популяции.
Так, в одном из проспективных исследований 842 пациента с тромбоэмболической болезнью в анамнезе (включая 181 онкологического больного) получали стандартную терапию АВК (варфарин) с целью вторичной профилактики тромботических осложнений. В течение 1 года наблюдения частота рецидивов тромбозов/тромбоэмболий была выше в 3,2 раза среди больных с опухолевыми новообразованиями, чем у больных, не имеющих рака (20,7% и 6,8% соответственно). В то же время геморрагические осложнения были значимо более частыми в группе больных с неоплазиями (12,4% против 4,9%) [14]. Повышенная кровоточивость коррелировала с распространенностью опухоли, чаще развивалась в первый месяц терапии, но не могла быть объяснена «перелеченностью». Аналогичные данные были получены и в другом исследовании, в котором было показано, что частота повторных тромбозов соответственно для онкологической и неонкологической групп больных, получавших антикоагулянтную терапию, составляла 27,1% и 9%.
При этом частота геморрагических осложнений в тех же группах была 13,3% и 2,1% [15].
Результаты исследований свидетельствуют о меньшей эффективности профилактического назначения непрямых антикоагулянтов (АВК) у онкологических больных в сравнении с аналогичными по степени тромботического риска группами больных без опухоли при большем риске геморрагических осложнений. Кроме того, терапия непрямыми антикоагулянтами может осложняться лекарственными взаимодействиями, а рвота, нарушение питания и опухолевое или метастатическое поражение печени приводит к непредсказуемым колебаниям концентрации этой группы препаратов. Необходимость экстренных оперативных вмешательств повышает риск осложнений в связи с противосвертывающим эффектом, сохраняющимся 2–3 дня после отмены непрямых антикоагулянтов. Проведение химиотерапии, осложняющейся тромбоцитопенией и диктующей необходимость прерывания противосвертывающей терапии, заставляет проводить постоянный лабораторный контроль уровня гипокоагуляции, что не всегда удобно у больных с ограниченным венозным доступом. Некоторым больным приходится делать до 80 определений МНО за период лечения.
Альтернативой непрямым коагулянтам могут стать низкомолекулярные гепарины. Последняя группа препаратов имеет благоприятный профиль лекарственного взаимодействия и может эффективно применяться у больных, резистентных к терапии антивитаминами К.
Среди контролируемых исследований, сравнивающих эффективность длительного вторичного профилактического назначения НМГ и АВК, самым крупным является CLOT (Comparison of Low Molecular Weight Heparin Versus Oral Anticoagulant Therapy for Long Term Anticoagulation in Cancer Patients With Venous Thromboembolism) [16]. В этом исследовании больным с опухолевыми заболеваниями и венозной тромботической болезнью (тромбозы глубоких вен голени и/или тромбоэмболии легочной артерии) назначался далтепарин или варфарин. Из включенных 676 больных 338 были рандомизированно определены в группу, получавших далтепарин в дозе 200 МЕ/кг в течение 1 месяца, затем по 150 МЕ/кг в течение 5 месяцев; 338 больных – в группу, получавших далтепарин в дозе 200 МЕ/кг в течение 5–7 дней и АВК перорально под контролем МНО 2,0–3,0 на протяжении 6 месяцев. Группы больных были уравновешены по факторам риска. Солидные опухоли имели 90% пациентов, распространенный процесс отмечался у 67% больных в обеих группах.
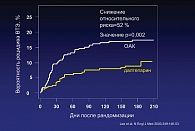
В течение 6 месяцев наблюдения повторные венозные тромбозы и/или тромбоэмболии легочной артерии возникли у 27 из 338 больных в группе далтепарина и у 53 больных из 338 в группе варфарина (HR 0,48 p = 0,002). Вероятность развития тромботических осложнений в течение 6 месяцев составила 17% в группе АВК и 9% в группе далтепарина. Риск геморрагических осложнений был сопоставим в обеих группах. Кровотечения имели место у 14% и 19% (большие кровотечения у 6% и 4%) больных в группах НМГ и непрямых антикоагулянтов соответственно. Общая выживаемость в период исследования (6 месяцев) составила 41% для группы далтепарина и 39% для группы антивитаминов К (р = 0,53). Авторы продолжили наблюдение за больными в течение еще полугода после окончания исследования и отметили, что если смертность тех, кто имел метастазы на момент тромбоза, была сопоставима – 69% и 72% (относительный риск 1,1 95%, конфиденциальный интервал 0,87–1,4, p = 0,46), то смертность пациентов без метастазов в эти сроки была почти вдвое ниже в группе далтепарина [17]. Год прожили 36% больных, получавших гепарин, и 20%, получавших альтернативную схему лечения (относительный риск 0,50 95%, конфиденциальный интервал 0,27–0,95, p = 0,03).
Таким образом, в исследовании показано преимущество НМГ (далтепарина) при профилактике повторных тромботических осложнений в сравнении с непрямыми антикоагулянтами у больных с опухолевыми заболеваниями без повышения риска геморрагических осложнений (рис. 1).
В другом сходном по схеме исследовании LITE (Longitudinal Investigation of Thromboembolism Etiology) 200 онкологических больных с симптомами острого тромбоза проксимальных вен нижних конечностей были рандомизированно разделены 1:1 на группы, применяющие НМГ (тинзапарин) или АВК (варфарин) на протяжении 3 месяцев [18]. В последующем они наблюдались в течение года. За период наблюдения рецидивы тромбозов и тромбоэмболий легочной артерии (ТЭЛА) были выявлены у 16 из 100 больных (16%), получавших гепарины с переходом на применение АВК в течение 3 месяцев. Во второй группе повторные тромботические осложнения развились у 7 из 100 больных (7%), получавших в течение 3 месяцев низкомолекулярный гепарин тинзапарин в дозе 175 МЕ/кг 1 раз в день. Частота кровотечений была равной (9%) в обеих группах.
Два меньших по объему исследования эффективности НМГ при вторичной профилактике тромбозов у онкологических больных было проведено с эноксапарином. В одном из них эноксапарин (1,5 мг/кг 1 раз в день) или варфарин (МНО 2,0–3,0) назначался течение 3 месяцев у 146 онкологических больных с тромбозом вен (ТВ) и ТЭЛА [19, 20].
В группе варфарина у 15 из 71 (21,1%) больного возникло серьезное осложнение в виде массивного кровотечения или рецидива ТВ либо ТЭЛА в течение 3 месяцев терапии, а в группе эноксапарина эти события наблюдались у 7 из 67 (10,5%) больных (p = 0,09). В группе варфарина в результате кровотечений наступило 6 смертей, в то время как в группе эноксапарина летальных исходов не было (таб. 1)
В другом рандомизированном клиническом исследовании 102 онкологических больных с острыми симптомами тромбоэмболии были разделены на группы АВК (варфарин) или эноксапарина в дозе 1 мг/кг (31 пациент) и 1,5 мг/кг (36 пациентов) в течение полугода [21]. Статистически значимых различий в частоте тромбозов – 6,9%, 6,3% и 10% для групп соответственно эноксапарина 1 мг/кг, 1,5 мг/кг и варфарина – достигнуто не было. Частота массивных кровотечений была существенно выше в группе эноксапарина 1,5 мг/кг (11,1%) в сравнении с его меньшей дозой (6,9%) и варфарином (2,9%). Эти данные находятся в некотором противоречии с результатами первого исследования, что ставит вопрос в отношении выбора эффективной и безопасной дозы препарата для вторичной профилактики тромбозов у онкологических больных. Напротив, только данные, полученные в исследовании CLOT с далтепарином и LITE с тинзапарином на значительном объеме наблюдений, показали значимое преимущество НМГ в сравнении АВК при вторичной профилактике тромбозов у онкологических больных при сопоставимой безопасности.
Это позволило Управлению по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) рекомендовать далтепарин натрия для продолжительного лечения тромбозов/ТЭЛА с клиническими проявлениями, чтобы снизить риск рецидива у онкологических больных [23].
В настоящее время ASCO (Американское общество клинической онкологии) рекомендует низкомолекулярные гепарины как препараты, имеющие преимущество при длительной вторичной профилактике тромбозов у онкологических больных [24] (таб. 2).
При невозможности использовать НМГ по экономическим или иным причинам, целесообразно применять АВК. Длительность вторичной профилактики должна составлять 6 месяцев и при некоторых обстоятельствах (сохранение опухоли и необходимость дальнейшего лечения повышающего риск тромбоза) она может быть увеличена.
В качестве контроля эффективности НМГ каких-либо лабораторных тестов не применяется. Для исключения гепарин-индуцированной тромбоцитопении, развивающейся у 0,5–1% больных, получающих НМГ, на первом этапе терапии контролируют содержание тромбоцитов крови раз в 10 дней. При необходимости проведения химиотерапии гепарины не отменяют и дозу не модифицируют при содержании тромбоцитов более 100х109/л. При снижении содержания тромбоцитов менее 50х109/л далтепарин отменяют полностью, а при содержании тромбоцитов крови в диапазоне от 50 до 100х109/л дозу модифицируют в зависимости от веса больного. Если вес больного менее 100 кг, то ее снижают на 2500 МЕ, если более 100 кг – на 3000 МЕ в сутки.
Новые препараты для длительной антикоагулянтной терапии у онкологических больных
Среди новых препаратов, которые имеют потенциал применения у онкологических больных с тромбозами, следует отметить ривароксабан и дабигатран. Ривароксабан – ингибитор фактора Ха для перорального применения, показавший некоторое преимущество перед НМГ (эноксапарин) при профилактике послеоперационных тромбозов после больших ортопедических операций [25]. Назначение ривароксабана 10 мг перорально однократно или эноксапарина 30 мг двукратно в сутки на протяжении 10 дней сопровождалось развитием тромбозов в 6,9% и 10,1% случаев соответственно (р = 0,0118). Пока нет данных об эффективности препарата при длительной вторичной тромбопрофилактике, однако удобство назначения (1 таблетка в день) и отсутствие необходимости постоянного инвазивного контроля антикоагулянтного эффекта позволяет рассматривать препарат как перспективный для данного показания.
Второй новый препарат – дабигатран – прямой ингибитор тромбина также для перорального применения, применялся для вторичной профилактики тромбозов в крупном контролируемом исследовании [26]. Недавно опубликованные данные свидетельствуют о равной эффективности дабигатрана и варфарина у больных с тромбозами – повторные тромбозы развились соответственно в 2,4% и 2,1% случаев при сопоставимой частоте массивных кровотечений (1,6% и 1,9%).
Лишь 5% больных в обеих группах имели рак, и вопрос о роли дабигатрана при вторичной профилактике тромбозов в онкологии остается открытым.
Тромбозы являются одной из ведущих причин смерти пациентов с опухолевыми заболеваниями, и существует необходимость использовать максимально эффективные методы лечения этого осложнения. Длительное применение антивитаминов К не позволяет гарантировать высокой эффективности и технически затруднено у онкологических больных из-за гастроинтестинальных проблем (тошнота, рвота) и трудностей сосудистого доступа для регулярного лабораторного контроля антикоагулянтного эффекта. Низкомолекулярные гепарины (далтепарин, тинзапарин) показали значимое преимущество над АВК, снизив риск повторных тромбозов и тромбоэмболий в два раза без увеличения риска геморрагических осложнений. Эти препараты не требуют постоянного лабораторного контроля и могут назначаться амбулаторно. Американское общество клинических онкологов рекомендует использовать низкомолекулярные гепарины у онкологических больных с тромбозами. В РФ далтепарин зарегистрирован для длительного применения в лечебных дозировках у онкологических больных.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.