количество статей
7261
Загрузка...
Пожалуйста, авторизуйтесь:
Теория
Тактика педиатра при острых гастроэнтеритах у детей: современные представления
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Педиатрия" №5
- Аннотация
- Статья
- Ссылки
Большинство случаев острых гастроэнтеритов у детей являются следствием вирусной инфекции, однако в нашей стране при острых кишечных инфекциях (ОКИ) в большинстве случаев шаблонно, вне зависимости от этиологии заболевания, назначаются антибиотики, использование которых нередко не достигает желаемого клинического и санирующего эффекта.
С учетом вариабельности клинической картины ОКИ различной этиологии, несвоевременной информативности бактериологического исследования, а также часто недостаточной специфичности результатов дополнительных лабораторных исследований обосновывается необходимость единого алгоритма ведения детей с острыми гастроэнтеритами.
В основу такого алгоритма, согласующегося с рекомендациями ESPGHAN, положена оценка тяжести состояния ребенка, определяющая тактику врача. Показано, что наиболее эффективным в качестве стартовой терапии у детей с острыми гастроэнтеритами вирусной этиологии является сочетание пероральной регидратации, пробиотиков и энтеросорбентов (препарат Смекта®).
Большинство случаев острых гастроэнтеритов у детей являются следствием вирусной инфекции, однако в нашей стране при острых кишечных инфекциях (ОКИ) в большинстве случаев шаблонно, вне зависимости от этиологии заболевания, назначаются антибиотики, использование которых нередко не достигает желаемого клинического и санирующего эффекта.
С учетом вариабельности клинической картины ОКИ различной этиологии, несвоевременной информативности бактериологического исследования, а также часто недостаточной специфичности результатов дополнительных лабораторных исследований обосновывается необходимость единого алгоритма ведения детей с острыми гастроэнтеритами.
В основу такого алгоритма, согласующегося с рекомендациями ESPGHAN, положена оценка тяжести состояния ребенка, определяющая тактику врача. Показано, что наиболее эффективным в качестве стартовой терапии у детей с острыми гастроэнтеритами вирусной этиологии является сочетание пероральной регидратации, пробиотиков и энтеросорбентов (препарат Смекта®).
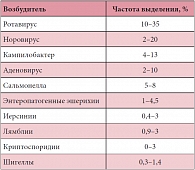
Острые кишечные инфекции (ОКИ) продолжают занимать ведущее место в структуре инфекционной патологии детского возраста, уступая по массовости, экономическому и социальному ущербу только острым респираторным заболеваниям и гриппу [1]. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно в мире ОКИ переносят около 2 млрд человек [2], при этом до 5 млн детей умирают от их осложнений [3, 4]. Не менее актуальна эта проблема и для Российской Федерации. Ежегодно на территории России регистрируется около полумиллиона диарейных заболеваний, бóльшая часть из которых приходится на пациентов раннего возраста. Из всех случаев ОКИ 60–65% регистрируется среди детей, особенно высока заболеваемость младенцев первых лет жизни (до 70%) [5]. Среди причин летальности, связанной с инфекционной патологией, ОКИ стойко занимают второе-третье место после заболеваний верхних дыхательных путей и ВИЧ-инфекции [2]. По данным европейских эпидемиологических исследований, большинство случаев острых гастроэнтеритов у детей являются следствием вирусной инфекции, наибольший удельный вес приходится на рота- и норовирусы. Сальмонелла и кампилобактер являются основными бактериальными агентами в этиологии ОКИ (Табл.) [6].
Вопросы диагностики острых кишечных инфекций до настоящего времени остаются предметом дискуссии. Клиническая картина заболевания может быть довольно вариабельной, при этом трудно выделить отдельные симптомы, которые могли бы свидетельствовать о конкретной этиологии гастроэнтерита. По мнению европейских исследователей, такие клинические проявления, как фебрильная лихорадка (свыше 40 °С), наличие примеси крови в стуле, выраженный абдоминальный синдром и неврологическая симптоматика с большей вероятностью могут указывать на бактериальную этиологию заболевания, в то время как рвота и сочетание кишечных и респираторных проявлений более свойственны вирусным ОКИ [6]. В практике отечественных педиатров ведущее место в диагностическом алгоритме острых гастроэнтеритов до настоящего времени продолжает занимать бактериологическое исследование кала. Данный подход расходится с рекомендациями Европейского общества детских гастроэнтерологов, гепатологов и нутрициологов (ESPGHAN) [6], в соответствии с которыми микробиологические тесты обычно не требуются по следующим причинам:
- возбудителей инфекции редко удается идентифицировать;
- результаты исследования становятся доступными лишь спустя 2–3 дня, при этом терапевтические мероприятия обычно следует начинать незамедлительно независимо от этиологического фактора ОКИ;
- затраты на исследование достигают 680–1100 евро на 1 положительный результат;
- выявление здоровых носителей усложняет интерпретацию полученных результатов.
Принимая во внимание вариабельность клинической картины, несвоевременную информативность бактериологического исследования, а также часто недостаточную специфичность результатов дополнительных лабораторных исследований, представляется необходимым наличие единого алгоритма ведения детей с острыми гастроэнтеритами, в основе которого первично будет лежать оценка тяжести состояния ребенка, определяющая тактику врача. Основополагающим фактором, определяющим тяжесть состояния ребенка при острых кишечных инфекциях, является степень дегидратации. Безусловно, лучшим критерием степени обезвоживания является процент потери веса, по сравнению с исходным показателем. В соответствии с рекомендациями ВОЗ, в зависимости от степени обезвоживания пациенты могут быть распределены на 3 группы:
- дегидратация минимальная или отсутствует (потери < 3% от первоначальной массы тела);
- дегидратация легкой – средней степени тяжести (потери 3–9% от первоначальной массы тела);
- тяжелая дегидратация (потери > 9%) [7].
К сожалению, данные о весе ребенка до начала заболевания не всегда доступны педиатру, поэтому на практике врачу, чтобы оценить тяжесть состояния больного, часто приходится ориентироваться на ряд других клинических проявлений (активность ребенка, частота стула, рвоты и мочеиспускания, состояние кожи и слизистых, тургор кожи и др.). В соответствии с рекомендациями рабочей группы ESPGHAN, наиболее чувствительными и специфичными маркерами дегидратации являются удлинение времени наполнения капилляров, снижение тургора кожи и дыхательные нарушения [6]. Адекватная оценка степени тяжести состояния ребенка лежит в основе дальнейшей тактики педиатра. В большинстве случаев своевременно начатые лечебные мероприятия позволяют продолжить терапию в домашних условиях. По мнению экспертов ESPGHAN, госпитализация показана лишь тем детям, которые нуждаются в манипуляциях, проводимых исключительно в условиях стационара (например, во внутривенной регидратации), в следующих случаях:
- шок;
- тяжелое обезвоживание (> 9% массы тела);
- неврологические нарушения (летаргия, судороги и т.д.);
- упорная рвота желчью;
- неэффективная пероральная регидратация;
- подозрение на хирургическую патологию;
- случаи заболевания, когда родители не могут обеспечить необходимый уход в домашних условиях или имеют социальные или материальные затруднения [6].
В нашей стране госпитализация показана также военнослужащим и детям, обучающимся в закрытых военных учреждениях (военные суворовские училища, Пансион воспитанниц Министерства обороны и др.) [8]. В качестве первой линии терапии пациентов с ОКИ, вне зависимости от этиологии заболевания, должна быть использована пероральная регидратация. Накопленный мировой опыт позволяет сделать заключение, что пероральная регидратация при легких и среднетяжелых формах ОКИ не только является предпочтительным методом лечения у детей, по сравнению с парентеральным методом введения жидкости, вследствие физиологического поступления растворов и отсутствия побочных эффектов, свойственных инфузионной терапии, но и позволяет добиться существенного сокращения сроков заболевания. Результаты рандомизированных контролируемых исследований убедительно показали, что при своевременном проведении оральной регидратации достоверно реже отмечаются побочные эффекты от терапии, сокращается продолжительность госпитализации, при этом отсутствуют различия в прибавке в весе пациентов, а доля случаев, когда терапия оказывается неэффективной, не превышает 4% [9].
Современные комплексные растворы для оральной регидратации позволяют добиться наиболее высокой эффективности применения при коррекции дегидратации умеренной степени у детей практически любого возраста [10]. Однако следует учитывать: регидратационные растворы не уменьшают частоту стула, не укорачивают продолжительность заболевания, но предотвращают тяжелые последствия, обусловленные дегидратацией [11], что особенно актуально у детей первых двух лет жизни в связи с высоким риском развития тяжелого обезвоживания. Принципиально важным моментом при всех ОКИ является отказ от водно-чайных пауз, а «голодные» диеты, особенно у детей первого года жизни, ослабляют защитные силы организма и замедляют процессы репарации слизистой оболочки кишечника [12].
Эффективность применения средств медикаментозной терапии при острых гастроэнтеритах у детей продолжает обсуждаться. К сожалению, в нашей стране по-прежнему при ОКИ в 70% случаев шаблонно, вне зависимости от этиологии заболевания, назначаются антибиотики. Проведен ряд работ, указывающих на нецелесообразность назначения антибактериальной терапии при острых гастроэнтеритах вирусной этиологии [13, 14]. При анализе результатов терапии было выявлено, что ведение больных с водянистой диареей без использования антибиотиков вполне оправдано, а назначение антибактериальной терапии по поводу сопутствующей бактериальной инфекции не влияет на сроки купирования гастроэнтерита. Аналогичные рекомендации представлены в протоколе ESPGHAN по ведению детей с острыми гастроэнтеритами, в соответствии с которым антибактериальная терапия может быть показана в тяжелых случаях шигеллеза, сальмонеллеза, а также на ранних стадиях инфекции, вызываемой кампилобактером [6].
Традиционное использование при ОКИ антибиотиков или других антибактериальных химиопрепаратов порой не достигает желаемого клинического и санирующего эффекта, как считают, вследствие резистентности патогена к широко используемым в клинической практике антибактериальным препаратам. Как правило, дальнейшая терапевтическая тактика в этих случаях строится по принципу дополнительного назначения или замены на антибиотики «резерва» [15–16]. При этом нередко не учитываются другие возможные причины неэффективности проводимой этиотропной антибактериальной терапии и, в первую очередь, состояние микробиоценоза кишечника. Установлено, что фуразолидон и гентамицин как лекарственные средства «стартовой» этиотропной терапии легких и среднетяжелых форм ОКИ у детей в настоящее время обладают низкой санирующей эффективностью, способствуют росту представителей условно-патогеннной микрофлоры и, тем самым, прогрессированию нарушений кишечного микробиоценоза.
Использование этих лекарственных средств этиотропной терапии ОКИ у детей в настоящее время является нерациональным. По данным литературы, независимо от этиологии ОКИ у детей в большинстве случаев в остром периоде заболевания имеют место выраженные изменения микрофлоры кишечника [17–20]. Естественно, что нарушение количественного и качественного состава микрофлоры кишечника и, соответственно, ее физиологических функций в организме не может не отразиться на течении заболевания. Использование антибиотиков в этих случаях не только не достигает нужного результата, но и нередко приводит к прогрессированию нарушений микробиоценоза кишечника, угнетению местного (кишечного) звена иммунитета, выполняющего наравне с нормофлорой кишечника основную функцию защиты и санации организма от возбудителей ОКИ [21]. С точки зрения рабочей группы ESPGHAN, эффективной альтернативой применения антибактериальных препаратов в лечении пациентов с острыми гастроэнтеритами могут стать пробиотики, однако при выборе пробиотических препаратов следует останавливаться на штаммах с доказанной клинической эффективностью. Результаты современных исследований позволяют отнести к подобным штаммам Lactobacillus GG, L. reuteri и S. boulardii [6]. Частым при ОКИ является назначение энтеросорбентов.
Энтеросорбция – метод эфферентной терапии, основанный на связывании и выведении из организма через желудочно-кишечный тракт с лечебной или профилактической целью эндогенных и экзогенных веществ, надмолекулярных структур и клеток. Применительно к вирусным гастроэнтеритам использование энтеросорбентов обеспечивает фиксацию на их поверхности и выведение свободно присутствующих в кишечном содержимом вирусов, снижение концентрации желчных кислот, усиливающих выраженность диарейного синдрома, непереваренных углеводов и газов. Эффективным дополнением к регидратационной терапии при острых гастроэнтеритах у детей может служить использование диоктаэдрического смектита (Смекты). Смекта® является препаратом природного происхождения, его производство осуществляется в соответствии со всеми стандартами GMP (Good Manufacturing Practice – надлежащая производственная практика). В силу уникальной структуры препарат обладает двойным механизмом действия:
- благодаря мощным адсорбционным свойствам Смекта® притягивает и удерживает полярные молекулы (желчные кислоты, HCl, пепсин, непереваренные углеводы, токсины, вирусы и газы), демонстрируя высокую обменную емкость;
- цитомукопротекторный эффект – в просвете кишки слои пластинок Смекты разворачиваются в виде ленты и обволакивают поврежденную поверхность, сохраняясь на слизистой оболочке в течение 6 часов после приема. Последнее обеспечивает предотвращение проникновения патогенных агентов сквозь слизистый барьер, защиту слизистой оболочки от дальнейшего повреждения, способствует восстановлению поврежденной слизистой оболочки кишечника.
В 2006 г. H. Szajewska и соавт. был проведен метаанализ рандомизированных контролируемых исследований эффективности применения диосмектита в терапии острых кишечных инфекций у детей. Авторы проанализировали результаты 9 таких исследований, 6 из которых показали достоверное сокращение продолжительности диареи у детей на фоне приема Смекты, по сравнению с плацебо. Вероятность выздоровления на 3-и сутки от начала заболевания в группе исследования была достоверно выше, чем в группе контроля, при одинаковой частоте побочных эффектов от терапии в обеих группах [22]. В двух двойных слепых плацебоконтролируемых исследованиях, проведенных под руководством C. Dupont (2009) в Перу и Малайзии (в оба исследования было включено более 600 детей в возрасте от 1 до 36 месяцев), было продемонстрировано, что использование Смекты при острых гастроэнтеритах достоверно уменьшает объем стула, особенно среди детей, инфицированных ротавирусом [23]. Результаты данных исследований стали основанием для рекомендации использования диосмектита в комплексной терапии ОКИ у детей в соответствии с протоколом ESPGHAN (2008) [6].
Российскими исследователями проведен ряд работ, указывающих на целесообразность «стартовой» терапии, предусматривающей использование сочетания пероральной регидратации, пробиотиков и энтеросорбентов при острых гастроэнтеритах вирусной этиологии [13, 14]. Проведенный ретроспективный анализ эффективности терапии больных ОКИ вирусной этиологии продемонстрировал, что наиболее эффективной стартовой терапией аденовирусных гастроэнтеритов является сочетание пероральной регидратации с энтеросорбентами (Смекта®) и пробиотиками [14].
В некоторых отечественных публикациях можно встретить рекомендации по использованию ферментотерапии в комплексном лечении пациентов с ОКИ с целью коррекции переваривающей и всасывательной функции желудочно-кишечного тракта. При инвазивном типе диареи препаратом стартовой терапии может являться панкреатин и его аналоги, при осмотическом типе – ферменты с высокой дисахаридазной активностью. При наличии явлений метеоризма независимо от типа диареи эффективными являются препараты на основе панкреатина с ди- или симетиконом, так как пеногасители, входящие в состав этих препаратов, препятствуют газообразованию, также при вздутиях может использоваться Смекта®.
В остром периоде заболевания независимо от типа диареи не следует назначать препараты на основе панкреатина с компонентами бычьей желчи, поскольку они могут усилить диарейный синдром. Компоненты бычьей желчи (желчные кислоты и др.) стимулируют моторику кишечника и желчного пузыря, усиливают осмотическое давление химуса, оказывают повреждающее действие на слизистую оболочку, а при микробной деконъюгации способствуют активации циклических аденозинфосфатов (цАМФ) энтероцитов с последующим развитием или усилением гиперсекреции или осмотического компонента диареи. Не следует также использовать ферментные препараты с высокой протеолитической активностью, так как в большинстве случаев протеолитическая активность химуса в остром периоде ОКИ повышена. Кроме того, назначение протеолитических ферментов при ротавирусной инфекции может стимулировать репродукцию вируса, усилить диарейный синдром и тяжесть заболевания.
Следует отметить, что, несмотря на опыт российских врачей по применению ферментов в комплексной терапии ОКИ у детей, европейскими экспертами данные препараты не рекомендуются к использованию, учитывая отсутствие убедительных доказательств их эффективности. Наряду с этим, анализ данных по применению цинка, пребиотиков, гомеопатии, проведенный в рамках создания современного протокола ESPGHAN по ведению детей с острыми гастроэнтеритами, также получил довольно противоречивые результаты, не позволяющие рутинно назначать данные препараты детям при ОКИ [6]. Применение энтеросорбентов обеспечит безопасное решение проблемы диареи без системного действия.
1. Горелов А.В., Милютина Л.Н., Усенко Д.В. Клинические рекомендации по диагностике и лечению острых кишечных инфекций у детей. М., 2005. 106 с.
2. Tolia V. Acute infections diarrea in children // Current Treat. Options Infect. Dis. 2002. Vol. 4. P. 183–194.
3. Воротынцева Н.В. Терапия острых кишечных инфекций у детей // Педиатрия. 1995. № 4. С. 76–78.
4. Покровский В.И., Онищенко Г.Г., Черкасский Б.А. Инфекционные болезни в конце XX века и санитарно-эпидемиологическое состояние в XXI веке // Журнал микробиологии. 2002. № 3. С. 16–23.
5. Васильев Б.Я., Сироткин А.К., Сухинин В.П. Применение ПЭМ в диагностике небактериальных гастроэнтеритов // Острые кишечные инфекции: Сборник научных трудов. Л., 1986. С. 40–42.
6. Guarino A., Albano F., Ashkenazi S. et al. European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe // J. Pediatr. Gastroenterol. Nutr. 2008. Vol. 46. Suppl. 2. P. S81–S122.
7. The treatment of diarrhea – a manual for physicians and other senior health workers. Geneva: World Health Organization, 2005. Fourth revision // www.whqlibdoc.who.int/hq/2003/WHO_FCH_CAH_03.7.pdf.
8. Дизентерия и другие острые кишечные диарейные инфекции. Указания по диагностике, лечению и профилактике в Вооруженных Силах РФ. М., 2000. 132 с.
9. Fonseca B.K., Holdgate A., Craig J.C. Enteral vs intravenous rehydration therapy for children with gastroenteritis: a meta-analysis of randomized controlled trials // Arch. Pediatr. Adolesc. Med. 2004. Vol. 158. № 5. P. 483–490.
10. Подколзин А.Т., Мухина А.А., Шипулин Г.А. и др. Изучение этиологии острых кишечных инфекций у детей, госпитализированных в инфекционные отделения стационаров г. Москвы // Инфекционные болезни. 2004. Т. 2. № 4. С. 85–91.
11. Шеянов Г.Г. Пути совершенствования метода пероральной регидратации при ОКИ у детей // Актуальные вопросы инфекционной патологии у детей: Материалы третьего конгресса педиатров-инфекционистов России. М., 2004. С. 265.
12. Шептулин А.А. Алгоритм диагностики и лечения при синдроме острой диареи // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2002. № 1. С. 18–22.
13. Дорошина Е.А. Клинико-эпидемиологические особенности и вопросы терапии норовирусной инфекции у детей: Дисс. канд. мед. наук. М., 2010. 113 с.
14. Козина Г.А. Клинико-эпидемиологические особенности и вопросы терапии острых кишечных инфекций аденовирусной этиологии у детей: Дисс. канд. мед. наук. М., 2010. 153 с.
15. Архипина С.А. Сравнительная оценка лечебного эффекта фуразолидона и эрсефурила при шигеллезе: Автореф. дисс. … канд. мед. наук. Курск, 2001. 116 с.
16. Грацианская А.Н. Нифуроксазид в лечении кишечных инфекций // Фарматека. 2004. № 13 (90). С. 53–69.
17. Горелов А.В. Современные подходы к стартовой терапии острых кишечных инфекций у детей // Вопросы современной педиатрии. 2003. Т. 2. № 3. С. 17–20.
18. Климовицкая Е.Г. Клинико-бактериологическая и иммунологическая эффективность пробиотиков Бифидумбактерина форте и Бифиформа при лечении острых кишечных инфекций у детей раннего возраста: Автореф. … дисс. канд. мед. наук. Иваново, 2002. 24 с.
19. Новокшонов А.А., Дорошенко Е.О., Мурашова А.О. Пробифор в лечении острых кишечных инфекций у детей и взрослых // Тезисы докладов Третьей Международной Ассамблеи «Новые медицинские технологии». М., 2001. С. 52–53.
20. Pedone C.A., Bernabeu A.O., Postaire E.R. et al. The effect of supplementation with milk fermented by Lactobacillus casei (strain DN-114 001) on acute diarrhoea in children attending day care centres // Int. J. Clin. Pract. 1999. Vol. 53. № 3. P. 179–184.
21. Погорельская Л.В., Травкина И.П. Программа восстановления микрофлоры (бифидокоррекция) и профилактика дисбактериоза: Методические рекомендации. М., 2002. 34 с.
22. Szajewska H., Dziechciarz P., Mrukowicz J. Meta-analysis: Smectite in the treatment of acute infectious diarrhoea in children // Aliment. Pharmacol. Ther. 2006. Vol. 23. № 2. P. 217–227.
23. Dupont C., Foo J.L., Garnier P. et al. Oral diosmectite reduces stool output and diarrhea duration in children with acute watery diarrhea // Clin. Gastroenterol. Hepatol. 2009. Vol. 7. № 4. P. 456–462.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Большинство случаев острых гастроэнтеритов у детей являются следствием вирусной инфекции, однако в нашей стране при острых кишечных инфекциях (ОКИ) в большинстве случаев шаблонно, вне зависимости от этиологии заболевания, назначаются антибиотики, использование которых нередко не достигает желаемого клинического и санирующего эффекта.
С учетом вариабельности клинической картины ОКИ различной этиологии, несвоевременной информативности бактериологического исследования, а также часто недостаточной специфичности результатов дополнительных лабораторных исследований обосновывается необходимость единого алгоритма ведения детей с острыми гастроэнтеритами.
В основу такого алгоритма, согласующегося с рекомендациями ESPGHAN, положена оценка тяжести состояния ребенка, определяющая тактику врача. Показано, что наиболее эффективным в качестве стартовой терапии у детей с острыми гастроэнтеритами вирусной этиологии является сочетание пероральной регидратации, пробиотиков и энтеросорбентов (препарат Смекта®).
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.