Терапия соматогенных психозов у больных с онкогематологическими заболеваниями
- Аннотация
- Статья
- Ссылки
Введение
Течение онкогематологических заболеваний часто осложняется развитием психических расстройств. По современным эпидемиологическим оценкам, распространенность таких нарушений среди больных с онкогематологическими заболеваниями достигает 44,1% [1].
Психические расстройства при онкогематологических заболеваниях представлены широким спектром нарушений – от невротических состояний до психозов. К числу наиболее тяжелых форм психических расстройств при онкогематологических заболеваниях относятся соматогенные психозы, частота которых при такой гематологической патологии составляет 7,3% [1]. Соматогенные психозы рассматривают как значимый неблагоприятный прогностический фактор, способствующий утяжелению соматической патологии вследствие существенных сложностей диагностики и терапии [2].
Терапия соматогенных психозов при онкогематологических заболеваниях представляет собой самостоятельную проблему. В качестве основных принципов терапии выделяют эмпирический подбор препаратов с учетом индивидуальных особенностей, назначение психотропных средств в соответствии с их основными показаниями на основе анализа клинической картины психопатологических расстройств, выбор психотропных средств на основании оценки пропорции риска/пользы с учетом профиля переносимости и безопасности, а также потенциальных лекарственных взаимодействий. Оценка эффективности терапии проводится по шкале общего клинического впечатления.
Материалы и методы
В исследование включали всех пациентов с диагностированными онкогематологическими заболеваниями, у которых в процессе наблюдения и лечения в Федеральном государственном бюджетном учреждении «Гематологический научный центр» Минздравсоцразвития РФ в период с 2007 по 2011 г. наблюдались соматогенные психозы, соответствовавшие диагностическим рубрикам F05 или F06 МКБ-10.
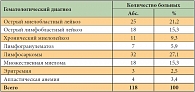
Клинически были обследованы 118 больных. Средний возраст пациентов составил 53 года (от 16 до 84 лет). Исследуемая выборка включала 64,7% мужчин. Распределение больных в соответствии с гематологическим диагнозом приведено в таблице 1.
В изученной выборке преобладали больные с острыми лейкозами и тяжелыми лимфопролиферативными заболеваниями, что соотносится с представлением о значимой роли соматогенного фактора в формировании соматогенных психозов при онкогематологических заболеваниях.
Результаты исследования обработаны с помощью компьютерной программы Statistica for Windows 5.5 с использованием двухстороннего t-критерия.
Результаты и обсуждение
Установлена типологическая гетерогенность психотических расстройств у больных с заболеваниями системы крови.
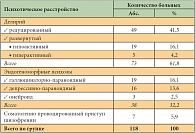
Выявлено три типа соматогенных психозов: 1) делирий (F05.0 «Делирий не на фоне деменции» по МКБ-10), 2) эндогеноморфные психозы (F06.2 «Органическое бредовое (шизофреноподобное) расстройство» по МКБ-10) (галлюцинаторно-бредовые, депрессивно-бредовые, онейроидные симптомокомплексы) и 3) соматогенно провоцированные обострения шизофрении (F20.01 «Параноидная шизофрения, приступообразное течение» и F30.2 «Мания с психотическими симптомами» по МКБ-10) (табл. 2).
Первый тип, делирий, выявлен в 73 (61,9%) наблюдениях. В этой группе клиническая картина в целом была сопоставима с делириозными состояниями при других тяжелых соматических заболеваниях [3] и включала нарушения сознания, наплывы зрительных галлюцинаций, острый чувственный (галлюцинаторный) бред, выраженное двигательное возбуждение. Делириозные расстройства носили преимущественно стертый характер, причем помрачение сознания протекало с выраженными астеническими и апатическими расстройствами. Явления помрачения сознания были представлены полной или частичной дезориентировкой в окружающем. В ряду аффективных нарушений преобладало чувство тревоги, страха с явлениями растерянности. В отдельных случаях (5 (6,8%) наблюдений) отмечались эпизоды тревожно-злобного возбуждения с агрессивными действиями в отношении медицинского персонала.
По завершении психоза (психопатологические расстройства редуцировались по мере улучшения соматического состояния) выявлялись признаки ретроградной амнезии (полная утрата воспоминаний, связанных с симптомами делирия).
На протяжении 5–7 дней после редукции психопатологической симптоматики сохранялась неустойчивость настроения со склонностью к подавленности, а также астения с повышенной утомляемостью, быстрой истощаемостью при минимальных физических или умственных нагрузках, капризность и обидчивость.
В клинической картине доминировали явления раздражительной слабости, кратковременные эпизоды повышенной возбудимости, сменявшиеся длительными периодами истощаемости. Выявлялась аффективная лабильность с преобладанием гипотимии; при этом подавленность с повышенной слезливостью чередовалась с апатией или элементами дисфории. В некоторых случаях отмечались явления астенического ментизма с потоком образных представлений. Резко расстраивалась функция внимания, а затем манифестировали нарушения ориентировки во времени и пространстве.
В нашем исследовании длительность делирия составляла в среднем 4,5 ± 0,8 дней. В 7 (29,2%) случаях развернутого делирия, несмотря на проводимую терапию, у больных сформировалось аментивное расстройство сознания с хаотическим беспорядочным возбуждением, сопровождавшееся развитие септического шока и завершившееся у 6 (25%) больных летальным исходом. Еще в 3 (12,5%) случаях развернутого делирия наблюдалось развитие неалкогольного корсаковского синдрома с массивной полинейропатией.
Второй тип, эндогеноморфные психозы, был представлен в 38 (32,2%) наблюдениях. Наряду с более длительным, чем при делирии, (7–11 дней) течением и сопоставимостью клинических проявлений (изменения сознания, обманы восприятия) в первые сутки, в картине таких психозов постепенно обнаруживались значительные отличия от картины делирия.
Эндогеноморфные психозы в изученной выборке были представлены следующими формами: галлюцинаторно-параноидными и депрессивно-бредовыми психозами, а также состояниями онейроидного помрачения сознания.
При галлюцинаторно-параноидных состояниях (19 (50%) наблюдений) с первых же дней психоза вербальные иллюзии, манифестирующие в дебюте по типу акоазмов (шипение, скрипы) или элементарных функциональных галлюцинаций (обращенные к пациенту отдельные слова или фразы, возникающие на фоне реальных звуков медицинской аппаратуры или речи персонала), постепенно усложнялись. Формировались вербальные псевдогаллюцинации и явления психического автоматизма (идеи воздействия с помощью медицинского оборудования). При этом манифестировали соответствующие содержанию обманов восприятия бредовые идеи преследования. Фабула бреда ограничивалась мало систематизированными идеями отношения. Больные придавали особое значение любым действиям медицинского персонала, «замечали», что врачи как-то по-особенному переглядываются в их присутствии либо что-то недоговаривают, вероятно, чтобы избежать сообщения «фатальной» информации. Доминировали представления о «предвзятости» медицинского персонала, однако фабула «заговора» не разрабатывалась.
В 16 наблюдениях (42,1%) манифестация депрессивно-бредовых состояний сопровождалась выраженной гипотимией с отчетливым тревожным аффектом, достигающим максимальной выраженности в вечерние часы. У 8 из 16 (50%) больных в ночное время отмечалось развитие обманов восприятия в форме истинных гипнагогических зрительных галлюцинаций, имевших элементарный характер. В 6 из 16 (37,5%) наблюдений депрессивные расстройства приобретали витальный характер с чувством тоски, беспомощности, идеями самообвинения и даже суицидальными мыслями. По мере нарастания тревожного и тоскливого аффекта присоединялись параноидные расстройства, представленные явлениями персекуторного бреда (идеи отношения, преследования). Последние отличались монотематичностью фабулы, не обнаруживая тенденции к систематизации, и ограничивались идеями предвзятого отношения и осуждения со стороны окружающих (медицинский персонал, пациенты) либо идеями преследования судебными органами за «прошлые проступки».
Преобладали (статистически значимо, р < 0,05) галлюцинаторно-параноидные и депрессивно-бредовые состояния с длительностью менее 2 недель. В процессе обратной динамики психоза последовательной редукции подвергались бредовые идеи, галлюцинации, а затем – депрессивные проявления и астенические расстройства.
В отдельных наблюдениях (3 (7,9%) пациента из 118) на фоне тяжелого соматического состояния, требующего наблюдения в условиях отделения интенсивной терапии, нарушения сознания приобретали признаки, свойственные онейроиду [4] с явлениями двойной ориентировки. Больные одновременно выступали в роли пациентов клиники и сторонних наблюдателей. Формирующиеся при этом сценоподобные галлюцинаторные расстройства характеризовались (в отличие от фантастически-иллюзорных картин, свойственных «классическим» онейроидным психозам) обыденным содержанием. Картина психоза дополнялась признаками кататонии с эпизодами ступора и мутизма. Наряду с онейроидно-кататоническими проявлениями выявлялись отрывочные идеи преследования.
Третий тип соматогенных психозов – соматогенно провоцированные приступы в рамках приступообразной шизофрении – был выявлен в 7 (5,9%) наблюдениях. У 6 больных приступы протекали с галлюцинаторно-параноидным, а у 1 – с маниакально-бредовым синдромом.
Психопатологическая структура психоза определялась сочетанием процессуально обусловленной и соматогенной патологии. Наряду с признаками, свойственными соматогенным психозам (помрачение сознания с дезориентировкой в месте и времени, психомоторное возбуждение, суточные колебания с усилением в вечернее и ночное время), уже в дебюте психоза выявлялись психопатологические нарушения, присущие эндогенно-процессуальному заболеванию. В дальнейшем, по мере нормализации соматического состояния пациента с обратным развитием нарушений сознания и других соматогенных расстройств, проявления психоза не редуцировались, а приобретали синдромально завершенный характер психотического приступа в рамках приступообразной шизофрении. При психозах с ведущей галлюцинаторно-параноидной симптоматикой восстановление соматического состояния сопровождалось кристаллизацией бреда (воздействие на мысли и поступки со стороны персонала либо спецслужб, в том числе с помощью медицинского оборудования), сменой устрашающих зрительных галлюцинаций вербальными псевдогаллюцинациями. Манифестация галлюцинаторно-бредовой симптоматики сопровождалась агрессией с попытками физического насилия в отношении «преследователей» – медработников и пациентов.
В случаях соматогенно провоцированных приступов шизофрении эндогенный психоз приобретал затяжное течение; ремиссия формировалась лишь спустя 2,5–3 месяца даже в условиях адекватной терапии.
При анализе эффективности терапии у изученных больных с соматогенными психозами становится очевидным, что проведение психофармакотерапии у таких больных с заболеваниями системы крови сопряжено со значительными сложностями, обусловленными следующими факторами. Первый из них – необходимость применения психотропных средств на фоне длительных курсов химиотерапии, включающей цитостатики, либо последние в сочетании с кортикостероидами. Применение этих средств не только повышает риск ятрогенных психических расстройств, усложняющих клиническую картину, но и затрудняет проведение психофармакотерапии в связи с возможностью побочных эффектов и нежелательных взаимодействий [5]. Второй фактор – коморбидность заболеваний системы крови с хроническим алкоголизмом, выявленная в анамнезе почти у 1/3 пациентов (28,1%). Последствия длительной алкоголизации способствуют облегчению декомпенсации соматического состояния (ацидоз, гипоксия, дефицит витаминов комплекса В, падение содержания калия и магния в крови, сдвиг лейкоцитарной формулы влево, повышение СОЭ), что диктует необходимость коррекции психофармакотерапии.
В соответствии со сложившимися стандартами препаратами выбора для купирования соматогенных психозов считаются антипсихотики [6], среди которых, наряду с современными атипичными антипсихотиками (рисперидон, кветиапин), используются и бутирофеноны (галоперидол), обладающие мощным антипсихотическим действием. Парентеральное и особенно внутривенное введение этих препаратов снижает риск токсических эффектов в отношении внутренних органов [7, 8]. При необходимости дополнительной седации в случаях тяжелого психомоторного возбуждения предполагается комбинированное применение бутирофенонов с инъекционными формами бензодиазепиновых транквилизаторов (лоразепам, диазепам, феназепам) или других антипсихотиков (производные фенотиазина, тиоксантены) [9]. Однако использование транквилизаторов при психозах у больных с заболеваниями системы крови сопряжено с определенными сложностями, связанными с вероятностью угнетения активности дыхательного центра, в связи с чем препараты этого класса рассматривают в качестве вспомогательных средств [10]. Как установлено в ряде исследований, наиболее безопасным является использование бензодиазепинов при тяжелом психомоторном возбуждении, резистентном к монотерапии антипсихотиками, а также у пациентов с явлениями непереносимости антипсихотических средств [11]. Дополнительным ограничивающим фактором является то, что бензодиазепины сами могут послужить причиной развития делирия [12] и не рекомендуются к применению у пациентов с лекарственной и алкогольной зависимостью в анамнезе, а также в пожилом возрасте.
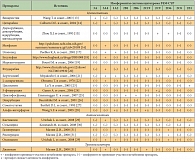
В ходе исследования не зафиксировано ни одного случая неблагоприятных лекарственных взаимодействий между психотропными средствами и препаратами, применяющимися для химиотерапии заболеваний системы крови. Учитывая данные по метаболизму цитостатиков, использовавшихся в терапии больных изученной выборки, риск взаимодействия психотропных препаратов с этими лекарственными средствами можно считать минимальным (табл. 3).
Данные о психотропных средствах, применявшихся при терапии пациентов, вошедших в настоящее исследование, представлены в таблице 4. Из этих данных следует, что схема лечения базировалось на сложившихся принципах.
Терапия соматогенных психозов у изученных больных носила поэтапный характер. Целью первого этапа являлось купирование психоза, второго – поддерживающее лечение, направленное на профилактику рецидива психотического расстройства.
Предпочтение отдавалось внутривенному введению психотропных средств (в большинстве случаев – через венозный катетер), что соответствует рекомендациям по ведению больных, страдающих заболеваниями системы крови [32].
При делириозных расстройствах сознания основной объем терапевтического вмешательства концентрировался на первом этапе; лечение непродолжительно и включает применение антипсихотиков бутирофенонового ряда (галоперидол до 15 мг/сут). При необходимости быстрой седации или купирования тревожных/инсомнических расстройств в терапевтическую схему вводился диазепам (до 20 мг/сут).
Терапия эндогеноморфных психозов требовала более интенсивных воздействий (суточные дозы антипсихотиков повышались: галоперидол до 10–30 мг) и большей длительности (до 2 недель).
Наиболее продолжительного (до 1,5–2 месяцев) лечения с использованием указанных в таблице 4 максимальных дозировок препаратов требовали соматогенно провоцированные приступы шизофрении. При этом назначения корректировались в соответствии с динамикой соматической патологии (дозы снижались при утяжелении соматического состояния).
На втором этапе лечения применялись в основном атипичные антипсихотики. Конкретные препараты, их дозировка и средняя продолжительность курса указаны в таблице 4. Несмотря на то что в отношении последних нередко указывается на неблагоприятное воздействие на систему кроветворения, значимых изменений в показателях периферической крови нами выявлено не было. Тем не менее при проведении терапии этими препаратами необходим периодический контроль лейкоцитарной формулы.
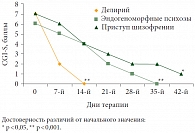
Динамика психического состояния при применении психотропных препаратов у больных с соматогенными психозами, оцениваемая при помощи шкалы общего клинического впечатления (Clinical Global Impression Scale – CGI-S), представлена на рисунке.
Клинически значимых побочных эффектов в ходе терапии применяемыми психотропными препаратами или их неблагоприятных взаимодействий с соматотропными препаратами (включая кортикостероиды – преднизолон, дексаметазон – и цитостатики – цитарабин, даунорубицин, винкристин, циклофосфамид) отмечено не было, хотя такая вероятность рассматривается в некоторых исследованиях [33, 34].
Заключение
Таким образом, предложены терапевтические мероприятия, направленные на купирование симптоматических психозов у больных с онкогематологическими заболеваниями. Такие мероприятия включают применение психотропных препаратов, назначаемых в зависимости от клинической картины расстройства и с учетом возможного возникновения побочных действий.
Материалы и методы. Было клинически оценено состояние 118 пациентов, у которых наблюдались соматогенные психозы, соответствовавшие на момент развития диагностическим рубрикам F05 или F06MKB-10. Пациентам проводилась психофармакотерапия
по поводу выделенных состояний.
Результаты. Выделено 3 типа соматогенных психозов при онкогематологических заболеваниях: делирий – в 73 (61,9%) наблюдениях, эндогеноморфные психозы – в 38 (32,2%) наблюдениях и соматогенно провоцированные обострения шизофрении – в 7 (5,9%) наблюдениях. Описана клиническая картина указанных расстройств у больных с онкогематологическими заболеваниями. Для делириев, формирующихся при онкогематологических заболеваниях, характерна тенденция к стертым формам психозов, эндогеноморфные психозы в изученной выборке представлены галлюцинаторно-параноидными и депрессивно-бредовыми психозами и онейроидными состояниями. Терапия выделенных состояний носит двухэтапный характер (на первом этапе – купирование психоза, на втором – профилактика рецидива). При этом применяются антипсихотические препараты, как классические, так и атипичные.
Заключение. Предлагаемая систематика соматогенных психозов непосредственно влияет на выбор методов лечения. Подтверждена эффективность психотропных препаратов с хорошо изученной клинической активностью, обладающих широким спектром терапевтического действия.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.