Внебольничные пневмонии у детей: принципы диагностики и этиотропной терапии
- Аннотация
- Статья
- Ссылки
Наиболее высокий уровень заболеваемости и летальности при пневмонии отмечен у новорожденных и детей первых лет жизни. При этом частота и тяжесть заболевания, а также его прогноз в различных странах мира неодинаковы. Так, по данным ВОЗ, заболеваемость пневмонией у детей раннего возраста в экономически развитых регионах не превышает 3-4% и составляет не более 8-9% среди всех причин смертности. В то же время в странах с низким культурным и социально-экономическим уровнем, неустойчивой политической обстановкой и продолжающимися военными конфликтами частота пневмонии в аналогичных возрастных группах превышает 10-20%, а ее удельный вес в структуре причин детской смертности составляет более 25% (5, 8, 9). При этом особо следует отметить, что в России заболеваемость и летальность при пневмонии у детей сопоставимы с уровнем показателей ведущих мировых держав (МЗиСР РФ, 2009).
Установлено, что благоприятный прогноз при пневмонии у детей во многом определяется ранней диагностикой и адекватной этиотропной терапией. При этом свое-временное выявление пневмонии основывается на результатах детального и последовательного анализа клинико-анамнестических и рентгенологических данных (1-4).
Основными клиническими симптомами, позволяющими заподозрить у ребенка пневмонию, являются одышка, лихорадка, токсикоз, цианоз, кашель, а также типичные физикальные данные. К последним относят укорочение перкуторного звука над участком поражения легких и локализованные здесь же аускультативные изменения (ослабление или усиление дыхания с последующим появлением крепитирующих или влажнопузырчатых хрипов). Следует, однако, отметить, что при пневмониях у детей раннего возраста зачастую сложно выявить аускультативную ассиметрию в легких. Это связано с тем, что у детей первых лет жизни воспаление легочной паренхимы редко бывает изолированным и, как правило, развивается на фоне бронхита. При этом на всем протяжении обоих легких могут выслушиваться сухие и/или разнокалиберные влажные хрипы, из-за чего типичная аускультативная картина пневмонии, особенно мелкоочаговой, может не улавливаться. Кроме этого при нарушении методики выслушивания легких у детей раннего возраста можно вообще не выявить аускультативных изменений. Так, если у ребенка дыхание поверхностное, то необходимо дождаться или спровоцировать глубокий вдох (изменить положение тела ребенка, отобрать у него пустышку или игрушку и т.д.). Обследование малыша при этом должно быть продолжено до тех пор, пока «на глубоких вдохах» не будет проведена аускультация всех участков легких. Определенные трудности с проведением аускультации возникают также в ситуациях, когда ребенок во время осмотра плачет. В таких случаях для получения полноценной информации (анализ дыхательных шумов как на вдохе, так и на выдохе) обследование необходимо проводить в динамике – не только во время плача, но и после того как ребенок успокоится. Следует особо отметить, что несоблюдение принципов аускультации новорожденных и детей раннего возраста, а также выслушивание их с помощью фонендоскопов «для взрослых» могут привести к диагностическим ошибкам.
В целом, если у лихорадящего ребенка, переносящего острую респираторную инфекцию, имеется хотя бы один из таких признаков, как токсикоз, одышка, цианоз и типичные физикальные данные, необходимо проводить рентгенологическое обследование органов грудной клетки. При этом обнаружение в легких гомогенных инфильтративных изменений очагового, очагово-сливного или сегментарного характера позволяет подтвердить клиническое предположение о развитии пневмонии, вызванной типичными возбудителями (пневмококк и др.). Мелкие негомогенные инфильтраты, име-ющие 2-стороннюю локализацию, выявленные на фоне усиленного сосудисто-интерстициального рисунка, как правило, свидетельствует в пользу атипичной этиологии пневмонии (микоплазмоз, хламидиоз, пневмоцистоз).
Рентгенологическое подтверждение пневмонии является «золотым стандартом» диагностики (1-4). В то же время отсутствие возможностей для проведения рентгенологического обследования у ребенка с клиническими признаками пневмонии не должно приводить к задержке с постановкой диагноза, а значит, и к отсроченному лечению (в первую очередь, – к запаздыванию с назначением антибиотиков!). Недопустимо также затягивать начало антибактериальной терапии до тех пор, пока не будут получены результаты клинического анализа крови. При этом необходимо особо отметить, что лейкоцитоз и ускоренное СОЭ в последние годы перестали рассматривать в качестве обязательных критериев диагностики пневмонии.
При выявлении у ребенка пневмонии в первую очередь определяют необходимость проведения неотложной терапии и срочной госпитализации. Наличие при этом таких ургентных состояний, как токсикоз, дыхательная и/или сердечно-сосудистая недостаточность, судорожный, гипертермический, геморрагический и др. патологические синдромы, является абсолютным критерием для экстренной госпитализации (10).
Показаниями для стационарного лечения детей с пневмониями, кроме тяжелых форм заболевания, являются неонатальный и младенческий возраст, а также серьезные фоновые состояния (тяжелая врожденная или приобретенная патология органов дыхания, кровообращения, нервной, иммунной и других систем). Это связано с тем, что именно у данной категории пациентов имеется высокий риск развития осложнений и неблагоприятного исхода заболевания.
К абсолютным показаниям для госпитализации детей с пневмониями, кроме перечисленных выше клинических состояний и возрастных критериев, относятся также и неблагоприятные социально-бытовые условия. Так, установлено, что частота тяжелых пневмоний у детей из неблагоприятных условий (из семей алкоголиков, наркоманов и др.) значительно выше, а прогноз заболевания при этом серьезнее.
Таким образом, госпитализация детей с пневмонией показана во всех случаях, когда тяжесть состояния и характер течения заболевания требуют проведения интенсивной терапии или имеется высокий риск развития осложнений. Во всех остальных случаях лечение пневмонии может осуществляться «на дому». Необходимо отметить особо, что, независимо от того где проводится лечение (в амбулаторных условиях или в стационаре), терапевтические мероприятия должны быть комплексными и включают адекватный уход за ребенком, правильный режим дня и питания, рациональное использование этиотропных и симптоматических средств. Ключевым звеном при этом является адекватная антибактериальная терапия.
Выбор антибактериальных препаратов при пневмонии, как и при других инфекционно-воспалительных заболеваниях, должен определяться, в первую очередь, особенностями этиологии заболевания. Однако в большинстве случаев, корректное микробиологическое обследование детей с пневмонией не проводится, несмотря на то что в соответствии с «Международной статистической классификацией болезней и проблем, связанных со здоровьем» десятого пересмотра (МКБ-Х) (11) рубрикация пневмоний должна строиться строго по этиологическому принципу.
Рубрикация пневмоний в соответствии с МКБ-Х (ВОЗ, 1994) – Класс X «Болезни органов дыхания»:
- J12. Вирусная пневмония;
- J12.0 Аденовирусная пневмония;
- J12.1 Пневмония, вызванная респираторно-синцитиальным вирусом;
- J12.2 Пневмония, вызванная вирусом парагриппа;
- J12.9 Вирусная пневмония неуточненная;
- J13. Пневмония, вызванная пневмококком;
- J14. Пневмония, вызванная гемофильной палочкой;
- J15. Пневмония, вызванная клебсиеллой пневмониа;
- J15.1 Пневмония, вызванная синегнойной палочкой;
- J15.2 Пневмония, вызванная стафилококком;
- J15.3 Пневмония, вызванная стрептококком группы В;
- J15.4 Пневмония, вызванная другими стрептококками;
- J15.5 Пневмония, вызванная кишечной палочкой;
- J15.6 Пневмония, вызванная другими аэробными грамотрицательными бактериями;
- J15.7 Пневмония, вызванная микоплазмой пневмониа;
- J15.8 Другие бактериальные пневмонии;
- J15.9 Бактериальные пневмонии неуточненные;
- J16.0 Пневмония, вызванная хламидиями;
- J16.8 Пневмония, вызванная другими уточненными инфекционными возбудителями;
- J17.3 Пневмония, вызванная паразитарными возбудителями;
- J18. Пневмония, без уточнения возбудителя.
Отсутствие данных об этиологии заболевания приводит к тому, что пневмонии, как правило, шифруют под кодом J18 (Пневмония, без уточнения возбудителя), а антибактериальную терапию, соответственно, проводят вслепую. В ряде случаев стартовый выбор антибиотиков может быть некорректен, что приводит к отсутствию эффекта от проводимого лечения.
Для уменьшения ошибок при проведении антибактериальной терапии пневмоний у детей в последние годы были разработаны рекомендации по эмпирическому выбору стартовых антибиотиков (12-13). Принципиальным положением разработанных алгоритмов является выбор препаратов в зависимости от эпидемиологических условий и возраста заболевших, так как установлено, что этиология пневмонии напрямую зависит от этих факторов. При этом эпидемиологическая руб-рикация пневмонии предусматривает выделение внебольничных, госпитальных и внутриутробных форм заболевания (3).
О внебольничной пневмонии говорят в тех случаях, когда инфицирование и заболевание ребенка не связано с его пребыванием в лечебном учреждении. Тем самым подчеркивается, что развитие пневмонии произошло в условиях обычного микробного окружения. Это позволяет с высокой долей вероятности предположить этиологию заболевания, так как было установлено, что основным возбудителем пневмонии при этом является Streptococcus pneumoniae. Реже внебольничную пневмонию вызывают Haemophilus influenzae, Мycoplasmae pneumonia, хламидии (Сhlamydia trachomatis – у детей первых месяцев жизни и Сhlamydia pneumonia – в последующие возрастные периоды) и респираторные вирусы. В тех же случаях, когда инфицирование и развитие пневмонии произошло спустя 48-72 часов с момента поступления ребенка в больницу или в течение 48 часов после его выписки из стационара, то ее классифицируют как внутрибольничную (синонимы: госпитальная, нозокомиальная) (3). При этом этиология госпитальной пневмонии зависит от эпидемиологических условий, сложившихся в данном лечебном учреждении. Так, установлено, что нозокомиальные пневмонии могут быть вызваны различными, нередко полирезистентными представителями энтеробактерий, синегнойной палочкой, золотистым стафилококком и другими госпитальными микроорганизмами.
К внутриутробным пневмониям относят такие варианты заболевания, при которых инфицирование произошло в анте- или интранатальный период, а реализация инфекционного воспаления – не позже первых 72 часов жизни ребенка. При этом потенциальными возбудителями внутриутробной пневмонии могут быть различные вирусы, Сhlamydia trachomatis, Streptococcus (гр. В), Staphylococcus aureus, Enterobacteriaceae (Klebsiella, Proteus, Escherihia) и другие микроорганизмы. Таким образом, эпидемиологическая рубрикация пневмоний имеет четкую практическую направленность, так как учитывает особенности этиологии различных форм заболевания и позволяет эмпирически выбрать адекватную антибактериальную терапию сразу же после установления диагноза.
Наиболее частой формой острого инфекционного воспаления легких у детей является внебольничная пневмония. При этом необходимо обратить особое внимание на то, что внебольничная пневмония может характеризоваться различной степенью тяжести – от легкой до крайне тяжелой. Внебольничная пневмония не всегда протекает гладко и в ряде случаев может сопровождаться развитием как легочных (деструкция, абсцесс, пневмоторакс, пиопневмоторакс), так и внелегочных осложнений (инфекционно-токсический шок, ДВС-синдром, сердечно-легочная недостаточность и др.) (1, 10, 14). Поэтому ошибочно считать, что внебольничные пневмонии – это нетяжелые формы заболевания, лечение которых всегда можно проводить в амбулаторных условиях. Таким образом, термин «внебольничная пневмония»» должен применяться исключительно для ориентировочной характеристики этиологии заболевания, а не для оценки его тяжести и прогноза.
Для адекватного эмпирического выбора стартовой антибиотикотерапии, помимо эпидемиологической характеристики, необходим детальный анализ индивидуальных данных ребенка (возраст, фоновые состояния, сопутствующая патология) и клинических особенностей заболевания. При этом отмечено, что на этиологию пневмонии, кроме эпидемиологических факторов, существенное влияние оказывают возраст пациента и его преморбидное состояние. Так, частое использование антибиотиков у детей с хроническими инфекционно-воспалительными заболеваниями (пиелонефрит, тонзиллит, отит и др.) может привести к селекции резистентных штаммов микроорганизмов. В случае развития пневмонии у таких детей этиология заболевания может быть представлена антибиотико-устойчивыми возбудителями.
Аналогичная ситуация может произойти и при возникновении пневмонии у детей с незаконченными курсами антибактериальной терапии или получавших антибиотики в неадекватно низких дозах. Наличие же у ребенка синдрома срыгиваний создает предпосылки для аспирации и развития пневмонии, вызванной не только аэробными (стрептококки, энтеробактерии, стафилококки и др.), но и неспорообразующими анаэробными (бактероиды, фузобактерии, пептострептококки, пептококки и др.) бактериями. Приведенные примеры, которые являются лишь частью возможных клинических ситуаций, свидетельствуют о важности подробного уточнения анамнестических данных в каждом конкретном случае.
Стартовая этиотропная терапия внебольничной пневмонии у детей первых месяцев жизни. У пациентов данной возрастной группы этиология пневмонии может быть связана с очень широким спектром возбудителей (вирусы, хламидии, стрептококки, стафилококки, протей, клебсиелла, кишечная палочка и др.). Учитывая это, для адекватного выбора стартовой терапии вначале эмпирически определяют – заболевание вызвано типичными или же атипичными микроорганизмами? Для этого оценивают клинико-анамнестические данные и анализируют результаты рентгенологического обследования. При этом такие симптомы, как лихорадка, токсикоз, четкие физикальные данные, а также очаговые и/или сливные рентгенологические изменения в легких позволяют с большей достоверностью предполагать типичную бактериальную этиологию пневмонии. В этих случаях лечение начинают с антибиотиков широкого спектра действия, введение которых, учитывая высокий риск развития тяжелых форм заболевания, целесообразно осуществлять парентерально.
В качестве стартовых препаратов используют аминопециллины и цефалоспорины, а при тяжелых вариантах пневмонии – их комбинацию с аминогликозидами. Такой выбор антибиотиков объясняется необходимостью воздействия на целый ряд грамположительных и грамотрицательных бактерий, которые могут быть причиной заболевания у детей данного возраста. Принимая во внимание высокий уровень b-лактамаза-продуцирующих штаммов среди потенциальных возбудителей, предпочтение должно отдаваться ингибитор-защищенным аминопенициллинам и цефалоспоринам 3 генерации.
Спектр антимикробного действия ингибитор-защищенных аминопенициллинов распространяется на грамположительные (стрептококки, стафилококки) и грамотрицательные бактерии (гемофильная палочка, некоторые штаммы клебсиеллы, протея), а также анаэробы (бактероиды и др.). Использование амоксициллина в комбинации с клавулановой кислотой (амоксициллин/клавуланат) или ампициллина с сульбактамом (ампициллин/сульбактам) позволяет сохранить высокую микробиологическую и терапевтическую эффективность препарата, даже в тех случаях, когда пневмония вызвана b-лактамаза-продуцирующими возбудителями. В то же время следует отметить, что ингибитор-защищенные аминопенициллины могут быть неэффективны, если заболевание вызвано микроорганизмами, резистентность которых не связана с образованием b-лактамаз (пневмококк, метициллин-резистентный стафилококк) (15).
В тяжелых случаях необходимо использовать внутривенное введение антибиотиков – при этом амоксициллин/клавуланат применяется в дозе (по амоксициллину): 30-60 мг/кг/сут., а базовые цефалоспорины 3 поколения (производные цефтриаксона и цефотаксима) – в дозе 50-100 мг/кг/сут.
Если пневмония развивается у ребенка, имеющего особенности анамнеза в виде генитального хламидиоза у матери, указаний на затяжной конъюнктивит у ребенка, который не купируется при использовании бета-лактамных антибиотиков, необходимо исключать возможность атипичной этиологии заболевания. При этом наличие сухого кашля с постепенным нарастанием интенсивности и частоты, медленное развитие других симптомов заболевания и преобладание интерстициальных изменений на рентгенограмме заставляют задуматься о возможной этиологической роли С. trachomatis. Верификация хламидийной пневмонии определяет необходимость назначения современных макролидных антибиотиков (Вильпрафен солютаб и др.), так как использование эритромицина часто сопровождается развитием побочных эффектов. Терапию макролидами при этом (за исключением азитромицина) проводят в течение 14 дней (7, 13, 19).
Стартовая этиотропная терапия внебольничной пневмонии у детей дошкольного возраста
Лечение детей данного возраста при нетяжелых пневмониях проводится, как правило, в амбулаторных условиях. При этом наиболее частым бактериальным возбудителем внебольничных пневмоний является S. pneumonia, реже заболевание вызывается H. influenzaе. Учитывая, что пневмококк и гемофильная палочка в последние годы все чаще проявляют устойчивость к природным пенициллинам, антибактериальную терапию рекомендуют начинать с аминопенициллинов (ампициллин, амоксициллин, амоксициллин/клавуланат).
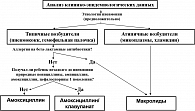
Поскольку для лечения легких и среднетяжелых форм пневмонии, как правило, не требуется парентеральное введение антибиотиков, предпочтение отдается оральным формам амоксициллина (Флемоксин солютаб и др.) или амоксициллин/клавуланата (Флемоклав солютаб и др.) (см. рисунок). Это связано с тем, что указанные препараты имеют более высокую, чем у ампициллина, активность по отношению к потенциальным возбудителям пневмонии и в целом характеризуются лучшей терапевтической эффективностью и переносимостью (15-16).
В тех случаях, когда пневмония развивается у ребенка, не получавшего ранее пенициллины, препаратом выбора является амоксициллин (Флемоксин солютаб и др.). Обычно амоксициллин при этом назначается по 10-20 мг/кг на прием с интервалом 8 часов (суточная доза – 30-60 мг/кг/сут.). Установлено, что более низкие дозы препарата недостаточны для эрадикации основных возбудителей пневмонии и поэтому не должны использоваться.
Особо необходимо отметить лучший профиль переносимости аминопенициллинов, когда используются его диспергируемые формы (Флемоксин солютаб, Флемоклав солютаб). При этом диспергиру-емые таблетки Флемоксин солютаб и Флемоклав солютаб в жидких средах распадаются на микросферы, каждая из которых имеет защитную оболочку. Защитная оболочка становится проницаемой только при воздействии бикарбонатов в кишечнике, определяя тем самым высвобождение активного действующего вещества в зоне максимального всасывания. Это повышает биодоступность препарата и снижает риск его побочных явлений. Благодаря этому при использовании диспергируемых форм амоксициллина (Флемоксин солютаб, Флемоклав солютаб) значительно реже отмечаются диспептические нарушения и развитие антибиотик-ассоциированной диареи.
В тех случаях, когда развитие заболевания обусловлено пенициллиноустойчивым пневмококком, амоксициллин рекомендуется назначать в более высоких дозах (до 90 мг/кг/сут.) или использовать базовые цефалоспорины 3 поколения (цефтриаксон и цефотаксим) в обычных дозах. Противопоказанием для назначения аминопенициллинов являются анамнестические указания на аллергию к пенициллину. В этих случаях используются макролиды.
При подозрении на атипичную этиологию пневмонии (хламидии, микоплазмы) терапия проводится современными макролидными антибиотиками (Вильпрафен солютаб и др.). Основанием для предположения атипичной этиологии пневмонии у детей раннего возраста являются такие клинико-анамнестические данные, как наличие в окружении ребенка «длительно кашляющих» лиц, подострое начало заболевания, длительный субфебрилитет, постепенно нарастающий и длительно сохраняющийся кашель (нередко спастического характера), рецидивирующий бронхообструктивный синдром, а также 2-сторонние диффузные изменения или негомогенные очаги на рентгенограмме. В пользу хламидиоза может также свидетельствовать лимфаденопатия, сопутствующая основному заболеванию (7, 18, 19).
Эмпирический выбор стартовой антибактериальной терапии, к сожалению, не всегда бывает безошибочным, поэтому очень важен свое-временный анализ успешности проводимого лечения. Эффективность терапии при этом оценивается в первую очередь по динамике температурной реакции и уменьшению проявлений интоксикации в течение первых 24-48 часов от начала лечения. При рационально проводимой антибактериальной терапии (своевременное назначение и адекватный выбор стартового антибиотика, строгое соблюдение рекомендуемого режима дозирования) улучшение состояния ребенка, как правило, отмечается уже на 2-3 день лечения. При этом ребенок становится более активным, у него улучшаются аппетит и самочувствие, а температура тела имеет тенденцию к нормализации. Если же в этот период положительная клиническая динамика отсутствует или отмечается ухудшение состояния, то следует проводить смену антибиотика. При этом если лечение начинали с амоксициллина, то решают следующие вопросы: возможно ли продолжать терапию другими бета-лактамными антибиотиками или же необходимо использовать макролиды. Если же детальный анализ эпидемиологических, клинико-анамнестических и рентгенологических данных не дает оснований считать этиологию пневмонии атипичной, то лечение можно продолжить ингибитор-защищенными аминопенициллинами (амоксициллин/клавуланат, ампициллин/сульбактам) или цефалоспоринами 2-3 поколения. В тех случаях, когда стартовая терапия пневмонии проводилась макролидами и при этом не было отмечено клинического эффекта, вероятнее всего этиология заболевания не была связана с такими атипичными возбудителями, как хламидии и микоплазмы. В этих ситуациях также показана коррекция проводимой антибактериальной терапии. При этом макролиды необходимо заменить на бета-лактамные антибиотики.
Критерием прекращения анти-биотикотерапии при лечении легких и среднетяжелых форм пневмонии является клиническое выздоровление. Так, если имеется полный регресс симптомов заболевания, то антибактериальные препараты должны быть отменены даже в тех ситуациях, когда еще сохраняются остаточные рентгенологические изменения. При этом особо следует подчеркнуть, что при благоприятном течении пневмонии нет необходимости проводить так называемый рентгенологический контроль эффективности лечения.
При достижении стойкого клинического эффекта терапия антибиотиком должна продолжается до окончания полного курса. Следует при этом обратить особое внимание на недопустимость раннего (на 3-5 день) прекращения терапии антибиотиками (кроме азитромицина), так как при этом не только не достигается полная эрадикация возбудителей, но и потенцируется развитие у них антибиотикорезистентности. В целом, продолжительность курса антибактериальной терапии при легких и среднетяжелых формах пневмонии, как правило, составляет 7-10 дней. Необходимо отметить, что при лечении пневмоний атипичной (хламидийной, микоплазменной) этиологии может быть оправдан 14-дневный курс терапии макролидами, за исключением тех случаев, когда используется азитромицин.
Стартовая терапия тяжелых и осложненных внебольничных пневмоний
Тяжелое и осложненное течение пневмонии, как правило, отмечается у детей с иммунодефицитными состояниями, тяжелыми пороками развития, органическими поражениями ЦНС и другими серьезными нарушениями здоровья. Однако нельзя забывать, что причинами данных форм пневмонии могут также являться поздняя диагностика и неадекватное лечение, в первую очередь – нерациональная антимикробная терапия.
Лечение детей с тяжелыми пневмониями включает рациональную антимикробную терапию, адекватную респираторную поддержку, иммунотерапию, коррекцию и поддержание гомеостатических параметров (водно-электролитный баланс и др.), а также купирование патологических синдромов (гипертермический, геморрагический, судорожный, синдром сердечной недостаточности и др.). Особо следует отметить, что лечение детей с легочными осложнениями пневмонии (абсцесс легкого, пиоторакс, пиопневмоторакс, эмпиема) должно осуществляться в условиях хирургического стационара или в отделениях интенсивной терапии и реанимации, но с обязательным привлечением детского хирурга. Важным компонентом лечения пневмонии является рациональная антимикробная терапии.
Стартовая антибактериальная терапия при этом проводится комбинациями препаратов (ингибитор-защищенный аминопенициллин + аминогликозид или цефалоспорин 3 поколения + аминогликозид). Следует подчеркнуть, что при тяжелых и осложненных формах пневмоний предпочтение должно отдаваться внутривенному введению антибиотиков. Антибиотики при этом должны назначаться в таких режимах дозирования, которые создают максимальные терапевтические концентрации. Так, амоксициллин/клавуланат при внутривенном введении используют в разовой дозе 30 мг/кг (по амоксициллину) с интервалом 6-8 часов. Цефотаксим и цефтазидим назначают в суточной дозе 100 мг/кг в 3-4 введения. В то же время особенности фармакокинетики таких цефалоспоринов 3 поколения, как цефтриаксон (75 мг/кг/сут.) и цефоперазон (100 мг/кг/сут.), позволяют использовать их соответственно 1 или 2 раза в сутки. Среди аминогликозидов, назначаемых в комбинации с защищенными аминопенициллинами или цефалоспоринами, наиболее часто используются гентамицин (суточная доза 3-5 мг/кг в 2-3 введения), амикацин (суточная доза 15 мг/кг в 2 введения) и нетилмицин (суточная доза 6-7,5 мг/кг в 2-3 введения). В последние годы имеются рекомендации по назначению аминогликозидов с интервалом в 24 часа – 1 раз в сутки как в неонатологической, так и в общей педиатрической практике.
Позитивный клинический эффект и положительная рентгенологическая динамика на фоне проводимой антибактериальной терапии свидетельствуют о том, что стартовый выбор препаратов и их режим дозирования были сделаны правильно. Достижение терапевтического эффекта при этом позволяет выстроить рациональную тактику дальнейшего применения антибиотиков. Так, если лечение ребенка начинали с комбинации аминогликозид + b-лактамный антибиотик (защищенный аминопенициллин или цефалоспорин) и при этом была достигнута положительная клиническая динамика, то целесообразно продолжить терапию стартовыми препаратами. При этом бета-лактамные антибиотики применяют до 10-14 дней, в то время как использование аминогликозидов не должно превышать 5-7 дней в связи с высоким риском развития ото- и нефротоксических эффектов. Примером бета-лактамных антибиотиков для перорального приема является Флемоклав Солютаб.
Отрицательная динамика заболевания, а также появление клинических и рентгенологических признаков деструкции легочной ткани или вовлечение в патологический процесс плевры свидетельствуют о неэффективности проводимой антибактериальной терапии и требуют ее коррекции. Развитие плевропневмонии, абсцесса, пиоторакса и других гнойно-воспалительных изменений в легких является абсолютным показанием для привлечения детских хирургов к совместной курации таких пациентов. Коррекция антимикробной терапии при этом должна обязательно учитывать результаты бактериологического обследования, предварительные результаты которого, как правило, в этот период уже готовы. В тех же случаях, когда приходится проводить смену антимикробной терапии эмпирически, должны назначаться препараты резерва – антибиотики сверхширокого спектра действия – карбопенемы (имипенем, меропенем) или цефалоспорин 4 генерации (цефепим – 100 мг/кг/сут. в 3 введения). Имипенем назначается в суточной дозе 60 мг/кг, которая вводится в 4 приема. Суточная доза меропенема – 30-60 мг/кг в 3 введения.
Особо следует отметить, что несмотря на чрезвычайно широкий спектр антибактериального действия карбопенемов и цефалоспоринов 4 поколения к ним устойчивы метициллинрезистентные стафилококки и энтерококки. Поэтому в тех случаях, когда одними из этиологических агентов пневмонии являются указанные возбудители, препаратом выбора считается ванкомицин (суточная доза 40 мг/кг в 2 приема). Однако ванкомицин и его аналоги имеют узкий спектр действия, так как не действуют на грамотрицательную флору. Поэтому в подавляющем большинстве случаев ванкомицин используется в комбинации с карбопенемом или цефалоспрорином 3-4 поколения.
В заключение следует еще раз подчеркнуть, что своевременная диагностика пневмонии и адекватная ее этиотропная терапия позволяют существенно снизить риск развития осложнений и неблагоприятных исходов заболевания.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.