количество статей
6992
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
XXII Национальный конгресс по болезням органов дыхания: Терапия ХОБЛ: все ли мы делаем для оптимального контроля заболевания?
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Пульмонология и оториноларингология" №1 (10)
- Аннотация
- Статья
- Ссылки
В рамках XXII Национального конгресса по болезням органов дыхания, прошедшего в октябре прошлого года в Москве, состоялся симпозиум «Терапия ХОБЛ: все ли мы делаем для оптимального контроля заболевания?». В докладах ведущих отечественных и зарубежных экспертов – профессора С.Н. Авдеева (НИИ пульмонологии, Москва), профессора А.И. Синопальникова (Российская медицинская академия последипломного образования, Москва), доктора А. Каплана (Группа семейных врачей Канады по лечению заболеваний дыхательных путей) – особое внимание было уделено оценке значения минимизации риска (частота обострений) и фенотипирования при выборе тактики ведения пациентов с ХОБЛ, были представлены убедительные доказательства целесообразности добавления рофлумиласта (препарат Даксас, компания «Такеда») к базисной терапии ХОБЛ у пациентов с тяжелым и очень тяжелым течением ХОБЛ, с частыми (≥ 2 в год) обострениями и бронхитическим фенотипом.
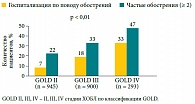
Рис. 1. Связь частоты обострений с тяжестью бронхообструкции у больных ХОБЛ (данные исследования ECLIPSE)

Профессор С.Н. Авдеев

Рис. 2. Эффективность рофлумиласта у пациентов с обострениями в анамнезе (обобщенный анализ данных исследования M2-124 и M2-125)

Профессор А.И. Синопальников
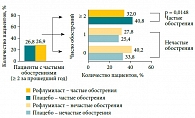
Рис. 3. Изменение статуса обострений у больных ХОБЛ через 1 год терапии рофлумиластом

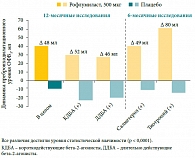
Рис. 4. Эффективность добавления рофлумиласта к бронхолитикам (изменение пребронходилатационного уровня ОФВ1)
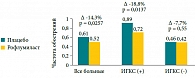
Рис. 5. Эффективность добавления рофлумиласта к ингаляционным глюкокортикостероидам (ИГКС) (частота обострений ХОБЛ)
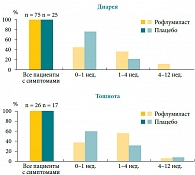
Рис. 6. Разрешение желудочно-кишечных нежелательных явлений, развившихся при приеме рофлумиласта

Рис. 7. Время до развития первого основного сердечно-сосудистого события на фоне терапии рофлумиластом в сравнении с плацебо (данные исследования MACE)

Таблица. Влияние рофлумиласта на различные типы клеток
Наши представления об этиологии, патогенезе, естественном течении хронической обструктивной болезни легких (ХОБЛ) постоянно расширяются, а вместе с ними совершенствуются подходы к лечению этого заболевания. Новое определение, классификация ХОБЛ и принципы ведения таких пациентов представлены в редакции международного клинического руководства GOLD, опубликованной в конце 2011 г. (Global initiative for chronic Obstructive Lung Disease – Глобальная инициатива по ХОБЛ). По оценке заместителя директора Научно-исследовательского института пульмонологии ФМБА России, доктора медицинских наук, профессора Сергея Николаевича АВДЕЕВА, важным нововведением GOLD 2011 стало то, что в основу разделения пациентов на группы и, следовательно, выбора для них схемы терапии была положена не только степень нарушения функции легких по данным спирометрии (показатель ОФВ1), как это было ранее, но и другие важные параметры – выраженность симптомов болезни и частота обострений в анамнезе.
Первая попытка разделить пациентов с ХОБЛ на группы в зависимости от особенностей течения заболевания и клинической картины была предпринята еще полвека назад, когда были выделены два типа болезни – бронхитический и эмфизематозный1. Сегодня характерная для ХОБЛ гетерогенность просто поражает своим многообразием – начиная от морфологической картины и заканчивая прогнозом заболевания. Патоморфолог при изучении гистологического материала, взятого у разных больных ХОБЛ, может обнаружить центриацинарную эмфизему, панацинарную эмфизему, респираторный бронхиолит, бронхоэктазы, бронхит. Не меньше отличий увидит на компьютерных томограммах рентгенолог, а в клинической картине – терапевт (пульмонолог). Таким образом, можно говорить о большом числе фенотипов ХОБЛ.
Согласно современному определению, клинический фенотип ХОБЛ – это характерный признак или комбинация таких признаков, которые описывают различия между пациентами с ХОБЛ, связанные с клинически значимыми исходами (симптомы, обострения, ответ на терапию, скорость прогрессирования заболевания, смерть)2. В настоящее время выделяют несколько таких признаков: эмфизема, хронический бронхит, частые обострения, сочетание с астмой, быстрое прогрессирование, первичная эмфизема (генетически обусловленная), колонизация нижних дыхательных путей, бронхоэктазы, коморбидные состояния, раннее начало симптомов, системное воспаление. Некоторые из клинических фенотипов ХОБЛ уже имеют доказательную базу, другие пока еще изучаются. Несмотря на то что доказательных данных в отношении фенотипов ХОБЛ пока не достаточно, чтобы включить соответствующий раздел в руководство GOLD, в некоторых национальных рекомендациях (например в испанском клиническом руководстве (2012 г.)) подходы к терапии ХОБЛ уже определяются клиническим фенотипированием пациентов.
Руководствуясь такими принципами, как выявляемость в реальной клинической практике, наличие влияния на прогноз и особого ответа на определенный вид терапии, испанские эксперты выделили три «прагматических» фенотипа: смешанный фенотип «ХОБЛ в сочетании с астмой», фенотип «с частыми обострениями» и фенотип «эмфизема – гиперинфляция». Согласно мнению испанских экспертов, хронический бронхит может сопровождать каждый из трех основных фенотипов, поэтому его предложено описывать как модифицирующий фактор этих фенотипов. Кроме того, основные фенотипы также могут сочетаться друг с другом3. Далее профессор С.Н. Авдеев кратко охарактеризовал основные клинические фенотипы ХОБЛ, выделяемые большинством исследователей. Бронхитический фенотип клинически проявляется кашлем с продукцией мокроты на протяжении, по крайней мере, трех месяцев в течение двух лет подряд.
При компьютерной томографии высокого разрешения у пациентов с хроническим бронхитом выявляется утолщение стенки бронха относительно площади его просвета. Клиническая значимость бронхитического фенотипа ХОБЛ показана в ряде исследований. Например, в исследовании COPDGene (Genetic Epidemiology of COPD – Эпидемиологическое исследование генетических факторов ХОБЛ) с участием 1071 пациента с ХОБЛ установлено, что наличие хронического бронхита существенно повышает риск обострений ХОБЛ: в группе больных ХОБЛ без хронического бронхита частота обострений составила 0,63 эпизода на 1 пациента, а в группе с хроническим бронхитом – 1,21 (р = 0,024), при этом доля тяжелых обострений составила 20 и 26,6% соответственно (р = 0,027)4. Эмфизематозный фенотип морфологически (диагностируется методом компьютерной томографии) определяют при наличии постоянного расширения дыхательных путей дистальнее терминальных бронхиол, ассоциированного с деструкцией стенок альвеол, не связанной с фиброзом. Выявление этого фенотипа также имеет большую клиническую значимость, поскольку скорость прогрессирования ХОБЛ (снижения ОФВ1) зависит от выраженности эмфиземы5.
Фенотип с частыми обострениями клинически определяют при наличии двух и более обострений за прошедший год. В ходе 3-летнего наблюдательного исследования ECLIPSE (Evaluation of COPD Longitudinally to Identify Predictive Surrogate Endpoints), в котором приняли участие 2138 пациентов с ХОБЛ, была не только подтверждена прямая корреляция частоты обострений с тяжестью бронхообструкции, но и показана правомерность выделения фенотипа больного ХОБЛ с частыми обострениями. Так, даже при умеренно выраженном нарушении функции легких – II стадия ХОБЛ по классификации GOLD – у значительной части больных (22%) уже имеют место частые обострения (≥ 2) (рис. 1). Данные исследования ECLIPSE позволили сделать вывод о том, что фенотип с частыми обострениями является устойчивым: у 71% пациентов с частыми обострениями в 1-й и 2-й год наблюдения отмечены 2 и более обострений ХОБЛ в 3-й год наблюдения (независимо от степени тяжести ХОБЛ)6.
По данным разных авторов, от 23 до 38% пациентов с ХОБЛ больны бронхиальной астмой. К маркерам фенотипа ХОБЛ в сочетании с астмой относят эозинофилию мокроты, довольно хороший ответ на терапию глюкокортикостероидами, высокую концентрацию оксида азота в выдыхаемом воздухе, положительный тест на обратимость бронхообструкции7–10. Чем может быть полезно фенотипирование пациентов с ХОБЛ? Это дает возможность выявить группы пациентов со сходными прогностическими, клиническими и иными характеристиками, что в повседневной практике врача позволяет выбрать наилучшую тактику лечения. Сегодня уже проведено немало исследований, в которых найдены закономерности между фенотипом ХОБЛ и ответом на терапию теми или иными препаратами. Так, у пациентов с бронхитическим фенотипом, в отличие от пациентов с эмфизематозным фенотипом, отмечен значимый прирост ОФВ1 (207 мл против 32 мл) и уменьшение выраженности одышки (снижение на 0,68 балла по шкале MRC (Medical Research Council Dyspnea Scale) против 0,16 балла) на фоне комбинированной терапии ингаляционными глюкокортикостероидами и бета-2-агонистами длительного действия11.
Доказано, что у больных ХОБЛ с эозинофилией мокроты (фенотип сочетания с астмой) применение глюкокортикостероидов позволяет достичь хороших результатов в отношении улучшения функции легких9, что оправдывает более раннее их назначение этой категории пациентов. Профилактическое применение антибиотиков позволяет снизить частоту обострений в общей популяции больных ХОБЛ на 25%, а в когорте лиц с наличием слизисто-гнойной и гнойной мокроты в стабильный период – на 45%12. Ярким примером высокой эффективности фенотип-ориентированной терапии может служить рофлумиласт – инновационный противовоспалительный препарат, созданный специально для лечения ХОБЛ (этот ингибитор фосфодиэстеразы 4-го типа (ФДЭ-4) показан, прежде всего, пациентам с тяжелым и очень тяжелым течением ХОБЛ, наличием хронического бронхита и частыми обострениями в анамнезе). Объединенный анализ данных двух 52-недельных рандомизированных плацебоконтролируемых исследований, в которых в общей сложности приняли участие 2686 пациентов с ХОБЛ, показал, что терапия рофлумиластом в дозе 500 мг снижает частоту обострений ХОБЛ на 14% по сравнению с плацебо в общей когорте больных ХОБЛ (p = 0,026) и на 26,2% в подгруппе пациентов с хроническим бронхитом (p = 0,001)13.
Ретроспективный анализ данных исследований AURA (M2-124) и HERMES (М-125) позволил установить, что на фоне терапии рофлумиластом частота обострений ХОБЛ у пациентов с обострениями заболевания в анамнезе снижается на 16,9%, при этом в подгруппе пациентов с нечастыми обострениями (< 2 за прошедший год) – на 16,5%, а в подгруппе с частыми (≥ 2 обострений за год) – на 22,3% (рис. 2)14. Как упоминалось выше, в ходе исследования ECLIPSE было показано, что фенотип с частыми обострениями характеризуется высокой устойчивостью. Однако эффективность рофлумиласта у этой категории больных настолько высока, что на фоне приема препарата возможна модификация фенотипа. По данным J.A. Wedzicha и соавт. (2011), к концу первого года терапии среди пациентов с частыми обострениями ХОБЛ в анамнезе этот фенотип сохранился у 40,8% пациентов группы плацебо и только у 32% группы рофлумиласта. Таким образом, 68% пациентов с ХОБЛ, до начала терапии рофлумиластом относившихся к фенотипу с частыми обострениями, через год приема препарата перешли в группу нечастых обострений (рис. 3)15.
В исследовании L.M. Fabbri и соавт. (2012) с участием 743 больных ХОБЛ с выраженной одышкой терапия рофлумиластом в комбинации с холинолитиком привела к снижению выраженности одышки на 23,2% по сравнению с монотерапией холинолитиком в общей популяции пациентов (p = 0,196) и на 45,5% в группе пациентов с исходным значением выраженности одышки ≥ 2 баллов по модифицированной шкале MRC (p = 0,0338)16. Уже в первых клинических исследованиях, изучавших профиль безопасности рофлумиласта, отмечено его свойство снижать массу тела, что вызвало у клиницистов некоторые опасения, поскольку известно, что тяжелые стадии ХОБЛ нередко сопровождаются кахексией. Однако дальнейший анализ данных и последующие исследования показали, что на фоне терапии рофлумиластом наиболее выраженное снижение массы тела отмечается у пациентов с избыточным весом/ожирением и происходит в основном за счет жировой ткани17.
Эта способность рофлумиласта позволила предположить наличие и других благоприятных метаболических эффектов у этого ингибитора ФДЭ-4. В исследованиях с участием пациентов с впервые выявленным сахарным диабетом 2 типа в стадии декомпенсации (уровень HbA1c 7,5–9%) было обнаружено, что на фоне терапии рофлумиластом происходит статистически значимое снижение натощаковой гликемии (на 1,18 ммоль/л) и уровня HbA1c (на 0,79%) по сравнению с плацебо18. На основании приведенных выше данных доказательной медицины можно выделить характерные признаки пациентов с ХОБЛ, у которых терапия рофлумиластом может быть наиболее успешной:
- III–IV стадия ХОБЛ по классификации GOLD (пациенты групп C–D) (ОФВ1 < 50%);
- частые обострения ХОБЛ (≥ 2 в год);
- бронхитический вариант/фенотип (наличие кашля и мокроты);
- сочетание ХОБЛ и метаболического синдрома (ожирение, сахарный диабет).
Противовоспалительные препараты в лечении ХОБЛ: что? кому? когда?
В рекомендациях GOLD 2011 предложен алгоритм терапии ХОБЛ с применением бронходилататоров (короткого и пролонгированного действия), ингаляционных глюкокортикостероидов (ИГКС) и ингибиторов ФДЭ-4. Однако, как известно, алгоритмы – это информация к клиническому размышлению, а управление заболеванием должно быть адаптировано к особенностям пациента. Вопросам выбора препарата при ХОБЛ был посвящен доклад заведующего кафедрой пульмонологии Российской медицинской академии последипломного образования (Москва), доктора медицинских наук, профессора Александра Игоревича СИНОПАЛЬНИКОВА. Доказано, что ключевым звеном патогенеза ХОБЛ является хроническое воспаление. Запускаемое такими триггерами, как курение и другие аэрополлютанты, хроническое воспаление приводит к повреждению и структурному изменению воздухоносных путей и, как следствие, к развитию бронхиальной обструкции. Основными клетками, принимающими участие в воспалительном процессе при ХОБЛ, являются нейтрофилы, Т-лимфоциты (CD8+) и макрофаги.
В этой связи основой патогенетического лечения при ХОБЛ является противовоспалительная терапия, что создает предпосылки для использования системных и ингаляционных глюкокортикостероидов. Влияние ИГКС на воспалительный процесс в легких при ХОБЛ оценивалось в опубликованном в 2012 г. метаанализе 8 исследований. Оказалось, что эти препараты способствовали уменьшению количества лимфоцитов в бронхоальвеолярном лаваже и биоптате слизистой бронхов, уменьшению количества нейтрофилов в бронхоальвеолярном лаваже, но не в биоптате, увеличению содержания макрофагов в бронхоальвеолярном лаваже, но не в биоптате19. Полученные данные позволили авторам предположить, что ИГКС могут быть наиболее эффективны у больных ХОБЛ с преимущественно лимфоцитарным типом воспаления в легких (однако у большинства пациентов с ХОБЛ доминирует нейтрофильное воспаление).
При оценке эффективности терапии у больных ХОБЛ следует учитывать такой параметр, как прогрессирование заболевания (обычно оценивается по скорости снижения показателя ОФВ1: у здоровых составляет около 25–30 мл/год, а у больных ХОБЛ – 40–80 мл/год). В большинстве клинических исследований, в которых изучалось длительное (около 3 лет) применение ИГКС у пациентов с ХОБЛ, не удалось показать статистически значимого влияния этих препаратов на ОФВ1 (ISOLDE, EUROSCOP, Copenhagen City Lung Study, Lung Health Study). Кроме того, не во всех исследованиях было продемонстрировано влияние ИГКС на такие конечные точки, как частота обострений и качество жизни. При этом существуют достаточно веские доказательства повышения риска серьезных нежелательных явлений, прежде всего пневмонии20.
Неоднозначность данных об эффективности и безопасности применения ИГКС у больных ХОБЛ побуждает клиницистов к поиску терапевтических подходов, в том числе с использованием новых препаратов. К таким препаратам можно отнести селективный ингибитор ФДЭ-4 рофлумиласт (Даксас). Подавляя активность ФДЭ-4, рофлумиласт обеспечивает повышение концентрации циклического аденозинмонофосфата (цАМФ) в клетках-мишенях и снижает их провоспалительную активность. Мишенями для рофлумиласта являются все ключевые клетки воспаления, участвующие в развитии воспаления при ХОБЛ (макрофаги, нейтрофилы, CD8+Т-лимфоциты, эозинофилы), а также гладкомышечные, эпителиальные, эндотелиальные, нервные клетки, фибробласты, что обеспечивает многофакторный механизм действия препарата (табл.)21. Эффективность и безопасность рофлумиласта у пациентов с ХОБЛ хорошо изучена в многочисленных контролируемых клинических исследованиях продолжительностью от 24 до 52 недель. В этих исследованиях была убедительно показана способность препарата улучшать показатели функции легких (ОФВ1)17, 22, причем выраженный эффект наблюдался в том числе при добавлении препарата к бронхолитикам (рис. 4)23.
Высокую клиническую значимость представляет собой способность рофлумиласта снижать частоту обострений ХОБЛ24, поскольку доказано, что наличие частых (≥ 2 в год) обострений ассоциируется со значимым снижением качества жизни, более выраженным воспалением, более стремительным прогрессированием заболевания, увеличением вероятности госпитализации, повышенным риском повторных обострений и смерти25. Интересно, что рофлумиласт обеспечивает снижение частоты обострений при добавлении не только к бронхолитикам, но и к ИГКС, что обусловлено различиями в механизме противовоспалительного действия этих препаратов (рис. 5)23. Как показал недавний обзор Кокрановского сотрудничества, включивший 23 исследования по изучению эффективности ингибиторов ФДЭ-4 рофлумиласта (n = 9211) и циломиласта (n = 6457), эти препараты обеспечивают улучшение показателя ОФВ1 в среднем на 45,59 мл, а снижение риска обострений ХОБЛ – на 22% (отношение шансов 0,78) по сравнению с плацебо26.
Поскольку циломиласт в связи с неблагоприятным профилем безопасности не был одобрен для клинического применения, в настоящее время единственным представителем класса, разрешенным для применения, является рофлумиласт. Важным преимуществом рофлумиласта является его благоприятный сердечно-сосудистый профиль безопасности. Было показано, что рофлумиласт по сравнению с плацебо на 35% сокращает риск серьезных сердечно-сосудистых событий, таких как нефатальный инфаркт миокарда, инсульт и сердечно-сосудистая смерть (р = 0,019)27. Этот положительный эффект рофлумиласта обусловлен его способностью воздействовать на системное воспаление, которое сегодня рассматривается как основное связующее звено между ХОБЛ и коморбидной сердечно-сосудистой патологией. Отдельно профессор А.И. Синопальников остановился на вопросах определения места рофлумиласта в лечении ХОБЛ. Поскольку в настоящее время препарат не показан в качестве монотерапии, а только в дополнение к стандартной базисной терапии ХОБЛ, очень важно понимать, в сочетании с какими препаратами он работает максимально эффективно.
К настоящему моменту в ходе ряда исследований доказана высокая эффективность рофлумиласта в комбинации с бета-2-агонистами длительного действия, тиотропием, ИГКС. Теперь мы ожидаем результатов крупного моногоцентрового исследования REACT (Roflumilast in the prevention of COPD Exacerbations while taking Appropriate Combination Treatment), в котором изучается эффективность добавления рофлумиласта 500 мкг/сут к фиксированным комбинациям бета-2-агонистов длительного действия и ИГКС28. Таким образом, у больных ХОБЛ с частыми обострениями в анамнезе (≥ 2 эпизодов за последний год), с бронхитическим фенотипом заболевания (наличием хронического кашля с отделением мокроты) совместное назначение рофлумиласта с любой поддерживающей терапией ХОБЛ будет способствовать дополнительному снижению частоты обострений и улучшению функции легких.
Обращая науку в реальную жизнь: рофлумиласт в клинической практике
В настоящее время основными препаратами для лечения ХОБЛ являются бронхолитики, помогающие уменьшить выраженность одышки, ключевого симптома заболевания. Однако согласно рекомендациям GOLD терапия ХОБЛ должна быть направлена не только на купирование симптомов, но и на предупреждение будущих рисков. Председатель FCFP (Family Physician Airways Group of Canada – Группа семейных врачей Канады по лечению заболеваний дыхательных путей) доктор Алан КАПЛАН (Колледж семейных врачей Канады, секция респираторных заболеваний) акцентировал внимание участников симпозиума на одном из таких рисков – обострениях ХОБЛ, оказывающих отрицательное влияние на течение болезни и прогноз. По данным исследования «Скрытые глубины ХОБЛ» (2010) (Hidden Depths of COPD), в рамках которого были опрошены 2000 пациентов и 1400 клиницистов в 14 странах мира, как минимум одно обострение за год переносят почти 70% больных ХОБЛ, а у половины пациентов обострения развиваются 2 и более раз в год. Убедительно показано, что обострения, особенно частые, приводят к усугублению симптомов болезни и ухудшению функции легких, к более быстрому снижению показателя ОФВ129, то есть к более быстрому прогрессированию болезни, к снижению качества жизни30, к увеличению затрат на лечение и, наконец, к повышению смертности31.
В отношении прогноза обострение ХОБЛ сопоставимо с инфарктом миокарда как по госпитальной летальности (8–10%), так и по годичной смертности после этих острых состояний (25–40%). В течение 5 лет после госпитализации по поводу ХОБЛ умирает примерно половина больных32. В этой связи сегодня профилактика обострений рассматривается как одна из приоритетных задач в лечении ХОБЛ. С практической точки зрения важно знать, у каких категорий пациентов самый высокий риск обострений. Как было показано в ходе исследования ECLIPSE, самым мощным предиктором развития обострений в будущем является наличие частых обострений (≥ 2 эпизодов за год) в анамнезе. Именно для таких пациентов наиболее актуальны мероприятия по профилактике обострений. Казалось бы, идентифицировать фенотип ХОБЛ с частыми обострениями просто – достаточно лишь спросить пациента, сколько обострений он перенес за прошедший год. Однако в реальной клинической практике пациенты не сообщают врачу примерно о половине случаев обострений ХОБЛ, так как не распознают их как обострения, а значит, необходимо, с одной стороны, более тщательно опрашивать пациентов на предмет эпизодов «простуды» и ухудшения самочувствия, а с другой – использовать дополнительные критерии. Одним из таких критериев, указывающих на повышенный риск обострений ХОБЛ, является наличие хронического бронхита. Установлена прямая корреляция между хроническим кашлем с отделением мокроты (бронхитический фенотип ХОБЛ) и частыми обострениями и госпитализациями при ХОБЛ33. Эффективными методами профилактики обострений ХОБЛ считаются:
- отказ от курения;
- вакцинация;
- обучение;
- легочная реабилитация;
- составление плана самостоятельного управления болезнью;
- фармакотерапия, включающая базисную терапию и адекватное лечение уже развившихся обострений с помощью антибиотиков и глюкокортикостероидов.
Как отметил в своем докладе профессор А.И. Синопальников, в основе ХОБЛ лежит хроническое воспаление, поэтому логично предположить, что его подавление может привести к снижению риска обострений. Поскольку глюкокортикостероиды, успешно применяемые при других воспалительных заболеваниях дыхательных путей, малоэффективны при ХОБЛ, то для купирования специфического для ХОБЛ нейтрофильного воспаления был разработан и внедрен в клиническую практику инновационный препарат из группы ингибиторов ФДЭ-4 – рофлумиласт. В исследованиях было показано, что на фоне терапии рофлумиластом происходит сокращение количества нейтрофилов и эозинофилов (по сравнению с плацебо на 35,5% и 50% соответственно), что позволяет на 40% уменьшить выраженность воспаления (число лейкоцитов в мокроте) у больных ХОБЛ36. С противовоспалительным свойством рофлумиласта связаны его клинические эффекты: по данным многочисленных исследований, препарат улучшал функцию легких (хотя и не является бронхолитиком) и, что наиболее важно, существенно сокращал частоту обострений у больных ХОБЛ, в том числе у лиц, уже получающих другую базисную терапию. Так, при добавлении рофлумиласта к сальметеролу частота обострений снизилась на 36,8%, к тиотропию – на 23,2%, к ИГКС – на 18,8%23.
Показатели эффективности рофлумиласта в отношении сокращения частоты обострений представляются весьма впечатляющими, но каково соотношение «польза/риск» для этого препарата? Как показывает анализ профиля безопасности, нежелательные явления со стороны желудочно-кишечного тракта (преимущественно диарея и тошнота) регистрировались на фоне терапии рофлумиластом чаще, чем в группе плацебо (5,1% против 0,8%), в то время как частота остальных нежелательных явлений была сопоставимой в обеих группах (9,2% и 8,4% соответственно). При принятии клинического решения следует помнить, что рофлумиласт (как, например, статины или метформин) – это не симптоматический препарат, а препарат, влияющий на прогноз заболевания, а значит, польза, то есть эффективность, выражающаяся в снижении риска обострений ХОБЛ, значительно перевешивает риск развития гастроинтестинальных нежелательных явлений, не являющихся жизнеугрожающими. Более того, у большинства больных и диарея, и тошнота исчезают в течение 1–4 недель терапии, у остальных их выраженность существенно уменьшается (рис. 6). Средняя продолжительность диареи в исследованиях была 11–12 дней. В отдельных случаях уместно применение противодиарейных препаратов в начале терапии рофлумиластом или его назначение через день, в так называемом “every other day” режиме.
Отмечается также влияние рофлумиласта на снижение массы тела, однако наиболее выраженное уменьшение массы тела наблюдается у лиц с избыточным весом или ожирением и происходит за счет жировой, а не мышечной ткани. Как показало проспективное наблюдение за пациентами, завершившими лечение рофлумиластом, вес восстанавливается в течение нескольких недель после окончания терапии. Рофлумиласт характеризуется высокой сердечно-сосудистой безопасностью. Так, в ходе исследования MACE (Reduced rate of Major Adverse Cardiovascular Events) показано, что на фоне терапии рофлумиластом риск инфаркта миокарда и сердечно-сосудистой смерти снижается по сравнению с плацебо (рис. 7)27, что, предположительно, связано с уменьшением системного воспаления. Что касается лекарственных взаимодействий, то единственным препаратом, который нежелательно применять вместе с рофлумиластом, является рифампицин. В практическом аспекте представляется важным, что рофлумиласт – простой и удобный в применении препарат. Высокой приверженности пациентов лечению позволяют добиться следующие особенности рофлумиласта:
- прием перорально один раз в день – в любое время суток на выбор пациента (но всегда в одно и то же, чтобы соблюсти интервал между дозами);
- отсутствие привязки к приему пищи;
- рекомендуемая доза – 500 мкг/сут, при этом не требуется коррекции дозы ни у пожилых пациентов, ни у курильщиков, ни у лиц с почечной недостаточностью.
Лечение пациента было начато с назначения тиотропия и сальбутамола по потребности, на фоне терапии которыми нарастала одышка, что потребовало добавления формотерола и теофиллина. Позже к терапии был добавлен ИГКС, но это привело к появлению синяков и молочницы, в связи с чем больной отказался от этих препаратов. На фоне комбинированной терапии бронхолитиками длительного действия у пациента сохранялись частые обострения (3–4 раза в год), в связи с чем было принято решение назначить рофлумиласт (Даксас). Расходы на приобретение препарата не покрывались страховкой, однако пациент был готов оплатить лечение из собственных средств, поскольку каждое обострение его серьезно выматывало, надолго лишая сил и вызывая депрессию, длившуюся от нескольких недель до нескольких месяцев.
При назначении Даксаса был отменен теофиллин по причине повышенного риска развития побочных эффектов (теофиллин является неселективным ингибитором ФДЭ, что объясняет большое количество побочных эффектов). Отмена теофиллина вызывала опасения у лечащего врача, так как, по его мнению, могло стать причиной усиления одышки, но этого не произошло. В начале лечения Даксасом пациент отмечал легкую диарею, в связи с чем ему был назначен антидиарейный препарат. Уже через 2 недели этого побочного эффекта не отмечалось. Через 9 месяцев лечения Даксасом ОФВ1 увеличился на 50 мл. За год было отмечено только одно обострение ХОБЛ. У пациента значительно улучшились настроение и активность, исчезло чувство бесполезности, ранее его беспокоившее. Больной пожелал и дальше продолжать лечение Даксасом.
Улучшение отметили и все члены семьи пациента. Вместе с семьей он стал часто выходить из дома – в кино, на бинго, в театр, чего не делал уже несколько лет из-за депрессии и страха сильного кашля. Пациент стал чаще заниматься с внуками, а раньше он избегал этого из-за страха заразить их во время кашля или же заразиться от них. Как видно из описания этого клинического случая, в реальной клинической практике мы можем оценить эффективность рофлумиласта по нескольким критериям. Прежде всего, это сокращение частоты обострений. Кроме того, может наблюдаться улучшение функции легких, однако с этим эффектом не стоит связывать большие ожидания, так как рофлумиласт не является бронхолитиком. И, наконец, это повышение качества жизни, которое отметят и сами пациенты, и члены их семей.
1. Burrows B., Fletcher C.M., Heard B.E. et al. The emphysematous and bronchial types of chronic airways obstruction. A clinicopathological study of patients in London and Chicago // Lancet. 1966. Vol. 1. № 7442. P. 830–835.
2. Han M.K., Agusti A., Calverley P.M. et al. Chronic obstructive pulmonary disease phenotypes: the future of COPD // Am. J. Respir. Crit. Care Med. 2010. Vol. 182. № 5. P. 598–604.
3. Miravitlles M., Soler-Cataluña J.J., Calle M. et al. Spanish COPD Guidelines (GesEPOC): pharmacological treatment of stable COPD. Spanish Society of Pulmonology and Thoracic Surgery // Arch. Bronconeumol. 2012. Vol. 48. № 7. P. 247–257.
4. Kim V., Han M.K., Vance G.B. et al. The chronic bronchitic phenotype of COPD: an analysis of the COPDGene Study // Chest. 2011. Vol. 140. № 3. P. 626–633.
5. Nishimura M., Makita H., Nagai K. et al. Annual change in pulmonary function and clinical phenotype in chronic obstructive pulmonary disease // Am. J. Respir. Crit. Care Med. 2012. Vol. 185. № 1. P. 44–52.
6. Hurst J.R., Vestbo J., Anzueto A. et al. Susceptibility to exacerbation in chronic obstructive pulmonary disease // N. Engl. J. Med. 2010. Vol. 363. № 12. P. 1128–1138.
7. Weiner P., Weiner M., Azgad Y. et al. Inhaled budesonide therapy for patients with stable COPD // Chest. 1995. Vol. 108. № 6. P. 1568–1571.
8. Soriano J.B., Davis K.J., Coleman B. et al. The proportional Venn diagram of obstructive lung disease: two approximations from the United States and the United Kingdom // Chest. 2003. Vol. 124. № 2. P. 474–481.
9. Leigh R., Pizzichini M.M., Morris M.M. et al. Stable COPD: predicting benefit from high-dose inhaled corticosteroid treatment // Eur. Respir. J. 2006. Vol. 27. № 5. P. 964–971.
10. Miravitlles M., Soriano J.B., García-Río F. et al. Prevalence of COPD in Spain: impact of undiagnosed COPD on quality of life and daily life activities // Thorax. 2009. Vol. 64. № 10. P. 863–868.
11. Lee J.H., Lee Y.K., Kim E.K. et al. Responses to inhaled long-acting beta-agonist and corticosteroid according to COPD subtype // Respir. Med. 2010. Vol. 104. № 4. P. 542–549.
12. Sethi S., Jones P.W., Theron M.S. et al. Pulsed moxifloxacin for the prevention of exacerbations of chronic obstructive pulmonary disease: a randomized controlled trial // Respir. Res. 2010. Vol. 11. P. 10.
13. Rennard S.I., Calverley P.M., Goehring U.M. et al. Reduction of exacerbations by the PDE4 inhibitor roflumilast – the importance of defining different subsets of patients with COPD // Respir. Res. 2011. Vol. 12. P. 18.
14. Bateman E., Calverley P.M.A., Fabbri L. et al. // Eur. Respir. J. 2010. Vol. 36. P. P4003.
15. Wedzicha J.A. et al. Efficacy of roflumilast in the frequent exacerbation COPD phenotype // 2011 European Respiratory Society Annual Meeting, Poster Discussion: Biomarkers and exacerbations of asthma and COPD, Tuesday 28 September 2011. P3355.
16. Fabbri L.M. et al. Effects of roflumilast in highly symptomatic COPD patients // European Respiratory Society's 22nd Annual Congress; 2012 Sept 1–5; Vienna, Austria. Abstract P742.
17. Calverley P.M., Rabe K.F., Goehring U.M. et al. Roflumilast in symptomatic chronic obstructive pulmonary disease: two randomised clinical trials // Lancet. 2009. Vol. 374. № 9691. P. 685–694.
18. Wouters E.F.M., Teichmann P., Brose M. et al. Effects of roflumilast, a phosphodiesterase 4 inhibitor, on glucose homeostasis in patients with treatment-naive diabetes (type 2) // Am. J. Respir. Crit. Care Med. 2010. Vol. 181. P. A4471.
19. Jen R., Rennard S.I., Sin D.D. Effects of inhaled corticosteroids on airway inflammation in chronic obstructive pulmonary disease: a systematic review and meta-analysis // Int. J. Chron. Obstruct. Pulmon. Dis. 2012. Vol. 7. P. 587–595.
20. Calverley P.M., Anderson J.A., Celli B. et al. Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease // N. Engl. J. Med. 2007. Vol. 356. № 8. P. 775–789.
21. Field S.K. Roflumilast, a Novel Phosphodiesterase 4 Inhibitor, for COPD Patients with a History of Exacerbations // Clin. Med. Insights Circ. Respir. Pulm. Med. 2011. Vol. 5. P. 57–70.
22. Rabe K.F., Bateman E.D., O’Donnell D. et al. Roflumilast – an oral anti-inflammatory treatment for chronic obstructive pulmonary disease: a randomised controlled trial // Lancet. 2005. Vol. 366. № 9485. P. 563–571.
23. Rabe K.F. Update on roflumilast, a phosphodiesterase 4 inhibitor for the treatment of chronic obstructive pulmonary disease // Br. J. Pharmacol. 2011. Vol. 163. № 1. P. 53–67.
24. Bateman E.D., Rabe K.F., Calverley P.M. et al. Roflumilast with long-acting β2-agonists for COPD: influence of exacerbation history // Eur. Respir. J. 2011. Vol. 38. № 3. P. 553–560.
25. Wedzicha J.A., Seemungal T.A. COPD exacerbations: defining their cause and prevention // Lancet. 2007. Vol. 370. № 9589. P. 786–796; Donaldson G.C., Wedzicha J.A. COPD exacerbations .1: Epidemiology // Thorax. 2006. Vol. 61. № 2. P. 164–168.
26. Chong J., Poole P., Leung B. et al. Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease // Cochrane Database Syst. Rev. 2011. № 5. CD002309.
27. White W.B. et al. Major adverse cardiovascular events in patients with chronic obstructive pulmonary disease: analysis of 14 pooled roflumilast studies // Am. J. Respir. Crit. Care Med. 2011. Vol. 183. P. A3092.
28. Calverley P.M., Martinez F.J., Fabbri L.M. et al. Does roflumilast decrease exacerbations in severe COPD patients not controlled by inhaled combination therapy? The REACT study protocol // Int. J. Chron. Obstruct. Pulmon. Dis. 2012. Vol. 7. P. 375–382.
29. Donaldson G.C., Seemungal T.A., Bhowmik A. et al. Relationship between exacerbation frequency and lung function decline in chronic obstructive pulmonary disease // Thorax. 2002. Vol. 57. № 10. P. 847–852.
30. Spencer S., Jones P.W.; GLOBE Study Group. Time course of recovery of health status following an infective exacerbation of chronic bronchitis // Thorax. 2003. Vol. 58. № 7. P. 589–593.
31. Soler-Cataluña J.J., Martínez-García M.A., Román Sánchez P. et al. Severe acute exacerbations and mortality in patients with chronic obstructive pulmonary disease // Thorax. 2005. Vol. 60. № 11. P. 925–931.
Новости на тему
28.12.2023
24.03.2022 16:00:00
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.