Заместительная терапия специфичными протеогликанами в лечении алопеции. XV научно-практическая конференция «Трихологические болезни в ревматологии и другие междисциплинарные вопросы». Сателлитный симпозиум компании «Гленмарк»
- Аннотация
- Статья
- Ссылки


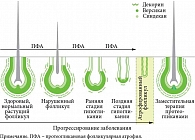






Фолликулярные протеогликаны как базовый компонент цикличного роста волос
Как отметил доктор Омар Мильхем, медицинский директор компании Pharma Medico ApS (Лондон, Великобритания), потеря волос является значимой проблемой в силу ее распространенности и недостаточной эффективности лечения. Кроме того, традиционные методы терапии (финастерид, миноксидил, спиронолактон) могут сопровождаться развитием побочных эффектов, что ухудшает комплаентность. В отношении адъювантной терапии биотином, витаминными комплексами представлена недостаточная доказательная база, к тому же получены данные о том, что только в 2% случаев выпадение волос обусловлено дефицитом витаминов (рис. 1).
На сегодняшний день весьма перспективным направлением считается заместительная терапия протеогликанами – особая методика интенсивного насыщения организма специфичными белками протеогликанами.
В большинстве случаев причиной выпадения волос является нарушение цикла роста волос из-за снижения количества протеогликанов в структуре волосяного фолликула. Установлено, что для оптимальной модуляции нормального роста волос такие специфичные протеогликаны, как версикан, декорин и синдекан, должны присутствовать в определенных концентрациях как внутри волосяного фолликула, так и вокруг него.
Снижение содержания протеогликанов в волосяном фолликуле сопровождается развитием состояния, при котором угасает активность селективных протеогликанов дермального сосочка, что в свою очередь приводит к увеличению выпадения волос, ограничению их роста и снижению качества волос. Кроме того, одновременно уменьшается производство протеогликанов фибробластами. Фолликул, теряя протеогликаны, не может нормально функционировать, развивается фолликулярная гипогликания, приводящая к протеогликановой фолликулярной атрофии и миниатюризации волосяных фолликулов (рис. 2).
Восстановление содержания ключевых протеогликанов в волосяном фолликуле позволяет:
- уменьшить миниатюризацию волосяного фолликула, которая возникает при преждевременном индуцировании фазы телогена;
- вернуть волосяные фолликулы в фазу анагена;
- оптимизировать и перенастроить продолжительность отдельных фаз роста волос;
- обеспечить выживание волосяных фолликулов.
Ключевые протеогликаны, которые модулируют цикличность роста волосяных фолликулов, были выявлены в 1978 г. S.R. Waldstein и E. Thom. Это инициировало ряд исследований. Изучению эффективности заместительной терапии протеогликанами в стимулировании фазы анагена волосяного фолликула было посвящено свыше 100 работ. В 1986 г. был разработан натуральный комплекс протеогликанов для заместительной терапии – Marilex®, являющийся активным компонентом продукта Нуркрин.
В 1992 г. продукт Нуркрин стал применяться в Великобритании, затем в других странах мира.
Нуркрин неоднократно удостаивался престижных международных наград. Так, в 2012 г. он получил золотую медаль Всемирного общества трихологии как передовой метод лечения разных форм алопеций у женщин и мужчин, в 2020 г. – признание российской ассоциации «Профессиональное общество трихологов» (рис. 3).
Как было отмечено ранее, активным компонентом Нуркрина является натуральный комплекс Marilex®. Основанием для его разработки послужил тот факт, что для обеспечения терапевтического эффекта получить достаточное количество протеогликанов из дермы достаточно сложно. Проведена ферментативная экстракция специфического хряща рыб, в ходе которой были получены протеогликаны, которые имитировали протеогликаны кожи тела и головы человека. Сегодня в качестве активного компонента продукта Нуркрин используется комплекс Marilex® шестого поколения (Mark VI-Mark VIв). Данный комплекс характеризуется высоким соотношением специфичных протеогликанов, участвующих в сохранении здорового физиологического состояния человеческих волосяных фолликулов: версикана, декорина, синдекана.
Помимо комплекса Marilex® в состав продукта Нуркрин входят биотин и витамин С, восполняющие недостаток питательных веществ в волосяном фолликуле.
По мере восстановления оптимальной пороговой концентрации протеогликанов на фоне заместительной терапии уменьшается фолликулярная гипогликания, прекращается миниатюризация волосяных фолликулов, нормализуется число волос в фазе телогена. Продление фазы анагена позволяет сохранить активные фолликулы и восстановить рост волос.
Установлено, что синдеканы регулируют Wnt-сигнальный путь, декорин индуцирует фибриллогенез, версикан участвует в поддержании фазы анагена1. Так, в исследовании G.E. Vestgate и соавт. доказано, что максимальное содержание версикана отмечалось в фазу анагена, минимальное – в фазах катагена и телогена2.
Нуркрин может быть рекомендован для лечения разных форм алопеций. Поскольку восстановление естественного цикла роста волос требует времени, лечение проводится в течение шести месяцев с оценкой первого клинического эффекта уже через три месяца.
При потере волос по женскому типу в комплексе с продуктом Нуркрин можно использовать миноксидил наружно, плазмотерапию, негормональные антиандрогенные препараты. Для лечения облысения по мужскому типу Нуркрин может быть применен в сочетании с финастеридом и топическим миноксидилом.
Резюмируя вышесказанное, доктор О. Мильхем подчеркнул, что специфичные протеогликаны следует рассматривать как неотъемлемую часть процесса регулирования роста волосяного фолликула, а заместительную терапию протеогликанами (продуктом Нуркрин) – как оптимальную стратегию при лечении разных форм алопеций у женщин и мужчин.
Фармакологические аспекты метаболизма протеогликанов в тканях
Протеогликаны – сложные протеины, на 5–10% состоящие из белка с высокой степенью гликозилирования. По словам Александра Сергеевича ДУХАНИНА, д.м.н., профессора кафедры молекулярной фармакологии и радиобиологии Российского национального исследовательского медицинского университета им. Н.И. Пирогова, особенностью протеогликанов также является высокое содержание углеводов, на долю которых приходится 90–95% общей массы. Углеводные цепи обеспечивают защиту белковой матрицы, что позволяет протеогликанам оставаться устойчивыми к расщеплению в проксимальном отделе желудочно-кишечного тракта и сохранять свои биологически активные свойства.
Протеогликаны характеризуются тканеспецифичностью, следовательно, те или иные участки тканей содержат свой специфичный набор протеогликанов. Для волосяного фолликула наиболее значимыми являются версикан, декорин и синдекан 1. Версикан и декорин являются внеклеточными протеогликанами, синдекан 1 – трансмембранным3.
Протеогликаны представляют собой сердцевинный белок, декорированный углеводными цепочками или гликозаминогликанами. Гликозаминогликаны представлены гепарансульфатом, дерматансульфатом, хондроитинсульфатом. Гиалуронан тоже принадлежит к гликозаминогликанам, но характеризуется высокой молекулярной массой (> 1000 кДа) и отсутствием сульфатирования. Синдекан преимущественно содержит гепарансульфат, декорин – дерматансульфат, версикан – хондроитинсульфат4.
Синдеканы, ассоциированные с мембраной, служат низкоаффинными рецепторами большого количества факторов роста, защищающими их от разрушения. Речь, в частности, идет об эпидермальном факторе роста (Epidermal Growth Factor – EGF), факторе роста фибробластов (Fibroblast Growth Factor – FGF), факторе роста эндотелия сосудов (Vascular Endothelial Growth Factor – VEGF). Наряду с буферной протективной активностью синдеканы участвуют в активации факторов роста за счет контроля их димеризации. Доказано, что синдеканы модулируют Wnt-сигнальный каскад, который начинается на уровне мембраны. Таким образом реализуется двухуровневая регуляция цикла развития волосяного фолликула: рецепторная и пострецепторная.
Следует отметить, что синдекан 1 преимущественно определяется в эпителиальных клетках волосяного фолликула.
Вторым важным протеогликаном считается версикан, трехдоменная структура (G1–G3) которого обеспечивает реализацию сразу нескольких задач. Версикан индуцирует фазу анагена за счет концевого домена, который содержит повторы пептидной последовательности, подобной эпидермальному фактору роста EGF. Наличие домена G1 определяет способность регулировать клеточную адгезию, что обусловлено его участием в межклеточном взаимодействии фибробластов и эпителия. Максимальные уровни версикана определяются в фазу анагена в богатых протеогликанами мезенхимальных частях фолликула – дермальном сосочке4.
Небольшая по меркам внеклеточных протеогликанов и высоколабильная молекула декорина обладает высокой степенью диффузии. Связываясь с интегриновыми рецепторами, декорин влияет на проведение сигнального пути инсулиноподобного фактора роста (Insulin-Like Growth Factor – IGF), тем самым способствуя индукции анагена. Блокируя трансформирующий фактор роста β1 (Transforming Growth Factor β1 – TGF-β1), являющийся индуктором апоптоза и катагена, декорин оказывает выраженное антиапоптотическое воздействие и обеспечивает поддержание фазы анагена3.
Распад протеогликанов происходит в межклеточном матриксе соединительной ткани под действием разных ферментов, прежде всего протеиназ и гликозидаз. В проксимальных отделах желудочно-кишечного тракта протеогликаны устойчивы к действию гидролаз, но чувствительны к бактериальным ферментам толстой кишки.
Далее профессор А.С. Духанин кратко охарактеризовал основные отличия протеогликанов от ксенобиотиков (табл. 1).
Ксенобиотики (ингибиторы 5-α-редуктазы, PPAR-γ, ингибиторы янус-киназ и др.) представляют собой чужеродные для организма химические соединения, имеющие, как правило, одну мишень действия, в то время как протеогликаны являются природными биоактивными молекулами.
Отличие биоактивных протеогликанов от ксенобиотиков также заключается в плейотропности действия первых, их возможности влиять сразу на несколько мишеней.
Между протеогликанами и ксенобиотиками существуют фармакокинетические и фармакодинамические различия. Ксенобиотики (синтетические, искусственные, антропогенные, неприродные) имеют заданную биодоступность, механизмы простой диффузии. Основная задача организма по отношению к ксенобиотикам – быстрая элиминация, так как их физиологическая концентрация в плазме крови должна быть равна нулю. Реакция организма на поступление биоактивных протеогликанов (биосовместимых, натуральных, естественных) – активное усвоение и поглощение, регулируемое биодоступностью. С этой целью используются природные механизмы депонирования, а также механизмы сопровождения/эскорта. Поэтому действие протеогликанов не ограничивается только временем их приема и является плейотропным5. Последнее включает анагенстимулирующий, анагенподдерживающий, антиапоптотический, противовоспалительный и иммунопротективный эффекты.
По словам профессора А.С. Духанина, у каждого фармацевтического продукта есть так называемая дорожная карта, состоящая из четырех этапов6.
Первый этап – фармацевтический предполагает переход действующего вещества в растворимую форму. Протеогликаны (активный комплекс Marilex®) продукта Нуркрин являются высокогидрофильными, заряженными и сульфатированными молекулами, поэтому они легко высвобождаются из матрицы таблетки.
Второй – фармакокинетический предусматривает всасывание и абсорбцию высвободившихся молекул с помощью эндоцитоза на уровне тощей и подвздошной кишки. После однократного применения протеогликанов примерно 50% подвергается эндоцитозу. Однако при длительном курсовом применении активность эндоцитоза возрастает и приближается к максимальным значениям. С помощью указанного механизма протеогликаны поступают в энтероциты, затем в лимфатические сосуды и возвращаются в кровеносное русло через грудной лимфатический проток, минуя печень7.
Третий этап – фармакодинамический. Установлено, что функциональная роль протеогликанов в регуляции цикла роста волосяного фолликула заключается в индукции и поддержании анагена, а также в модификации иммунного ответа.
Способность протеогликанов стимулировать пролиферацию и выживаемость клеток, оказывать противовоспалительные, регуляторные и антиоксидантные эффекты, защищать микробиоту кишечника продемонстрирована в ряде исследований8.
Многочисленные данные свидетельствуют, что повышение концентрации фолликулярных протеогликанов в результате заместительной терапии Нуркрином может усилить пролиферацию и выживаемость основных популяций фолликулярных клеток и, таким образом, нивелировать патологические изменения механизмов инициации и поддержания фазы анагена.
Прямой противовоспалительный эффект терапии протеогликанами, выделенными из хрящей глубоководных рыб, был верифицирован в нескольких экспериментальных моделях.
В эксперименте in vitro показано, что повышение экспрессии версикана обеспечивает защиту от индуцированного перекисью водорода апоптоза. В клетках, экспрессировавших версикан, отмечалось усиление адгезии и жизнеспособности в ответ на окислительный стресс по сравнению с контрольными образцами. Эта функция критична для поддержания жизнеспособности активных фолликулярных клеток в течение фазы анагена.
Специфичные протеогликаны, выделенные из морепродуктов, могут служить потенциальным пребиотическим комплексом, что было подтверждено в исследовании in vivo. Протеогликаны вызывали достоверное повышение популяции сахаролитических бактерий, продуцирующих короткоцепочечные жирные кислоты из сложных гликанов. Данный класс жирных кислот относится к эффективным противовоспалительным средствам, защищающим кишечный барьер и регулирующим иммунную систему.
«На сегодняшний день пероральная заместительная терапия с помощью таких специфичных протеогликанов, как версикан, синдекан и декорин, является фармакологически обоснованной. Именно этими протеогликанами богат единственный в России запатентованный комплекс Marilex®, содержащий специфичные протеогликаны и входящий в состав продукта Нуркрин», – констатировал профессор А.С. Духанин.
Заместительная протеогликановая терапия при разных видах алопеций
Совместное выступление Аиды Гусейхановны ГАДЖИГОРОЕВОЙ, д.м.н., главного научного сотрудника Московского научно-практического центра дерматовенерологии и косметологии (МНПЦДК), главного врача клиники «Институт красивых волос», президента российской ассоциации «Профессиональное общество трихологов», и Юлии Юрьевны РОМАНОВОЙ, младшего научного сотрудника МНПЦДК, врача-дерматолога клиники «Институт красивых волос», было сфокусировано на обосновании возможностей заместительной протеогликановой терапии в восстановлении жизненного цикла волос и практических аспектах комплексного лечения разных видов алопеций с использованием продукта Нуркрин.
По словам А.Г. Гаджигороевой, на сегодняшний день уже не вызывает сомнений тот факт, что фолликулярные протеогликаны играют структурную, функциональную и регулирующую роль в развитии волосяных фолликулов, обеспечивая нормальный баланс сигнальных молекул. Экспрессия уникального состава протеогликанов волосяного фолликула, который отличается от состава дермального окружения, подтверждена данными гистологических исследований. Установлено, что распределение этих специализированных протеогликанов значительно меняется в течение цикла роста волос.
В настоящее время в волосяных фолликулах выявлен целый ряд факторов роста (FGF, VEGF, Shh, Wnt, BMPs, HGF), которые непосредственно участвуют в развитии волосяного фолликула, но при этом регулируются протеогликанами9.
В свою очередь Ю.Ю. Романова напомнила, что ключевыми фолликулярными протеогликанами считаются версикан, декорин и синдекан 1. Версикан экспрессируется в дермальном сосочке и проксимальных частях оболочки волосяного фолликула, декорин идентифицируется в дермальном сосочке и в зоне bulge, синдекан 1 специфичен для эпителиальных частей волосяного фолликула, наружной и внутренней корневых оболочек10. При этом характеристики перераспределения фолликулярных протеогликанов соответствуют упреждающему, а не пассивному сценарию.
А.Г. Гаджигороева уточнила, что сначала изменения будут касаться синтеза протеогликанов и лишь по мере его снижения можно наблюдать определенные морфологические изменения в волосяном фолликуле.
Версикан определяется в зрелых волосяных фолликулах с максимальной экспрессией в фазе анагена, постепенным уменьшением в катагеновой и исчезновением в телогеновой фазах. При этом его присутствие в зоне bulge постоянно. Доказано, что экспрессия версикана в дермальном сосочке снижается у лиц старше 50 лет, что предполагает мощную связь с развитием сенильной алопеции11. Более того, снижение версикана наблюдается в пушковых волосах при андрогенетической алопеции вследствие прямого воздействия андрогенов12.
Ключевая роль версикана в индуцировании роста волос доказана в экспериментах in vivo и in vitro. Так, он признан важным звеном для передачи сигнала от клеток дермального сосочка к стволовым клеткам фолликула и запуска регенерации волос13.
Синдеканы – трансмембранные протеогликаны. Они регулируют сигналы адгезии, миграции и роста посредством растворимых лигандов внеклеточного матрикса, служат низкоаффинными рецепторами большого количества факторов роста, защищая последние от разрушения14.
В частности, синдекан 1 регулирует различные циклические процессы в волосяных фолликулах на рецепторном и пострецепторном уровнях. В фазе анагена синдекан 1 обнаруживается в эпителиальном отделе наружного корневого влагалища и сосочке. В фазе телогена его количество уменьшается.
Далее Ю.Ю. Романова дала характеристику еще одному ключевому протеогликану – декорину. Данный протеогликан богат лейцином. Он высоко экспрессирован в области bulge. Декорин блокирует действие различных эпидермальных факторов роста с отрицательными эффектами в отношении роста волос, в частности TGF-β1, ингибирующего рост волос и участвующего в стимулировании местного синтеза андрогенов, а также EGF, участвующего в реализации андрогенетической алопеции.
Экспрессия декорина с возрастом снижается, равно как и количество кератин-15-позитивных клеток, которые принято считать стволовыми клетками волосяного фолликула. Выявлено, что удаление декорина в моделях in vitro способствовало дифференцировке стволовых клеток. И напротив, если стволовые клетки фолликула культивировались на чашках с покрытием декорина, их состояние становилось еще более недифференцированным.
Таким образом, декорин функционирует как компонент ниши стволовых клеток. Дефицит декорина может быть причиной возраст-ассоциированного выпадения волос15.
Установлено, что значительная концентрация протеогликанов внутри и вокруг фолликулярного эпителия и дермального сосочка в фазе анагена необходима для обеспечения иммунологической толерантности волосяного фолликула.
Иммунопротективный эффект протеогликанов может реализовываться за счет ограничения миграции клеток иммунной системы. В качестве «пограничного патруля» может выступать перлекан16.
Вторым участником сохранности иммунной привилегии волосяных фолликулов в фазе анагена считаются хондроитин-протеогликаны. Данные протеогликаны препятствуют активации цитотоксических клеток, формируя защитный барьер вокруг луковицы.
А.Г. Гаджигороева пояснила, что, когда способность фолликулярных клеток синтезировать протеогликаны снижается, а концентрация биоактивных протеогликанов падает ниже порогового, наблюдается прогрессивная фолликулярная гипогликания, что убедительно продемонстрировано при андрогенетической алопеции в рамках анализа версикана12. Выраженная фолликулярная гипогликания может привести к изменению соотношения длительности фаз телогена и анагена. На ранней стадии фолликулярная гипогликания ассоциируется с субклиническим изменением размера фолликула – протеогликановой фолликулярной гипотрофией, которая впоследствии может усугубляться развитием протеогликановой атрофии фолликула, клинически проявляясь прогрессивным уменьшением размеров фолликула.
Первоначально фолликулярная гипогликания вызывает гипотрофию фолликулов, не влияя на их макроскопический размер. В случае ее длительного течения происходит макроскопическое истощение протеогликанов и, как следствие, развитие протеогликановой фолликулярной атрофии и таких процессов, как грубая дисфункция ключевых фолликулярных клеток и нарушение цикла волос, а также видимый структурный распад дермальных сосочков, ведущий к постепенной миниатюризации волос.
Полагают, что за миниатюризацией волос при их выпадении стоит протеогликановая фолликулярная атрофия, которая не может быть устранена путем удаления андрогенов, поскольку эти механизмы независимы от андрогеновых рецепторов8.
Далее докладчики проанализировали современные терапевтические подходы к лечению разных типов облысения, начав с андрогенетической алопеции.
Согласно современной теории, наиболее значимым фактором развития андрогенетической алопеции является негативное влияние на волосяные фолликулы 5-α-редуктазы и дигидротестостерона. Однако данный фактор в большей степени имеет значение у мужчин.
У женщин влияние андрогенов не может быть признано единственным этиологическим фактором, поскольку этот тип потери волос отмечается у лиц с синдромом полной нечувствительности к андрогенам. В патогенезе андрогенетической алопеции у женщин большая роль отводится таким гормонам, как 17-β-эстрадиол и пролактин17, 18.
При формировании андрогенетической алопеции активация андрогеновых рецепторов приводит к блокаде Wnt-β-катенин-сигнального пути. Его блокирование активирует выработку TGF-β, который инициирует фазу катагена и процессы фиброзирования, в частности процессы перифолликулярного фиброза. Первым морфологическим признаком инициации фазы катагена является уменьшение богатого протеогликанами папиллярного экстрацеллюлярного матрикса в конце фазы анагена. Важно то, что отдельные протеогликаны (синдекан 1, бигликан, декорин) напрямую способны стимулировать Wnt-β-катенин-сигнальный путь19.
Как отметила А.Г. Гаджигороева, повышение концентрации фолликулярных протеогликанов с помощью приема продукта Нуркрин с запатентованным комплексом Marilex® может нивелировать влияние половых гормонов на более низком уровне, чем рецептор. Этот подход способен прервать порочный круг дефицита экстрацеллюлярного матрикса, приводящий к клеточной дисфункции, завершающейся протеогликановой фолликулярной атрофией и уменьшением размеров фолликулов. Нуркрин может быть использован в качестве заместительной протеогликановой терапии андрогенетической алопеции у мужчин и женщин, рекомендуемая схема приема – по одной таблетке два раза в день в течение четырех – шести месяцев (табл. 2).
Докладчики поделились собственным опытом применения продукта Нуркрин в комплексной терапии андрогенетической алопеции.
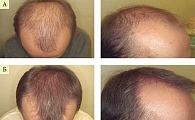
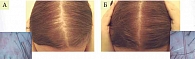
В клиническом примере, представленном А.Г. Гаджигороевой, пациент с андрогенетической алопецией получал комплексное лечение миноксидилом 5% два раза в день наружно в сочетании с введением обогащенной тромбоцитами плазмы (Platelet-Rich Plasma – PRP) и приемом продукта Нуркрин по одной таблетке два раза в день в течение пяти месяцев. Подобный комплексный подход оказался эффективным в плане предотвращения выпадения волос и возобновления их роста (рис. 4).
В комплексном лечебном подходе, продемонстрированном в клиническом примере Ю.Ю. Романовой, применение лосьона на основе стемоксидина 5% наружно в сочетании с плазмотерапией один раз в месяц и заместительной протеогликановой терапией Нуркрином по одной таблетке два раза в день привело к нормализации цикла роста волос уже через три месяца лечения.
Еще одним часто встречающимся типом потери волос является телогеновая алопеция. По мнению А.Г. Гаджигороевой, независимо от причины все виды невоспалительной телогеновой алопеции предполагают повышение в коже волосистой части головы фолликулов, пребывающих в фазе телогена. Регуляция перехода фазы телогена в фазу анагена с помощью заместительной протеогликановой терапии (Нуркрин с комплексом Marilex®) при таком типе облысения также может быть перспективной20.
Ю.Ю. Романова, затронув проблему сенильной алопеции, проследила наличие связи между ее развитием и снижением уровня протеогликанов. Версикан и декорин принимают важное участие в регуляции синтеза коллагена. Установлено, что с возрастом уменьшается не только синтез протеогликанов, но и их качество. Снижение синтеза протеогликанов может быть связано с возраст-ассоциированным снижением эстрогенов: у мышей, подвергнутых овариоэктомии, толщина дермы и экспрессия декорина были снижены. Аналогичные изменения наблюдались при блокировании рецептора эстрогенов.
При фотостарении в зонах солнечного эластоза наблюдалось изменение дермального матрикса, что сочеталось с отсутствием декорина в этих областях21.
А.Г. Гаджигороева отметила, что в ряде исследований доказана связь процессов старения с истончением капилляров и снижением концентраций протеогликанов11. Снижение уровня протеогликанов в дермальном сосочке фолликулов, обусловленное процессом старения, было продемонстрировано в исследовании с использованием метода иммуногистохимического окрашивания лобной и затылочной областей волосистой части головы у пожилых пациентов и здоровых детей. Более значительное количество протеогликанов регистрировалось на гистологических срезах у последних21.
В исследовании, проведенном T. Erling и соавт., показано, что заместительная терапия протеогликанами, в частности версиканом и декорином, уменьшала процесс старения капилляров, обусловленный внешними и внутренними механизмами22.
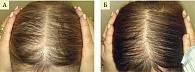
Морфологические изменения при сенильной алопеции характеризуются истончением дермы с изменением коллагеновых и эластиновых волокон, уменьшением количества и размера долек сальных желез, эккриновых потовых желез, снижением количества кровеносных сосудов, нарушением соотношения «веллусные/терминальные» волосы, уменьшением диаметра фолликулов и стержней. По словам Ю.Ю. Романовой, с учетом плейотропного действия на клетки волосяного фолликула и декорин, и версикан можно рассматривать как весьма перспективный метод заместительной протеогликановой терапии у таких пациентов. Это подтверждает и собственный клинический опыт использования продукта Нуркрин в комплексном лечении сенильной алопеции пациентки 65 лет с фиброзом и выраженным истончением волос (рис. 5).
Заместительная терапия протеогликанами может быть востребована при лечении ишемической алопеции, поскольку гипоксия является важным фактором нарушения роста волос. Исследования продемонстрировали, что при культивировании клеток волосяных фолликулов при различном парциальном давлении ишемия ассоциировалась с замедлением роста волос. Известно, что протеогликаны обладают цитопротективным эффектом, поэтому их применение можно рассматривать как потенциальную терапевтическую стратегию при ишемической алопеции (рис. 6, клинический пример Ю.Ю. Романовой).
Применение заместительной протеогликановой терапии обоснованно также при проведении регенеративных медицинских процедур.
Установлено, что версикан стимулирует выработку эластина, способствует ангиогенезу. Повышенная экспрессия синдекана активирует миграцию кератиноцитов и эндотелиальных клеток. Декорин рассматривается в качестве терапевтической опции для предотвращения патологического рубцевания в регенеративной медицине23, 24.
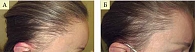
В подтверждение Ю.Ю. Романова представила участникам симпозиума клинический случай комплексного использования методов регенеративной медицины в сочетании с заместительной терапией Нуркрином при андрогенетической алопеции (рис. 7).
Пациентке с выраженной андрогенетической алопецией, сопровождающейся фиброзом кожи, было назначено комплексное лечение, которое включало стромально-васкулярную активацию роста волос однократно, лосьон стемоксидина 5% наружно один раз в день и продукт Нуркрин по одной таблетке два раза в день в течение двух месяцев. Синергичный комплексный подход позволил быстро добиться активации роста здоровых волос.
Подводя итог, А.Г. Гаджигороева отметила, что таргетная заместительная протеогликановая терапия в комплексных методиках возможна:
- при андрогенетической алопеции (мужской и женский тип);
- сенильной алопеции;
- алопеции, вызванной ишемией;
- регенеративных методах лечения (пересадка волос, стромально-васкулярная активация роста волос).
Заключение
Открытие роли протеогликанов как ключевых факторов в биологии волосяного фолликула позволило создать уникальный продукт Нуркрин, содержащий эксклюзивный комплекс Marilex®. Комплекс Marilex® является природным источником ключевых протеогликанов, участвующих в регуляции роста волос. По оценкам экспертов, использование продукта Нуркрин у пациентов, страдающих выпадением волос разной этиологии, позволяет нормализовать концентрацию протеогликанов в волосяных фолликулах и таким образом восстановить естественный цикл роста волос. В настоящее время продукт Нуркрин успешно применяется в 46 странах, в том числе в России, в качестве заместительной протеогликановой терапии при разных видах выпадения волос.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.