Интрасклеральная фиксация интраокулярной линзы при дислокации хрусталиковых масс
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В ретроспективное исследование (серия случаев) было включено 100 пациентов (100 глаз) с дислокацией собственных хрусталиковых масс или ранее имплантированных ИОЛ, которым в период с января 2023 г. по декабрь 2025 г. выполнялась имплантация заднекамерной ИОЛ с интрасклеральной фиксацией опорных элементов.
Результаты. Во всех случаях имплантация и фиксация заднекамерной ИОЛ выбранным способом прошли успешно. В послеоперационном периоде в 100 глазах отмечалось центральное положение ИОЛ в зрачковом отверстии. Признаков децентрации или смещения ИОЛ при обычном осмотре не выявлено. Частота повторной дислокации ИОЛ составила 2%. Уже через месяц после операции наблюдалось значительное повышение зрения по сравнению с исходным уровнем.
Заключение. Полученные результаты продемонстрировали, что методика интрасклеральной фиксации заднекамерной ИОЛ является эффективным способом реабилитации пациентов с дислокацией хрусталика, повышает остроту зрения и обеспечивает достаточный рефракционный контроль.
Материал и методы. В ретроспективное исследование (серия случаев) было включено 100 пациентов (100 глаз) с дислокацией собственных хрусталиковых масс или ранее имплантированных ИОЛ, которым в период с января 2023 г. по декабрь 2025 г. выполнялась имплантация заднекамерной ИОЛ с интрасклеральной фиксацией опорных элементов.
Результаты. Во всех случаях имплантация и фиксация заднекамерной ИОЛ выбранным способом прошли успешно. В послеоперационном периоде в 100 глазах отмечалось центральное положение ИОЛ в зрачковом отверстии. Признаков децентрации или смещения ИОЛ при обычном осмотре не выявлено. Частота повторной дислокации ИОЛ составила 2%. Уже через месяц после операции наблюдалось значительное повышение зрения по сравнению с исходным уровнем.
Заключение. Полученные результаты продемонстрировали, что методика интрасклеральной фиксации заднекамерной ИОЛ является эффективным способом реабилитации пациентов с дислокацией хрусталика, повышает остроту зрения и обеспечивает достаточный рефракционный контроль.

Введение
Дислокация хрусталика или интраокулярной линзы (ИОЛ) вместе с хрусталиковыми массами – одно из наиболее серьезных осложнений в офтальмохирургии. Такое состояние значительно снижает зрительные функции и сопряжено с риском развития вторичных осложнений – эндофтальмита, увеита, вторичной глаукомы, цистоидного макулярного отека, отслойки сетчатки и др. [1]. По данным разных авторов, частота подобных дислокаций после операций экстракции катаракты составляет от 0,2 до 3% [2]. Основными предрасполагающими факторами являются слабость цинновых связок, чаще всего при псевдоэксфолиативном синдроме (ПЭС), на долю которого приходится около 50% случаев поздней дислокации хрусталика или ИОЛ [2]. Другие факторы риска включают высокую степень миопии, травмы, предшествующие витреоретинальные вмешательства, а также системные заболевания соединительной ткани (например, синдром Марфана) [3].
При выраженной сублюксации или выпадении хрусталика адекватная капсульная поддержка отсутствует, поэтому стандартная имплантация ИОЛ в капсульный мешок невозможна. В таких ситуациях применяют альтернативные методы фиксации ИОЛ – в углу передней камеры (переднекамерные ИОЛ), иридо-клапанные или ирис-клипс-ИОЛ (фиксация к радужке), а также фиксацию заднекамерной ИОЛ к склере с помощью швов или бесшовной технологии (интрасклерально) [4]. Из перечисленных методик наиболее физиологичным представляется расположение ИОЛ в задней камере (в привычной плоскости хрусталика) [5]. Интрасклеральная фиксация гаптических элементов ИОЛ обеспечивает именно заднекамерное положение, что позволяет избежать контакта линзы с эндотелием роговицы и углом передней камеры и снизить риск корнеальной декомпенсации, хронического воспаления и вторичной глаукомы по сравнению с переднекамерными ИОЛ. Кроме того, отсутствие постоянного контакта фиксаторов ИОЛ с радужкой или конъюнктивой минимизирует риск их эрозии, смещения и связанных с этим осложнений в отдаленном периоде [6]. Именно поэтому методика транcсклеральной (интрасклеральной) фиксации ИОЛ, несмотря на техническую сложность вмешательства, быстро завоевала популярность среди витреохирургов. Первые описания подобных операций относятся к 1986 г., а широкое распространение метод получил в 2000-х гг. с развитием техники шовной фиксации и бесшовных технологий (glued IOL, техника Yamane и др.) [7, 8].
Цель – оценить эффективность и безопасность метода интрасклеральной фиксации заднекамерной ИОЛ у пациентов с дислокацией хрусталиковых масс (subluxation или полная дислокация хрусталика/ИОЛ) с помощью ретроспективного анализа 100 операций, проведенных в гБУЗ МО МОНИКИ им. М.Ф. Владимирского в 2023–2025 гг.
Материал и методы
Дизайн исследования
В ретроспективное исследование (серия случаев) было включено 100 пациентов (100 глаз) с дислокацией собственных хрусталиковых масс или ранее имплантированных ИОЛ, которым в период с января 2023 г. по декабрь 2025 г. выполнялась имплантация заднекамерной ИОЛ с интрасклеральной фиксацией опорных элементов. Критериями включения в исследование были отсутствие или выраженное повреждение капсульного аппарата хрусталика (подвывих 2-й степени и более или вывих хрусталика/ИОЛ), снижение остроты зрения вследствие данной патологии, возраст старше 18 лет. В исследование не включались пациенты с тяжелой сопутствующей патологией роговицы или сетчатки, способной повлиять на зрительные результаты, а также пациенты, находившиеся под наблюдением менее шести месяцев.
Характеристика пациентов
Средний возраст пациентов составил 60,3 ± 13,8 года (от 22 до 84 лет). Мужчин было 58 (58%), женщин – 42 (42%). В 53 (53%) случаях выявлен ПЭС как причина спонтанной дислокации хрусталика. У 19 (19%) пациентов имела место тяжелая миопия (≥ 6 дптр) с дегенерацией зонулы, у 15 (15%) – травматическая дислокация хрусталика; у 8 (8%) – вывих ИОЛ, имплантированной в ходе предыдущего вмешательства. У 5 (5%) пациентов зарегистрированы наследственные системные болезни соединительной ткани (синдром Марфана, гомоцистинурия и др.). Из сопутствующей патологии глаз встречались первичная глаукома – 18% случаев, диабетическая ретинопатия – 5%, возрастная дегенерация макулы – 4%.
Офтальмологическое обследование
До операции всем пациентам измеряли остроту зрения (корригированную и некорригированную), проводили рефрактометрию, биометрию для расчета оптической силы ИОЛ, тонометрию, биомикроскопию и офтальмоскопию. Остроту зрения оценивали по десятичной шкале (Snellen эквивалент). Рефракция выражалась в виде сферического эквивалента (СЭ). Уровень внутриглазного давления (ВГД) > 21 мм рт. ст. считался повышенным. О повышенном уровне ВГД свидетельствовала также потребность в гипотензивной терапии.
Хирургическая тактика
Все операции выполнялись по одному хирургическому протоколу: через лимбальный разрез удалялись смещенные хрусталиковые массы (при интактном хрусталике проводилась факоэмульсификация с удалением масс из витреальной полости), после чего имплантировалась гибкая заднекамерная ИОЛ. Фиксация ИОЛ осуществлялась транссклерально (интрасклерально) с помощью проленовых швов: два отрезка 9–0 (в 40 случаях) или 10–0 (в 60 случаях) полипропиленовой нити (Prolene) проводились ab externo через цилиарную борозду с захватом гаптических элементов ИОЛ с последующим завязыванием узлов на склере. Узлы погружались под конъюнктиву, в 35 случаях дополнительно формировались склеральные карманы длиной около 3 мм или тонкие склеральные лоскуты 4 × 4 мм для надежного укрытия узлов (предотвращает их эрозию в дальнейшем). При необходимости выполнялась закрытая витрэктомия (25 G) – 22 (22%) пациентам потребовались удаление выпавших хрусталиковых масс из стекловидной полости и выполнение передней витрэктомии. В конце операции роговичный разрез герметизировали, конъюнктиву ушивали Vicryl 8–0. Профилактика инфекций предусматривала интракамерное введение 0,1 мл раствора цефуроксима (1 мг) и назначение топических антибиотиков. Послеоперационное ведение было стандартным: кортикостероидные и антибактериальные капли в течение 4–6 недель с постепенной отменой.
Статистическая обработка
Количественные показатели (острота зрения, рефракция) сравнивали с помощью парного t-теста (при нормальном распределении) или критерия Вилкоксона. Для частотных показателей (процент осложнений) рассчитывали 95%-ный доверительный интервал. Долевые величины сравнивали с помощью χ²-теста. Различия считались статистически значимыми при p < 0,05.
Результаты
Всего прооперировано 100 глаз (100 пациентов). У 74 (74%) пациентов дооперационная максимально корригированная острота зрения (МКОЗ) была ниже 0,3, в том числе у 18 (18%) ≤ 0,1 (в пяти случаях отмечалось светоощущение или счет пальцев), что указывало на выраженное ухудшение зрения при дислокации хрусталика. Средняя МКОЗ до операции составила 0,22 ± 0,15. Средний расчетный СЭ дооперационной рефракции (при наличии хрусталика на месте) статистически не анализировался из-за большого разброса: у пациентов с полной афакией он достиг +10–+12 дптр, тогда как при подвывихах хрусталика чаще отмечался миопический сдвиг (до -5–-10 дптр) из-за смещения хрусталика. Таким образом, у большинства пациентов имело место значимое рефракционное нарушение, которое не поддавалось полной коррекции на фоне ношения очков. Уровень ВГД до операции в среднем составил 18,9 ± 3,5 мм рт. ст. У 12% пациентов наблюдалась офтальмогипертензия, компенсированная медикаментозно.
Анатомические результаты
Во всех случаях имплантация и фиксация заднекамерной ИОЛ выбранным способом прошли успешно. В послеоперационном периоде в 100 глазах отмечалось центральное положение ИОЛ в зрачковом отверстии. Признаков децентрации или смещения ИОЛ при обычном осмотре не выявлено. У 3 (3%) пациентов в течение первого месяца обнаружен небольшой наклон плоскости ИОЛ относительно горизонтальной оси, существенно не влиявший на остроту зрения. Двум из этих пациентов впоследствии были выполнены дополнительная подтяжка и центрирование ИОЛ хирургическим путем. К шестому месяцу наблюдения в 98 глазах из 100 ИОЛ оставались стабильно фиксированными. У 2 (2%) пациентов произошла частичная поздняя дислокация ИОЛ (соскальзывание одного гаптического элемента из склерального кармана) спустя пять-шесть месяцев, что потребовало повторной фиксации. Таким образом, частота повторной дислокации ИОЛ в наблюдаемом периоде составила 2%.
Зрительные функции
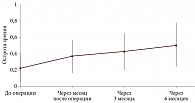
Уже через месяц наблюдалось значительное улучшение остроты зрения по сравнению с исходным уровнем (рис. 1). МКОЗ через месяц составила в среднем 0,35 ± 0,20, а через три месяца – 0,42 ± 0,22. К шестому месяцу от момента операции средняя МКОЗ достигла 0,50 ± 0,25, что значительно превысило исходные показатели (p < 0,001). Иными словами, в среднем зрение улучшилось с 0,22 до 0,5 (в 2,3 раза). Улучшение зрения происходило в основном в первые три месяца после хирургического вмешательства. Между третьим и шестым месяцем различия были незначительны (прирост 0,08; p = 0,07). Некорригированная острота зрения (НКОЗ) также возросла благодаря оптимальному положению и рассчитанной оптической силе ИОЛ: к шестому месяцу НКОЗ в среднем составила 0,32 ± 0,20 (для сравнения: до операции большинство пациентов без коррекции не различали даже крупные объекты из-за смещения хрусталика). Доля пациентов с функционально значимым зрением (МКОЗ ≥ 0,5) увеличилась с 10% до операции до 58% к шестому месяцу после нее (p < 0,001). При этом 84% пациентов достигли МКОЗ ≥ 0,3 (табл. 1).
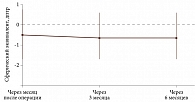
Особого внимания заслуживают рефракционные результаты после фиксации ИОЛ. Оптическую силу ИОЛ рассчитывали по формуле SRK-II, целевой рефракцией во всех случаях была эмметропия. Фактически к первому месяцу после операции средний СЭ составил 0,50 ± 1,2 дптр, к трем месяцам – -0,60 ± 1,1 дптр, к шести – -0,65 ± 1,0 дптр. Таким образом, наблюдалась тенденция к небольшому миопическому смещению рефракции (в среднем на -0,5–-0,7 дптр), что объяснялось незначительным наклоном или смещением ИОЛ в отдельных случаях, а также возможной гиперметропической погрешностью при расчетах оптической силы ИОЛ у пациентов с отсутствием хрусталика. Разница среднего СЭ между первым и шестым месяцем была статистически незначима (-0,15 дптр; p = 0,36), что свидетельствовало о стабильности рефракции после первичного периода адаптации. На рисунке 2 представлена динамика средней рефракции: уже через месяц был достигнут результат, близкий к целевому. В дальнейшем существенных сдвигов не зафиксировано.
В рефракционном отношении большинству пациентов удалось добиться результата, близкого к запланированному: у 75 (75%) пациентов из 100 итоговая рефракция отличалась от целевой не более чем на ±1,0 дптр, у 90 (90%) – в пределах ±2,0 дптр. Лишь у десяти пациентов отклонение превысило 2 дптр (у семи – гиперметропический сдвиг из-за недокоррекции афакии, у трех – миопический сдвиг вследствие легкого смещения ИОЛ). Эти пациенты получили удовлетворительную коррекцию за счет ношения очков. Таким образом, методика продемонстрировала хорошую предсказуемость рефракционного результата. По данным литературы, при транссклеральной фиксации ИОЛ средний рефракционный сдвиг также составляет около -0,5–-1,0 дптр (миопия) [9], что согласуется с нашими данными.
Осложнения
Интра- и послеоперационные осложнения за время наблюдения представлены в табл. 2. Интраоперационно значимых осложнений не зафиксировано. В частности, не зарегистрировано ни одного случая массивного интраокулярного кровотечения или повреждения структуры глаза в ходе вмешательства. У 3 (3%) пациентов произошел разрыв задней капсулы хрусталика во время факоэмульсификации, однако это не повлияло на дальнейший ход операции, так как изначально планировалась фиксация ИОЛ вне капсулы. Все указанные случаи потребовали выполнения тотальной витрэктомии и были успешно завершены имплантацией ИОЛ. В одном случае отмечалась кратковременная корнеальная декомпенсация в раннем послеоперационном периоде (роговичный отек, разрешившийся в течение месяца на фоне терапии).
В раннем послеоперационном периоде (первые 7–10 суток) у большинства пациентов наблюдалась ожидаемая воспалительная реакция: у 28% она проявлялась значимой реакцией со стороны радужки (иридоциклит 1–2-й степени) с клетками в передней камере, требовавшей интенсификации стероидной терапии, однако через две недели у всех пациентов воспаление успешно купировалось. У 11 (11%) пациентов в первые дни после операции регистрировалось повышение уровня ВГД > 25 мм рт. ст. вследствие стероидного ответа или пигментации трабекулы. Во всех случаях ВГД нормализовалось консервативно (на фоне назначения местных бета-блокаторов и ингибиторов карбоангидразы в течение 2–4 недель). Транзиторная послеоперационная гипотония отмечалась у 2 (2%) пациентов: давление снизилось до 5–6 мм рт. ст. в первый день после операции из-за негерметичного склерального отверстия. Оба случая успешно скорректированы дополнительным швом, на итоговое состояние глаза это не повлияло.
В позднем периоде (в течение шести месяцев) наиболее частым осложнением был кистозный макулярный отек (КМО) – 6 (6%) случаев. Все случаи КМО зафиксированы спустя один-два месяца после операции. У четырех пациентов отек купировался консервативной противовоспалительной терапией в течение двух-трех месяцев, двум пациентам потребовалось проведение курса парабульбарных инъекций депо-стероидов, после чего отек макулы полностью регрессировал, острота зрения восстановилась до 0,5 и 0,6 соответственно. Повышение уровня ВГД > 21 мм рт. ст. спустя месяц и более после операции (стойкая офтальмогипертензия) отмечалось у 10 (10%) пациентов. У восьми из них нормализация достигнута при переходе на постоянную гипотензивную терапию (топический простагландин). Еще у двух пациентов сформировалась клинически значимая глаукома, потребовавшая трабекулопластики. Смещение или дислокация ИОЛ в позднем периоде имели место в 3 (3%) случаях: два из них упоминались ранее (частичная дислокация одного гаптического элемента), в третьем случае произошел медленный диффузный сдвиг ИОЛ вниз (децентрация на 1 мм), не повлиявший на остроту зрения. Во всех трех случаях выполнена повторная хирургическая корректировка положения ИОЛ. Вторичная отслойка сетчатки возникла у 1 (1%) пациента. Он имел исходно высокий риск из-за выраженной миопии и периферической дегенерации сетчатки. Отслойка, произошедшая на четвертом месяце от момента операции, была успешно пролечена (витрэктомия с эндотампонадой силиконовым маслом) с восстановлением анатомического прилегания, однако финальная острота зрения снизилась до 0,1. Случаев эндофтальмита не зафиксировано.
Как видно из табл. 2, частота осложнений в целом невысока. Ни одного случая тяжелого инфекционного или воспалительного осложнения (эндофтальмит, токсический иридоциклит) не зарегистрировано. Большинство выявленных осложнений поддавались терапевтической коррекции и не влияли на конечный функциональный результат. Общая частота вторичных хирургических вмешательств составила 5% (три коррекции позиции ИОЛ + одна витрэктомия при отслойке + одна лазерная коагуляция сетчатки при выявленных разрывах). Согласно суммарным данным метаанализа, частота КМО после транссклеральной фиксации ИОЛ составляет около 5,7%, частота отслойки сетчатки – 3,5% [10], транзиторного витреального кровоизлияния – до 8,8% [10]. В нашем исследовании частота осложнений, например КМО (6%) и транзиторной гипертензии (11%), соответствует опубликованным данным (5–7 и 8% соответственно) [11]. Частота же повторной децентрации/дислокации ИОЛ (3%) была несколько ниже, чем в других исследованиях (3–5%) [11].
В случае фиксации ИОЛ с узлами без укрытия склеральным лоскутом в отдаленные сроки не исключено появление эрозии конъюнктивы и экспозиции узла, что чревато развитием инфекции. По данным литературы, эрозия швов наблюдается у 15–18% пациентов через год и у 70% – через два года от момента операции [12]. В нашем исследовании подобных случаев за шесть месяцев наблюдения не зарегистрировано, однако планируется более длительное наблюдение.
Обсуждение
Полученные результаты продемонстрировали, что методика интрасклеральной фиксации заднекамерной ИОЛ является эффективным способом реабилитации пациентов с дислокацией хрусталика, повышает остроту зрения и обеспечивает достаточный рефракционный контроль. Острота зрения достоверно увеличилась уже в первые недели после вмешательства (в среднем с 0,22 до 0,35 через месяц) и продолжила увеличиваться к трем и шести месяцам. Более половины пациентов (58%) достигли остроты 0,5 и выше, что позволяет им вести независимый образ жизни. У 84% пациентов зрение восстановилось до уровня 0,3 и выше. Улучшение МКОЗ в среднем на 0,28 (или 28%) согласуется с данными других исследований, в которых наблюдалось сопоставимое улучшение зрения после склеральной фиксации ИОЛ [12, 13]. Например, C.-H. Hsiao и соавт. (2025) показали, что после склеральной фиксации ИОЛ (103 глаза) средняя острота зрения повысилась с LogMAR 1,12 (≈0,08 десятично) до 0,50 (0,32 десятично) [9]. В отечественных исследованиях также отмечалось значимое повышение НКОЗ в отдаленном периоде до значений, сопоставимых с исходной корригированной остротой [14]. Таким образом, наши данные подтверждают, что возвращение ИОЛ в заднюю камеру глаза (пусть и на склере, вне капсулы) позволяет восстановить центральное зрение у большинства пациентов.
Что касается рефракционных результатов, они показали высокую предсказуемость: более 75% глаз имели отклонение от заданной рефракции не более ±1,0 дптр, а средний СЭ (-0,65 дптр) лишь немного отличался от целевого нуля. В литературе описано, что склеральная фиксация ИОЛ может давать небольшой систематический миопический сдвиг (-0,5–-1 дптр) [9, 10], что совпадает с нашими результатами. Достигнутая нами точность рефракции сравнима с таковой при первичной имплантации ИОЛ в капсулу при неосложненной факоэмульсификации. Это свидетельствует о том, что при правильном расчете оптической силы ИОЛ и стабильной фиксации можно обеспечить хороший фокус и минимизировать астигматизм даже в случаях афакии без капсульной поддержки. Небольшое остаточное смещение (в сторону миопии) может быть связано с минимальным наклоном ИОЛ или смещением узлов, однако на остроту зрения это не влияет.
Анализ 100 случаев подтверждает, что интрасклеральная фиксация ИОЛ – относительно безопасная процедура. Ни в одном случае не возникло тяжелых интраоперационных осложнений, а послеоперационные нежелательные явления встречались с допустимой частотой и, как правило, успешно купировались консервативно. Основные опасения при фиксации ИОЛ вне капсулы связаны с риском дислокации ИОЛ и повреждением внутренних структур глаза. В нашем исследовании повторная дислокация произошла лишь в 3% случаев. Все они были исправлены при повторной операции. Это соответствует мировым данным: частота вторичного смещения ИОЛ составляет 2–5% [11]. Использование склеральных карманов и укрытие узлов, по-видимому, снижает этот риск. Для сравнения: при фиксации ИОЛ в передней камере риск дислокации минимален, зато выше вероятность повреждения эндотелия роговицы и развития глаукомы [1]. При иридофиксации линзы (Artisan, Iris-claw) возникают другие проблемы – хронический иридоциклит, пигментная дисперсия, ограничение расширения зрачка [15, 16]. В данном аспекте склеральная фиксация представляется предпочтительной ввиду нахождения линзы в задней камере, ближе к естественному положению хрусталика [5].
Частота КМО в нашей когорте составила 6%, что согласуется с данными метаанализа (около 5–6%) [10]. Это осложнение встречается и при обычной хирургии катаракты, но при витреоретинальных вмешательствах вероятность его возникновения несколько выше из-за большего травматизма. Все случаи КМО были успешно пролечены без стойкого снижения зрения. Повышение уровня ВГД в раннем периоде (11% транзиторно), вероятно, обусловлено воспалительной реакцией и применением стероидов. Этот показатель сопоставим с данными литературы (8%) [11]. Длительная гипертензия (свыше трех месяцев) наблюдалась у 10% пациентов, причем лишь у 2% развилась полноценная вторичная глаукома, потребовавшая хирургической коррекции. Это приемлемый уровень для данной категории больных с учетом того, что многие имели отягощающие факторы (в частности, ПЭС, травмы, которые сами по себе повышают риск развития глаукомы). Отслойка сетчатки возникла у одного пациента. Формально это 1%, тем не менее следует помнить, что данное осложнение больше связано с исходной патологией (высокая миопия) и витреотомией, чем с фактом фиксации ИОЛ. В зарубежном исследовании частота отслойки после склеральной фиксации ИОЛ составила 2,5%, при этом большинство случаев были успешно оперированы. В нашем случае исход также был благоприятным, хотя острота зрения осталась ограниченной. Показательно полное отсутствие инфекционных осложнений (ни одного случая эндофтальмита). Это говорит об эффективности профилактических мер (антибиотикопрофилактика) и адекватном выполнении хирургического этапа.
Сравнивая два метода склеральной фиксации – шовный и бесшовный, можно отметить следующие моменты. В нашем исследовании применялась техника шовной транссклеральной фиксации (проленовая нить), которая хорошо зарекомендовала себя благодаря относительной простоте и доступности. Ее недостатком является потенциальный риск деградации или миграции швов в отдаленном периоде. Известны случаи, когда через несколько лет после операции происходил разрыв шовного материала с повторной дислокацией ИОЛ [12]. В ряде исследований уже через год после операции эрозия или ослабление шва наблюдались у 15% пациентов, а через два года – более чем у 70% [12]. В связи с этим ряд хирургов переходит на бесшовные методики фиксации (интрасклеральная фиксация гаптиков ИОЛ в туннелях по методике Yamane, фиксация с помощью клея и т.п.) [7, 8]. Бесшовная интрасклеральная фиксация, по данным литературы, демонстрирует сопоставимые краткосрочные результаты и безопасность [13], однако требует специального инструментария и опыта, а долгосрочные результаты пока ограниченны [17]. Наше исследование фокусировалось на классической шовной технике, и за один-два года наблюдения нами не выявлено проблем с узлами. Тем не менее мы планируем более длительный мониторинг пациентов (3–5 лет), чтобы оценить отдаленную надежность фиксации и при необходимости своевременно провести профилактическое укрепление (например, дополнительно зафиксировать ИОЛ методом Yamane, если начнется разрыв шва).
Клинический случай
Пациентка Ж., 67 лет, с ПЭС. Жалобы на резкое снижение зрения правого глаза. Пять лет назад – факоэмульсификация катаракты, установка ИОЛ в капсуле. При осмотре: острота зрения (призматическая коррекция астигматизма) – 0,05, ИОЛ частично вывихнута в стекловидное тело. Проведена задняя витрэктомия, удалена смещенная ИОЛ, имплантирована новая ИОЛ с интрасклеральной фиксацией (техника Yamane). Послеоперационный период без осложнений, через месяц острота зрения – 0,5, ИОЛ центрирована. Данный случай демонстрирует возможность успешного применения как шовной, так и бесшовной методики: выбор зависит от конкретной ситуации (наличие витреальной патологии, состояние второго глаза и т.д.).
Наше исследование имело два ограничения. Во-первых, не проводилось рандомизированного сравнения с другими способами лечения (например, переднекамерными или иридо-фиксируемыми ИОЛ) – всем пациентам выполнялась интрасклеральная фиксация как наиболее приемлемый в их ситуации метод. Тем не менее сопоставление с данными литературы позволяет сделать вывод, что этот метод не уступает альтернативным в эффективности и, вероятно, превосходит их по безопасности в долгосрочной перспективе [5]. Во-вторых, период наблюдения был относительно короткий (медиана 12 месяцев). Для оценки стойкости фиксации и отдаленных осложнений требуется более длительное сопровождение пациентов (несколько лет). Мы продолжаем сбор данных и планируем последующие публикации по отдаленным исходам.
Выводы
На основании изложенного можно сделать несколько выводов.
- Интрасклеральная фиксация заднекамерной ИОЛ – надежный и эффективный метод хирургического лечения пациентов с дислокацией хрусталика или ИОЛ в отсутствие капсульной поддержки. Метод позволяет достигать значимого улучшения остроты зрения (в среднем более чем в два раза) и обеспечивать стабильную, предсказуемую рефракцию у большинства пациентов.
- Анатомическая стабильность положения ИОЛ при интрасклеральной фиксации высокая. В 98–100% случаев достигается центрированное положение ИОЛ, сохраняющееся в течение как минимум шести месяцев. Надежная фиксация ИОЛ в задней камере минимизирует риск смещения линзы и связанных с этим осложнений, присущих альтернативным методам фиксации (переднекамерные или ирис-клипс-ИОЛ).
- Профиль безопасности метода интрасклеральной фиксации удовлетворительный. Частота серьезных интра- и послеоперационных осложнений невысока и сопоставима с таковой при стандартной экстракции катаракты. Выявленные осложнения (КМО, транзиторная гипертензия и др.) в большинстве случаев успешно поддаются медикаментозной или повторной хирургической коррекции и не приводят к стойкой потере зрительных функций.
- Интрасклеральная (транссклеральная) фиксация ИОЛ должна быть в арсенале современного офтальмохирурга, особенно если он занимается факоэмульсификацией осложненных катаракт и витреоретинальной хирургией. Данный метод обеспечивает более физиологичное положение искусственного хрусталика и ассоциируется с лучшими функциональными результатами по сравнению с альтернативными способами коррекции афакии. Освоение современных хирургических методов, в том числе новых бесшовных модификаций, и тщательное ведение пациентов со сложной офтальмологической патологией призваны существенно повысить их качество жизни.
A.S. Azimov, S.A. Abakarov, PhD, Z.I. Mamedov, I.A. Loskutov, PhD, R.Kh. Melikakhmedov, P.Sh. Nukhova
Moscow Regional Research and Clinical Institute
Contact person: Adlan S. Azimov, adlan.azimov.088@gmail.com
The aim was to evaluate the effectiveness and safety of the method of intrascleral fixation of the posterior chamber intraocular lens (IOL) in patients with dislocation of the lens masses.
Material and methods. A retrospective study (a series of cases) included 100 patients (100 eyes) with dislocation of their own lens masses or previously implanted IOLs, who underwent posterior chamber IOL implantation with intrascleral fixation of supporting elements between January 2023 and December 2025.
Results. In all cases, implantation and fixation of the posterior chamber IOL using the chosen method were successful. In the postoperative period, the central position of the IOL in the pupillary opening was noted in 100 eyes. There were no signs of decentration or displacement of the IOL during a routine examination. The frequency of repeated dislocation of the IOL was 2%. A month after the operation, there was a significant improvement in visual acuity compared to baseline.
Conclusion. The results demonstrated that the technique of intrascleral fixation of the posterior chamber IOL is an effective way to rehabilitate patients with lens dislocation, improves visual acuity and provides sufficient refractive control.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.