Отдаленные результаты применения липофилинга у детей с линейной склеродермией
- Аннотация
- Статья
- Ссылки
- English

Введение
Линейная склеродермия (ЛС) – это аутоиммунное воспалительное склерозирующее заболевание кожи и подкожных тканей, связанное с их атрофией. В зависимости от подтипа, тяжести течения заболевания и локализации очага отмечается вовлечение в патологический процесс жировой ткани, мышц, суставов и костей, но не внутренних органов [1]. Ежегодная первичная заболеваемость ЛС в детском возрасте составляет 3,4 случая на 1 млн детского населения, у лиц женского пола заболевание встречается в 2,6–6 раз чаще [2]. ЛС наблюдается примерно у 40–70% пациентов детского возраста [3].
Линейная форма очаговой склеродермии характеризуется наличием одного или нескольких линейных патологических очагов, в которые могут вовлекаться не только структуры кожи, но и подкожная клетчатка, мышцы и подлежащая костная ткань. Обычно это единичное унилатеральное повреждение с линейным распространением, поражающее лицо, волосистую часть головы, нижние конечности [4]. При данной форме склеродермии характерно продольное расположение очагов по длине конечности или сагиттально на коже лица и волосистой части головы. Склеродермия, развивающаяся на лице, представляет собой грубый атрофический очаг в виде линейной полосы на коже лба, известный как удар сабли (en coup de sabre), с возможным вовлечением в патологический процесс волосистой части головы.
Гипотеза о генетическом происхождении ЛС как аутоиммунного заболевания подтверждается ассоциацией случаев болезни с семейным анамнезом аутоиммунных заболеваний и наличием общих типов HLA с ревматоидным артритом [5]. На аутоиммунный характер болезни также указывают наличие аутоантител и повышенные концентрации циркулирующих в крови хемокинов и цитокинов, связанных с Т-хелперами [6]. Клинически для ЛС характерны признаки заболевания, вызванного воспалительным фиброзом, а именно формирование лимфоцитарного и макрофагального инфильтрата с отложением коллагена и фибробластов [7]. Фиброз при этом индуцируется повышенной концентрацией трансформирующего фактора роста β и интерлейкина 4 [8].
Материал и методы
Под нашим наблюдением находилось 56 пациентов от 6 до 18 лет с диагнозом «очаговая склеродермия, линейная форма». Все участники исследования были разделены на две группы: первая (основная) – 35 пациентов в возрасте от 6 до 18 лет с диагнозом линейной склеродермии, получивших более шести месяцев назад иммуносупрессивную терапию препаратом метотрексат и с последующим применением липофилинга в области очага склеродермии (проводили от одной до трех процедур липофилинга, количество операций определяли по клинической картине и послеоперационной потере объема тканей); вторая (контрольная) – 21 пациент от 6 до 18 лет с диагнозом линейной склеродермии, получившие стандартный метод терапии метотрексатом без липофилинга. У 100% пациентов диагноз линейной склеродермии был выставлен год или более года назад, средняя давность заболевания – 2,9 ± 1,3 года. Оценку эффективности липофилинга проводили через год.
У 56 (100%) пациентов были проанализированы триггерные факторы, которые повлияли на начало заболевания: стрессовые ситуации (17,8% пациентов), различные травмы (26,7% пациентов), инфекционные заболевания (8,9% пациентов), гормональные нарушения у лиц женского пола (2,3% пациентов), солнечная инсоляция (3,5% пациентов), 39,6% пациентов не смогли ответить на вопрос о предположительных триггерных факторах начала заболевания.
В ходе исследования до проведения липофилинга оценивали показатели в основной и контрольной группах: возраст, пол, длительность заболевания, индекс активности кожного поражения при локализованной склеродермии (LoSSi), качество жизни (индекс CDLQI), размеры очага (ширина, длина, глубина) и показатели ультразвукового исследования (УЗИ).
На момент включения в исследование медианы [Q1; Q3] в группах исследования были однородны по изучаемым параметрам p-value < 0,05 (табл. 1).
Статистическую обработку выполняли с использованием пакета IBM SPSS (ver. 21) и языка программирования для обработки статистических данных R (ver. 4.2.2) в среде RStudio (ver. 2023.06.2, build 561).
С целью выбора статистического критерия и параметров описания количественных величин был проведен тест Шапиро – Уилка в каждой из исследуемых групп. В связи с тем что ни одно из распределений статистически значимо не соответствовало нормальному (p-value для всех групп составило более 0,05), в работе использовали непараметрические критерии. Описание количественных признаков осуществлялось при помощи медианы и интерквартильного размаха (Me [Q1; Q3]), соответствующих 50%, 25% и 75%-ному квартилю распределения.
Результаты
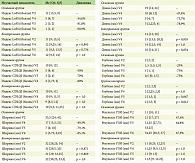
В результате проведенного исследования была доказана эффективность применения липофилинга у детей с ЛС. Результаты анализа представлены в табл. 2. Показатель p-value≤ 0,01 указывает на статистически значимое различие для каждого признака в двух выборках. Так, по данным динамики показателей LoSSi отмечались следующие результаты: до терапии средний показатель по группам исследования составил 11 баллов, а в отдаленном периоде наблюдения в группе контроля – 12 баллов и 1 балл в основной группе (p-value ≤ 0,01).
По данным динамики показателей размера очага отмечались следующие результаты: до проведения аутотрансплантации жировой ткани средняя длина очага склеродермии составила 19 мм в основной и 14 мм в контрольной группе. После проведения липофилинга и оценки результатов в отдаленном периоде наблюдения медиана длины очага уменьшилась более чем в четыре раза (p-value ≤ 0,01) и составила 3 мм в основной группе и 16 мм в группе контроля.
Ширина очага до терапии в среднем составила 33,5 мм в основной группе и 32 мм в контрольной группе. В отдаленном периоде наблюдения медиана ширины очага уменьшилась более чем в 5 раз (p-value ≤ 0,01) и составила 6 мм в основной группе и не изменилась в группе контроля – 32 мм.
Глубина очага ЛС в исходном состоянии составила 2 мм в обеих группах. В отдаленном периоде наблюдения в группе контроля достоверно значимых изменений не наблюдалось, в то время как в основной группе медиана показателя уменьшилась в четыре раза (p-value ≤ 0,01), составив 0,5 мм.
По данным УЗИ, показатель толщины дермы составил 11 в обеих группах, в отдаленном периоде наблюдения в основной группе он увеличился до 34,2 мм, то есть в три раза (p-value ≤ 0,01), в контрольной группе равнялся 11 мм (отсутствие динамики).
Таким образом, значительные изменения по всем изучаемым показателям после проведения аутотрансплантации жира у пациентов основной группы превосходят таковые у пациентов группы контроля после системной терапии препаратом метотрексат с учетом результатов отдаленных наблюдений.
До проведения липофилинга у 90% пациентов, особенно у пациентов 14–18 лет, отмечались жалобы на эстетическую непривлекательность, что проявлялось раздражительностью, нежеланием посещения образовательных учреждений, замкнутостью, ограничением общения со сверстниками и свидетельствовало о снижении качества жизни. Также эти пациенты отмечали утомляемость, расстройство сна, аппетита.
До лечения медиана индекса качества жизни (CDLQI) у всех пациентов, находящихся под наблюдением, была значительно повышена и составляла 10 баллов (p-value ≤ 0,01), у подавляющего большинства больных после лечения полностью исчезли все имеющиеся в исходном состоянии жалобы – CDLQI составил 2 балла в основной группе (p-value ≤ 0,01), в то время как в группе контроля индекс достоверно значимо не изменился.
Побочных эффектов и нежелательных явлений и осложнений у пациентов основной группы на фоне применения аутотрансплантации жировой ткани не зафиксировано. У пациентов контрольной группы не отмечалось побочных явлений при приеме препарата метотрексат.
Заключение
Полученные результаты позволяют сделать вывод о высокой эффективности применения и стойком результате через год после проведения липофилинга у детей с ЛС. Консервативная терапия ЛС позволяет замедлить прогрессирование процесса и уменьшить воспаление, при этом не удается полностью устранить дефекты и атрофию подлежащих тканей. Пересадка жира, включающего адипоциты, жировые стволовые клетки, эндотелиальные клетки и гладкомышечные клетки сосудов, может способствовать уменьшению воспаления, а также фиброза вследствие ограничения синтеза белков внеклеточного матрикса и повышения активности коллагеназы, а также обеспечить структурную поддержку благодаря пролиферации и дифференцировке стволовых клеток.
A.R. Misbakhova, N.E. Manturova, PhD, L.S. Kruglova, PhD, Prof., N.N. Murashkin, PhD, Prof.
Institute of Plastic Surgery and Cosmetology, Moscow
Central State Medical Academy of Department of Presidential Affairs, Moscow
National Medical Research Center for Children's Health
Contact person: Alina. R. Misbakhova, alina.m92@mail.ru
The effectiveness of lipofilling in children with linear scleroderma was analyzed. As is known, linear scleroderma is an autoimmune process, lipofilling is an ideal filler due to its biocompatibility, without the risk of an allergic reaction. The study involved 56 patients aged 6 to 18 years with a diagnosis of linear scleroderma. The study was conducted for 1 year. Patients underwent 1 to 3 stages of lipofilling. Upon completion of the treatment, a reliable change in all the studied parameters was noted. The results obtained allow us to conclude that lipofilling is highly effective in children with linear scleroderma.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.