количество статей
7385
Загрузка...
Пожалуйста, авторизуйтесь:
Обзоры
Анализ современных принципов лечения аллергического риносинусита с назальным полипозом
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Пульмонология и оториноларингология" № 2 (29)
- Аннотация
- Статья
- Ссылки
- English
В статье изложен современный взгляд на лечение хронического риносинусита с назальным полипозом с позиции доказательной медицины. Проанализированы результаты исследований медикаментозной терапии хронического риносинусита, а также показания для хирургии.

Рис. 1. Эндоскопическая картина полости носа при хроническом риносинусите с назальным полипозом: гнойные выделения (А), бесцветные (Б), вязкие (В), в виде корок (Г)

Таблица. Первые результаты функциональной эндоскопической ринохирургии
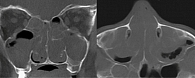
Рис. 2. Компьютерная томография при ХРС с назальным полипозом (полипы полностью заполняют полость носа и все группы околоносовых пазух)
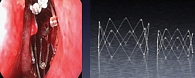
Рис. 3. Стент с мометазона фуроатом в области соустья
Хронический риносинусит (ХРС) с назальным полипозом (НП) – следствие иммунной дисфункции, приводящей к циклу воспалительных реакций, микробному инфицированию, повреждению слизистой оболочки полости носа и нарушению мукоцилиарного транспорта.
Известно несколько теорий развития ХРС, в частности теория микробных биопленок и теория влияния суперантигенов Staphylococcus aureus и локального повышения выработки иммуноглобулинов класса E. На развитие ХРС влияют также аномалии защитной функции слизистой оболочки и неблагоприятные факторы окружающей среды. Генетическая предрасположенность в сочетании с модификациями заболевания способна приводить к различным клиническим проявлениям ХРС с НП, таким как аспириновая триада, аллергический грибковый риносинусит и неаллергический хронический риносинусит с НП [1].
Эндоскопическая картина при ХРС с НП различна. При наличии полипов выделения могут быть гнойными, жидкими и прозрачными, густыми и в виде корок [1]. Дифференцировать лечение ХРС по этим признакам не всегда удается (рис. 1).
В настоящее время особое внимание уделяется сочетанию полипозного риносинусита и аллергического ринита. Согласно последним данным, бронхиальная астма у пациентов с ХРС с НП развивается чаще (51%), чем у пациентов с ХРС без полипов (26%). Аналогичная ситуация и с чувствительностью к аэроаллергенам – 47 и 26% соответственно [2]. Это означает, что ХРС с НП – очень серьезное заболевание, особенно при тотальной обструкции полости носа и околоносовых пазух (ОНП), при наличии пиоцеле (рис. 2).
При тотальном полипозе лечение может осложниться из-за деструкции различных анатомических структур и отсутствия хирургических ориентиров вследствие ранее перенесенных радикальных оперативных вмешательств.
Компьютерная томография (КТ) считается «золотым стандартом» в диагностике ХРС с НП, однако ее специфичность очень низка – 2% [3]. КТ можно рассматривать как «хирургическую карту» для оценки состояния анатомических структур.
Кроме того, КТ позволяет выявить структурные аномалии, такие как костная эрозия и экстрасинусное распространение процесса, которое может быть обусловлено врожденными особенностями.
В лечении ХРС с НП широко применяются назальные глюкокортикостероиды (ГКС). Единственным назальным ГКС, предназначенным для лечения полипозного риносинусита, является мометазона фуроат. Однако тотальная обструкция полипами затрудняет проникновение топических ГКС в полость носа. В подобной ситуации применяются короткие курсы системных ГКС – медикаментозная полипотомия. Обычно используется преднизолон в дозе от 25 до 50 мг в сутки или дексаметазон 8–14 мг в сутки в течение семи дней [1, 4].
При назначении препаратов необходимо тщательно изучать анамнез пациента, чтобы проанализировать возможные противопоказания и риск нежелательных явлений. Такую схему можно рассматривать как предоперационную подготовку, поскольку можно уменьшить размеры полипов, но достичь проходимости синусов и соустий пазух, как правило, не удается.
Кроме того, системная ГКС-терапия позволяет избежать обострений сопутствующей бронхиальной астмы в послеоперационном периоде.
Функциональная эндоскопическая ринохирургия
В России функциональную эндоскопическую ринохирургию (Functional Endoscopic Sinus Surgery – FESS) впервые внедрил Г.З. Пискунов около 20 лет назад. В таблице представлены результаты, обобщенные Г.З. Пискуновым за период 1992–1994 гг. Как видим, в когорте 142 пациентов рецидив составлял 49,3%. С началом применения топических ГКС (1995–1997 гг.) ситуация изменилась и рецидив снизился до 19,5%. Это говорит о том, что хирургия всего лишь одна из многочисленных составляющих лечения ХРС с НП.
Основная задача FESS – максимально сохранить анатомические структуры полости носа и ОНП [5]. FESS предусматривает:
- удаление полипозной ткани с помощью шейвера с сохранением средних и нижних носовых раковин;
- коррекцию искривлений перегородки носа;
- открытие остеомеатального комплекса с тщательным открытием клеток решетчатого лабиринта.
Кроме того, FESS обеспечивает доступ к синусу и тем самым восстанавливает вентиляцию и дренаж через естественные соустья ОНП. Обратите внимание: хирургическое лечение ХРС следует проводить только после максимальной медикаментозной терапии.
Эффективность первичного хирургического вмешательства при ХРС с НП достаточно высока и, безусловно, зависит от степени подготовки хирурга и уровня оснащенности лечебного учреждения. В особо сложных случаях применяют хирургическую навигацию.
Концепция FESS предполагает обратимость патологических структурных изменений слизистой оболочки, хотя нередко это противоречит результатам хирургического лечения.
Результаты немногочисленных гистологических исследований показывают, что, несмотря на клиническое улучшение, электронная микроскопия демонстрирует необратимые изменения слизистой оболочки после хирургического вмешательства. Именно поэтому некоторые хирурги отстаивают радикальные хирургические техники.
Основная цель оперативного вмешательства – восстановление аэрации и дренажа придаточных пазух носа, а также обеспечение доставки лекарственных препаратов к слизистой оболочке ОНП.
В исследованиях показано, что по сравнению с радикальной операцией FESS уменьшает симптомы заболевания и улучшает качество жизни пациентов с ХРС. Хирургическое лечение оказывается неудачным из-за рецидива воспалительного и полипозного процессов, образования синехий, латерализации средней носовой раковины, послеоперационного стеноза соустья ОНП. Именно поэтому рекомендуется применять мометазона фуроат в достаточно раннем послеоперационном периоде. Контроль этих факторов позволяет улучшить результаты хирургии.
Медикаментозная терапия
На наш взгляд, к категории наиболее сложных относятся пациенты, которые ранее подверглись агрессивной хирургии без должного послеоперационного лечения. В таких случаях имеет место утрата важных анатомических структур, естественных путей мукоцилиарного транспорта. Повторная хирургия не способна восстановить анатомию и физиологию.
В отсутствие тотальной обструкции полости носа при ХРС с НП приоритетной должна быть консервативная терапия. Решение о хирургическом лечении принимается только в случае неэффективности максимальной медикаментозной терапии или серьезных затруднений для консервативного лечения (искривление носовой перегородки с нарушением носового дыхания, риск развития осложнений или значительная обструкция полипами).
С позиции доказательной медицины медикаментозная терапия включает в себя ирригационную терапию солевыми растворами [6–8]. При обострении применяются короткие курсы системной и топической антибиотикотерапии. В ряде случаев используются длительные курсы терапии низкими дозами макролидных антибиотиков [9, 10].
В лечении ХРС с НП широко применяются топические ГКС. Их терапевтический эффект основан на универсальном противовоспалительном действии. Основная проблема при использовании ингаляционных назальных ГКС – отсутствие гарантии, что препарат попадет на слизистую оболочку ОНП в необходимом количестве [11–14].
S.A. Shach и соавт. (2012) изучали распределение мометазона фуроата в полости носа. Через 20 минут после использования 37% дозы находилось в полости носа, но через 60 минут – преимущественно в носоглотке с незначительным попаданием в ОНП. Сегодня это считается основным недостатком ингаляционных ГКС, что особенно критично при ХРС [15–17]. Этот кажущийся недостаток оборачивается преимуществом, особенно у детей при наличии гипертрофии аденоидов. Их уменьшение под воздействием мометазона фуроата доказано в десятке исследований.
Топические ГКС, используемые в лечении ХРС, способствуют обратной трансформации слизистой оболочки за счет уменьшения отложения коллагена в субэпителиальном слое базальной мембраны. В то же время за счет противовоспалительного действия ГКС способны препятствовать или изменять процесс ремоделирования слизистой оболочки. Таким образом, хирургическое вмешательство является дополнением к медикаментозному лечению с использованием топических ГКС.
Ирригационная терапия как одна из послеоперационных процедур крайне важна. Она способствует очищению полости носа, размягчению образовавшихся корок и восстановлению мукоцилиарного транспорта. По мнению экспертов, промывание полости носа следует начинать через 24–48 часов после операции, используя большие объемы растворов [1, 8, 18–20]. Промывание оперированной пазухи способствует более быстрому восстановлению слизистой оболочки за счет уменьшения воспаления. Санация пазухи осуществляется под контролем эндоскопа и с помощью отсоса. Большинство экспертов сходятся во мнении, что оптимальная санация пазухи должна быть выполнена в первую неделю после FESS.
Топические назальные ГКС являются важным компонентом противовоспалительной терапии ХРС. В этих целях используются назальные спреи с ГКС, разрешенными для местного применения. Однако назальные спреи обеспечивают доставку лекарственных средств в основном в полость носа. Топическую ГКС-терапию мометазона фуроатом необходимо начинать между второй и шестой неделей после операции [2, 21, 22].
В послеоперационном периоде также рекомендуется применять системные ГКС короткими курсами: преднизолон по четыре дня сначала 30 мг, затем 20 мг и наконец 10 мг. Общая продолжительность курса – 12 дней с суммарной дозой 240 мг. Целесообразно также применение системных ГКС в дозе 30 мг в течение пяти дней до операции и в течение девяти дней после (14 дней, суммарная доза 420 мг) [1, 4].
Стент с лекарственным покрытием
Перспективным способом прямой доставки лекарственных средств в ОНП в необходимой дозе считается установка в области соустья специального стента с лекарственным покрытием (рис. 3). Данное устройство является растворимым и содержит мометазона фуроат. Стент помещается в область вскрытых клеток решетчатого лабиринта и расправляется для лучшего контакта со слизистой оболочкой. Стент состоит из полилактид-гликолида – полимера, который входит в состав многих видов шовного материала и, как показано в исследованиях у животных, не вызывает воспалительных реакций [23]. Мометазона фуроат в дозе 370 мкг, растворенный в полимере, выделяется путем диффузии в течение приблизительно 30 дней. В этот период пациенты не используют топические и системные ГКС.
При использовании стента уменьшается необходимость послеоперационного вмешательства, рассечения синехий, применения системных ГКС, а также снижается вероятность рецидива полипозного риносинусита [24].
Заключение
Как показывают результаты исследований, при ХРС эффективны короткие курсы системной ГКС-терапии. При неэффективности медикаментозной терапии применяется хирургическое лечение. Ведущее место отводится функциональной эндоскопической ринохирургии, направленной на обеспечение проходимости естественных соустий ОНП и сохранение основных анатомических структур полости носа.
1. Pigret D., Jankowski R. Management of post-ethmoidectomy crust formation: randomized single-blind clinical trial comparing pressurized seawater versus antiseptic/mucolytic saline // Rhinology. 1996. Vol. 34. № 1. P. 38–40.
2. DelGaudio J.M., Wise S.K. Topical steroid drops for the treatment of sinus ostia stenosis in the postoperative period // Am. J. Rhinol. 2006. Vol. 20. № 6. P. 563–567.
3. Hwang P.H., Irwin S.B., Griest S.E. et al. Radiologic correlates of symptom-based diagnostic criteria for chronic rhinosinusitis // Otolaryngol. Head. Neck Surg. 2003. Vol. 128. № 4. P. 489–496.
4. Welch K.C., Thaler E.R., Doghramji L.L. et al. The effects of serum and urinary cortisol levels of topical intranasal irrigations with budesonide added to saline in patients with recurrent polyposis after endoscopic sinus surgery // Am. J. Rhinol. Allergy. 2010. Vol. 24. № 1. P. 26–28.
5. Khalil H.S., Nunez D.A. Functional endoscopic sinus surgery for chronic rhinosinusitis // Cochrane Database Syst. Rev. 2006. № 3. CD004458.
6. Bachmann G., Hommel G., Michel O. Effect of irrigation of the nose with isotonic salt solution on adult patients with chronic paranasal sinus disease // Eur. Arch. Otorhinolaryngol. 2000. Vol. 257. № 10. P. 537–541.
7. Harvey R., Hannan S.A., Badia L., Scadding G. Nasal saline irrigations for the symptoms of chronic rhinosinusitis // Cochrane Database Syst. Rev. 2007. № 3. CD006394.
8. Staffieri A., Marino F., Staffieri C. et al. The effects of sulfurous-arsenical-ferruginous thermal water nasal irrigation in wound healing after functional endoscopic sinus surgery for chronic rhinosinusitis: a prospective randomized study // Am. J. Otolaryngol. 2008. Vol. 29. № 4. P. 223–229.
9. Desrosiers M.Y., Salas-Prato M. Treatment of chronic rhinosinusitis refractory to other treatments with topical antibiotic therapy delivered by means of a large-particle nebulizer: results of a controlled trial // Otolaryngol. Head. Neck Surg. 2001. Vol. 125. № 3. P. 265–269.
10. Taccariello M., Parikh A., Darby Y., Scadding G. Nasal douching as a valuable adjunct in the management of chronic rhinosinusitis // Rhinology. 1999. Vol. 37. № 1. P. 29–32.
11. Cannady S.B., Batra P.S., Citardi M.J., Lanza D.C. Comparison of delivery of topical medications to the paranasal sinuses via ‘vertex-to-floor’ position and atomizer spray after FESS // Otolaryngol. Head. Neck Surg. 2005. Vol. 133. № 5. P. 735–740.
12. Lal D., Hwang P.H. Oral corticosteroid therapy in chronic rhinosinusitis without polyposis: a systematic review // Int. Forum Allergy Rhinol. 2011. Vol. 1. № 2. P. 136–143.
13. Lund V.J., Flood J., Sykes A.P., Richards D.H. Effect of fluticasone in severe polyposis // Arch. Otolaryngol. Head Neck Surg. 1998. Vol. 124. № 5. P. 513–518.
14. Schlosser R.J., Soler Z.M. Evidence-based treatment of chronic rhinosinusitis with nasal polyps // Am. J. Rhinol. Allergy. 2013. Vol. 27. № 6. P. 461–466.
15. Shah S.A., Berger R.L., Gurta P. et al. Human nasal deposition of mometasone furoate aqueaus nasal spray. Americal College of Allergi and Immunology Annual Meeting, 2012.
16. Snidvongs K., Kalish L., Sacks R. et al. Topical steroid for chronic rhinosinusitis without polyps // Cochrane Database Syst. Rev. 2011. № 8. CD009274.
17. Stjarne P., Olsson P., Alenius M. Use of mometasone furoate to prevent polyp relapse after endoscopic sinus surgery // Arch. Otolaryngol. Head. Neck Surg. 2009. Vol. 135. № 3. P. 296–302.
18. Freeman S.R., Sivayoham E.S., Jepson K., de Carpentier J. A preliminary randomised controlled trial evaluating the efficacy of saline douching following endoscopic sinus surgery // Clin. Otolaryngol. 2008. Vol. 33. № 5. P. 462–465.
19. Fooanant S., Chaiyasate S., Roongrotwattanasiri K. Comparison on the efficacy of dexpanthenol in sea water and saline in postoperative endoscopic sinus surgery // J. Med. Assoc. Thai. 2008. Vol. 91. № 10. P. 1558–1563.
20. Pinto J.M., Elwany S., Baroody F.M., Naclerio R.M. Effects of saline sprays on symptoms after endoscopic sinus surgery // Am. J. Rhinol. 2006. Vol. 20. № 2. P. 191–196.
21. Bhalla R.K., Payton K., Wright E.D. Safety of budesonide in saline sinonasal irrigations in the management of chronic rhinosinusitis with polyposis: lack of significant adrenal suppression // J. Otolaryngol. Head. Neck Surg. 2008. Vol. 37. № 6. P. 821–825.
22. Wei C.C., Kennedy D.W. Mometasone implant for chronic rhinosinusitis // Med. Devices (Auckl). 2012. Vol. 5. P. 75–80.
23. Uren B., Psaltis A., Wormald P.J. Nasal lavage with mupirocin for the treatment of surgically recalcitrant chronic rhinosinusitis // Laryngoscope. 2008. Vol. 118. № 9. P. 1677–1680.
24. Na Y., Kim K., Kim S.K., Chung S.K. The quantitative effect of an accessory ostium on ventilation of the maxillary sinus // Respir. Physiol. Neurobiol. 2012. Vol. 181. № 1. P. 62–73.
Analysis of modern curative principles in treatment of allergic rhinosinusitis with nasal polyposis
S.Ya. Kosyakov, E.V. Pchelenok
Russian medical academy of postgraduate education
Contact person: Sergey Yakovlevich Kosyakov, serkosykov@yandex.ru
Here, we share with a modern view on treatment of chronic rhinosinusitis with nasal polyposis in terms of evidence-based medicine. Results of the studies about medicated therapy of chronic rhinosinusitis including indications for surgical intervention are analyzed.
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.