Эозинофильный энтерит: клиническое наблюдение
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – демонстрация особенностей диагностики и возможного варианта лекарственной терапии мышечно-серозной формы эозинофильного энтерита (ЭоЭт). Пациенту с жалобами на абдоминальные боли, нарушение стула, снижение массы тела проведено обследование для исключения патологии, наиболее часто вызывающей подобные симптомы, в том числе инфекции пищеварительной системы, целиакию, панкреатит. При этом выявлены утолщение стенки тонкой кишки, асцит, эозинофилия и увеличение эозинофильного катионного белка, поставлен диагноз ЭоЭт, мышечно-серозная форма, назначена успешная терапия блокаторами лейкотриеновых и Н1-рецепторов, стабилизатором мембран тучных клеток. Представленный случай демонстрирует сложности диагностики и, как следствие, несвоевременность терапии ЭоЭт, что обусловливает необходимость создания клинических рекомендаций и повышения настороженности врачей относительно ЭГИЗ.
Цель исследования – демонстрация особенностей диагностики и возможного варианта лекарственной терапии мышечно-серозной формы эозинофильного энтерита (ЭоЭт). Пациенту с жалобами на абдоминальные боли, нарушение стула, снижение массы тела проведено обследование для исключения патологии, наиболее часто вызывающей подобные симптомы, в том числе инфекции пищеварительной системы, целиакию, панкреатит. При этом выявлены утолщение стенки тонкой кишки, асцит, эозинофилия и увеличение эозинофильного катионного белка, поставлен диагноз ЭоЭт, мышечно-серозная форма, назначена успешная терапия блокаторами лейкотриеновых и Н1-рецепторов, стабилизатором мембран тучных клеток. Представленный случай демонстрирует сложности диагностики и, как следствие, несвоевременность терапии ЭоЭт, что обусловливает необходимость создания клинических рекомендаций и повышения настороженности врачей относительно ЭГИЗ.
Согласно международному консенсусу (2022) по номенклатуре, эозинофильные гастроинтестинальные заболевания (ЭГИЗ) – это хронические иммуноопосредованные расстройства, клинически характеризующиеся желудочно-кишечными симптомами, а гистологически – воспалением с патологическим преобладанием эозинофилов при отсутствии вторичных причин эозинофилии. ЭГИЗ – зонтичный термин, включающий поражение пищевода, желудка, тонкой и толстой кишки по отдельности или в любой комбинации с вовлечением различных слоев желудочно-кишечного тракта [1]. Наиболее известным ЭГИЗ является эозинофильный эзофагит (ЭоЭ). В отличие от ЭоЭ, ЭГИЗ других локализаций пищеварительной трубки изучены меньше и в настоящее время рекомендации по их диагностике и лечению отсутствуют [1].
Распространенность ЭГИЗ, не связанных с ЭоЭ, около 5,1–5,3 на 100 000 населения, чаще встречаются у женщин, европеоидов и детей младше 5 лет, могут сочетаться с лекарственной и пищевой аллергией, риносинусопатией, астмой, дерматитом, целиакией [1–3]. Их развитию способствуют генетические и внешнесредовые факторы. Выделены гены, ассоциированные с цитокинами, хемокинами, эозинофилией, которые могут рассматриваться в качестве потенциальных биомаркеров ЭГИЗ [3, 4]. Точный патофизиологический механизм ЭГИЗ, не связанных с ЭоЭ, помимо участия эозинофилов, неясен; исследования подчеркивают роль IgE-опосредованных и клеточно-опосредованных реакций [4].
Симптомы внепищеводных локализаций ЭГИЗ неспецифичны и могут варьироваться, что делает их малоинформативными для верификации заболевания и нередко приводит к задержкам и ошибкам в диагностике [3, 5].
В классификации Klein выделяют три подтипа ЭГИЗ без ЭоЭ [6]. Слизистый подтип преобладает по частоте встречаемости, возможно из-за доступности материала для биопсии; характерны вздутие и боли в животе, диарея, снижение веса. При мышечном подтипе инфильтрируется мышечный слой, что приводит к его утолщению и нарушению кишечной моторики, возможны перфорация, инвагинация, дивертикулез и тонкокишечная непроходимость. Серозный подтип менее известен, проявляется эозинофильным асцитом, реже – перитонитом и эозинофильным плевральным выпотом. В случае трансмуральной эозинофильной инфильтрации можно думать о смешанном типе ЭГИЗ [5].
Эозинофилия встречается в 80% случаев, а повышение концентрации общего IgE – более чем в 70%, в случае серозного подтипа эозинофилы увеличены в асцитической жидкости.
Эндоскопическая картина неспецифична, и гистопатологическое выявление плотной эозинофильной инфильтрации является диагностическим признаком [7].
С помощью ультразвукового исследования и компьютерной томографии можно обнаружить асцит, сегментарное утолщение стенки пораженного участка, лимфаденопатию и осложнения. Для диагностики также возможно использовать с 99mTc-HMPAO-WBC-сцинтиграфию. Разработан диагностический молекулярный критерий ЭГИЗ (EGDP18 score) с использованием транскрипта мРНК желудка и уровней циркулирующего белка [5, 7].
Диагностические критерии ЭГИЗ (Тэлли, 1990 г.) включают: 1) гастроинтестинальные симптомы; 2) инфильтрацию эозинофилами, характерные рентгенологические данные, эозинофилию; 3) отсутствие признаков паразитарного или внекишечного заболевания [5, 8].
В рамках лечения ряд ретроспективных, небольших исследований и наблюдений демонстрирует помимо гипоаллергенной диеты возможность применения нескольких групп препаратов: кортикостероидов, селективных H1-антигистаминных препаратов и стабилизаторов тучных клеток, антагонистов лейкотриеновых рецепторов, иммунодепрессантов, биологических препаратов [3–5, 7].
Примером редкой и длительно не диагностируемой смешанной мышечно-серозной формы эозинофильного поражения тонкой кишки может служить представленное клиническое наблюдение.
Больной Л., 37 лет, обратился в ГАСТРОЦЕНТР (г. Пермь) в мае 2022 г. с жалобами на тупые боли в верхней половине живота, усиливающиеся при движении, изменении положения тела, на фоне давления поясом на переднюю брюшную стенку, выраженное урчание и вздутие живота после приема пищи, общую слабость, нарушение стула. Стул ежедневный до двух раз в день, кашицеобразный, обильный, периодически с зеленоватым оттенком, без патологических примесей. Отмечает снижение массы тела на 7 кг за две недели, что связывает с ограничением в питании.
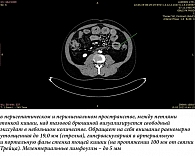
Из анамнеза заболевания известно, что с подросткового возраста страдает дискинезией желчевыводящих путей (ДЖВП), более 10 лет – без обострений. Настоящее ухудшение с 27 апреля 2022 г., когда через несколько недель после перенесенной новой коронавирусной инфекции появились интенсивные ноющие и/или схваткообразные боли в верхней половине живота до 8 баллов по визуальной аналоговой шкале боли. В связи с высокой интенсивностью болевого синдрома пациент был госпитализирован в хирургическое отделение, где находился в течение семи дней с диагнозом «острый панкреатит». При этом в клиническом и биохимическом анализах крови, а также по данным ультразвукового исследования органов брюшной полости отклонений от нормы выявлено не было. Уточняющие обследования не проводились. На фоне инфузионной терапии с анальгетиками выраженность болевого синдрома уменьшилась, пациент выписан на амбулаторное лечение, где наблюдался с последовательными диагнозами: обострение хронического панкреатита, ДЖВП, синдром раздраженного кишечника и функциональная диспепсия. В течение месяца безуспешно получал следующее лечение: тримебутин, ребамипид, Saccharomyces boulardii, даларгин, орнитин, полиферментные препараты, пиколинат цинка, селанк, папаверин. Единственное, что купировало абдоминальные боли, – применение нестероидных противовоспалительных препаратов (нимесулид). В связи с сохранением симптоматики пациент самостоятельно прошел мультиспиральную компьютерную томографию (МСКТ) органов брюшной полости, где были выявлены признаки асцита и утолщения стенки тонкой кишки до 19 мм, на протяжении 100 мм от связки Трейца (рис. 1). Для верификации диагноза и лечения пациент обратился в ГАСТРОЦЕНТР.
Из анамнеза жизни известно, что пациент страдает витилиго и псориазом в легкой форме. Аллергологический анамнез – без особенностей. Много лет не употребляет молочные продукты в связи с развитием диареи на фоне их употребления. Наследственность по заболеваниям желудочно-кишечного тракта не отягощена. Лекарственные препараты и биологически активные добавки на регулярной основе не употребляет. Профессиональную вредность, злоупотребление алкоголем отрицает. Операций не было.
Объективно: состояние удовлетворительное; кожные покровы физиологической окраски, единичные пятна витилиго и псориатические бляшки без активного воспаления; отеков нет; периферические лимфатические узлы не увеличены; температура тела – 36,7 °C, рост – 186 см; масса тела – 96 кг; индекс массы тела – 27,7 кг/м2; язык влажный с беловатым налетом; живот мягкий, умеренно болезненный при пальпации в верхнем отделе; печень по краю реберной дуги, край ровный, безболезненный; симптомы Менделя, I–III группы холецистита и панкреатита отрицательные; селезенка не увеличена.
Предварительный диагноз включал в себя энтерит неуточненной этиологии, постковидный синдром с перивисцеритом, болезнь Крона, лимфому. При дальнейшем обследовании были исключены кишечные инфекции: посев кала на острые кишечные инфекции, комплексное молекулярно-генетическое исследование возбудителей острых кишечных инфекций в кале, иммуноферментный анализ кала на токсины А и В Clostridioides difficile, исследование кала на паразитов и яйца глист – результаты отрицательные. Биохимический анализ крови, форез белков, С-реактивного белка, уровень тиреотропного гормона, общий IgA и IgE, антитела к глиадину и тканевой трансглутаминазе IgA и IgG – в пределах нормы. В клиническом анализе крови обращает на себя внимание выраженная эозинофилия до 24%; эозинофильный катионный белок (ЕСР) при этом без подсчета – более 200 нг/мл. В рамках диагностики эозинофильного поражения желудочно-кишечного тракта проведена видеоэзофагогастродуоденоскопия с биопсией слизистой оболочки (СО) постбульбарного отдела двенадцатиперстной кишки, тела и антрального отдела желудка, а также видеоилеоколоноскопия с биопсией СО терминального отдела подвздошной кишки, правого и левого отделов толстой кишки, по результатам которых эозинофильная инфильтрация или признаки другого органического заболевания СО желудка и кишечника исключены.
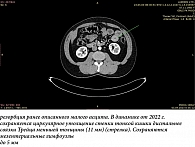
Таким образом, с учетом стойкой абдоминальной боли с признаками утолщения стенки тонкой кишки и асцитом по данным визуализирующих методов обследования, а также выраженной эозинофилии в клиническом анализе крови с увеличением ЕСР был предположен диагноз мышечно-серозной формы эозинофильного энтерита (ЭЭ). Оценив состояние пациента как удовлетворительное, от применения системных глюкокортикоидов решили воздержаться. Рекомендована гипоаллергенная диета. Лекарственная терапия включала терапию второй линии, а именно комбинацию антагониста лейкотриеновых рецепторов монтелукаста 10 мг, стабилизатора мембран тучных клеток кетотифена 1 мг два раза в день и блокатора гистаминовых Н1-рецепторов левоцетиризина 5 мг на протяжении трех месяцев. На фоне лечения состояние быстро улучшилось, болевой синдром был купирован в течение первой недели, в течение месяца нормализовался стул, стабилизировалось общее самочувствие. При контрольном обследовании через месяц наблюдалась выраженная положительная динамика в виде снижения эозинофилии крови до 8,3% и ЕСР до 85,4 нг/мл, через три месяца уровень эозинофилов крови и ЕСР нормализовался (4,2% и 23,4 нг/мл соответственно). Пациенту рекомендовано продолжить соблюдать гипоаллергенную диету, а также в рамках исключения развития ЭоЭ на фоне болезни Крона или лимфомы кишечника выполнить обследование кишечника в динамике через шесть месяцев. Однако МСКТ-контроль органов брюшной полости пациент выполнил лишь через год по причине рецидива заболевания с абдоминальной болью, эозинофилией крови до 18% и увеличением ЕСР до уровня более 200 нг/мл, возникшего после перенесенной вирусной инфекции и погрешности в диете. При визуализации наблюдалась резорбция ранее описанного малого асцита, сохранялось или рецидивировало менее выраженное циркулярное утолщение стенки тонкой кишки дистальнее связки Трейца (11 мм) (рис. 2).
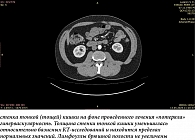
Пациент самостоятельно повторил курс терапии с достижением в течение месяца регресса всех наблюдаемых изменений. В настоящее время в течение двух лет данные о рецидиве ЭЭ отсутствуют. Контрольные анализы и КТ органов брюшной полости в норме (рис. 3).
Заключение
ЭГИЗ являются растущими по частоте заболеваниями пищеварительной системы, нуждающимися в разработке клинических рекомендаций. В связи с отсутствием специфической симптоматики и низкой настороженностью врачей диагноз ЭГИЗ нередко ставится с большим опозданием и приводит к несвоевременному лечению. Представленное клиническое наблюдение пациента с ЭоЭт иллюстрирует связь дебюта заболевания с перенесенной вирусной инфекцией, длительный диагностический поиск и хорошую эффективность терапии с применением гипоаллергенной диеты и нестероидной лекарственной терапии.
От пациента было получено письменное добровольное информированное согласие на публикацию результатов обследования и лечения.
Авторы заявляют об отсутствии возможных конфликтов интересов.
L.G. Vologzhanina, PhD, I.P. Petukhova, PhD, A.L. Leonidov
E.A. Vagner Perm State Medical University
Contact person: Lyudmila G. Vologzhanina, ludovica@mail.ru
No guidelines exist at present for diagnosis or treatment of the non eosinophilic esophagitis eosinophilic gastrointestinal diseases (non-EoE EGID), what makes management of patients with this rare pathology difficult. The aim of study is to demonstrate features of diagnosis and a possible of treatment option of the muscular – serosal subtype of eosinophilic enteritis (EoEt).
The patient with complaints of abdominal pain, bowel disturbances, and weight loss was examined to rule out other diseases which might cause such symptoms, including digestive system infections, celiac disease, and pancreatitis. At the same time, thickening of the small intestinal wall, ascites, eosinophilia, and increased eosinophil cationic protein were detected, which lead to the diagnosis of EoEt, muscular – serosal subtype; we prescribed treatment with leukotriene receptor antagonists, histamine H1 receptor antagonists, mast cell stabilizers to the patient and our therapy was successful. This medical case demonstrates the difficulties of diagnosing and, consequently, delay of treatment with EoEt, which requires the development of the guidelines and raise the awareness of doctors regarding non-EoE EGID.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.