Оптико-фармакологическое лечение прогрессирующей миопии у детей
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить влияние комбинированного оптико-фармакологического лечения на динамику рефракции, аккомодацию, зрительные функции и толщину хориоидеи (ТХ) у детей с прогрессирующей миопией в сравнении с оптическим воздействием.
Материал и методы. Обследовано 40 детей в возрасте 8–13 лет (в среднем 10,5 года) с миопией от 1,75 до 6,37 (в среднем 3,98) дптр. Всем детям были назначены новые очки со встроенными кольцами высокоасферичных микролинз с полной коррекцией. Через месяц от начала ношения новых очков дети были рандомизированы на две группы. Основную группу (оптико-фармакологическое лечение, капли) представляли 20 детей, которым назначали глазные капли Мидримакс® один раз в день на ночь в течение месяца курсами – четыре курса в год. В контрольную группу вошли 20 детей, получавших только оптическое воздействие. Дети обеих групп проходили осмотр до начала назначения новых очков и через один, шесть и 12 месяцев. Исследовали остроту зрения в очках, сферэквивалент циклоплегической рефракции, длину переднезадней оси глаза, аккомодацию, диаметр зрачка и ТХ.
Результаты. Острота зрения в очках в течение наблюдения оставалась стабильной в обеих группах. Через 12 месяцев рефракция незначительно усилилась – на 0,09 ± 0,04 дптр в основной группе и на 0,12 ± 0,07 дптр в контрольной. Усиление рефракции на 0,5 дптр и более наблюдали у 7,5% детей основной и 22,5% детей контрольной групп. В случаях, когда привычный тонус аккомодации открытого поля (ПТА-ОП) на фоне ношения очков с полной коррекцией был 0,5 дптр и выше, в основной группе наблюдалось ослабление рефракции на 0,12 ± 0,09 дптр через 12 месяцев наблюдения, в контрольной группе рефракция усилилась на 0,54 ± 0,07 дптр. Запасы относительной аккомодации (ЗОА) повысились до минимальных нормальных значений в обеих группах. Диаметр зрачка имел тенденцию к увеличению в обеих группах. ТХ в основной группе увеличилась на 12 мкм от исходных значений, в контрольной – на 6 мкм.
Заключение. За 12-месячный период наблюдения в обеих группах отмечались стабилизация рефракции, увеличение ЗОА до минимальных нормальных значений. Оптико-фармакологическое воздействие, включая использование глазных капель Мидримакс® один раз в день на ночь в течение месяца курсами – четыре курса в год, ассоциировалось со стабилизирующим влиянием в случаях повышения ПТА-ОП до 0,5 дптр и более (на фоне ношения очков с полной коррекцией). В контрольной группе (без капель) в таких случаях отмечалась устойчивая тенденция к усилению рефракции. Более значимое и стабильное увеличение ТХ при оптико-фармакологическом лечении по сравнению с оптическим воздействием требует особого изучения. Назначение оптико-фармакологического лечения целесообразно при выявлении признаков сопутствующего миопии привычно-избыточного напряжения аккомодации.
Цель – оценить влияние комбинированного оптико-фармакологического лечения на динамику рефракции, аккомодацию, зрительные функции и толщину хориоидеи (ТХ) у детей с прогрессирующей миопией в сравнении с оптическим воздействием.
Материал и методы. Обследовано 40 детей в возрасте 8–13 лет (в среднем 10,5 года) с миопией от 1,75 до 6,37 (в среднем 3,98) дптр. Всем детям были назначены новые очки со встроенными кольцами высокоасферичных микролинз с полной коррекцией. Через месяц от начала ношения новых очков дети были рандомизированы на две группы. Основную группу (оптико-фармакологическое лечение, капли) представляли 20 детей, которым назначали глазные капли Мидримакс® один раз в день на ночь в течение месяца курсами – четыре курса в год. В контрольную группу вошли 20 детей, получавших только оптическое воздействие. Дети обеих групп проходили осмотр до начала назначения новых очков и через один, шесть и 12 месяцев. Исследовали остроту зрения в очках, сферэквивалент циклоплегической рефракции, длину переднезадней оси глаза, аккомодацию, диаметр зрачка и ТХ.
Результаты. Острота зрения в очках в течение наблюдения оставалась стабильной в обеих группах. Через 12 месяцев рефракция незначительно усилилась – на 0,09 ± 0,04 дптр в основной группе и на 0,12 ± 0,07 дптр в контрольной. Усиление рефракции на 0,5 дптр и более наблюдали у 7,5% детей основной и 22,5% детей контрольной групп. В случаях, когда привычный тонус аккомодации открытого поля (ПТА-ОП) на фоне ношения очков с полной коррекцией был 0,5 дптр и выше, в основной группе наблюдалось ослабление рефракции на 0,12 ± 0,09 дптр через 12 месяцев наблюдения, в контрольной группе рефракция усилилась на 0,54 ± 0,07 дптр. Запасы относительной аккомодации (ЗОА) повысились до минимальных нормальных значений в обеих группах. Диаметр зрачка имел тенденцию к увеличению в обеих группах. ТХ в основной группе увеличилась на 12 мкм от исходных значений, в контрольной – на 6 мкм.
Заключение. За 12-месячный период наблюдения в обеих группах отмечались стабилизация рефракции, увеличение ЗОА до минимальных нормальных значений. Оптико-фармакологическое воздействие, включая использование глазных капель Мидримакс® один раз в день на ночь в течение месяца курсами – четыре курса в год, ассоциировалось со стабилизирующим влиянием в случаях повышения ПТА-ОП до 0,5 дптр и более (на фоне ношения очков с полной коррекцией). В контрольной группе (без капель) в таких случаях отмечалась устойчивая тенденция к усилению рефракции. Более значимое и стабильное увеличение ТХ при оптико-фармакологическом лечении по сравнению с оптическим воздействием требует особого изучения. Назначение оптико-фармакологического лечения целесообразно при выявлении признаков сопутствующего миопии привычно-избыточного напряжения аккомодации.



Медикаментозное лечение прогрессирующей миопии с использованием разных вегетотропных средств, влияющих на аккомодацию миопических глаз, используется более 50 лет [1, 2]. Лекарственные средства для нормализации аккомодации и лечения миопии применяют 96,5% офтальмологов (в монорежиме или в составе комплексного лечения) [3]. Симпатомиметик фенилэфрин (S01FB01) рекомендован как средство улучшения ослабленной аккомодационной способности миопических глаз и профилактики прогрессирования миопии [1, 2, 4–9]. Антихолинергическое средство тропикамид (S01FA06) позволяет преодолеть привычно-избыточное напряжение аккомодации [10, 11]. С учетом двойственного характера иннервации цилиарной мышцы медикаментозная терапия привычно-избыточного напряжения аккомодации, в том числе сопутствующего миопии, проводимая по двум направлениям, путем инстилляции комбинированного препарата Мидримакс® (S01FA56), содержащего фенилэфрин 5% и тропикамид 0,8%, дает выраженные и устойчивые результаты, воздействует на динамическую рефракцию глаза и ширину зрачка, а следовательно, на рефрактогенез миопических глаз в детском возрасте [12–17]. Подобное влияние отмечается даже у детей, использующих оптические средства, формирующие относительный периферический миопический дефокус и замедляющие рост глаза [16, 17]. Попытка соединить оптическое и медикаментозное воздействие представляется интересной и амбициозной.
Цель – оценить влияние комбинированного оптико-фармакологического лечения на динамику рефракции, аккомодацию, зрительные функции и толщину хориоидеи (ТХ) у детей с прогрессирующей миопией в сравнении с оптическим воздействием.
Материал и методы
В исследовании участвовало 40 детей в возрасте 8–13 лет (в среднем 10,5 года) с миопией от 1,75 до 6,37 (в среднем 3,98) дптр. Все участники исследования ранее носили монофокальные очки, не соответствовавшие рефракции, либо не имели очков. Величина средней недокорригированной миопии составила 1,38 ± 0,15 дптр. Всем детям были назначены новые очки со встроенными кольцами высокоасферичных микролинз, формирующих градиентный миопический дефокус. Назначали полную коррекцию миопии, рекомендовали постоянное ношение очков. Через месяц от начала ношения новых очков дети были рандомизированы на две группы. Основную группу (оптико-фармакологическое воздействие, капли) представляли 20 детей, которым дополнительно назначили комбинированные глазные капли один раз в день на ночь в течение месяца курсом каждые три месяца – всего четыре курса в год. В государственном реестре лекарственных средств зарегистрировано несколько фиксированных комбинаций фенилэфрина и тропикамида. Первой из них стал препарат Мидримакс® (Mydrimax®, SENTISS PHARMA, Pvt. Ltd, Индия), содержащий 50 мг фенилэфрина и 8 мг тропикамида на 1 мл раствора. В качестве вспомогательного вещества в состав препарата входит гипромеллоза в дозе 5 мг на 1 мл. Гипромеллоза обладает оптимальными физико-химическими характеристиками, обеспечивающими высокую гисто- и цитосовместимость, прозрачность, способность повышать вязкость растворов, пролонгировать время нахождения препарата в прекорнеальной зоне, повышать величину его концентрации в тканях глаза, а также модифицировать высвобождение. Важно отметить оптимальный профиль безопасности гипромеллозы и отсутствие токсических эффектов, как местных, так и системных. В исследовании использовались глазные капли Мидримакс®, выпускаемые во флаконах-капельницах по 5 мл.
20 детей контрольной группы не получали какого-либо дополнительного лечения, кроме оптического воздействия.
Дети обеих групп проходили осмотр до начала назначения новых очков и через один, шесть и 12 месяцев. Детей основной группы осматривали также после первого курса закапывания капель. Результаты осмотра детей через месяц от начала ношения очков со встроенными микролинзами и по завершении первого курса медикаментозного лечения (основная группа) были опубликованы ранее [16], поэтому в рамках данной статьи воспроизводятся частично. В основной группе (капли) осмотры через шесть и 12 месяцев проводили спустя месяц после завершения месячного курса фармакотерапии Мидримаксом.
Остроту зрения проверяли с использованием проектора знаков и тестов «Е». Для исследования рефракции применяли авторефрактометрию (Nidek ARK-530A, Япония) в естественных условиях и условиях циклоплегии (циклопентолат 1%), рассчитывали величину привычного тонуса аккомодации (ПТА). С помощью авторефрактометра открытого поля (ОП) (Grand Seiko WAM-5500, Япония) объективно оценивали центральную рефракцию ОП, периферическую рефракцию, бинокулярный и монокулярный аккомодационный ответ (БАО, МАО). Определяли величину ПТА-ОП. Объем абсолютной аккомодации (амплитуду аккомодации, АА), рефракцию в ближайшей точке ясного зрения (punctum proximum, PP) и дальнейшей точке ясного зрения (punctum remotum, PR) измеряли объективно с использованием прибора Tonoref III (Nidek, Япония). Этим же прибором объективно измеряли диаметр зрачка. Запасы относительной аккомодации (ЗОА) исследовали с помощью печатной таблицы. ТХ измеряли прибором ОКТ Mirante (Nidek, Япония) с применением протокола сканирования Macula radial в режиме Choroidal. ТХ определяли как расстояние между пигментным эпителием сетчатки и мембраной Бруха с получением карты ТХ диаметром 6 мм в соответствии с таблицей ETDRS (Early Treatment of Diabetic Retinopathy Study). В исследовании использовали центральную зону диаметром 1 мм, что является средним значением ТХ по всем сканам.
Результаты
Острота зрения в очках
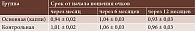
Через шесть месяцев от начала ношения очков с микролинзами, формирующими градиентный миопический дефокус, монокулярная острота зрения в очках несколько увеличилась по сравнению с исходными значениями в обеих группах: достоверно в основной группе (р < 0,01), недостоверно – в контрольной (р > 0,1). Через 12 месяцев острота зрения в основной группе (капли) приблизилась к исходным значениям, в контрольной – несколько снизилась относительно исходных (табл. 1).
Рефракция и длина переднезадней оси
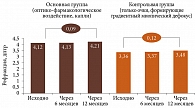
Исходные значения сферэквивалента (СЭ) рефракции, измеренной методом авторефрактометрии в условиях циклоплегии (циклопентолат 1%), составили -4,12 ± 0,22 дптр в основной группе и -3,36 ± 0,33 дптр – в контрольной. Через шесть месяцев от начала ношения очков рефракция в обеих группах не изменилась. Через 12 месяцев рефракция незначительно усилилась в обеих группах: на 0,09 ± 0,04 дптр в основной группе (капли) и на 0,12 ± 0,07 дптр – в контрольной (рис. 1, табл. 2). Разница недостоверна (р > 0,7). Усиление рефракции в течение шести и 12 месяцев наблюдения оказалось несколько меньше, чем в предыдущих исследованиях по оценке стабилизирующего влияния очков с микролинзами на миопию, когда через шесть месяцев наблюдения рефракция усилилась на 0,11 ± 0,04 дптр, а через 12 месяцев – на 0,19 ± 0,07 дптр [18]. Разница с группой капель особенно заметна.
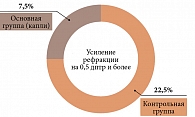
Усиление циклоплегической рефракции на 0,5 дптр и более в группе капель наблюдали в 7,5% случаев (максимальное усиление в течение срока наблюдения – 0,63 дптр). В контрольной группе усиление рефракции на 0,5 дптр и более наблюдали в 22,5% случаев (максимальное усиление – 1,0 дптр) (рис. 2).
Изменение длины переднезадней оси (ПЗО) соответствовало изменениям циклоплегической рефракции (табл. 2).
Аккомодация
Сразу после начала ношения очков ПТА, измеренный с помощью авторефрактометра, ожидаемо повысился и оставался стабильным в течение всего срока наблюдения в обеих группах (табл. 3).
Исходный тонус покоя аккомодации (ТПА), измеренный в темноте, имел отрицательное значение (рефракция в условиях безориентирного пространства сильнее циклоплегической) и составил исходно (начало наблюдения) -0,48 ± 0,08 дптр в основной группе (капли) и -0,63 ± 0,08 дптр – в контрольной. Через шесть месяцев ТПА несколько усилился в обеих группах, а через 12 месяцев приблизился к исходным значениям (табл. 3).
Особое значение имеет ПТА-ОП, который исходно в основной группе составлял -0,17 ± 0,04 дптр, в контрольной – 0,19 ± 0,06 дптр, через месяц ношения очков – -0,13 ± 0,06 и -0,22 ± 0,09 дптр соответственно. Разница значений ПТА-ОП в двух группах, получавших на этом этапе одинаковое воздействие (только очки), объясняется тем, что через месяц от начала ношения очков в основной группе (капли) было выявлено пять случаев ПТА-ОП в 0,5 дптр и более, в то время как в контрольной группе – восемь. После месяца закапывания капель средний ПТА-ОП (основная группа) уменьшился до положительного значения 0,01 ± 0,04 дптр, что сопровождалось повышением остроты зрения в очках до 1,05 [16]. Через шесть и 12 месяцев значения ПТА-ОП оставались близкими к исходным (табл. 3).
В случаях, когда ПТА-ОП через месяц от начала ношения очков, соответствовавших рефракции, был 0,5 дптр и выше, в основной группе (капли) рефракция через шесть месяцев оставалась стабильной. Через 12 месяцев в основной группе выявлена тенденция к ослаблению рефракции, разница с исходными значениями через 12 месяцев составила -0,12 ± 0,09 дптр. В контрольной группе в таких случаях отмечалась устойчивая тенденция к усилению рефракции. Разница с исходными значениями через 12 месяцев составила 0,54 ± 0,07 дптр (рис. 3).
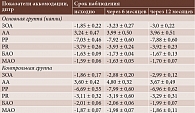
За период наблюдения выявлено клинически значимое, достоверное (p < 0,01) и одинаковое увеличение ЗОА в обеих группах. Напомним, что нормальные значения ЗОА в возрасте 5–9 лет составляют 2,0–4,0 дптр, в возрасте 10–14 лет – 3,0–5,0 дптр [19]. Исходно ЗОА был ниже возрастных нормальных значений в обеих группах. К концу наблюдения ЗОА повысился до минимальных нормальных возрастных значений. Объективный БАО и МАО, измеренный с расстояния 33 см, исходно был ниже нормальных расчетных значений и в течение срока наблюдения незначительно изменился. Объем АА измеряли объективно. В течение периода наблюдения отмечалась тенденция к увеличению АА за счет приближения к глазу ближайшей точки ясного зрения. Тенденция была наиболее выраженной в основной группе (капли) (табл. 4).
Диаметр зрачка
Типичных для какой-либо группы изменений диаметра зрачка не выявлено. Отмечалась лишь общая для обеих групп тенденция к незначительному увеличению диаметра зрачка в период наблюдения. В основной группе (капли) исходно средний диаметр зрачка составил 5,96 ± 0,21 мм, через шесть месяцев – 6,11 ± 0,14 мм, через 12 месяцев – 6,31 ± 0,15 мм, в контрольной группе – 5,93 ± 0,16, 5,92 ± 0,31 и 6,17 ± 0,14 мм соответственно.
Толщина хориоидеи
В основной группе (капли) исходно средняя величина ТХ составила 256 ± 11,5 мкм, после ношения очков в течение месяца – 265 ± 11,2 мкм, по окончании первого курса капель – 268 ± 12,8 мкм. Впоследствии ТХ оставалась стабильной. За 12-месячный период наблюдалось увеличение ТХ на 12 мкм, или 4,7% исходного значения.
В контрольной группе исходно средняя величина ТХ составила 281 ± 8,7 мкм, после ношения очков в течение месяца – 292 ± 9,6 мкм, через 12 месяцев уменьшилась до 287 ± 10,6 мкм. За период наблюдения в контрольной группе отмечалось увеличение ТХ на 6 мкм, или 2,1% исходного значения.
Согласно данным литературы, увеличение ТХ в ходе лечения прогрессирующей миопии (на фоне коррекции с помощью ортокератологических линз) может достигать 21 мкм [20]. Половина этой величины была достигнута за период наблюдения в основной группе (капли). И хотя увеличение ТХ оказалось недостоверным в обеих группах, а разница между группами незначительной, полагаем, что этот факт заслуживает особого внимания и изучения.
Заключение
За 12-месячный период наблюдения в обеих группах отмечались увеличение ЗОА до минимальных нормальных возрастных значений и стабилизация рефракции, более выраженная в группе оптико-фармакологического воздействия (капли).
В группе оптико-фармакологического воздействия выявлена тенденция к увеличению АА, которое в основном было обусловлено приближением к глазу ближайшей точки ясного зрения.
В группе оптико-фармакологического лечения отмечалось ослабление ПТА-ОП до нулевых значений после первого курса инстилляций препарата Мидримакс®.
Оптико-фармакологическое воздействие ассоциировалось с выраженным стабилизирующим влиянием на динамику рефракции у детей с миопией в случаях повышения ПТА-ОП до 0,5 дптр и более (на фоне ношения очков с коррекцией, соответствовавшей рефракции). В контрольной группе в таких случаях отмечалась устойчивая и клинически значимая тенденция к усилению рефракции.
Выявленное более значительное и стабильное увеличение ТХ при оптико-фармакологическом лечении по сравнению с оптическим воздействием требует особого изучения.
Оптико-фармакологическое лечение целесообразно назначать детям с миопией при выявлении признаков сопутствующего ей привычно-избыточного напряжения аккомодации. Такое лечение должно применяться в целях нормализации ослабленной аккомодационной способности миопических глаз и профилактики прогрессирования миопии.
Исследование в очередной раз подтвердило описанные в Клинических рекомендациях «Миопия» обоснованность и эффективность применения комбинации фенилэфрина и тропикамида (Мидримакс®) в комплексном лечении близорукости наряду с оптической коррекцией и функциональным лечением.
Ye.P. Tarutta, PhD, Prof.1, O.V. Proskurina, PhD, Prof.1, 2, N.A. Tarasova, PhD1, S.G. Arutyunyan1, 2, G.A. Markosyan1, S.V. Milash, PhD1
Helmholtz National Medical Research Center of Eye Diseases
Russian University of Medicine
Contact person: Olga V. Proskurina, proskourina@mail.ru
Sympathomimetics and anticholinergic agents and their combinations have an effect on dynamic refraction and refractogenesis of myopic eyes. This effect is noticeable even in children using lens designs to decrease peripheral hyperopic retinal defocus or invert hyperopic defocus into myopic defocus.
Purpose to evaluate the effect of combined opto-pharmacological treatment on the dynamics of refraction, accommodation, visual functions and choroidal thickness in children with progressive myopia in comparison with optical exposure.
Material and methods. 40 children aged 8 to 13 (average 10.5) years with myopia from 1.75 to 6.37 D (average 3.98) were examined. All children were assigned new spectacle lenses with aspherical lenslets. After 1 month of wearing new glasses, the children were randomly assigned to 2 groups. The group using opto-pharmacological treatment (drop group) consisted 20 children who were prescribed Midrimax eye drops once a day at night for 1 month, in courses of 4 courses per year. 20 children used only optical exposure (control group). All children of both groups were examined before the appointment of new glasses and after 1, 6 and 12 months. Visual acuity in glasses, SER, AL, accommodation, pupil diameter, and choroidal thickness were studied.
Results. Visual acuity in glasses remained stable in both groups during the follow-up. After 12 months, refraction increased slightly in both groups: by 0.09 ± 0.04 D in the droplet group and by 0.12 ± 0.07 D in the control group. An increase in refraction by 0.5 D or more was observed in 7.5% in the drop group and in 22.5% in the control group. In cases where the open field accommodative tonus was 0.5 D or more while wearing glasses with full correction, refraction decreased by 0.12 ± 0.09 D after 12 months of follow-up in the droplet group, and refraction increased by 0.54 ± 0.07 D in the control group. PRA increased to the minimum normal values in both groups. Pupil diameter tended to increase in both groups. Choroidal thickness in the drop group increased by 12 microns from the initial values, in the control group by 6 microns.
Conclusion. During the 12-month follow-up period, refraction stabilization and an increase in PRA to the minimum normal values were noted in both observation groups. The opto-pharmacological effect had a stabilizing effect in cases of an increase in open field accommodative tonus to 0.5 D or higher. In such cases, the control group showed a steady tendency to increase refraction. The revealed greater and stable increase in choroidal thickness during opto-pharmacological treatment compared with optical exposure requires special study. The appointment of opto-pharmacological treatment is advisable when identifying signs of concomitant myopia of habitual excessive tension of accommodation.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.