Оценка результатов хирургического лечения пациентов с катарактой и глаукомой методом оптической когерентной томографии
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследование было включено 82 пациента (35 мужчин и 47 женщин) с осложненной катарактой и первичной открытоугольной глаукомой, которым выполнялась одномоментная комбинированная операция с имплантацией дренажа по запатентованной методике (патент РФ № 2726457 от 14.07.2020). Пациенты в возрасте 49–78 лет были разделены на две группы: с имплантацией дренажа «Репегель А-1» (n = 39) и с имплантацией дренажа «Ксенопласт» (n = 43).
Результаты. Интраоперационный период у всех пациентов протекал без значимых осложнений. В раннем послеоперационном периоде гифема передней камеры развилась у 1 (2,6%) пациента первой группы и 2 (4,8%) пациентов второй группы. Десцеметит отмечался у пяти пациентов с дренажем «Репегель А-1» и шести – с дренажем «Ксенопласт». Через два года после операции зафиксировано достоверное снижение внутриглазного давления: в первой группе до 18,8 ± 0,9 мм рт. ст., во второй – до 19,2 ± 1,1 мм рт. ст. (p < 0,01). Некорригированная острота зрения составила 0,51 ± 0,08 и 0,57 ± 0,1, максимальная корригированная острота зрения – 0,6 ± 0,1 и 0,7 ± 0,09 соответственно (p < 0,001). ОКТ-контроль показал наличие гипорефлективных кистозных полостей в конъюнктиве, что свидетельствовало о фильтрационной активности путей оттока. Положение дренажей в структурах переднего сегмента глаза также отслеживали с помощью ОКТ. У дренажа «Репегель А-1» дистальный конец располагался дальше от роговицы (963 ± 27 мкм) и радужки (941 ± 18 мкм), чем у дренажа «Ксенопласт» (396 ± 32 и 241 ± 29 мкм соответственно). Контакт дренажа с эндотелием роговицы выявлен у 2 (5,1%) пациентов первой группы и 3 (7,1%) пациентов второй, но признаков эндотелиальной дистрофии за весь период наблюдения не зафиксировано. По данным кератопахиметрии, установлена зависимость выраженности отека роговицы от плотности хрусталика. Наибольшая толщина роговицы в раннем послеоперационном периоде зарегистрирована у пациентов с плотностью хрусталика NC 6 по шкале LOCS III: на первые сутки – 636 ± 19 мкм в первой группе и 641 ± 16 мкм во второй с постепенным снижением в течение двух месяцев к исходным значениям.
Заключение. ОКТ переднего отрезка глаза – важный инструмент послеоперационного контроля у пациентов с катарактой и глаукомой. Она позволяет точно оценить положение дренажа, его проксимального и дистального отделов, а также выявить контакт с окружающими структурами. Обнаружение гипорефлективных кистозных полостей в конъюнктиве свидетельствует о функционировании путей оттока внутриглазной жидкости. Данные кератопахиметрии помогают отслеживать восстановление роговицы после ультразвукового воздействия.
Материал и методы. В исследование было включено 82 пациента (35 мужчин и 47 женщин) с осложненной катарактой и первичной открытоугольной глаукомой, которым выполнялась одномоментная комбинированная операция с имплантацией дренажа по запатентованной методике (патент РФ № 2726457 от 14.07.2020). Пациенты в возрасте 49–78 лет были разделены на две группы: с имплантацией дренажа «Репегель А-1» (n = 39) и с имплантацией дренажа «Ксенопласт» (n = 43).
Результаты. Интраоперационный период у всех пациентов протекал без значимых осложнений. В раннем послеоперационном периоде гифема передней камеры развилась у 1 (2,6%) пациента первой группы и 2 (4,8%) пациентов второй группы. Десцеметит отмечался у пяти пациентов с дренажем «Репегель А-1» и шести – с дренажем «Ксенопласт». Через два года после операции зафиксировано достоверное снижение внутриглазного давления: в первой группе до 18,8 ± 0,9 мм рт. ст., во второй – до 19,2 ± 1,1 мм рт. ст. (p < 0,01). Некорригированная острота зрения составила 0,51 ± 0,08 и 0,57 ± 0,1, максимальная корригированная острота зрения – 0,6 ± 0,1 и 0,7 ± 0,09 соответственно (p < 0,001). ОКТ-контроль показал наличие гипорефлективных кистозных полостей в конъюнктиве, что свидетельствовало о фильтрационной активности путей оттока. Положение дренажей в структурах переднего сегмента глаза также отслеживали с помощью ОКТ. У дренажа «Репегель А-1» дистальный конец располагался дальше от роговицы (963 ± 27 мкм) и радужки (941 ± 18 мкм), чем у дренажа «Ксенопласт» (396 ± 32 и 241 ± 29 мкм соответственно). Контакт дренажа с эндотелием роговицы выявлен у 2 (5,1%) пациентов первой группы и 3 (7,1%) пациентов второй, но признаков эндотелиальной дистрофии за весь период наблюдения не зафиксировано. По данным кератопахиметрии, установлена зависимость выраженности отека роговицы от плотности хрусталика. Наибольшая толщина роговицы в раннем послеоперационном периоде зарегистрирована у пациентов с плотностью хрусталика NC 6 по шкале LOCS III: на первые сутки – 636 ± 19 мкм в первой группе и 641 ± 16 мкм во второй с постепенным снижением в течение двух месяцев к исходным значениям.
Заключение. ОКТ переднего отрезка глаза – важный инструмент послеоперационного контроля у пациентов с катарактой и глаукомой. Она позволяет точно оценить положение дренажа, его проксимального и дистального отделов, а также выявить контакт с окружающими структурами. Обнаружение гипорефлективных кистозных полостей в конъюнктиве свидетельствует о функционировании путей оттока внутриглазной жидкости. Данные кератопахиметрии помогают отслеживать восстановление роговицы после ультразвукового воздействия.





Введение
Оптическая когерентная томография (ОКТ) является безопасным и бесконтактным методом визуализации тканей глаза, позволяет получить результат в режиме реального времени и провести количественную и качественную оценку структур [1, 2]. Особую популярность приобретает исследование анатомических особенностей фильтрационной зоны после антиглаукомной операции [3–5]. С помощью ОКТ можно анализировать длину и высоту фильтрационной подушки, толщину и рефлективность ее стенки, проводить морфометрию трабекулярной сети, шлеммова канала, склеральной шпоры, трабекулярно-десцеметовой мембраны, измерять толщину склерального лоскута и интрасклерального пространства, визуализировать местоположение антиглаукомного дренажа, а также его смещение, диагностировать плоскую отслойку цилиарного тела [6–11]. Мониторинг фильтрационной зоны после гипотензивной операции помогает установить активность сформированных путей оттока, выявить показания к повторному хирургическому лечению и сформулировать оперативную тактику (реактивация фильтрационной зоны, ревизия антиглаукомного дренажного устройства, нидлинг) [12].
Таким образом, использование ОКТ переднего отрезка глаза после антиглаукомных операций с имплантацией дренажей, в том числе сочетанных с факоэмульсификацией, является неотъемлемой диагностической составляющей послеоперационного наблюдения пациентов с осложненной катарактой и глаукомой.
Цель – оценить с помощью ОКТ анатомо-топографические параметры переднего отрезка глаза пациентов с осложненной катарактой и глаукомой после хирургического лечения.
Материал и методы
В исследование было включено 82 пациента (35 (42,7%) мужчин и 47 (57,3%) женщин) с осложненной катарактой и первичной открытоугольной глаукомой, которым выполнялась одномоментная комбинированная операция катаракты и некомпенсированной глаукомы с имплантацией дренажа по разработанной методике (патент РФ на изобретение № 2726457 от 14.07.2020). Возраст больных составил 49–78 лет. Все пациенты были разделены на две группы: 39 пациентам первой группы имплантировали дренаж «Репегель А-1», 43 пациентам второй – дренаж «Ксенопласт».
В таблице 1 представлена характеристика пациентов обеих групп с указанием остроты зрения, уровня внутриглазного давления, стадии развития глаукомы, плотности хрусталика по классификации LOCS III (The Lens Opacities Classification System III). Всем пациентам перед оперативным вмешательством проводили обследование в объеме визометрии, биомикроскопии, гониоскопии, офтальмоскопии, периметрии, тонометрии (по Маклакову), пахиметрии, офтальмометрии, альфа-сканирования, ОКТ переднего отрезка глаза (фильтрационной зоны, угла передней камеры, толщины роговицы).
Кератопахиметрия выполнялась на оптическом когерентном томографе Optovue RTVue XR Avanti (США, 2019) с дополнительной насадкой CAM (Cornea Anterior Module) для исследования структур переднего отдела глаза. При этом использовался тип сканирования Cornea Pachymetry и Cornea PachymetryWide. С помощью данной насадки также выполнялось сканирование фильтрационной подушки и расположение дренажа в интрасклеральном тоннеле после антиглаукомной операции с использованием типа сканирования Cornea Line и Cornea Cross Line. При исследовании ширины угла передней камеры применяли тип сканирования Cornea Angle, для оценки расположения в углу передней камеры дренажа «Репегель А-1» или «Ксенопласт» – тот же тип сканирования.
Кандидатами на хирургическое лечение были пациенты с некомпенсированным внутриглазным давлением, которые применяли различные гипотензивные лекарственные комбинации, включая неселективные блокаторы бета-2-адренорецепторов, ингибиторы карбоангидразы и аналоги простагландина.
Для усиления гипотензивного эффекта антиглаукомного компонента сочетанной операции использовались различные по материалу и размеру дренажи «Репегель А-1» и «Ксенопласт». Дренаж «Репегель А-1» представляет собой прямоугольную пластину с закругленными краями длиной 6,0 мм, шириной 4,0 мм, толщиной 0,1 мм с 96 отверстиями размером 0,25 мм. «Ксенопласт» – нерастворимый пористый коллаген, выделенный из костной ткани сельскохозяйственных животных, размером 4,0 × 1,5 × 0,5–0,8 мм. Данный имплантат эластичен, не рассасывается, не обладает токсичностью, иммуногенностью.
Техника операции
Длина основного тоннеля рассчитывается в зависимости от размера применяемого дренажа («Репегель А-1» – 6,0 мм, «Ксенопласт» – 4,0 мм). При использовании дренажа «Репегель А-1» в 4,0 мм от лимба (для дренажа «Ксенопласт» – в 3,0 мм от лимба) на 11 часах склеротомом шириной 2,2 мм через конъюнктиву в переднезаднем направлении формируются интрасклеральный тоннель в поверхностных слоях склеры с выходом ножа через дренажный угол в переднюю камеру и два лимбальных парацентеза диаметром 1,0 мм. Затем проводятся круговой капсулорексис при наполненной вискоэластиком передней камере и гидродиссекция. С помощью ультразвука выполняются разлом и аспирация ядра хрусталика; аспирационно-ирригационной системой удаляется кортекс и отполировывается задняя капсула хрусталика. Склеральный тоннель расширяется до 3 мм. Через него при помощи инжектора имплантируется эластичная интраокулярная линза в наполненный вискоэластиком капсульный мешок. Цанговым пинцетом через парацентез и ножницами через склеральный тоннель формируется сквозная базальная колобома радужки. Глубокий лоскут основания склерального тоннеля отделяется шпателем от плоской части цилиарного тела, затем полностью удаляется вместе с трабекулярным аппаратом. В результате обнажается плоская часть цилиарного тела с активацией увеосклерального оттока. Перед имплантацией дренажа «Репегель А-1» предварительно из него моделируется Т-образная форма за счет удаления боковых частей. Дренаж «Ксенопласт» применяется без коррекции формы и размеров. Далее любой из предложенных дренажей имплантируется в интрасклеральный тоннель следующим образом: один конец направляется в переднюю камеру над коломбой радужки, другой выводится из склерального тоннеля в субконъюнктивальное пространство. На конъюнктиву накладывается непрерывный шов 10/0, выполняются гидратация парацентезов и инстилляция антибиотика.
Статистическая обработка полученных данных проводилась с использованием лицензионного программного обеспечения Statistica v. 8.0 (StatSoft Inc., США). Параметры с нормальным распределением представлены в формате М ± m, где М – среднее значение, m – стандартная ошибка среднего.
Результаты
У всех пациентов интраоперационный период протекал без значимых осложнений. Из эпиретинальных сосудов через интрасклеральный тоннель формировалась гифема передней камеры у 1 (2,6%) пациента первой группы и двух (4,8%) пациентов второй. Данное геморрагическое осложнение разрешилось в течение пяти дней послеоперационного периода. В ранние сроки после операции десцеметит наблюдался у пяти больных с дренажем «Репегель А-1» и шести пациентов с дренажем «Ксенопласт». В таблице 2 представлены результаты зрительных функций и уровня внутриглазного давления через два года после сочетанной комбинированной операции катаракты и глаукомы.
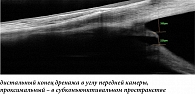
При изучении фильтрационной зоны с помощью ОКТ выявлены гипорефлективные кистообразные полости в толще конъюнктивы (рис. 1), что говорит о фильтрационной способности сформированных путей оттока внутриглазной жидкости. Визуализация проксимального отдела дренажа на снимках ОКТ (рис. 1) позволяет определить его положение в структуре склеро-конъюнктивального пространства, а также проследить в динамике тенденцию к дислокации или прорезыванию конъюнктивы.
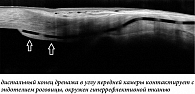
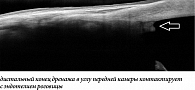
Иллюстрация дистального отдела дренажа в углу передней камеры позволяет определить длину выхода дренажа из склеральной фистулы и его положение по отношению к роговице и радужке (табл. 2). За счет большей длины и плоской формы дренажа «Репегель А-1» его дистальный конец глубже проникает в полость передней камеры (рис. 2) и располагается в отдалении от соседних структур (963 ± 27 мкм от роговицы, 941 ± 18 мкм от радужки) в отличие от дренажа «Ксенопласт» (рис. 3) (396 ± 32 мкм от роговицы, 241 ± 29 мкм от радужки).
У 2 (5,1%) пациентов с дренажем «Репегель А-1» на снимках ОКТ выявлен контакт дистального отдела с эндотелием роговицы с гиперрефлективным тканным отграничением дренажа в месте соприкосновения (рис. 4). У 3 (7,1%) пациентов с дренажем «Ксенопласт» наблюдался контакт дистального отдела с эндотелием роговицы, но с меньшей площадью, чем в случае дренажа «Репегель А-1» (рис. 5). За весь срок наблюдения признаков эндотелиальной дистрофии роговицы не выявлено.
Кератопахиметрия с помощью ОКТ показала зависимость между отеком роговицы и плотностью хрусталика (табл. 3). В течение первого месяца наблюдения наибольшая толщина роговицы определена у пациентов обеих групп с плотностью хрусталика NC 6. Можно предположить, что длительность ирригационного потока BSS и продолжительность работы ультразвука для дробления плотного хрусталика у этих больных вызвали больший отек роговицы по сравнению с пациентами с плотностью хрусталика NC 1–5.
Заключение
ОКТ переднего отрезка глаза играет значимую роль в послеоперационном наблюдении пациентов с катарактой и глаукомой. Визуализация дренажа на снимках ОКТ позволяет выявить его положение, локализацию проксимального и дистального отделов, контакт края дренажа с близлежащими структурами. Наличие кистозных гипорефлективных полостей в толще конъюнктивы указывает на фильтрационную активность сформированных путей оттока внутриглазной жидкости. Результаты кератопахиметрии позволяют определить этап восстановления роговицы после воздействия ультразвука.
Прозрачность финансовой деятельности. Никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Ye.A. Ivachev, PhD, A.I. Fedorova, I.A. Loskutov, PhD
Clinical Hospital ‘Russian-Railroads-Medicine’, Penza
Penza State University
M.F. Vladimirsky Moscow Regional Scientific Research Clinical Institute
Contact person: Anastasiya I. Fedorova, FedorovaAnastasyaIg@yandex.ru
The aim is to evaluate the anatomical and topographic parameters of the anterior segment of the eye of patients with complicated cataracts and glaucoma after surgical treatment using optical coherence tomography (OCT).
Material and methods. The study included 82 patients (35 men and 47 women) with complicated cataracts and primary open-angle glaucoma who underwent simultaneous combined surgery with drainage implantation using a patented technique (RF Patent № 2726457 dated 07/14/2020). Patients aged 49–78 years were divided into two groups: those with Repegel A-1 drainage implantation (n = 39) and those with Xenoplast drainage implantation (n = 43).
Results. The intraoperative period in all patients proceeded without significant complications. In the early postoperative period, hyphema of the anterior chamber developed in 1 (2.6%) patient of the first group and 2 (4.8%) patients of the second group. Descemetitis was observed in five patients with Repegel A-1 drainage and six with Xenoplast drainage. Two years after the operation, a significant decrease in intraocular pressure was recorded: in the first group to 18.8 ± 0.9 mmHg, in the second to 19.2 ± 1.1 mmHg (p < 0.01). Uncorrected visual acuity was 0.51 ± 0.08 and 0.57 ± 0.1, and maximum corrected visual acuity was 0.6 ± 0.1 and 0.7 ± 0.09, respectively (p < 0.001). OCT control showed the presence of hyporeflective cystic cavities in the conjunctiva, which indicated the filtration activity of the outflow pathways. The position of the drains in the structures of the anterior segment of the eye was also monitored using OCT. The distal end of the Repegel A-1 drainage was located further from the cornea (963 ± 27 microns) and the iris (941 ± 18 microns) than the Xenoplast drainage (396 ± 32 and 241 ± 29 microns, respectively). Drainage contact with the corneal endothelium was detected in 2 (5.1%) patients of the first group and 3 (7.1%) patients of the second, but no signs of endothelial dystrophy were recorded during the entire follow-up period. According to keratopachimetry data, the dependence of the severity of corneal edema on the density of the lens has been established. The greatest corneal thickness in the early postoperative period was recorded in patients with a lens density of NC 6 on the LOCS III scale: on the first day – 636 ± 19 microns in the first group and 641 ± 16 microns in the second, with a gradual decrease over two months to baseline values.
Conclusion. OCT of the anterior segment of the eye is an important tool for postoperative control in patients with cataracts and glaucoma. It allows you to accurately assess the position of the drainage, its proximal and distal sections, as well as identify contact with surrounding structures. The detection of hyporeflective cystic cavities in the conjunctiva indicates the functioning of the outflow pathways of intraocular fluid. Keratopachimetry data allows you to track the restoration of the cornea after ultrasound exposure.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.