Семейный случай ретинальных капиллярных ангиом при синдроме Гиппеля – Линдау
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Лечение назначалось трем пациентам из одной семьи (отец, сын и дочь) с диагностированными у них РКА, ассоциированными с СГЛ. Использовались лазерная коагуляция, криодеструкция, транспупиллярная термотерапия и эндорезекция.
Результаты. У всех пациентов выявлены стабилизация остроты зрения и регрессия опухолей. Комбинированные методы лечения эффективно контролировали рост опухолей и устраняли осложнения, в частности экссудативную отслойку сетчатки.
Заключение. Комплексный подход к лечению РКА при СГЛ эффективен. Раннее выявление и своевременное лечение позволяют сохранить зрение.
Материал и методы. Лечение назначалось трем пациентам из одной семьи (отец, сын и дочь) с диагностированными у них РКА, ассоциированными с СГЛ. Использовались лазерная коагуляция, криодеструкция, транспупиллярная термотерапия и эндорезекция.
Результаты. У всех пациентов выявлены стабилизация остроты зрения и регрессия опухолей. Комбинированные методы лечения эффективно контролировали рост опухолей и устраняли осложнения, в частности экссудативную отслойку сетчатки.
Заключение. Комплексный подход к лечению РКА при СГЛ эффективен. Раннее выявление и своевременное лечение позволяют сохранить зрение.
Введение
Синдром Гиппеля – Линдау (СГЛ) – редкое аутосомно-доминантное заболевание, обусловленное мутацией гена VHL на коротком плече третьей хромосомы (3p25–26), ассоциированное с развитием сосудистых и солидных опухолей различных органов, в том числе сетчатки, мозжечка, спинного мозга, надпочечников, почек и поджелудочной железы [1, 2]. Ретинальные капиллярные ангиомы (РКА) считаются одними из первых и наиболее частых проявлений СГЛ, обнаруживаются у 49–85% пациентов [3, 4] и нередко диагностируются задолго до возникновения системных признаков заболевания.
Несмотря на достижения в диагностике и лечении, выбор оптимальной тактики ведения пациентов остается сложной задачей. Основными методами лечения являются транспупиллярная термотерапия, криодеструкция, эндорезекция опухоли [5]. Представляем клинический случай семейного поражения сетчатки при СГЛ с анализом применяемых методов лечения и их эффективности в предотвращении прогрессирования заболевания.
Материал и методы
В исследование были включены три пациента с генетически подтвержденным СГЛ – члены одной семьи: отец (36 лет), дочь (12 лет) и сын (10 лет). Все пациенты прошли генетическое тестирование, подтвердившее наличие мутации гена VHL. У всех пациентов имело место двустороннее поражение сетчатки. Таким образом, проанализировано шесть глаз, десять опухолевых очагов, выявленных на сетчатке.
Методы диагностики
Все пациенты прошли стандартное офтальмологическое обследование, включая визометрию, офтальмоскопию, оптическую когерентную томографию и ультразвуковую диагностику глазного яблока. Данные методы позволили точно определить локализацию и размеры ангиом, наличие экссудации, изменение диаметра и извитости питающих сосудов, а также остроту зрения.
Методы лечения
Транспупиллярная термотерапия (ТТТ) применялась при небольших РКА (высотой до 2–2,5 мм). Лечение проводилось с использованием комбинации лазеров с длиной волны 577 и 810 нм. Параметры лазерного излучения: мощность – 100–550 мВт (среднее значение – 210 мВт), экспозиция – от 5 до 20 с для лазера с длиной волны 577 нм и 5–30 с для лазера с длиной волны 810 нм, диаметр пятна – от 300 до 1000 мкм.
Лазерная коагуляция сетчатки (ЛКС) использовалась для формирования барьера в секторе сетчатки с ангиомой с целью профилактики распространения отслойки сетчатки в центральную область перед криодеструкцией. Лечение проводилось с использованием лазера с длиной волны 577 нм. Параметры лазерного излучения: мощность – 120 мВт, экспозиция – 0,08 с, диаметр пятна – 200 мкм.
Криодеструкция (КД) использовалась при опухолях высотой более 2,5 мм. КД проводилась по стандартной технологии «замораживание – оттаивание» до образования ледяной сферы с вовлечением верхушки ангиомы и преретинальных отделов стекловидного тела с двукратной криоаппликацией продолжительностью 45–60 с. В качестве хладагента во всех случаях использовалась углекислота.
Эндорезекция внутриглазных новообразований осуществлялась в сочетании с микроинвазивной витрэктомией по стандартной трехпортовой технологии с проведением эндолазеркоагуляции вокруг зон ретинотомии, мембранопилинга и тампонадой силиконовым маслом при выявлении крупных опухолевых узлов (около 4,0 мм) и наличии сопутствующих осложнений, повлекших грубые изменения сетчатки, в частности отслойку и эпиретинальный фиброз.
Критерии оценки эффективности лечения
Эффективность лечения оценивали по следующим критериям:
- регрессия опухоли (или частичная);
- отсутствие экссудации;
- стабилизация или полная улучшение зрительных функций;
- состояние питающих сосудов (калибр и извитость).
Результаты
Пациент 1 (дочь)
Пациентка, 12 лет, жалобы на снижение остроты зрения правого глаза. У девочки генетически подтвержден СГЛ (VHL). При офтальмологическом обследовании выявлено наличие трех РКА: две на левом глазу, одна на правом. По данным визометрии, острота зрения составила: правый глаз (OD) – 0,2 (неизменна), левый (OS) – 1 (неизменна).
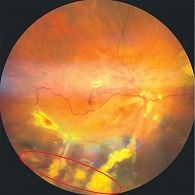
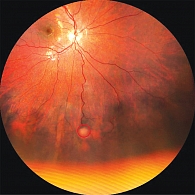
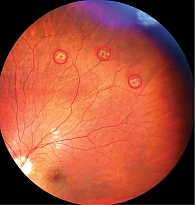
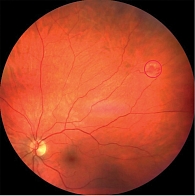
OD, средняя периферия, нижнетемпоральный сектор. В нижневисочном секторе средней периферии сетчатки правого глаза выявлена капиллярная ангиома размером 4,0 × 7,5 мм. Очаг сопровождался выраженной экссудацией, извитостью питающих сосудов и локальной отслойкой сетчатки в проекции новообразования (рис. 1).
С учетом осложненного течения и размера опухоли выполнено комбинированное хирургическое лечение: микроинвазивная витрэктомия с введением силиконового масла и эндорезекция новообразования. В профилактических целях одновременно проведена факоэмульсификация хрусталика с имплантацией интраокулярной линзы (ИОЛ) с учетом риска помутнения хрусталика в условиях силиконовой тампонады.
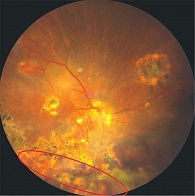
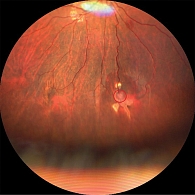
В ходе операции опухоль полностью удалена, выполнена эффективная тампонада зоны локальной отслойки сетчатки. Установленная ИОЛ обеспечила сохранение прозрачности оптических сред и стабильность анатомических структур переднего сегмента (рис. 2).
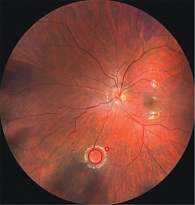
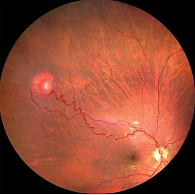
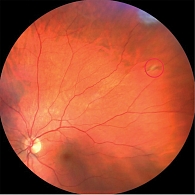
OS, средняя периферия, нижненазальный сектор. На левом глазу в нижненосовом секторе средней периферии обнаружена капиллярная ангиома размером 1,6 × 2,7 мм. Клинически очаг характеризовался умеренной экссудацией и расширением питающих сосудов. С учетом размера и ангиографических особенностей в качестве метода лечения выбрана ТТТ (рис. 3).
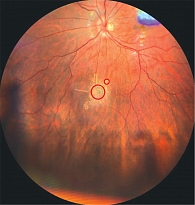
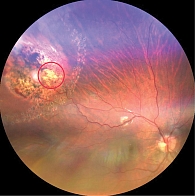
В послеоперационном периоде зафиксированы полная регрессия опухоли, уменьшение калибра питающих сосудов и полное разрешение экссудативных проявлений. Размер образования уменьшился до 1,0 × 2,3 мм (рис. 4).
OS, средняя периферия, нижненазальный сектор. Вблизи предыдущего очага в том же секторе выявлена еще одна ангиома небольшого размера – 0,8 × 1,1 мм, также сопровождавшаяся экссудацией. Пациентке проведена ТТТ.
В ходе динамического наблюдения зарегистрирована стабильная положительная динамика: полная регрессия опухолевой ткани, отсутствие признаков экссудации. Размер очага уменьшился до 0,3 × 0,5 мм.
Пациент 2 (сын)
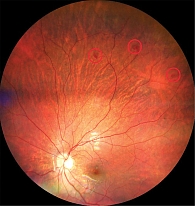
Пациент, 10 лет, активных жалоб не предъявлял, заболевание диагностировано в ходе семейного обследования после выявления патологии у пациента 1. Подтвержден синдром СГЛ. При офтальмологическом обследовании выявлено пять РКА (две на правом глазу, три на левом). Острота зрения стабильна: OD – 0,8, OS – 0,9 (до и после лечения неизменна) (рис. 5).
OD, крайняя периферия, нижнетемпоральный сектор. В нижнетемпоральном секторе крайней периферии сетчатки правого глаза выявлена ангиома размером 1,87 × 2,35 мм с признаками экссудации и питающими сосудами. Проведена ТТТ, в результате которой опухоль уменьшилась до 1,3 × 1,5 мм. На данном этапе лечение не завершено, требуется повторное проведение ТТТ через три месяца после последнего сеанса (рис. 6).
OD, крайняя периферия, верхнетемпоральный сектор. Обнаружена ангиома размером 2,5 × 3,2 мм с выраженной экссудацией и увеличенными извитыми питающими сосудами (рис. 7). В качестве метода лечения применена ограничительная ЛКС по периметру очага с последующим сеансом КД. Через месяц после лечения зафиксированы регрессия опухоли (до 1,5 × 2,24 мм), полное разрешение экссудативного компонента и достоверное снижение калибра и извитости питающих сосудов (рис. 8).
OS, крайняя периферия, верхнетемпоральный сектор. Капиллярная ангиома небольшого размера – 0,8 × 1,5 мм, без признаков осложнений (рис. 9). Проведена ТТТ, после которой достигнута полная регрессия опухолевого очага.
OS, крайняя периферия, верхнетемпоральный сектор. Очаг размером 0,9 × 1,3 мм, визуализировались питающие сосуды без экссудации. Выполнена ТТТ, на фоне которой достигнута полная регрессия опухоли.
OS, крайняя периферия, верхнетемпоральный сектор. Еще одна ангиома в том же секторе размером 0,85 × 1,5 мм с минимально выраженными питающими сосудами. Проведена ТТТ. На фоне лечения достигнута полная регрессия новообразования (рис. 10).
Пациент 3 (отец)
Пациент, 36 лет, активных жалоб не предъявлял. Заболевание диагностировано в ходе семейного обследования. Подтвержден СГЛ. При офтальмологическом обследовании выявлено две РКА (одна на правом глазу, одна на левом). Острота зрения обоих глаз – 1 (неизменна).
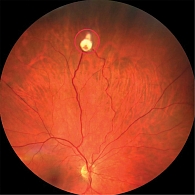
OD, крайняя периферия, верхненазальный сектор. В верхненосовом секторе крайней периферии правого глаза выявлена капиллярная ангиома размером 1,93 × 2,85 мм с расширением и извитостью сосудов. Пациенту проведено два сеанса ТТТ с девятимесячным интервалом (рис. 11).
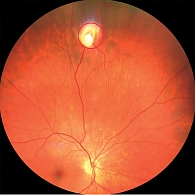
На фоне лечения достигнута полная регрессия опухолевой ткани, а также снижение калибра и извитости питающих сосудов (рис. 12).
OS, крайняя периферия, верхнетемпоральный сектор.
Еще один очаг на левом глазу – ангиома размером 1,64 × 2,09 мм – сопровождался умеренной извитостью питающих сосудов (рис. 13). После ТТТ наблюдались полная регрессия опухоли и отчетливое уменьшение диаметра и извитости питающих сосудов (рис. 14).
Обсуждение
Настоящее наблюдение представляет интерес в связи с семейной природой заболевания, мультифокальностью и разнообразием клинических проявлений РКА у пациентов разного возраста. Выявление патологии у дочери инициировало обследование других членов семьи, что позволило своевременно диагностировать болезнь и начать лечение до развития тяжелых осложнений. Сказанное подчеркивает необходимость активного скрининга и генетического тестирования родственников первой линии родства, как рекомендовано в клинических руководствах [6].
Тактика лечения при РКА зависит от размера, локализации и стадии опухоли, а также наличия осложнений. Согласно данным литературы, ТТТ, эффективно используемая при небольших и средних опухолях (до 2,5 мм в толщину), обеспечивает регрессию очагов и контроль над экссудативными проявлениями [7, 8]. Наш опыт подтверждает это.
КД остается методом выбора при более массивных ангиомах с выраженной экссудацией или при их локализации в крайней периферии. В ряде работ отмечается ее высокая эффективность, особенно при адекватной дозе воздействия и формировании атрофического рубца [9]. В нашем наблюдении КД применялась у 12-летней девочки с опухолью размером 2,5 × 3,2 мм и дала удовлетворительный результат при комбинировании с ограничительной ЛКС.
Эндорезекция с микроинвазивной витрэктомией, как более инвазивный подход, применяется при крупных очагах, сопровождающихся вторичной отслойкой сетчатки, эпиретинальным фиброзом, или при неэффективности других методов. Результаты современных исследований подтверждают, что при тщательном соблюдении этапов операции и адекватной тампонаде силиконовым маслом можно достичь стойкой анатомической стабилизации и полной резекции опухоли [10, 11]. Подобный результат наблюдался у нашей пациентки с наиболее массивной ангиомой (длина – 7,5 мм, высота – 4 мм).
Необходимо отметить, что даже при наличии крупных опухолей с осложнениями в случае своевременного вмешательства можно сохранить высокую остроту зрения, как показано в нашем наблюдении.
Таким образом, полученные результаты подчеркивают важность:
- раннего выявления РКА в рамках диспансерного наблюдения за семьями с СГЛ;
- индивидуального подбора метода лечения в зависимости от анатомо-клинических характеристик очага;
- комплексного подхода к ведению пациентов с участием офтальмолога, генетика, онколога и нейрохирурга.
Комплексное этапное лечение позволяет контролировать прогрессирование заболевания и сохранить зрительные функции даже при множественных поражениях.
Заключение
Лечение РКА при СГЛ требует комплексного подхода, включая как традиционные методы (ТТТ, КД), так и более инвазивные вмешательства, например эндорезекцию опухолей. В нашем исследовании показана эффективность ТТТ и КД. Эти методы лечения в большинстве случаев обеспечивают полную регрессию опухолей. Микроинвазивная витрэктомия с эндорезекцией признана высокоэффективной в осложненных случаях с отслойкой сетчатки.
Полученные данные подтверждают необходимость раннего диагностического скрининга пациентов с СГЛ и индивидуализированного подхода к лечению, что особенно важно в контексте семейного наблюдения.
Информация о финансовой поддержке. Исследование выполнено без финансовой поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
A.A. Yarovoy, PhD, R.A. Loginov, PhD, U.A. Yataev, I.M. Gorshkov, PhD, D.A. Magaramov, PhD, D.P. Volodin, PhD
Interdisciplinary Scientific and Technical Complex ’Eye Microsurgery‘ named after Academician S.N. Fedorov
Contact person: Umar A. Yataev, yataevumar@gmail.com
The aim is to study a family case of Hippel – Lindau syndrome (HLS) and evaluate the effectiveness of various treatments for retinal capillary angiomas (RCAs).
Material and methods. The treatment was carried out in three patients from the same family (father, son and daughter) with diagnosed RCAs associated with HLS. Laser coagulation, cryodestruction, transpupillary thermotherapy and endoresection were used.
Results. All patients showed stabilization of visual acuity and tumor regression. Combined treatment methods effectively controlled tumor growth and eliminated complications, in particular exudative retinal detachment.
Conclusion. A comprehensive approach is effective for treating retinal capillary angiomas in HLS. Early diagnosis and timely treatment can preserve vision.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.