V Всероссийский конгресс «Амбулаторно-поликлиническая практика в эпицентре женского здоровья»: НоваРинг и Чарозетта в гинекологической практике: контрацептивы и их дополнительные лечебные свойства
- Аннотация
- Статья
- Ссылки







В своем выступлении заместитель директора по научной работе ФГБУ «НЦАГиП им. В.И. Кулакова» Минздравсоцразвития России, профессор, д. м. н., заслуженный деятель науки РФ В.Н. ПРИЛЕПСКАЯ обобщила новейшие достижения в области гормональной контрацепции. Появление во второй половине прошлого века контрацептивных таблеток произвело революцию в медицине и в жизни миллионов женщин. По словам Веры Николаевны Прилепской, двести ведущих историков планеты пришли к заключению: гормональные контрацептивы оказали более сильное влияние на общество в ХХ веке, чем теория относительности Эйнштейна, ядерная бомба или изобретение компьютеров и Интернета.
«Активное развитие гормональной контрацепции в мировой медицине продолжается, и примеров тому немало, – уточняет профессор В.Н. Прилепская. – Претерпели значительные изменения режимы гормональной оральной контрацепции: на смену стандартному режиму приема “21 + 7” приходит новый режим “24 + 4”, реализованный в препаратах Джес и Зоэли». Разработано новое вагинальное средство – гель на основе препарата тенофовир – с контрацептивным и антиретровирусным действием, которое может способствовать профилактике ВИЧ-инфекции, препараты, содержащие фетальный эстроген (эстетрол), с отсутствием системных эффектов. Внедряются в клиническую практику новые комбинированные оральные контрацептивы (КОК), содержащие эстрогены, идентичные по структуре натуральным: Клайра (эстрадиола валерат + диеногест) и инновационный препарат, проходящий заключительный этап регистрации в России, – Зоэли (зарегистрирован в России в апреле 2012 г. – Прим. ред.). Отличительная особенность этого препарата в том, что в нем оба компонента максимально приближены к гормонам, естественным образом вырабатывающимся в организме женщины. В его состав входит абсолютно идентичный натуральному эстроген – 17-бета-эстрадиол – и производное прогестерона – номегэстрола ацетат, структура которого схожа с эндогенным прогестероном. Синтезирован новый препарат для экстренной контрацепции, содержащий улипристала ацетат, который эффективен в течение 5 дней после незащищенного полового акта; используется контрацептивный имплантат длительного действия с этоногестрелом (Implanon) и рентгеноконтрастный имплантат Implanon NXT.
За последние 50 лет в качестве компонентов пероральных контрацептивов использовалось множество прогестагенов, каждый из которых обладает определенными уникальными свойствами, включая лечебные. Однако эстрогенный компонент в большинстве препаратов оставался прежним – этинилэстрадиол, имеющий системные побочные эффекты. По сравнению с ним эстрадиол оказывает меньшее влияние на гемостаз, функции печени, синтез глобулина, связывающего половые стероиды (ГСПС), ренин-ангиотензин-альдостероновую и сердечно-сосудистую системы. Компанией «МСД Фармасьютикалс» создан инновационный монофазный комбинированный гормональный контрацептив Зоэли, который содержит 17-бета-эстрадиол и номегэстрола ацетат с новым оптимизированным режимом применения «24 + 4». Номегэстрола ацетат – высокоселективный прогестаген, производное натурального прогестерона, обладает идентичными прогестерону гормональными эффектами, отличается очень длительным периодом полувыведения (46 часов), что обеспечивает беспрецедентную надежность контрацепции, даже если женщина забыла принять таблетку вовремя, высокой антигонадотропной активностью, выраженным подавлением овуляции и способностью увеличивать вязкость цервикальной слизи1. Изучено более 42 тысяч циклов у женщин, принимающих Зоэли. Результаты клинических исследований подтвердили, что режим приема «24 + 4» способствует уменьшению длительности менструаций и более выраженному подавлению роста фолликула за счет более короткого промежутка без гормонов. Препарат обладает высокой контрацептивной эффективностью, обеспечивает хороший контроль цикла, практически не влияет на массу тела и, в отличие от многих других КОК, по результатам лабораторных данных, оказывает минимальное воздействие на гемостаз, липидный профиль и метаболизм углеводов.
Кроме эффективности и безопасности, современные гормональные контрацептивы обладают и неконтрацептивными преимуществами: на фоне их приема снижается риск возникновения рака яичников и эндометрия, частота воспалительных заболеваний органов малого таза; уменьшается менструальная кровопотеря и опасность развития железодефицитной анемии. Современные гормональные контрацептивы способны купировать дисменорею, предменструальные симптомы, тазовые боли, регулировать длительность менструального цикла, обеспечивать профилактику эндометриоза и миомы матки, поликистоза яичников и мастопатии.
Наряду с оральными контрацептивами в настоящее время широкое применение получают и такие методы контрацепции, как гормональные рилизинг-системы. Они отличаются парентеральным, а не пероральным путем введения и удобными режимами использования (еженедельный, ежемесячный и долгосрочный). Например, комбинированная влагалищная эстроген-гестагенная рилизинг-система с режимом применения «один на месяц» НоваРинг представляет собой эластичное прозрачное кольцо диаметром 54 мм и толщиной 4 мм, которое женщина может самостоятельно вводить во влагалище. Из кольца ежедневно выделяется всего 15 мкг этинилэстрадиола и 120 мкг этоногестрела, это самая низкая доза гормонов среди всех существующих комбинированных контрацептивов, однако, несмотря на низкие дозы гормонов, НоваРинг обеспечивает эффективную контрацепцию (более 99%) и отличный контроль цикла. По суточному выделению этинилэстрадиола НоваРинг соответствует микродозированным оральным контрацептивам, а способ введения и режим применения обеспечивают наименьшие колебания уровней – «монотонность» гормонального фона на протяжении целого месяца, что так важно для организма женщины. Трансдермальная контрацептивная система Евра также обеспечивает постоянную и равномерную доставку гормонов в течение недели, ежесуточно выделяя в кровь 20 мкг этинилэстрадиола и 150 мкг норэлгестромина.
Подводя итоги выступления, профессор В.Н. Прилепская подчеркнула: в современном обществе гормональная контрацепция уже не считается способом «борьбы» с рождаемостью, а является эффективным методом сохранения репродуктивного здоровья женщины и обеспечения планируемой, а значит, желанной беременности и рождения желанных детей.
Гестагены в лечении и профилактике гинекологических заболеваний
Доклад ведущего научного сотрудника ФГБУ «НЦАГиП им. В.И. Кулакова» Минздравсоцразвития России, д. м. н. Е.А. МЕЖЕВИТИНОВОЙ был посвящен прогестагенной контрацепции, или чисто прогестиновым контрацептивам (ЧПК): классификации, составу, механизму действия, а также контрацептивным и лечебным свойствам и достоинствам этих препаратов.
Различают следующие формы выпуска ЧПК: таблетки (Чарозетта, Эксклютон, Микролют), частота неудач при использовании которых составляет 0,3%; инъекции (Depot MPA), частота неудач в первый год применения варьирует в диапазоне 0,1–0,6%; имплантаты, содержащие левоноргестрел (ЛНГ), – 0,2% неудач в первый год использования; внутриматочные системы (ЛНГ-ВМГС) – процент неудач составляет 0,1–0,3.
Прогестиновые таблетки мини-пили (МП) – Эксклютон, Микролют – отличаются меньшей эффективностью, чем комбинированные оральные контрацептивы (КОК). При их применении ановуляция наблюдается только у 20–40% женщин. Микродозы гестагенов обеспечивают контрацепцию благодаря способности повышать вязкость цервикальной слизи и снижать секреторную активность эндометрия. Максимальная концентрация достигается в течение 3–4 часов, период полувыведения очень короткий – всего 15–20 часов, эффективность контрацепции резко снижается уже через 3 часа после пропуска таблетки, что предполагает строгое соблюдение режима приема. Мини-пили обладают выраженным прогестиновым эффектом и слабым андрогенным действием, могут незначительно увеличивать риск развития внематочной беременности и вызывать появление акне. Мини-пили в настоящее время отходят на второй план по причине появления препарата Чарозетта. Благодаря входящему в его состав дезогестрелу (75 мкг в сутки) Чарозетта не относится к мини-пили, а обладает свойствами, сопоставимыми с КОК: надежно подавляет овуляцию и обеспечивает эффективность контрацепции более 99%. Дезогестрел – синтетический прогестин, по химической структуре близок к левоноргестрелу. Он быстро и практически полностью абсорбируется из желудочно-кишечного тракта (ЖКТ), метаболизируется в печени и в стенке кишечника превращается в 3-кето-дезогестрел. Максимальная концентрация препарата достигается уже через 1,5 часа, биодоступность варьирует в диапазоне 62–81%, период полувыведения составляет 38 часов. Окно безопасности составляет 12 часов, следовательно, если женщина опоздала с приемом очередной таблетки менее чем на 12 часов, то контрацептивная надежность Чарозетты не снизится. Контрацептивное действие путем подавления овуляции достигается у 97–99% женщин, что сопоставимо с эффективностью комбинированных эстроген-гестагенных препаратов.
Спектр применения чисто прогестиновых контрацептивов широк и не ограничивается исключительно контрацептивными возможностями. ЧПК с успехом используются для лечения заболеваний, связанных с менструальным циклом (дисменорея, меноррагия, предменструальный синдром), а также с целью профилактики многих гинекологических заболеваний (миома матки, эндометриоз, гиперплазия эндометрия, рак матки и яичников, воспалительные заболевания органов малого таза, остеопороз и доброкачественные заболевания молочной железы). Использование прогестагенов при дисменорее снижает концентрацию эстрогенов, количество и митотическую активность клеток эндометрия, локальный уровень простагландинов, а также сократительную функцию миометрия и порог возбудимости мышечной ткани. Прогестагены положительно влияют на состояние костной системы женщин. Они стимулируют специфические рецепторы остеобластов, блокируют рецепторы к глюкокортикостероидам, снижают их ингибирующее влияние на остеосинтез, оказывают антирезорбтивное действие, что существенно уменьшает риск развития остеопороза в менопаузе. Воспалительные заболевания половых органов при использовании ЧПК наблюдаются в 2 раза реже, чем на фоне приема КОК. Прогестагены снижают концентрацию рецепторов к эстрогенам в тканях молочной железы, активность 17-бета-оксистероиддегидрогеназы, трансформирующей неактивный эстроген в активный, и концентрацию эстрадиола в молочной железе, вызывают пролиферацию эпителиальных клеток и стимулируют как апоптоз, так и митоз. Прогестерон и его метаболиты связываются с рецепторами гамма-аминомасляной кислоты (ГАМК) и оказывают некоторое психотропное действие, поэтому их применяют для лечения некоторых форм депрессии, мигрени, эмоциональной возбудимости.
Наиболее частое нежелательное явление, развивающееся на фоне применения ЧПК, – нерегулярные кровянистые выделения, особенно в первые три месяца использования. Они возникают не у всех женщин, не являются признаком гинекологической патологии, и со временем частота их возникновения уменьшается. Данные зарубежных исследований показывают, что не более 25% женщин прекращают прием прогестагенсодержащих контрацептивов из-за нерегулярных кровянистых выделений.
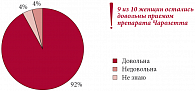
В ходе исследования, целью которого явилось изучение эффективности и приемлемости препарата Чарозетта, проведенного под руководством профессора В.Н. Прилепской, высокую удовлетворенность приемом контрацептива выразили 9 из 10 женщин (рис. 1).
В заключение Елена Анатольевна Межевитинова отметила, что ЧПК отличаются высокой контрацептивной эффективностью и обладают широким спектром терапевтических и профилактических действий при гинекологических заболеваниях. ЧПК могут применять женщины, которым противопоказаны эстрогенсодержащие препараты, относящиеся к группам риска (больные сахарным диабетом, артериальной гипертензией, страдающие мигренью, ожирением (при индексе массы тела более 30 кг/м2), женщины старше 35 лет, особенно курящие). ЧПК могут быть показаны в период лактации, а также при наличии в анамнезе эстрогензависимых реакций на фоне применения КОК.
Гормональная контрацепция в алгоритме органосохраняющего лечения и профилактики эндометриоза и миомы матки
В современной гинекологической практике миома матки и эндометриоз занимают лидирующее место среди причин, по которым женщины подвергаются оперативному лечению. Очень часто эти заболевания сочетаются, что обусловлено возможной общностью их этиологии и патогенеза. По мнению профессора кафедры акушерства и гинекологии лечебного факультета МГМСУ, д. м. н. А.Л. ТИХОМИРОВА, миому матки и эндометриоз нужно начинать лечить на самых ранних стадиях, при минимальных размерах миоматозных узлов и максимально щадящим способом.
Натуральный прогестерон является основным гормоном, стимулирующим рост миомы матки, а большинство клеток пролиферирующих лейомиом (до 90%) содержат активные рецепторы к прогестерону. Иммуногистохимические исследования выявили способность современных гестагенов в составе КОК блокировать эти рецепторы, что объясняет механизм профилактического действия контрацептивов. Стабилизирующий эффект КОК распространяется на миоматозные узлы 1–1,5 см в диаметре. Результат их назначения при больших размерах узлов может быть двояким: в одних случаях размер узла стабилизируется, в других может наблюдаться рост миомы. При малых множественных миомах матки лечение проводится поэтапно: вначале назначаются агонисты гонадотропин-рилизинг-гормона (ГнРГ), затем – гормональная контрацепция.
Миома матки больших размеров является абсолютным показанием к хирургическому вмешательству. Оперативное лечение должно быть органосохраняющим, что может быть достигнуто путем консервативной миомэктомии или эмболизации миомы матки. Консервативная миомэктомия, особенно у молодых женщин, должна сопровождаться послеоперационной гормонотерапией.
По словам Александра Леонидовича Тихомирова, миома матки и эндометриоз – достаточно примитивные, изначально управляемые заболевания, являющиеся результатом «нерационального использования» репродуктивных возможностей, следовательно, их развитие можно предупредить. Проведенный в клинике на базе МГМСУ анамнестический анализ 1400 больных миомой матки указывает на то, что миома возникает у женщин, практически никогда не использовавших гормональную контрацепцию. Оценено соотношение 2- и 16-гидроксиэстрогенов в сыворотке крови у женщин с миомой матки по сравнению с нормой и показателями контрольной группы. Анализ полученных результатов свидетельствует об отсутствии зависимости миомы матки от нарушения метаболизма эстрогенов, в частности гиперэстрогенемии. Следовательно, миома не является эстрогенобусловленным заболеванием, поэтому для ее профилактики и лечения не показаны гормональные контрацептивы с высоким содержанием эстрогена.
К препаратам первой линии для профилактики миомы матки относится НоваРинг, представляющий собой ультрамикродозированное влагалищное кольцо, отличающийся отсутствием побочных эффектов и обеспечивающий высокую комплаентность. НоваРинг способен сокращать заболеваемость миомой матки за счет предотвращения ежемесячных не реализовавшихся в беременность циклических процессов, обеспечения стабильной гормональной монотонности в отсроченном репродуктивном потенциале молодых женщин, подавления овуляции, замены эндогенного прогестерона на аналог без пролиферативного воздействия на клетки миометрия, обеспечения надежной контрацепции и профилактики абортов как одной из главных причин роста гинекологической заболеваемости, подрывающей репродуктивный потенциал нации. Применение НоваРинга, наряду с его контрацептивным эффектом, обеспечивает патогенетическую профилактику эндометриоза, поскольку этим заболеванием чаще страдают женщины репродуктивного возраста с сохраненным двухфазным менструальным циклом, овуляцией и нереализованной репродукцией.
Подводя итог своему выступлению, профессор А.Л. Тихомиров констатировал: гормональная контрацепция в настоящее время является одним из компонентов здорового образа жизни, а применение НоваРинга облегчает молодым женщинам заботу о своем здоровье.
Возможности профилактики функциональныхкист яичников. Теория и практика
В начале своего доклада профессор кафедры акушерства и гинекологии лечебного факультета МГМСУ, д. м. н. М.А. ГЕВОРКЯН обратила внимание слушателей на существующее на сегодняшний день различие во взглядах ученых-медиков на тактику ведения пациенток при функциональных кистах яичников. К функциональным кистам, обусловленным постоянными ежемесячными циклическими процессами, относятся фолликулярные кисты и кисты желтого тела. Одни авторы придерживаются тактики наблюдения таких кист в течение 2–3 месяцев, поскольку в течение этого периода до 30% случаев разрешаются самостоятельно2. Другие считают, что применение комбинированных гормональных контрацептивов ускоряет регрессию функциональных кист на 15–30%3. Третья группа авторов рекомендуют применять оперативное лечение после 2–3 месяцев наблюдения4.
По мнению Марияны Арамовны Геворкян, не всегда возможно избежать оперативного вмешательства, однако следует ежегодно оценивать статистику хирургической активности и принимать меры по снижению частоты удаления функциональных кист. Выжидательная тактика также не помогает эффективно решить проблему. Современная гормональная контрацепция, обладающая значимыми дополнительными преимуществами, способствует профилактике формирования функциональных кист.
К причинам развития функциональных кист яичников в репродуктивном возрасте относятся эмоциональные стрессы, физические перегрузки, смена климата, гистерэктомия без придатков, односторонняя аднексэктомия, резекция яичников по поводу доброкачественных опухолей и другие вмешательства на органах малого таза лапаротомным или эндоскопическим доступом, спаечный процесс, наружный эндометриоз. Функциональные кисты, возникающие в результате гипергонадотропной стимуляции яичников, являются одним из клинических признаков снижения овариальных резервов. Период пременопаузы также чреват вероятностью развития функциональных кист. В это время в организме женщины происходят инволютивные процессы в центральной нервной системе, рецепторном аппарате, нарушение механизмов обратной связи в системе «гипоталамус – гипофиз – яичники» (ГГЯ), характеризующееся флюктуирующими выбросами фолликулостимулирующего гормона (ФСГ). Высокие уровни эстрадиола не снижают секрецию лютеинизирующего гормона (ЛГ), нарушается нормальное соотношение ЛГ/ФСГ, что также повышает риск развития функциональных кист.
Профилактику образования функциональных кист необходимо осуществлять исходя из знания физиологии угасания репродуктивной системы. Принципы гормонотерапии кист заключаются в подавлении гонадотропной функции яичников и, соответственно, овариального фолликулогенеза. При кистах желтого тела особенно важно подавить секрецию ЛГ во II фазе цикла, поскольку они растут по типу синдрома гиперстимуляции яичников (СГЯ). В качестве гормонотерапии можно использовать КОК, содержащие дезогестрел, который метаболически инертен и обладает антиандрогенным действием. Агонисты ГнРГ в данном случае не показаны, поскольку на первом этапе (10–14 дней) они стимулируют овуляцию, что может привести к разрыву кисты. Нецелесообразно использовать и антагонисты ГнРГ.
Комплексная терапия функциональных кист, помимо гормональных средств, предполагает использование негормональных препаратов: антибактериальных (при кистах желтого тела, апоплексии в течение 5–10 дней), нестероидных противовоспалительных средств (инъекции или ректальные суппозитории), антиоксидантов и детоксикантов, седативных и антигистаминных средств. «У женщин пременопаузального возраста часто встречаются персистирующие фолликулы, поэтому им необходимы надежные и максимально безопасные гормональные контрацептивы с минимальными дозами эстрогенов», – пояснила профессор М.А. Геворкян. Этим требованиям отвечает влагалищная гормональная система НоваРинг. При противопоказаниях к эстрогенам можно назначать Норколут и Чарозетту. В молодом возрасте следует использовать НоваРинг в циклическом режиме, а в перименопаузальном возрасте – НоваРинг в пролонгированном режиме. Пролонгированный режим предполагает применение НоваРинга непрерывно со сменой кольца каждые 3 недели на протяжении 42, 63, 84 дней с последующим перерывом на 7 дней. Докладчик привела данные собственного исследования эффективности влагалищной рилизинг-системы НоваРинг в подавлении фолликулогенеза: динамика изменений диаметра фолликулов на фоне циклического и пролонгированного использования НоваРинга продемонстрировала достоверно значимое снижение роста фолликулов (рис. 2).
В перименопаузальном возрасте возрастает риск развития функциональных кист, гинекологических заболеваний, клинически проявляющихся менометроррагиями, поэтому система НоваРинг, отличающаяся минимальным эстрогенным влиянием на организм по сравнению с КОК, является альтернативой заместительной гормональной терапии (ЗГТ) до возраста менопаузы. Система НоваРинг – эффективное средство контрацепции от менархе до менопаузы. Внутривлагалищная гормональная рилизинг-система НоваРинг стабильно высвобождает в организм 15 мкг этинилэстрадиола и 120 мкг этоногестрела в сутки. Данное сочетание обеспечивает оптимальную для достижения контрацептивного эффекта концентрацию гормонов в плазме крови. Кроме того, НоваРинг, обеспечивая контроль менструального цикла, способствует профилактике формирования функциональных кист и гиперпластических процессов эндометрия, является альтернативой оральным контрацептивам и препаратом выбора у женщин с метаболическим синдромом. «Широкое применение внутривлагалищной гормональной рилизинг-системы НоваРинг в конечном итоге позволит сократить число разноплановых оперативных вмешательств и сохранить репродуктивное здоровье женщин», – заключила свое выступление профессор М.А. Геворкян.
Микробиоценоз влагалища и гормональная рилизинг-система НоваРинг
По словам старшего научного сотрудника научно-поликлинического отделения ФГБУ «НЦАГиП им. В.И. Кулакова» Минздравсоцразвития России, д. м. н. Н.М. НАЗАРОВОЙ, за более чем семилетнее присутствие на российском рынке препарат НоваРинг занял достойное место среди гормональных методов контрацепции – ему отдают предпочтение порядка 30% москвичек, использующих контрацептивы. Такая востребованность НоваРинга объясняется удобным ежемесячным режимом применения, минимальным системным влиянием низких доз гормонов, поддержанием их постоянного уровня в крови, отсутствием эффекта первичного прохождения через печень и взаимодействия с ЖКТ. Системное действие НоваРинга к настоящему времени подробно изучено, в то время как его локальные эффекты продолжают оставаться предметом исследований. Актуальным является изучение возможного негативного влияния влагалищного пути введения на шейку матки, влагалище и его микробиоценоз.
Известно, что прием КОК ассоциируется с повышением частоты возникновения кандидоза влагалища – эстрогенный компонент способствует формированию обогащенной гликогеном среды, благоприятной для грибов рода Candida. Влагалищная флора индивидуальна у каждой женщины, ее качественный и количественный состав варьирует в зависимости от фазы менструального цикла. На состав микрофлоры влагалища могут оказывать влияние сексуальная активность, использование контрацепции, интимная гигиена, экстрагенитальная патология. Наиболее важным показателем резистентности вагинального эпителия является количество гликогена, который является питательным субстратом для нормальной микрофлоры. Количество гликогена в клетках вагинального эпителия колеблется у женщины на протяжении жизни, а также изменяется в зависимости от фазы менструального цикла. Основным механизмом, обеспечивающим колонизационную резистентность вагинального биотопа, является способность лактобактерий к кислотообразованию. Лактобактерии продуцируют молочную кислоту в количествах, достаточных для создания выраженной кислой среды вагинального отделяемого, и тем самым препятствуют размножению ацидофобных бактерий.
При анализе влияния гормонов на эпителий шейки матки и влагалища отмечается следующее: эстрогены в первой фазе цикла вызывают рост и созревание многослойного эпителия (МПЭ), синтез и накопление гликогена, выработку слизистого секрета в цервикальном канале, выработку IgА; прогестерон во второй фазе вызывает обратные процессы: десквамацию, цитолиз МПЭ, высвобождение гликогена и расщепление его лактобактериями до молочной кислоты. Это приводит к сдвигу рН в кислую сторону, что ограничивает рост и размножение микроорганизмов, чувствительных к кислой среде.
Эстроген-гестагенный компонент гормональных контрацептивов обеспечивает равномерное развитие дифференцированного многослойного эпителия влагалища и шейки матки. Установлено, что у большинства женщин, использующих НоваРинг, отсутствуют изменения в цитологических мазках с шейки матки5.
Нисо Мирзоевна Назарова ознакомила участников симпозиума с результатами сравнительного исследования (уровень доказательности I), в котором изучались вагинальные симптомы при использовании влагалищного кольца и КОК6. Методы исследования включали оценку вагинальных выделений, бактериоскопическое и бактериологическое исследования, ежедневную оценку симптомов до начала применения контрацептивов и через 2–4 месяца. Результаты показали увеличение вагинальной секреции в обеих группах. Однако при использовании вагинального кольца было выше число колоний лактобактерий, продуцирующих перекись водорода H2O2 (2,67 против 1,49; доверительный интервал (ДИ) 95%; p < 0,001). Повышение концентрации лактобактерий свидетельствует о положительном влиянии вагинального кольца НоваРинг на состояние микробиоценоза влагалища. Важно, что совместное использование НоваРинга с противогрибковыми препаратами не снижает его эффективности7. «Отсутствие отрицательного влияния на микробиоценоз влагалища и эпителий шейки матки, стабильное выделение гормонов и удобный режим применения позволяют расценивать влагалищное кольцо НоваРинг как контрацептив выбора», – подчеркнула Н.М. Назарова, завершая выступление.
Заключение
Докладчики были единодушны в своей оценке эстроген-гестагенной рилизинг-системы НоваРинг (15 мкг этинилэстрадиола, 120 мкг этоногестрела в сутки) и чисто прогестинового препарата Чарозетта (75 мкг дезогестрела) как высокоселективных микродозированных средств, отличающихся высокой контрацептивной эффективностью, низкой частотой побочных эффектов и обеспечивающих высокий уровень комплаентности. НоваРинг и Чарозетта обладают широким спектром лечебных и профилактических свойств. Применение этих контрацептивов позволяет в ряде случаев избежать хирургических вмешательств и обеспечить профилактику при функциональных кистах яичников, эндометриозе, миоме матки.Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.