количество статей
7360
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
Восемнадцатая Российская гастроэнтерологическая неделя: Клинико-терапевтическая парадигма абдоминальной боли и метеоризма
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Гастроэнтерология" №5
- Аннотация
- Статья
- Ссылки
В частности, было отмечено, что метеоризм может стать причиной не только болевого синдрома, но и трудностей в социальной адаптации, что, в свою очередь, влечет за собой расстройства психоэмоциональной сферы, а хронический панкреатит даже на относительно ранних стадиях болезни приводит к упадку сил и снижению работоспособности.
Поскольку адекватное лечение гастроэнтерологических заболеваний в отсутствие точной диагностики невозможно, заключительный доклад симпозиума был посвящен особенностям подготовки пациентов к гастроэнтерологическому ультразвуковому исследованию с целью повышения его качества.
На симпозиуме рассматривались вопросы диагностики и лечения наиболее распространенных гастроэнтерологических заболеваний – метеоризма и хронического панкреатита, – широко обсуждаемые на сегодняшний день в кругах гастроэнтерологов и терапевтов.
В частности, было отмечено, что метеоризм может стать причиной не только болевого синдрома, но и трудностей в социальной адаптации, что, в свою очередь, влечет за собой расстройства психоэмоциональной сферы, а хронический панкреатит даже на относительно ранних стадиях болезни приводит к упадку сил и снижению работоспособности.
Поскольку адекватное лечение гастроэнтерологических заболеваний в отсутствие точной диагностики невозможно, заключительный доклад симпозиума был посвящен особенностям подготовки пациентов к гастроэнтерологическому ультразвуковому исследованию с целью повышения его качества.

Профессор Ю.П. Успенский
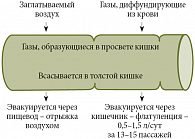
Рис. 1. Схема поступления и элиминации кишечных газов
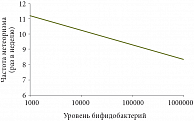
Рис. 2. Взаимосвязь частоты метеоризма с уровнем бифидобактерий
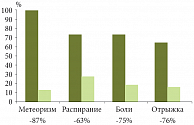
Рис. 3. Оценка эффективности препарата Эспумизан® при симптоматической терапии метеоризма
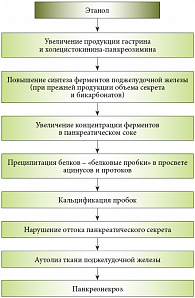
Рис. 4. Патогенез алкогольного панкреатита
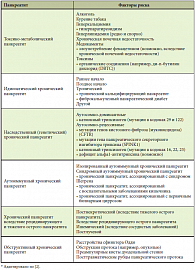
Таблица 1. Этиологические факторы риска, ассоциированные с хроническим панкреатитом: классификационная система TIGAR-O (Toxic-metabolic, Idiopathic, Genetic, A

Таблица 2. Диагностика хронического панкреатита по балльной системе

Таблица 3. Симптомы нарушения пищеварения и всасывания и механизмы их развития у больных хроническим панкреатитом
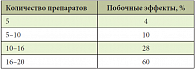
Таблица 4. Вероятность развития побочных эффектов в зависимости от числа одновременно принимаемых препаратов
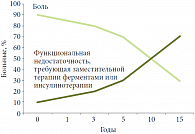
Рис. 5. Динамика развития хронического панкреатита

Таблица 5. Варианты, режимы дозирования и длительность приема препарата Мезим® 10000 в терапии хронического панкреатита (ХП)

Профессор В.В. Митьков
Открывая симпозиум, д.м.н., профессор Ю.П. УСПЕНСКИЙ (Санкт-Петербургский государственный медицинский университет им. академика И.П. Павлова) подчеркнул, что метеоризм как патологическое состояние является симптомокомплексом, а не отдельным симптомом. Согласно приведенному определению, метеоризмом называется избыточное скопление газа в желудочно-кишечном тракте (ЖКТ) вследствие его повышенного образования или нарушения выведения, проявляющееся срыгиванием, отрыжкой воздухом, ощущениями переполнения, вздутия живота с увеличением его окружности, урчания в кишечнике, учащением пассажа (флатуленцией) кишечных газов.
Как отметил профессор Ю.П. Успенский, метеоризм не следует рассматривать как безобидное транзиторное нарушение, не требующее ни диагностики, ни лечения. Во-первых, метеоризм является маркером нарушения кишечного пищеварения и дисбиоза кишечника. Во-вторых, клинические проявления метеоризма, как правило, усугубляются в стрессовых ситуациях: при смене климата, на фоне изменений в рационе, а также в периоды психоэмоционального напряжения. И, наконец, метеоризм создает целый ряд социальных проблем и тем самым непосредственно влияет на качество жизни.
Прежде чем приступать к лечению метеоризма, необходимо разобраться в его патогенезе, выяснить, каково происхождение кишечных газов, являющихся причиной метеоризма. Считается, что в норме кишечных газов экзогенного происхождения – 65–70%, эндогенного – 30–35%. Основными источниками газов в кишечнике являются аэрофагия (заглатывание воздуха), диффузия азота из крови и образование газа в просвете кишечника (бактериальный метаболизм) на фоне дисбиоза.
Оказавшиеся в кишечнике газы могут быть удалены из него двумя путями – через пищевод (что приводит к появлению распространенного симптома отрыжки воздухом) или через кишечник (рис. 1). В норме через анальное отверстие в течение суток должно эвакуироваться 0,5–1,5 л газов за 13–15 пассажей. Увеличение количества выделяемых газов или пассажей свидетельствует о развитии патологического процесса.
В норме в просвете кишечника содержится около 200 мл смеси газов. Среди них может выявляться азот (11–92%), кислород (0–11%), углекислый газ (3–54%), водород (1–10%), метан (0–56%), сероводород (0–30%), а также индол и скатол. Однако клинические проявления синдрома метеоризма обусловлены в первую очередь не химическим составом, а физической формой кишечных газов, которые представляют собой пену, состоящую из мелких пузырьков, окруженных слоем вязкой слизи, из-за которой нарушаются процессы абсорбции газов кишечной стенкой. В результате количество пены увеличивается и формируется порочный круг. Пена эвакуируется из просвета кишечника с большим трудом, доставляя пациентам серьезный дискомфорт.
Список причин возникновения метеоризма обширен и наряду со стрессами и нарушениями кишечного пищеварения включает органические и функциональные расстройства, препятствующие нормальному кишечному транзиту, и ферментопатии. Изменение рациона, в частности, употребление в соответствии с нормами Всемирной организации здравоохранения 400–500 г овощей и фруктов ежедневно, также может стать причиной развития метеоризма. Существуют данные, указывающие на наличие корреляции между содержанием бифидо- и лактобактерий и вероятностью развития метеоризма (рис. 2).
Несмотря на многочисленные социальные проблемы, вызываемые метеоризмом, пациенты с данным синдромом чаще всего обращаются к врачу не по этой причине, а из-за боли и выраженного дискомфорта в животе по ходу толстой кишки. Для пожилых пациентов метеоризм является не только неприятным, но и опасным заболеванием: повышая уровень стояния купола диафрагмы и затрудняя нормальную работу сердца, скопление газов может спровоцировать обострение имеющихся сердечно-сосудистых заболеваний.
Лечение метеоризма включает диету (продукты, вызывающие повышенное газообразование, исключаются из рациона или ограничиваются), симптоматическую (пеногасители и адсорбенты) и этиопатогенетическую терапию. Последняя должна быть направлена на устранение моторно-эвакуаторных кишечных расстройств, нормализацию стула, замещение нарушенной внешнесекреторной функции поджелудочной железы (пациентам назначается полиферментная терапия, например, препаратом Мезим®), а также на коррекцию дисбиоза кишечника и психоэмоциональных нарушений.
Симптоматическая терапия с использованием адсорбентов обладает рядом недостатков: активированный уголь, препараты висмута и подобные средства действуют неселективно и могут адсорбировать необходимые организму соединения; кроме того, в ряде случаев адсорбенты затрудняют пассаж кишечного содержимого и усугубляют существующие запоры.
Механизм действия пеногасителей основан на ослаблении поверхностного натяжения пузырьков газа, что приводит к их разрыву и выведению из организма. Среди имеющихся на рынке пеногасителей особый интерес представляет Эспумизан® – препарат на основе симетикона, смеси полимера диметилсилоксана с диоксидом кремния (SiO2). Он действует по всему ходу ЖКТ, поэтому может использоваться для лечения как желудочной (отрыжка), так и кишечной (собственно метеоризм) диспепсии. Эспумизан® характеризуется быстрым действием и превосходной переносимостью, препарат может применяться во всех возрастных группах.
Эффективность препарата Эспумизан® была подтверждена в многочисленных клинических исследованиях, например в работе П.Л. Щербакова и соавт. (2005), в ходе которой Эспумизан® был назначен 68 детям в возрасте от 4 до 15 лет, страдавшим различными заболеваниями ЖКТ. Дискомфорт и спастические боли в животе исчезли уже в первый день приема препарата. В Учебно-научном медицинском центре Управления делами Президента РФ д.м.н., профессором кафедры гастроэнтерологии ФГБУ «УНМЦ» УД Президента РФ О.Н. Минушкиным и к.м.н. Г.А. Елизаветиной проведено исследование оценки эффективности препарата Эспумизан® при метеоризме. В ходе этой работы взрослые пациенты (n = 33) получали по 2 капсулы Эспумизана 3–4 раза в день на протяжении 1–2 недель. Было установлено, что прием Эспумизана влияет на выраженность симптомов метеоризма (рис. 3), а значит, может применяться для симптоматической терапии данного вида диспепсии.
Хорошие результаты применения Эспумизана в лечении синдрома повышенного газообразования у пациентов с заболеваниями ЖКТ были продемонстрированы и в работе С.Г. Буркова и соавт. (2009)1. Больные, включенные в работу (n = 48), принимали по 2 капсулы Эспумизана 5 раз в день. Выраженное снижение симптомов метеоризма было зарегистрировано у 93,8% больных, что позволило авторам работы рекомендовать Эспумизан® как дополнительное средство на фоне базисной терапии гастроэнтерологических заболеваний, сопровождающихся синдромом повышенного газообразования.
Боль панкреатического происхождения как основание для назначения ферментов
Продолжая выступление на симпозиуме, профессор Ю.П. Успенский во втором докладе коснулся вопроса назначения полиферментной терапии больным с хроническим панкреатитом (ХП). ХП является одним из наиболее распространенных гастроэнтерологических заболеваний и составляет 5–20% всех случаев заболеваний органов пищеварения. Начиная с 1980-х годов заболеваемость ХП в мире увеличилась в 2 раза. В России за последние 10 лет распространенность ХП среди взрослых возросла в 3 раза, а среди подростков – в 4 раза. Как отметил профессор Ю.П. Успенский, в основе этого феномена, по всей видимости, лежат социальные причины: злоупотребление фаст-фудом, слабоалкогольными коктейлями, пивом и другими спиртными напитками. Актуальность проблемы ХП связана и с тем, что данное заболевание, по-видимому, диагностируют реже, чем оно фактически встречается в популяции.
На сегодняшний день насчитывается несколько десятков этиологических факторов риска развития ХП (табл. 1)2, однако наиболее значимыми в общей картине заболеваемости являются два из них: употребление алкоголя (75–90% случаев) и заболевания желчевыводящих путей (10–25%)3 . Патогенетический каскад алкогольного ХП начинается с повышения интенсивности синтеза ферментов поджелудочной железы (ПЖ) и в конечном счете заканчивается панкреонекрозом (рис. 4). ПЖ впитывает алкоголь подобно губке. Концентрация этанола в клетках ПЖ достигает 60% от уровня его концентрации в крови. В результате прямого воздействия этанола развивается жировая инфильтрация ПЖ.
Алкогольный панкреатит – и в этом его ключевое отличие от алкогольной жировой болезни печени – может развиться даже при употреблении небольших, социально приемлемых доз алкоголя. Более того, определить пороговую дозу, превышение которой чревато развитием ХП, пока не представляется возможным, что указывает на различную индивидуальную чувствительность к алкоголю и возможную роль других факторов в развитии алкогольного ХП. Однако известно, что у лиц, употребляющих более 100 г этанола в сутки, риск развития ХП по сравнению с непьющими людьми увеличивается в 11 раз4. Тяжелое течение алкогольного панкреатита может быть обусловлено еще и высоким содержанием жира в пище, принимаемой одновременно с алкоголем.
Клинические проявления ХП разнообразны. Проще всего классифицировать их по механизмам развития: раннее насыщение, вздутие, метеоризм, отрыжка, тошнота и рвота появляются из-за задержки эвакуации содержимого желудка; осмолярная диарея, стеаторея, метеоризм в результате избыточного образования газов связаны с нарушениями пристеночного и полостного пищеварения, а нарушения обмена питательных веществ, снижение массы тела, слабость и нарушение трудоспособности – с нарушениями всасывания.
Причиной обращения к врачу на ранних стадиях ХП, как правило, оказывается боль. Болевой синдром варьирует от слабовыраженной боли до постоянной, нестерпимой. Существует два механизма развития боли у пациентов с ХП. Первый связывают с дуоденальной гипертензией, а второй – с воспалительными изменениями ПЖ – гиперсекрецией на фоне нарушенного оттока, фиброза органа либо вторичного воспаления на фоне органических изменений. Хотя боль является далеко не единственным клиническим признаком ХП, она включена в список диагностических критериев (табл. 2)5.
Течение ХП подразделяется на несколько этапов. Начальный период (в среднем 1–5 лет, иногда до 10 лет) характеризуется болями различной интенсивности в верхней части правой половины живота при поражении головки ПЖ, в эпигастральной области – при поражении тела ПЖ, в левом подреберье – при поражении хвоста ПЖ. Боли опоясывающего характера встречаются нечасто. Диспепсический синдром имеет явно сопутствующий характер.
По завершении начального этапа наступает развернутая картина заболевания (продолжительность 5–10 лет): боли в это время выражены меньше, но появляется все больше признаков внешнесекреторной и инкреторной недостаточности. Стихание патологического процесса через 7–15 лет заболевания наблюдается у 2/3 больных, происходит оно за счет адаптации к ХП (отказа от алкоголя, санации билиарной системы, соблюдения диеты). У 1/3 больных развиваются осложнения (рис. 5)6. Характерными признаками ХП являются стеаторея (появление в кале непереваренных жиров), увеличение объема кала и уменьшение массы тела (при нормальном или сниженном аппетите). В ряде случаев на фоне развернутого течения ХП возникают симптомы нарушения не только пищеварения, но и всасывания: развиваются судороги, боли в костях, остеопороз и другие нарушения (табл. 3).
Прогноз заболевания при серьезной экзокринной недостаточности ПЖ напрямую зависит от готовности пациента выполнять рекомендации врачей, в частности, отказаться от алкоголя. 50% больных с выраженным панкреатитом, продолжающих употреблять алкоголь, умирают в течение 5–12 лет. И напротив, категорический отказ от спиртного является единственным этиотропным методом лечения алкогольного ХП. Важна и диета, особенно ее соблюдение во время первого приема пищи (категорически запрещен прием жирной, острой или копченой пищи натощак). Для фармакотерапии ХП применяются препараты следующих групп:
Как подчеркнул профессор Ю.П. Успенский, полиферментная терапия рекомендована больным с выраженным болевым абдоминальным синдромом, клиническими проявлениями расстройств пищеварения и мальабсорбции, длительным анамнезом заболевания, пациентам с прогрессирующим снижением массы тела. В силу физиологической обусловленности назначение таблетированных форм полиферментных препаратов при ХП более эффективно для купирования абдоминальной боли панкреатического происхождения, так как они активируются еще в проксимальном отделе двенадцатиперстной кишки (при pH = 5,0–6,5) и создают функциональный покой ПЖ. Использование таблетированных форм позволяет также эффективно устранять проявления внешнесекреторной недостаточности ПЖ7–9.
Одним из таких препаратов является Мезим®форте 10000, содержащий оптимальный состав ферментов в физиологической пропорции. Эффективность препарата Мезим® 10000 доказана в рандомизированных открытых сравнительных клинических исследованиях по оценке клинической эффективности препаратов Мезим® 10000 и капсулированного микрогранулированного панкреатина в аналогичной дозировке по липазе (Креон® 10000) в лечении ХП. Данные исследования были проведены на кафедре гастроэнтерологии Военно-медицинской академии им. С.М. Кирова МО РФ (Санкт-Петербург) в 2003 г. под руководством д.м.н., профессора В.Б. Гриневича и И.В. Богданова и в Клинике пропедевтики, гастроэнтерологии и гепатологии им. В.Х. Василенко ММА под руководством В.Т. Ивашкина и О.С. Шифрина в 2009 г.
Данные исследования доказали, что Мезим® 10000 более эффективен при лечении панкреатической боли, чем капсулированные формы панкреатина (p < 0,05), и обеспечивает сравнимую с капсулированными микрогранулированными препаратами панкреатина компенсацию недостаточности внешнесекреторной функции ПЖ (табл. 5). На фоне терапии Мезимом 10000 осложнения в виде запоров регистрируются существенно реже, чем при аналогичной терапии капсулированными микрогранулированными препаратами панкреатина (p < 0,05), что позволяет рекомендовать Мезим® 10000 в качестве препарата выбора для больных с болевой формой ХП и с умеренными проявлениями внешнесекреторной недостаточности ПЖ. На сегодняшний день ультразвуковое исследование (УЗИ) является одним из лидирующих методов медицинской визуализации. Как отметил в начале своего выступления д.м.н., профессор В.В. МИТЬКОВ (заведующий кафедрой ультразвуковой диагностики ГБОУ ДПО «РМАПО» МЗ РФ), о высокой востребованности данного метода свидетельствует тот факт, что только в системе Министерства здравоохранения РФ имеется около 25 000 ставок врачей ультразвуковой диагностики.
Ультразвуковые волны были впервые применены в медицине для диагностики опухолей головного мозга неврологом Венского университета Карлом Теодором Дюссиком в конце 30-х годов прошлого века. Первые приборы для ультразвуковых исследований не позволяли получать двухмерное изображение – на экране отображалась одномерная амплитудная кривая. Аппарат, способный демонстрировать двухмерное изображение, хотя бы отдаленно напоминающее то, к которому мы привыкли сегодня, был разработан Дугласом Ховри в 1951 г. С тех пор прошло много лет. Эра полностью цифрового ультразвука, ставшего сегодня «золотым стандартом» диагностики многих заболеваний, началась в 1996 г. с появления цифровой ультразвуковой диагностической системы Acuson Sequoia 512.
Перспективным направлением ультразвуковой диагностики является применение ультразвуковых контрастных веществ. К сожалению, в России на сегодняшний день не зарегистрировано ни одного ультразвукового контрастного вещества, в то время как в Европе ультразвуковые контрастные вещества широко применяются для диагностики различных заболеваний. Они, например, весьма информативны для дифференциальной диагностики заболеваний печени: при использовании ультразвукового контрастного вещества ультразвуковое исследование оказывается сопоставимо по точности с магнитно-резонансной томографией с контрастным усилением, притом что стоимость ультразвукового исследования на порядок ниже.
Эластография и эластометрия – диагностические методики, работающие на основе ультразвука и позволяющие давать в том числе и количественную информацию о механических (упругих) свойствах тканей. Они получили распространение в исследовании печени, молочной, щитовидной и предстательной желез. В последнее время появились работы, посвященные использованию трехмерной эластографии, но пока рано говорить о клиническом применении данной методики. Большой интерес с практической точки зрения вызывает и трехмерная эхография, применяемая сегодня преимущественно в акушерстве. Ультразвуковое исследование применяется не только в диагностике – под контролем этого метода проводятся пункции и другие малоинвазивные вмешательства, например радиочастотная абляция, HIFU-абляция (ультразвуковая абляция).
Ультразвуковая диагностика является динамично развивающейся областью клинической медицины. Наряду с большим количеством преимуществ, эхография обладает одним существенным ограничением: ее эффективность в гастроэнтерологии напрямую зависит от подготовки пациента. Например, наличие газов в кишечнике может сделать исследование малоинформативным или совершенно неинформативным. Для улучшения информативности ультразвукового исследования применяется препарат Эспумизан®. Его способность повышать точность эхографии доказана рядом исследований. В одном из них применение Эспумизана позволяло визуализировать при ультразвуковом исследовании патологические структуры (метастазы в печени, полипы желчного пузыря и др.), которые не были видны без предварительной подготовки. Это свойство препарата стало основанием для включения Эспумизана в рекомендации Российской ассоциации специалистов ультразвуковой диагностики в медицине по применению препарата для подготовки к ультразвуковому исследованию.
Алкогольный панкреатит – и в этом его ключевое отличие от алкогольной жировой болезни печени – может развиться даже при употреблении небольших, социально приемлемых доз алкоголя. Более того, определить пороговую дозу, превышение которой чревато развитием ХП, пока не представляется возможным, что указывает на различную индивидуальную чувствительность к алкоголю и возможную роль других факторов в развитии алкогольного ХП. Однако известно, что у лиц, употребляющих более 100 г этанола в сутки, риск развития ХП по сравнению с непьющими людьми увеличивается в 11 раз4. Тяжелое течение алкогольного панкреатита может быть обусловлено еще и высоким содержанием жира в пище, принимаемой одновременно с алкоголем.
Клинические проявления ХП разнообразны. Проще всего классифицировать их по механизмам развития: раннее насыщение, вздутие, метеоризм, отрыжка, тошнота и рвота появляются из-за задержки эвакуации содержимого желудка; осмолярная диарея, стеаторея, метеоризм в результате избыточного образования газов связаны с нарушениями пристеночного и полостного пищеварения, а нарушения обмена питательных веществ, снижение массы тела, слабость и нарушение трудоспособности – с нарушениями всасывания.
Причиной обращения к врачу на ранних стадиях ХП, как правило, оказывается боль. Болевой синдром варьирует от слабовыраженной боли до постоянной, нестерпимой. Существует два механизма развития боли у пациентов с ХП. Первый связывают с дуоденальной гипертензией, а второй – с воспалительными изменениями ПЖ – гиперсекрецией на фоне нарушенного оттока, фиброза органа либо вторичного воспаления на фоне органических изменений. Хотя боль является далеко не единственным клиническим признаком ХП, она включена в список диагностических критериев (табл. 2)5.
Течение ХП подразделяется на несколько этапов. Начальный период (в среднем 1–5 лет, иногда до 10 лет) характеризуется болями различной интенсивности в верхней части правой половины живота при поражении головки ПЖ, в эпигастральной области – при поражении тела ПЖ, в левом подреберье – при поражении хвоста ПЖ. Боли опоясывающего характера встречаются нечасто. Диспепсический синдром имеет явно сопутствующий характер.
По завершении начального этапа наступает развернутая картина заболевания (продолжительность 5–10 лет): боли в это время выражены меньше, но появляется все больше признаков внешнесекреторной и инкреторной недостаточности. Стихание патологического процесса через 7–15 лет заболевания наблюдается у 2/3 больных, происходит оно за счет адаптации к ХП (отказа от алкоголя, санации билиарной системы, соблюдения диеты). У 1/3 больных развиваются осложнения (рис. 5)6. Характерными признаками ХП являются стеаторея (появление в кале непереваренных жиров), увеличение объема кала и уменьшение массы тела (при нормальном или сниженном аппетите). В ряде случаев на фоне развернутого течения ХП возникают симптомы нарушения не только пищеварения, но и всасывания: развиваются судороги, боли в костях, остеопороз и другие нарушения (табл. 3).
Прогноз заболевания при серьезной экзокринной недостаточности ПЖ напрямую зависит от готовности пациента выполнять рекомендации врачей, в частности, отказаться от алкоголя. 50% больных с выраженным панкреатитом, продолжающих употреблять алкоголь, умирают в течение 5–12 лет. И напротив, категорический отказ от спиртного является единственным этиотропным методом лечения алкогольного ХП. Важна и диета, особенно ее соблюдение во время первого приема пищи (категорически запрещен прием жирной, острой или копченой пищи натощак). Для фармакотерапии ХП применяются препараты следующих групп:
- анальгетики;
- спазмолитики;
- синтетические аналоги соматостатина;
- антисекреторные средства.
Как подчеркнул профессор Ю.П. Успенский, полиферментная терапия рекомендована больным с выраженным болевым абдоминальным синдромом, клиническими проявлениями расстройств пищеварения и мальабсорбции, длительным анамнезом заболевания, пациентам с прогрессирующим снижением массы тела. В силу физиологической обусловленности назначение таблетированных форм полиферментных препаратов при ХП более эффективно для купирования абдоминальной боли панкреатического происхождения, так как они активируются еще в проксимальном отделе двенадцатиперстной кишки (при pH = 5,0–6,5) и создают функциональный покой ПЖ. Использование таблетированных форм позволяет также эффективно устранять проявления внешнесекреторной недостаточности ПЖ7–9.
Одним из таких препаратов является Мезим®форте 10000, содержащий оптимальный состав ферментов в физиологической пропорции. Эффективность препарата Мезим® 10000 доказана в рандомизированных открытых сравнительных клинических исследованиях по оценке клинической эффективности препаратов Мезим® 10000 и капсулированного микрогранулированного панкреатина в аналогичной дозировке по липазе (Креон® 10000) в лечении ХП. Данные исследования были проведены на кафедре гастроэнтерологии Военно-медицинской академии им. С.М. Кирова МО РФ (Санкт-Петербург) в 2003 г. под руководством д.м.н., профессора В.Б. Гриневича и И.В. Богданова и в Клинике пропедевтики, гастроэнтерологии и гепатологии им. В.Х. Василенко ММА под руководством В.Т. Ивашкина и О.С. Шифрина в 2009 г.
Данные исследования доказали, что Мезим® 10000 более эффективен при лечении панкреатической боли, чем капсулированные формы панкреатина (p < 0,05), и обеспечивает сравнимую с капсулированными микрогранулированными препаратами панкреатина компенсацию недостаточности внешнесекреторной функции ПЖ (табл. 5). На фоне терапии Мезимом 10000 осложнения в виде запоров регистрируются существенно реже, чем при аналогичной терапии капсулированными микрогранулированными препаратами панкреатина (p < 0,05), что позволяет рекомендовать Мезим® 10000 в качестве препарата выбора для больных с болевой формой ХП и с умеренными проявлениями внешнесекреторной недостаточности ПЖ. На сегодняшний день ультразвуковое исследование (УЗИ) является одним из лидирующих методов медицинской визуализации. Как отметил в начале своего выступления д.м.н., профессор В.В. МИТЬКОВ (заведующий кафедрой ультразвуковой диагностики ГБОУ ДПО «РМАПО» МЗ РФ), о высокой востребованности данного метода свидетельствует тот факт, что только в системе Министерства здравоохранения РФ имеется около 25 000 ставок врачей ультразвуковой диагностики.
Ультразвуковые волны были впервые применены в медицине для диагностики опухолей головного мозга неврологом Венского университета Карлом Теодором Дюссиком в конце 30-х годов прошлого века. Первые приборы для ультразвуковых исследований не позволяли получать двухмерное изображение – на экране отображалась одномерная амплитудная кривая. Аппарат, способный демонстрировать двухмерное изображение, хотя бы отдаленно напоминающее то, к которому мы привыкли сегодня, был разработан Дугласом Ховри в 1951 г. С тех пор прошло много лет. Эра полностью цифрового ультразвука, ставшего сегодня «золотым стандартом» диагностики многих заболеваний, началась в 1996 г. с появления цифровой ультразвуковой диагностической системы Acuson Sequoia 512.
Перспективным направлением ультразвуковой диагностики является применение ультразвуковых контрастных веществ. К сожалению, в России на сегодняшний день не зарегистрировано ни одного ультразвукового контрастного вещества, в то время как в Европе ультразвуковые контрастные вещества широко применяются для диагностики различных заболеваний. Они, например, весьма информативны для дифференциальной диагностики заболеваний печени: при использовании ультразвукового контрастного вещества ультразвуковое исследование оказывается сопоставимо по точности с магнитно-резонансной томографией с контрастным усилением, притом что стоимость ультразвукового исследования на порядок ниже.
Эластография и эластометрия – диагностические методики, работающие на основе ультразвука и позволяющие давать в том числе и количественную информацию о механических (упругих) свойствах тканей. Они получили распространение в исследовании печени, молочной, щитовидной и предстательной желез. В последнее время появились работы, посвященные использованию трехмерной эластографии, но пока рано говорить о клиническом применении данной методики. Большой интерес с практической точки зрения вызывает и трехмерная эхография, применяемая сегодня преимущественно в акушерстве. Ультразвуковое исследование применяется не только в диагностике – под контролем этого метода проводятся пункции и другие малоинвазивные вмешательства, например радиочастотная абляция, HIFU-абляция (ультразвуковая абляция).
Ультразвуковая диагностика является динамично развивающейся областью клинической медицины. Наряду с большим количеством преимуществ, эхография обладает одним существенным ограничением: ее эффективность в гастроэнтерологии напрямую зависит от подготовки пациента. Например, наличие газов в кишечнике может сделать исследование малоинформативным или совершенно неинформативным. Для улучшения информативности ультразвукового исследования применяется препарат Эспумизан®. Его способность повышать точность эхографии доказана рядом исследований. В одном из них применение Эспумизана позволяло визуализировать при ультразвуковом исследовании патологические структуры (метастазы в печени, полипы желчного пузыря и др.), которые не были видны без предварительной подготовки. Это свойство препарата стало основанием для включения Эспумизана в рекомендации Российской ассоциации специалистов ультразвуковой диагностики в медицине по применению препарата для подготовки к ультразвуковому исследованию.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.