количество статей
7385
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
XXI Национальный конгресс по болезням органов дыхания: Баланс эффективности и безопасности антибиотикотерапии: уроки доказательной медицины
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Пульмонология и оториноларингология" №1
- Аннотация
- Статья
- Ссылки
При выборе антибактериальной терапии врач должен руководствоваться принципами эффективности и безопасности. Следует назначать препараты с доказанной эффективностью в отношении основных возбудителей инфекций, хорошим профилем безопасности и высоким уровнем комплаентности. Большой проблемой остается клиническая и терапевтическая эквивалентность оригинальных препаратов и дженериков, которые во многих случаях не отвечают указанным требованиям. Эти и другие важные вопросы антибактериальной терапии обсуждались на сателлитном симпозиуме компании «Тева», организованном в рамках XXI Национального конгресса по болезням органов дыхания.

Профессор Р.С. Козлов
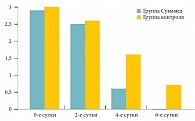
Рис. 1. Динамика субъективных симптомов риносинусита

Профессор А.Ю. Овчинников

Профессор А.И. Синопальников

К.м.н. О.У. Стецюк
Профессор Р.С. Козлов затронул вопросы этиологии инфекционных заболеваний дыхательных путей – одних из наиболее распространенных в амбулаторной практике, которые являются самой частой инфекционной причиной преждевременной летальности (18%). Около 40% от общего числа острых риносинуситов и острых средних отитов, а также минимум 50% внебольничных пневмоний вызывают S. pneumoniae. В развитии инфекционного обострения хронической обструктивной болезни легких (ХОБЛ) наибольшее значение имеет H. influenzae (32%), которая наряду с S. pneumoniae является причиной около 30% от общего числа острых риносинуситов и 38% средних отитов. Роль M. catarrhalis в России довольно невелика – на ее долю приходится не более 1–2% острых риносинуситов и острых средних отитов и инфекционных обострений ХОБЛ. К сожалению, резистентность к антимикробным препаратам у S. pneumoniae отмечается во всех странах мира. S. pneumoniae обладает способностью вырабатывать устойчивость к пенициллину, другим бета-лактамам, тетрациклинам, ко-тримоксазолу, хлорамфениколу, фторхинолону и др.
Основная проблема резистентности H. influenzae и M. сatarrhalis заключается в их устойчивости к пенициллинам за счет выработки бета-лактамаз.Ведущими антимикробными средствами в лечении дыхательных путей остаются бета-лактамы, макролиды и респираторные фторхинолоны (следует помнить, что последние не разрешены к применению у детей). Среди макролидов клинически значимой активностью в отношении H. influenzae обладают только два – азитромицин и кларитромицин, причем азитромицин обладает более высокой природной активностью. Резистентность S. pneumoniae к азитромицину в России на протяжении многих лет сохраняется на низком уровне, не превышая 6–7%. Профессор Р.С. Козлов затронул еще один важный вопрос – качества антимикробных препаратов, который приобретает особое значение с точки зрения роста резистентности микроорганизмов. Если качество оригинального препарата тщательно контролируется производителем, то дженерики часто не обладают подтвержденной терапевтической эквивалентностью.
Об этом свидетельствуют результаты неопубликованного исследования фармацевтической эквивалентности внутривенных форм азитромицина, в рамках которого сравнивались оригинальный препарат – Сумамед («Тева») – и дженерические препараты – Азитрал и Азинорт. Применялся метод высокоэффективной жидкостной хроматографии, который позволяет определить концентрацию и стабильность активного вещества в растворе. В оригинальном препарате содержалась стабильная концентрация азитромицина, в то время как концентрация активного вещества в отдельных флаконах одного из дженериков падала до 75%, а другого – до 90%. Таким образом, было показано, что исследованные дженерики не являются фармацевтически эквивалентными оригинальному препарату и не могут выступать в качестве его адекватной терапевтической замены. Можно представить, насколько не соответствуют оригиналу таблетированные формы этих же производителей. Между тем использование даже маленьких доз таких псевдодженериков опасно, потому что может привести к неуклонному росту устойчивости микроорганизмов.
В заключение профессор Р.С. Козлов подчеркнул, что необходимо бережно относиться к существующим эффективным антибиотикам, потому что в ближайшее время появления новых препаратов для лечения дыхательных путей ожидать не приходится. Профессор, д.м.н. А.Ю. ОВЧИННИКОВ образно назвал путь развития антибактериальной терапии от начала ее возникновения до сегодняшнего дня «великим шелковым путем». Несмотря на то что с 1928 г. антибиотики успешно помогают бороться с микроорганизмами, инфекционные заболевания остаются ведущей причиной смертности в странах с различным уровнем экономического развития. Как отметил профессор А.Ю. Овчинников, помимо роста резистентности микроорганизмов, о которой говорил профессор Р.С. Козлов, существует еще одна проблема – назначение системных антибиотиков без соответствующих показаний: в 22 из 92% случаев антибактериальная терапия при риносинуситах назначается необоснованно.
Другая проблема – неправильный выбор препарата или назначение неадекватной дозировки. В качестве примера можно назвать назначение ранних макролидов (эритромицин) при H. influenzae или ранних фторхинолонов (ципрофлоксацин, офлоксацин) и пероральных цефалоспоринов III поколения, не обеспечивающих надежной эрадикации возбудителя, для лечения инфекции, вызванной S. pneumoniae. Профессор А.Ю. Овчинников обратил внимание также на нелогичное комбинирование антибактериальных препаратов, назначение антибиотиков с несовместимыми препаратами; нерациональную замену антибактериальных препаратов (ранее 48–72 часов, в результате чего невозможно проследить активность этого препарата); а также несоблюдение больным правил приема антибактериального препарата. К наиболее эффективным антибиотикам для системной терапии острого риносинусита среднетяжелого и тяжелого течения относятся бета-лактамы, «новые» макролиды (кларитромицин и азитромицин) и респираторные фторхинолоны. Особенно популярен среди оториноларинголов азитромицин. Спектр активности азитромицина является оптимальным при инфекциях дыхательных путей.
Он включает грамположительные и грамотрицательные кокки, грамотрицательные палочки, внутриклеточные микроорганизмы, анаэробные возбудители. Если говорить о чувствительности S. рneumoniae к азитромицину, то она достаточно высокая и не уступает чувствительности к ряду других антибактериальных препаратов. В отношении H. influenzae, согласно исследованию, проведенному С.В. Сидоренко в Москве, азитромицин по эффективности сравним с фторхинолонами, которые относятся к препаратам второй линии терапии. Если говорить о безопасности препаратов макролидного ряда, то с 1965 по 2008 г. в базе публикаций PubMed из 25 зарегистрированных случаев пируэтной тахикардии, индуцированной макролидами, у лиц старше 80 лет не было ни одного случая, связанного с приемом азитромицина. Профессор А.Ю. Овчинников отметил, что причиной недостаточной эффективности антибиотиков может стать использование некачественных дженериков. В Первом МГМУ им. И.М. Сеченова в 2004 г. было проведено исследование, в основу которого были положены данные комплексного клинико-инструментального и лабораторного обследования и лечения 50 больных бактериальным риносинуситом (25 больных в основной группе, 25 больных в контрольной группе), которые находились на стационарном лечении в клинике болезней уха, горла и носа.
Целью исследования было изучение клинической эффективности и безопасности применения препарата Сумамед в сравнении с дженериком, названным условно «азитромицин А», у пациентов с острым бактериальным риносинуситом. Методика исследования была стандартной, включавшей оториноларингологическое обследование, рентгенографию, компьютерную томографию околоносовых пазух, бактериологическое исследование (мазок слизистой оболочки среднего носового хода, анализ пунктата из верхнечелюстной пазухи, ПЦР-диагностика атипичной микрофлоры). Основная группа получала Сумамед по 500 мг 1 раз в день, контрольная группа – «азитромицин А» по 500 мг 1 раз в день, курс приема составил 3 дня. Всем пациентам были назначены деконгестанты – ксилометазолин по 2 дозы в каждую половину носа первые 3 дня, далее по необходимости. Результаты лечения оценивали на основании объективных и субъективных признаков.
Динамика субъективных симптомов риносинусита (головная боль, заложенность носа, гнойный насморк) представлена на рисунке 1. После курса антибиотикотерапии положительный результат был достигнут в основной группе у 85,7% пациентов, в группе контроля – у 62,5%, отрицательный результат в основной группе составил всего 2,4%, в группе контроля – 15,4%. Таким образом, подчеркнул профессор А.Ю. Овчинников, врач должен не только определить оптимальный антимикробный препарат, но и помнить о качестве антибиотика, без которого эффективное лечение невозможно. В начале своего доклада д.м.н., профессор, зав. кафедрой пульмонологии РМАПО А.И. СИНОПАЛЬНИКОВ очертил круг слагаемых эффективной антибактериальной терапии внебольничных инфекций нижних дыхательных путей, к числу которых отнес:
- активность антимикробных препаратов (АМП) в отношении основных бактериальных возбудителей респираторных инфекций;
- оптимальные параметры легочной фармакокинетики/фармакодинамики АМП;
- приемлемый профиль безопасности;
- удобный режим дозирования;
- доказанную в ходе рандомизированных клинических исследований (РКИ) высокую терапевтическую эффективность АМП.
- при первом типе обострения ХОБЛ (увеличение объема мокроты, усиление гнойности мокроты, появление или усиление одышки в течение ≥ 2 последовательных дней);
- при втором типе обострения ХОБЛ (наличие двух из перечисленных выше признаков, одним из которых должно быть усиление гнойности мокроты);
- при тяжелом обострении ХОБЛ, осложненном развитием острой дыхательной недостаточности.
Переходя к анализу рандомизированных клинических исследований, А.И. Синопальников подчеркнул, что их результаты свидетельствуют о сопоставимой терапевтической эффективности «новых» макролидов (азитромицин – Сумамед), бета-лактамов и «респираторных» фторхинолонов у больных с нетяжелым течением ВП. Столь же высокую терапевтическую результативность демонстрирует азитромицин (Сумамед) и при лечении больных, переносящих инфекционное обострение ХОБЛ. Наряду с доказанной клинической эффективностью весьма важным, особенно для больных с внебольничными инфекциями нижних дыхательных путей, получающих лечение на дому, является и комплаентность, то есть приверженность пациента врачебным рекомендациям. При этом самыми надежными способами ее повышения являются простой режим дозирования (желательно 1 р/сут) и непродолжительный прием АМП. В этом контексте наиболее привлекательным представляется применение азитромицина, прием которого (500 мг 1 р/сут) в течение трех последовательных дней оказывается сопоставимым по эффективности с 10-дневной терапией амоксициллином/клавуланатом, кларитромицином и др.
В этой связи не случайно «новые» макролиды (прежде всего азитромицин) упоминаются на страницах современных международных и национальных рекомендаций в числе препаратов выбора в лечении нетяжелой ВП (в частности, лечение в амбулаторных условиях больных без серьезных сопутствующих заболеваний, не принимавших в течение последних 3 месяцев АМП) и «простого» обострения ХОБЛ. В заключение своего доклада А.И. Синопальников представил результаты недавно опубликованного многоцентрового российского фармакоэпидемиологического исследования (С.А. Рачина и соавт., 2011), согласно результатам которого азитромицин является самым часто назначаемым АМП у амбулаторных больных ВП. Безопасность и переносимость назначенного лечения имеют не менее важное значение, чем его эффективность. По имеющимся данным, нежелательные лекарственные реакции, вызванные антибактериальными препаратами, являются причиной 20% случаев обращений за неотложной медицинской помощью, связанных с побочными эффектами медикаментозной терапии. Нежелательные лекарственные реакции – это вредные и непредвиденные эффекты, которые возникают при применении лекарственных средств в терапевтических дозах в целях профилактики, лечения или диагностики.
Как отметила к.м.н. О.У. СТЕЦЮК (кафедра клинической фармакологии Смоленской государственной медицинской академии Минздравсоцразвития России), если препарат обладает терапевтически значимым эффектом, он также обладает и нежелательными побочными реакциями. К сожалению, фармакоэпидемиология нежелательных побочных реакций в нашей стране изучена недостаточно. Источниками данных о нежелательных побочных реакциях до регистрации лекарственного средства являются результаты клинических исследований. В большинстве случаев они позволяют выявить только те нежелательные побочные реакции, которые встречаются с достаточно высокой частотой, например, 1 на 10 или на 100 случаев применения препарата. Нежелательные побочные реакции, встречающиеся реже, достаточно сложно определить до внедрения препарата в практику. Этим объясняются случая изъятия с рынка уже зарегистрированных препаратов.
Все нежелательные побочные реакции, возникающие после разрешения применения препарата в клинической практике, регистрируются в системе Фармаконадзора. Учитываются данные пострегистрационных клинических исследований, результаты ретро- и проспективного мониторинга в лечебных учреждениях, фармакоэпидемиологических исследований, метаанализов, социологических исследований. Одним из наиболее распространенных способов регистрации побочных реакций является метод так называемых спонтанных сообщений, когда пациенты, врачи или фармацевтические компании сообщают о случаях развития побочных реакций при использовании того или иного лекарственного средства. По законодательству РФ врач обязан сообщать о непредвиденных побочных реакциях препарата. Согласно оценкам, в нашей стране с населением в 142 млн человек ежегодно в Фармаконадзор должно поступать 40–60 тысяч сообщений о нежелательных побочных реакциях. Между тем на практике их поступает примерно в 10 раз меньше. Прежде всего, это связано с недостаточной осведомленностью врачей, а также с отсутствием времени для регистрации побочных эффектов, боязнью служебного или судебного расследования.
По данным мониторинга распространенности различных нежелательных побочных реакций в поликлинических учреждениях г. Москвы, наиболее часто реакции отмечаются при применении препаратов для лечения сердечно-сосудистых заболеваний – бета-блокаторов, антагонистов кальция. Антибиотики занимают 4-е место и являются причиной 13,5% случаев всех нежелательных побочных реакций. По частоте возникновения аллергических реакций лидирует ко-тримоксазол, на втором месте – линкозамиды и только на третьем – пенициллины. Макролиды в этом списке занимают последнее место. Помимо аллергических реакций в клинической практике могут отмечаться гепато-, нефро-, нейро-, кардио- и гематотоксичность, а также поражение костно-мышечного аппарата. Еще один важный аспект – влияние антибактериальной терапии на функции желудочно-кишечного тракта. Диспепсические расстройства часто встречаются при применении различных групп антибактериальных препаратов. При назначении эритромицина и амоксициллина/клавуланата высока вероятность развития диареи, однако такое серьезное нарушение, как антибиотикоассоциированная диарея, практически не встречается при применении макролидных антибиотиков.
В последнее время довольно активно обсуждается проблема гепатотоксических реакций на антибактериальные препараты. В апреле 2010 г. Федеральный центр мониторинга безопасности лекарственных средств опубликовал письмо, содержащее информацию о возможности развития редких, но потенциально тяжелых гепатотоксических реакций при приеме азитромицина. Поиск в базе данных Национальной медицинской библиотеки США Medline позволил обнаружить описания всего 4 случаев обратимой гепатотоксичности у взрослых пациентов, принимавших азитромицин, причем трое пациентов принимали другие потенциально гепатотоксичные лекарственные средства. В российской системе регистрации нежелательных побочных реакций не было зарегистрировано ни одного случая гепатотоксических реакций, связанных с приемом азитромицина. Профессор Ю.Б. Белоусов в своей статье «Лекарственные поражения печени, ассоциируемые с макролидами. Очевидна ли связь?» указывает, что гепатотоксичность свойственна всем макролидным антибиотикам, причем чем больше доза, тем выше риск данной нежелательной побочной реакции.
Если сравнивать используемые суточные и курсовые дозы макролидов, то для обычной лекарственной формы азитромицина стандартная курсовая доза составляет 1,5 г, для азитромицина пролонгированного действия – 2 г, для остальных макролидов, особенно первого поколения, – от 7 до 20 г на курс лечения. Таким образом, риск гепатотоксичности для азитромицина является минимальным. О.У. Стецюк ознакомила участников симпозиума с письмом НИИ антимикробной химиотерапии по поводу проблемы гепатотоксичности азитромицина, которое было поддержано ведущими экспертами – оториноларингологами и пульмонологами, Российским обществом ринологов, МАКМАХ. В письме указано, что более чем 20-летний опыт успешного применения азитромицина в клинической практике подтверждает его безопасность для пациентов. В связи с этим «…единичные случаи гепатотоксичности азитромицина, зарегистрированные в мире, не должны лимитировать его применение в клинической практике, и мы не вправе лишать наших пациентов возможности получать лечение доступным, эффективным и безопасным антибиотиком, каковым, несомненно, является азитромицин», подчеркнула в заключение О.У. Стецюк.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.