количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Болевая диабетическая нейропатия: международный опыт комбинированной терапии
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эндокринология" №6
- Аннотация
- Статья
- Ссылки
К началу XXI века рост заболеваемости сахарным диабетом (СД) превзошел самые неутешительные прогнозы. Диабетическая болевая нейропатия (ДН) является одним из наиболее распространенных осложнений СД. В лечении ДН габапентин занимает лидирующую позицию, так как является структурным аналогом нейротрансмиттера гамма-аминомасляной кислоты (ГАМК), играющей существенную роль в модуляции и трансмиссии боли.
Габапентин взаимодействует с моноаминовыми рецепторами, уменьшает приток кальция в пресинаптический нейрон, стабилизирует мембраны и увеличивает порог деполяризации, усиливает синтез ГАМК. Анальгезирующий эффект препарата реализуется на уровне спинного мозга. Показано, что при сочетании габапентина и комплекса нейротропных витаминов – B1, B6 и B12 – возможно достижение более быстрого эффекта при использовании меньших доз препаратов.
К началу XXI века рост заболеваемости сахарным диабетом (СД) превзошел самые неутешительные прогнозы. Диабетическая болевая нейропатия (ДН) является одним из наиболее распространенных осложнений СД. В лечении ДН габапентин занимает лидирующую позицию, так как является структурным аналогом нейротрансмиттера гамма-аминомасляной кислоты (ГАМК), играющей существенную роль в модуляции и трансмиссии боли.
Габапентин взаимодействует с моноаминовыми рецепторами, уменьшает приток кальция в пресинаптический нейрон, стабилизирует мембраны и увеличивает порог деполяризации, усиливает синтез ГАМК. Анальгезирующий эффект препарата реализуется на уровне спинного мозга. Показано, что при сочетании габапентина и комплекса нейротропных витаминов – B1, B6 и B12 – возможно достижение более быстрого эффекта при использовании меньших доз препаратов.
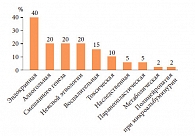
Рис. 1. Распространенность различных этиологических видов нейропатий (по данным при госпитализации)
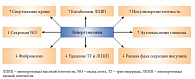
Рис. 2. Негативные эффекты гипергликемии

Рис. 1. Распространенность различных этиологических видов нейропатий (по данным при госпитализации)
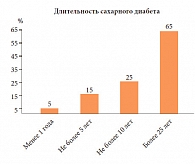
Рис. 3. Частота диабетической нейропатии в зависимости от длительности сахарного диабета

Таблица 2. Этапность диагностики и лечения пациентов с диабетической нейропатией
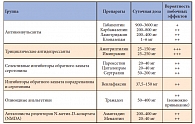
Таблица 3. Препараты, используемые для купирования нейропатической боли
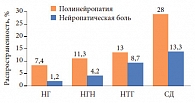
Рис. 4. Распространенность полинейропатии и нейропатической боли
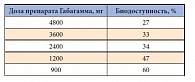
Таблица 4. Дозозависимая биодоступность препарата Габагамма
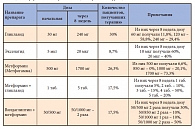
Таблица 5. Пероральная сахароснижающая терапия и коррекция доз
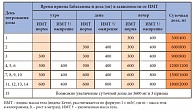
Таблица 6. Принципы титрования дозы препарата Габагамма
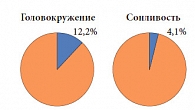
Рис. 5. Частота побочных явлений

Таблица 7. Динамика субъективной симптоматики нейропатии на фоне монотерапии габапентином

Таблица 8. Основные свойства препаратов Габагамма и Мильгамма
Сахарный диабет (СД) можно назвать «болезнью цивилизации». К началу XXI века заболеваемость СД перешагнула планку самых неутешительных прогнозов. По данным Международной диабетической федерации (IDF, International Diabetes Federation), в настоящее время СД страдают 366 млн человек. Полинейропатия на сегодняшний день рассматривается как заболевание всего организма с реализацией патологического процесса на уровне периферической нервной системы в виде множественного поражения периферических нервов. Среди различных видов полинейропатии эндокринная нейропатия занимает лидирующую позицию – ее частота составляет 40% (рис. 1) [1].
Диабетическая нейропатия (ДН) является одним из наиболее распространенных осложнений СД. По данным эпидемиологических исследований, в зависимости от используемых методов обследования частота выявления ДН при СД варьирует от 5% до 100%. Такой разброс значений обусловлен различиями в используемых критериях диагностики ДН. Частота верификации ДН при впервые выявленном СД 2 типа составляет 7,5%. Однако через 25 лет после установления диагноза более 50% пациентов имеют те или иные проявления ДН. Основным фактором риска развития ДН является декомпенсация СД (рис. 2) [2]. В ходе исследования DCCT (Diabetes Control and Complications Trial) было продемонстрировано, что достижение компенсации СД с начала заболевания снижает риск развития ДН на 69%, а обеспечение компенсации СД на любом этапе заболевания – на 57% [3]. В настоящее время индивидуализированы целевые значения гликемии (табл. 1) [4]. При планировании целей лечения необходимо учитывать следующие показатели:
- возраст пациента;
- наличие тяжелых осложнений СД и сопутствующие патологии;
- ожидаемая продолжительность жизни;
- тяжелые гипогликемии в анамнезе и риск их развития в будущем и др.
ДН повышает смертность больных СД, в основном это происходит за счет такой формы ДН, как кардиальная автономная нейропатия, косвенно – из-за осложнений, в частности, синдрома диабетической стопы и его последствий. Нейропатия лежит в основе 50–75% всех нетравматических ампутаций при СД [5–7]. Частота выявления ДН зависит о ряда факторов: «cтажа» диабета, компенсации заболевания, пола пациента, возраста пациента, антропометрических показателей пациента, сопутствующих заболеваний и др. Так, было доказано, что длительность СД коррелирует с частотой выявления ДН (рис. 3) [8].
При прогрессировании ДН наблюдается определенная стадийность. Если первые две стадии – раздражение (парестезии) и повреждение (онемение и нарушение рефлексов) – являются обратимыми, то третья и четвертая – дегенерация (структурные изменения нервов) и некроз – необратимы. Таким образом, раннее выявление СД 2 типа, а следовательно, и его осложнений, как и своевременное назначение терапии, позволит предотвратить переход ДН в более тяжелую стадию. При этом курация пациента с СД должна быть комплексной и включать наблюдение эндокринологом, неврологом, кардиологом, офтальмологом, подиологом и другими специалистами. Так, согласно «Алгоритмам специализированной медицинской помощи больным сахарным диабетом» [4], в диагностике и лечении ДН должны соблюдаться этапность и преемственность (табл. 2).
Важно учитывать, что наиболее тяжелым и травмирующим, по мнению пациента с ДН, является ощущение боли. По данным исследования MONICA/KORA [9, 10], при СД повышена распространенность полинейропатии и нейропатической боли (рис. 4). Согласно определению экспертов Международной ассоциации по изучению боли (IASP, International Association for Study of Pain), «боль – неприятное ощущение и эмоциональное переживание, связанное с реальным или потенциальным повреждением тканей или описываемое в терминах такого повреждения». Боль – не только особый психофизиологический феномен, но и важнейший симптом многих различных по природе и тяжелых острых и хронических заболеваний и патологических процессов. Боль в процессе онтогенеза – постоянный спутник и важнейшая составляющая жизни человека.
Боль сигнализирует о возникновении повреждений целостности наружных и внутренних тканей и органов. Она информирует также о грозящей опасности дальнейших нарушений. Боль вызывает отрицательное психоэмоциональное состояние и стимулирует устранение этого негативного ощущения. Длительно существующая боль сопровождается изменением физиологических параметров (повышение уровня артериального давления, пульса, расширение зрачков, изменение концентрации ряда гормонов и т.д.). Однако следует учитывать, что на приеме врач может столкнуться как с болевыми, так и безболевыми вариантами поражений при СД [11]. Среди болевых форм нейропатий выделяют острую и хроническую [12].
Продолжительность острой болевой формы составляет 6 месяцев. Появляются колющие, стреляющие, ноющие боли в стопах и голенях; чувство жжения, онемения, стягивания стоп. Интенсивность болевого синдрома может усиливаться в вечернее и ночное время. Для хронической нейропатии характерно наличие болевой симптоматики в течение свыше полугода. Клиническая картина болевого синдрома разнообразна по интенсивности и частоте. Характерные жалобы больного, данные анамнеза (давность симптоматики, наличие сопутствующей патологии), данные объективного осмотра помогают диагностировать ДН. Одним из основных исследований, проводимых врачом на амбулаторном приеме, является определение нарушения различных видов чувствительности. Для купирования болевого синдрома целесообразно комплексное воздействие, включающее проведение следующих мероприятий:
- Нормализация показателей углеводного обмена.
- Применение медикаментозных методов купирования болевого синдрома, включающее использование препаратов следующих групп:
- местные анестетики;
- опиоидные препараты;
- центральные миорелаксанты;
- антидепрессанты;
- антиконвульсанты и др.
3. Использование немедикаментозных методов воздействия, к которым относятся методы, усиливающие активность антиноцицептивных систем:
- акупунктура;
- чрескожная электронейростимуляция;
- стимуляция спинного мозга;
- физиотерапия;
- биологическая обратная связь;
- психотерапия;
- методы блокады и нейрохирургические методы лечения (разрушение зоны вхождения заднего корешка), блокирующие поступление ноцицептивной афферентации и др.
В таблице 3 систематизированы данные по использованию основных групп препаратов для купирования и лечения нейропатической боли у пациентов с СД. Препараты группы антиконвульсантов применяются в лечении нейропатической боли с 1960-х гг., когда с этой целью был впервые использован карбамазепин. Позднее, в 1993 г., Управление США по надзору за качеством пищевых продуктов и лекарственных средств (FDA, Food and Drug Administration) одобрило применение препарата габапентина при парциальных судорогах, в 1997 г. доказана эффективность этого препарата при лечении нейропатической боли. В период с 1998 по 2003 г. терапию габапентином получили 8,7 млн человек. Важно отметить, что не зафиксировано ни одного случая осложнений, угрожающих жизни пациента. Механизм действия препарата основан на следующих «точках воздействия» [13]:
- усиление синтеза гамма-аминомасляной кислоты (ГАМК) (нейромедиатор, участвующий в процессах центрального торможения);
- модулирующее действие на NMDA-рецепторы;
- блокада альфа-2-дельта-субъединицы кальциевых каналов, препарат не связывается с другими субъединицами кальциевого канала;
- снижение высвобождения моноаминов (адреналина, ацетилхолина, серотонина и др.);
- уменьшение синтеза и транспорта глутамата (медиатор боли);
- уменьшение частоты потенциалов действия периферических нервов;
- взаимодействие с моноаминовыми рецепторами;
- уменьшение притока ионов кальция в пресинаптический нейрон;
- стабилизация мембран;
- увеличение порога деполяризации.
Биодоступность препарата габапентина Габагаммы (антиконвульсант последнего поколения) уменьшается с увеличением дозы препарата, таким образом, при суточной дозе 900 мг биодоступность составляет 60% (табл. 4). Сотрудниками кафедры эндокринологии и диабетологии ГБОУ ДПО РМАПО на протяжении 3 месяцев проводилось обследование и лечение пациентов с СД. В исследовании наблюдалось 57 пациентов с СД 2 типа, с диагностированной ДН. Длительность СД составила от 2 до 25 лет. Средний возраст включенных в исследование пациентов составлял 59,7 ± 11 лет. На начальном этапе все пациенты прошли обучение в специализированной школе для больных СД, где пристальное внимание было уделено правилам подиатрического ухода. На протяжении всего периода наблюдения пациенты активно мониторировали уровень гликемии натощак и через 2 часа после основных приемов пищи. В таблице 5 обобщены данные по получаемой пациентами пероральной сахароснижающей терапии. На фоне активной сахароснижающей терапии лишь 36,8% пациентов достигли целевых значений уровня HbA1c, остальные пациенты отметили лишь положительную динамику. По данным анализа предшествующего лечения, в 43,8% случаев проводилась ежегодная терапия препаратами группы альфа-липоевой кислоты, 35% пациентов систематически получали лечение витаминами группы B. При этом 8,8% пациентов отметили, что им ни разу не проводилось лечения, направленного на устранение проявлений или профилактику ДН. Из наблюдаемых пациентов только 42,1% систематически наблюдались у невролога и подиатра, а 57,9% – только у эндокринолога.
Пациенты методом случайных чисел были разделены на 2 группы. В первой группе пациентам проводилась терапия препаратом Габагамма («Вёрваг Фарма», Германия), во второй – использовалось сочетание препаратов Габагамма и Мильгамма («Вёрваг Фарма», Германия). Инъекционный курс Мильгаммы составил 10 дней с дальнейшим переходом на прием драже Мильгамма композитум (в стандартной дозе). Препарат группы габапентина – Габагамма – применялся в течение 8 недель. Первые 4 недели проводилось титрование дозы по стандартной схеме (табл. 6) [14]. Максимальная доза была достигнута к 4-й неделе лечения и составила 1200 мг утром и 1800 мг вечером. При анализе побочных явлений у 11% пациентов отмечены головокружение и сонливость, что соответствует данным международных исследований [15]. Однако при постепенном титровании дозы и применении более высокой дозы препарата в вечернее время частота нежелательных явлений уменьшалась. На рисунке 5 представлены данные о частоте побочных явлений, наблюдаемых у пациентов, участвовавших в исследовании.
На наш взгляд, из противосудорожных препаратов наиболее рационально применение Габагаммы в дозе 1800 мг/сут и выше, поскольку, в отличие от карбамазепина, габапентин хорошо переносится, почти не вызывает сонливости и оказывает достаточный терапевтический эффект – уровень доказательности А для ДН с болевым синдромом. Габапентин является структурным аналогом нейротрансмиттера ГАМК, играющей существенную роль в модуляции и трансмиссии боли. Он взаимодействует с рецепторами моноаминов, уменьшает приток кальция в пресинаптический нейрон, усиливает стабилизацию мембран и увеличивает порог деполяризации, усиливает синтез ГАМК. Анальгезирующий эффект препарата реализуется на уровне спинного мозга.
С патогенетической точки зрения у пациентов с СД оправдано применение нейротропных витаминов группы B, которые блокируют механизмы гипергликемической памяти и образование конечных продуктов гликирования. Тиаминдифосфат – производное тиамина (витамин B1) – является коферментом ряда ферментов, участвующих в углеводном обмене. Недостаток тиамина ведет к нарушению окисления углеводов, а в тканях – к накоплению недоокисленных продуктов обмена, изменению пластического и энергетического обеспечения жизненных функций организма.
Согласно данным недавно проведенного в Латинской Америке многоцентрового рандомизированного открытого сравнительного клинического исследования [16], у пациентов с умеренно выраженной ДН комбинация габапентина в сочетании с витаминами B1 и B12 обеспечивала значительно более выраженный анальгетический эффект, чем прием прегабалина. В этом исследовании 323 пациента наблюдались в течение 12 недель, из них 52% пациентов получали комбинацию габапентина с витаминами группы B, 48% получали прегабалин. Эффективность обезболивания оценивалась по показателям визуально-аналоговой шкалы (ВАШ) и шкалы LANSS (Leeds Assessment of Neuropathic Symptoms and Signs – Лидский опросник для оценки симптомов нейропатии).
Было отмечено, что в группе габапентина ослабление боли наблюдалось при величине дозы 900 мг в сутки (p < 0,001), в группе прегабалина – при использовании дозы 150 мг в сутки. Частота побочных эффектов в группе комбинации «габапентин + витамины группы B» была ниже, чем в группе прегабалина, – у 65 (44,52%) из 146 пациентов и у 76 (52,41%) из 145 пациентов соответственно. Анальгетический эффект в обеих группах к концу 12-й недели терапии был одинаковым и изменился с 6,5 мм до 2,5 мм по шкале ВАШ (p < 0,562). Таким образом, при одинаковой выраженности анальгетического эффекта профиль безопасности комбинации габапентина с витаминами группы B превосходил профиль безопасности прегабалина [16].
Учитывая, что сочетание витаминов группы B обеспечивает торможение ноцицептивных нейронов в дорсальных ядрах спинного мозга и в ядрах таламуса за счет стимуляции норадренергических и серотонинергических антиноцицептивных систем [17], а также данные зарубежных исследований, в нашем исследовании к терапии габапентином 11 пациентам был добавлен нейротропный комплекс – комбинация витаминов B1, B6 и B12. Уже через 9–10 дней отмечена положительная динамика – уменьшение болевого синдрома, улучшение чувствительности – болевой и тактильной. В таблице 7 суммирована динамика жалоб пациентов.
Средняя доза габапентина в группе пациентов, получавших комбинацию «габапентин + витамины группы B», была ниже, чем в группе монотерапии габапентином, и составила 900 мг (300–300–300 мг). Габапентин и комплекс витаминов B, воздействующие на патогенетические аспекты формирования проявлений ДН, при совместном применении существенным образом ускоряют анальгетическое действие друг друга за счет взаимной кумуляции эффекта: значительное ослабление боли и жжения в группе пациентов, принимавших комбинированную терапию, наблюдалось уже на 10-й день терапии. Пациенты, получавшие только габапентин, отметили ослабление боли и жжения только на 15–30-й день терапии. В таблице 8 систематизированы основные «направления воздействия» терапии, а также некоторые другие характеристики изучаемых препаратов. Помимо медикаментозных воздействий огромную роль в профилактике поздних осложнений СД имеют следующие немедикаментозные методы:
- систематическое и адекватное обучение больных в специализированной школе;
- активный самоконтроль уровня гликемии не только натощак, но и постпрандиально;
- уход за ногами;
- работа с семьей пациента с целью повышения приверженности лечению. Так, еще Гиппократ писал: «Врач должен не только сам делать все от него зависящее, но и уметь направить на пользу больного его самого, его домашних и все его окружение»;
- применение методов разгрузки стоп;
- использование хорошо подобранной обуви, исключающей механическое повреждение кожи стоп;
- применение ортопедических приспособлений, стелек, обуви, которые уменьшают повышенное давление на проблемные участки стоп, то есть значительно снижают угрозу развития язвенных дефектов стоп, натоптышей и, в конечном счете, ампутаций конечностей;
- активное наблюдение больных группы высокого риска развития язвенных дефектов, специализированная подиатрическая и терапевтическая помощь также значительно снижают частоту ампутаций нижних конечностей у больных СД.
Таким образом, комплексное применение медикаментозного и немедикаментозного воздействия позволит предупредить потерю трудоспособности и раннюю инвалидизацию вследствие неврологических осложнений СД, а также повысить качество жизни пациента с СД.
1. Ахвердиева М.К. Диабетическая вегетативная кардиальная нейропатия // Южно-Российский медицинский журнал. 2004. № 2. С. 15–26.
2. Hanefeld M. Postprandial hyperglycaemia: noxious effects on the vessel wall // Int. J. Clin. Pract. Suppl. 2002. № 129. P. 45–50.
3. Albers J.W., Herman W.H., Pop-Busui R. et al. Effect of prior intensive insulin treatment during the Diabetes Control and Complications Trial (DCCT) on peripheral neuropathy in type 1 diabetes during the Epidemiology of Diabetes Interventions and Complications(EDIC) Study // Diabetes Care. 2010. Vol. 33. № 5. P. 1090–1096.
4. Алгоритмы специализированной медицинской помощи больных сахарным диабетом / Под ред. И.И. Дедова, М.В. Шестаковой. 5-й вып. М., 2011.
5. Дедов И.И., Анциферов А.С. Основные задачи здравоохранения по выполнению Сент-Винсентской декларации, направленной на улучшение качества лечебно-профилактической помощи больным сахарным диабетом // Проблемы эндокринологии. 1992. Т. 2. № 1. С. 4–12.
6. Betteridge D.J. Epidemiology of the сardiac сomplications of type 2 diabetes mellitus // Medicographia. 2001. Vol. 23. P. 95–99.
7. Metzger B.E., Coustan D.R. Summary and recommendations of the Fourth International Workshop-Conference on Gestational Diabetes Mellitus. The Organizing Committee // Diabetes Care. 1998. Vol. 21. Suppl. 2. P. B161–B167.
8. Балаболкин М.И. Эндокринология. М.: Универсум паблишинг, 1996. С. 28–29.
9. Ziegler D., Rathmann W., Dickhaus T. et al. Neuropathic pain in diabetes, prediabetes and normal glucose tolerance: the MONICA/KORA Augsburg Surveys S2 and S3 // Pain Med. 2009. Vol. 10. № 2. P. 393–400.
10. Ziegler D., Rathmann W., Dickhaus T. et al. Prevalence of polyneuropathy in pre-diabetes and diabetes is associated with abdominal obesity and macroangiopathy: the MONICA/KORA Augsburg Surveys S2 and S3 // Diabetes Care. 2008. Vol. 31. № 3. P. 464–469.
11. International Guidelines on the Out-patient Management of Diabetic Peripheral neuropathy. Abingdon: The Medicine Group (Education) Ltd., 1998.
12. Kempler P. Neuropathies. Budapest: Springer, 2002.
13. Зинченко В.П., Долгачева Л.П. Внутриклеточная сигнализация. Пущино, 2003.
14. Guidance on the Use of Gabapentin. VHA Pharmacy Benefits Management Strategic Healthcare Group and the Medical Advisory Panel.
15. Sandercock D., Cramer M., Wu J. et al. Gabapentin extended release for the treatment of painful diabetic peripheral neuropathy: efficacy and tolerability in a double-blind, randomized, controlled clinical trial // Diabetes Care. 2009. Vol. 32. № 2. P. e20.
16. Alpizar M., Mimenza A.J. Gabapentin/vitamins B1/B12: an efficacious and safe combination for painful diabetic peripheral neuropathy control S479 // EASD 2012.
17. Reyes-García G., Medina-Santillán R., Terán-Rosales F. et al. Characterization of the potentiation of the antinociceptive effect of diclofenac by vitamin B complex in the rat // J. Pharmacol. Toxicol. Methods. 1999. Vol. 42. № 2. P. 73–77.
Новости на тему
02.02.2024
21.09.2023
СТАТЬИ по теме
Отправить статью по электронной почте
Ваш адрес электронной почты:
К началу XXI века рост заболеваемости сахарным диабетом (СД) превзошел самые неутешительные прогнозы. Диабетическая болевая нейропатия (ДН) является одним из наиболее распространенных осложнений СД. В лечении ДН габапентин занимает лидирующую позицию, так как является структурным аналогом нейротрансмиттера гамма-аминомасляной кислоты (ГАМК), играющей существенную роль в модуляции и трансмиссии боли.
Габапентин взаимодействует с моноаминовыми рецепторами, уменьшает приток кальция в пресинаптический нейрон, стабилизирует мембраны и увеличивает порог деполяризации, усиливает синтез ГАМК. Анальгезирующий эффект препарата реализуется на уровне спинного мозга. Показано, что при сочетании габапентина и комплекса нейротропных витаминов – B1, B6 и B12 – возможно достижение более быстрого эффекта при использовании меньших доз препаратов.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
