Антибактериальные, противогрибковые, противовирусные и иммуномодулирующие эффекты лизоцима: от механизмов к фармакологическому применению
- Аннотация
- Статья
- Ссылки
- English
Введение
Для лечения инфекционно-воспалительных заболеваний полости рта и глотки создано множество препаратов для местного применения, действие которых основано на антисептических свойствах. Вместе с тем разрушение болезнетворных микроорганизмов при использовании большинства таких препаратов носит неселективный характер, и антисептики в той или иной степени подавляют рост симбионтов/комменсалов. В связи с этим логичной представляется стратегия, ориентированная прежде всего на естественные антимикробные молекулы, к которым симбионты/комменсалы в ходе длительной коэволюции приобрели устойчивость. Такая биоценозосберегающая стратегия одновременно с подавлением роста патогенов в полости рта и глотке обеспечивает сохранение механизмов колонизационной резистентности, препятствующих затяжному течению и повторному возникновению инфекций указанных биотопов.
Лизоцим рассматривается как краеугольный камень врожденного иммунитета у большого числа таксономически далеких друг от друга представителей животного мира. У разных животных лизоцим обладает гидролитическими свойствами и способен расщеплять бета-1,4-гликозидную связь между N-ацетилмурамилом и N-ацетилглюкозаминилом пептидогликана – главного полимера бактериальной клеточной стенки. Идентифицированы три основных типа лизоцима: c (куриный, или обычный), g (гусиный) и i (беспозвоночный). У человека и в белке куриного яйца присутствует главным образом c-тип, который стал объектом углубленных исследований [1].
Цель настоящего обзора – осветить основные биологические и фармакологические свойства лизоцима как филогенетически древней молекулы, обеспечивающей не только врожденную защиту от патогенных бактерий, грибов и вирусов, но и иммунный гомеостаз в полости рта и ротоглотке. Это обусловлено тем, что лизоцим, в частности выделенный из белка куриных яиц, давно привлекает внимание разработчиков лекарственных средств как фармакологическая субстанция. Кроме того, эффективность лизоцим-содержащих препаратов клинически доказана. Однако практикующие врачи зачастую недостаточно осведомлены о спектре биологического/фармакологического действия лизоцима, что приводит к недооценке потенциальной пользы препаратов, содержащих эту молекулу, в ряде клинических ситуаций.
Антибактериальное действие
Полость рта и глотка служат входными воротами для патогенных микроорганизмов. Неудивительно, что в этом биотопе, в частности в слюне, присутствует значительное количество разнообразных антимикробных молекул [2], среди которых особое место занимает лизоцим.
Известно два механизма уничтожения лизоцимом бактерий [3]:
- ферментативный: гидролиз бета-1,4-гликозидной связи между N-ацетилмурамилом и N-ацетилглюкозаминилом пептидогликана клеточной стенки бактерий. Указанное ферментативное свойство объединяет все типы лизоцима разного происхождения и отражено в одном из широко используемых вариантов названия этого белка – мурамидазе;
- катионный: молекулы лизоцима встраиваются в клеточную мембрану бактерий, образуя в ней поры. Благодаря этому механизму лизоцим не только вызывает осмотическую гибель бактериальной клетки, но и увеличивает проницаемость мембран бактерий для других антимикробных молекул, в том числе антибактериальных фармакологических веществ [4].
Наличие двух взаимодополняющих бактерицидных механизмов снижает вероятность полного ускользания патогенных бактерий от антибактериального действия лизоцима. В случае модификации структуры пептидогликана, увеличивающей устойчивость микроорганизма к ферментативному действию лизоцима, и даже при полной потере клеточной стенки (L-формы) бактерии a priori должны в той или иной степени сохранить чувствительность к катионным механизмам этого белка.
Противовирусное действие
С учетом того что ряд заболеваний полости рта и ротоглотки, по поводу которых назначают лизоцим-содержащие топические препараты, имеют вирусную или сочетанную этиологию, особого внимания заслуживает противовирусный эффект лизоцима. Установлено, что подобный эффект характерен для типов лизоцима разного природного происхождения.
Одним из первых (в 1973 г.) противовирусное действие этого белка описал H. Arimura. По его данным, лизоцим, выделенный из плаценты человека, снижал адсорбцию вируса эктромелии на поверхности клеток. Это позволило сделать предположение о важной защитной роли данного белка во время беременности, когда некоторые другие звенья противоинфекционной защиты частично подавлены [5].
S. Lee-Huang и соавт. через четверть века продемонстрировали способность лизоцима белка куриного яйца, а также человеческого лизоцима с-типа, выделенного из разных источников (моча, молоко и нейтрофилы), дозозависимо подавлять репликацию ВИЧ-1 в культурах Т-лимфоцитов и моноцитов, чувствительных к этому вирусу. Обращает на себя внимание широкий диапазон концентраций (0,01–10 мкг/мл), в котором этот белок демонстрировал виростатические эффекты. При этом даже самые высокие концентрации лизоцима, использованные в работе, не оказывали цитотоксического действия на Т-клетки и моноциты [6].
Чуть позже было обнаружено свойство лизоцима связывать ДНК и РНК. Мотивационным триггером исследования стало выявление сходства строения лизоцима и гистонов по данным рентгеноструктурного анализа кристаллизованных белков. Взаимодействие лизоцима и родственных молекул с нуклеиновыми кислотами, подтвержденное разными методами (гель-электрофорез, определение ферментативной активности, соосаждение), позволило авторам сформулировать тезис о том, что именно данное свойство лизоцима лежит в основе его способности подавлять репликацию ВИЧ-1, а возможно, и других вирусов [7].
Для определения структурных компонентов, ответственных за анти-ВИЧ-эффекты лизоцима, проведены фрагментация этого белка и картирование функциональной активности составных пептидов. Идентифицировано два пептида, состоящих из 18 и 9 аминокислот (HL18 и HL9), соответствующих фрагментам 98-115 и 107-115 лизоцима человека. HL18 и HL9 оказались мощными ингибиторами репликации и инфекционной активности ВИЧ-1. При этом изменение аминокислотной последовательности или замена ключевых остатков аргинина или триптофана в этих пептидах приводили к потере противовирусного действия. Установлено, что HL9 (ArgAlaTrpValAlaTrpArgAsnArg) является наименьшим пептидом, полностью воспроизводящим анти-ВИЧ-эффекты лизоцима. Этот нанопептид блокирует проникновение в клетки-мишени и репликацию ВИЧ-1, а также модулирует экспрессию ряда генов ВИЧ-инфицированных клеток. В нативном лизоциме человека HL9 образует альфа-спираль и не связан с участками белка, обеспечивающими мурамидазную (бета-1,4-гликозидазную) активность [8].
Не исключено, что этот нанопептид, не идентифицированный в тканях или жидкостях человека, может появляться в естественных условиях в результате биодеградации лизоцима под влиянием трипсина или других протеаз [9].
Поскольку в клинической практике используется лизоцим, получаемый из белка куриных яиц, внимания заслуживает недавняя работа, посвященная изучению противовирусных свойств лизоцима яиц представителей отряда куриных. M. Behbahani и соавт. определяли анти-ВИЧ-1-активность и ее возможные механизмы у лизоцима, выделенного из белка яиц курицы, индейки и перепела. Показано, что все варианты лизоцима, особенно выделенные из белка яиц перепела и курицы, увеличивают устойчивость мононуклеарных клеток периферической крови к заражению ВИЧ-1. Лизоцим птичьих яиц обладает высоким сродством к молекуле СD4 – главной мишени ВИЧ-1 и снижает частоту и интенсивность экспрессии этой молекулы в культуре мононуклеаров периферической крови. Любопытно, что экспрессия других молекул, облегчающих вход ВИЧ-1 в клетки, в частности хемокиновых рецепторов CCR5 и CXCR4, не менялась в результате обработки мононуклеаров лизоцимом птичьих яиц. Авторы пришли к заключению, что лизоцим ограничивает прикрепление ВИЧ-1 к молекуле CD4 на мембране клеток-мишеней [10].
Противовирусные свойства лизоцима описаны и в других таксонах. Например, вирусная инфекция у голубых креветок Litopenaeus stylirostris стимулирует экспрессию гена лизоцима, а внутримышечная инъекция рекомбинантного белка, идентичного лизоциму креветок, увеличивает устойчивость этих ракообразных к заражению вирусом синдрома белого пятна (WSSV). Кроме того, лизоцим восстанавливает клеточные и гуморальные врожденные механизмы защиты, подавленные WSSV [11].
Вероятно, лизоциму как эволюционно древней и весьма консервативной молекуле врожденного иммунитета у разных видов животных присуща способность оказывать разные по молекулярным механизмам, но универсальные противовирусные эффекты в отношении различных вирусов.
Противогрибковое действие
Противогрибковые эффекты лизоцима, в частности в отношении Candida albicans и Coccidioides immitis, впервые были описаны на рубеже 1960–70-х гг. [12–14]. Примерно тогда же появились первые работы, указывавшие на способность лизоцима потенцировать эффективность противогрибковых средств, в частности амфотерицина В, в отношении названных грибов [15]. Однако конкретные механизмы реализации фунгицидного действия лизоцима долгое время оставались неизученными.
Позднее с помощью электронной и световой микроскопии было установлено, что подавление роста C. albicans микрограммовыми концентрациями лизоцима куриного яйца сопровождается рядом ультраструктурных изменений дрожжевых клеток, затрагивающих клеточную стенку грибов, периплазму и внутриклеточное пространство. Кроме того, доказано, что лизоцим увеличивает проницаемость цитоплазматической мембраны. Авторы предположили, что на C. albicans лизоцим воздействует с помощью двух различных взаимодополняющих механизмов: ферментативного гидролиза N-гликозидных связей, которые связывают полисахариды (маннаны) и структурные гликопептиды клеточной стенки (мурамидазоподобное действие), и повреждения цитоплазматической мембраны по катионному механизму [16].
В дальнейших исследованиях этой научной группы лизоцим вызывал дезорганизацию и уменьшение толщины внешних слоев клеточной стенки C. albicans, что подтверждает участие ферментативных (мурамидазоподобных) механизмов в фунгицидном действии лизоцима [17].
Очевидно, катионная природа лизоцима и его способность дезинтегрировать и увеличивать проницаемость клеточной мембраны грибов [18] дополняют энзиматически обусловленные противогрибковые эффекты лизоцима, что в целом сближает эти защитные механизмы с таковыми против бактерий.
В серии работ подтверждена способность лизоцима потенцировать эффективность антимикотических лекарственных средств, таких как полиены (нистатин, амфотерицин В) и азолы (флуконазол, ланоконазол), в отношении C. albicans [19–21].
Изучена чувствительность 16 клинических изолятов Cryptococcus neoformans к противогрибковым препаратам и/или лизоциму in vitro. Обнаружено, что лизоцим дозозависимым образом подавляет рост C. neoformans, хотя и не вызывает полной гибели грибковых клеток в концентрациях до 20 мкг/мл. Кроме того, лизоцим усиливает эффективность флуконазола и тербинафина, снижая их средние минимальные ингибирующие концентрации в полтора и восемь раз соответственно. Противогрибковая активность итраконазола под влиянием лизоцима дополнительно не увеличивается, что можно отчасти объяснить исходно высокой эффективностью этого препарата против C. neoformans [22].
Противогрибковые свойства лизоцима иногда остаются в информационной тени более изученных и известных практикующим врачам антибактериальных эффектов этой молекулы, что препятствует рациональному применению лизоцим-содержащих препаратов, в том числе в комбинации с антимикотическими средствами, при заболеваниях грибковой или связанной с грибами этиологии.
Разрушение лизоцимом биопленок бактерий и грибов
Антимикробное действие лизоцима обусловлено его способностью разрушать биопленки патогенных бактерий и грибов.
C. Sheffield и соавт. установили, что лизоцим в диапазоне концентраций 5–50 мкг/мл подавляет рост биопленок Escherichia coli и в еще большей степени Klebsiella pneumoniae [23].
В недавней работе лизоцим продемонстрировал способность разрушать биопленку Staphylococcus aureus и потенцировать противобиопленочное действие левофлоксацина в низких (ниже минимальных ингибирующих) концентрациях. Кроме того, ингаляционное применение липосом, содержащих комбинацию левофлоксацина и лизоцима, приводит к стойкому и выраженному подавлению образования биопленок, снижению микробной обсемененности, а также морфологических и молекулярных признаков воспаления в легких у крыс, инфицированных S. aureus [24].
Очевидно, лизоцим отвечает за описанную ранее способность нефракционированного белка куриных яиц подавлять адгезию и рост биопленок S. aureus [25].
Эти данные любопытны в свете информации о высокой резистентности большинства штаммов S. aureus к катионным и мурамидазным механизмам антибактериального действия лизоцима [26]. Вероятно, даже лизоцим-устойчивые штаммы патогена чувствительны к противобиопленочному действию этого белка.
В отношении влияния лизоцима на биопленки грибов информация более противоречива. Большинство специалистов высказывают мнение о способности лизоцима разрушать и предотвращать образование биопленок C. albicans [21]. Однако в недавней работе выявлена более сложная зависимость характера влияния лизоцима на рост биопленок от концентрации действующего белка и штаммовой принадлежности C. albicans. Вместе с тем данные этого исследования подтверждают, что в физиологических концентрациях (< 30 мкг/мл) лизоцим действует главным образом как ингибитор образования биопленок не только коллекционных штаммов C. albicans, но и клинических изолятов этого патогена [27].
Свойство лизоцима разрушать биопленки должно приниматься во внимание практикующими врачами, поскольку биопленки, с одной стороны, представляют собой серьезный физико-химический барьер, защищающий патогены от этиотропных препаратов [28], с другой – маскируют микроорганизмы от протективных иммунных механизмов хозяина [29].
Иммунодемпфирующий (противовоспалительный) эффект экстрацеллюлярного, в том числе введенного извне, лизоцима
Вторичное иммуномодулирующее действие лизоцима обычно рассматривается только в контексте высвобождения иммуностимулирующих низкомолекулярных фрагментов после разрушения пептидогликана клеточных стенок бактерий. Действительно, в результате мурамидазной активности лизоцим обеспечивает увеличение локального уровня NOD2- и NOD1-агонистов (мурамилпептидов) [30], известных как стимуляторы ключевых врожденных механизмов защиты от патогенных микроорганизмов [31–33].
Вместе с тем на моделях инфекций in vivo показано, что при дефиците лизоцима происходит не только экспансия K. pneumoniae, Streptococcus pneumoniae и некоторых других патогенов, но и снижение выработки противовоспалительных цитокинов, в частности интерлейкина 10 [34, 35].
Следует напомнить, что лизоцим – это не только антимикробный фактор слюны, молока, слезы и других биологических жидкостей, но и важнейшая составляющая микробицидных систем лизосом-фагоцитирующих клеток. Анализ биологических эффектов этого белка позволил S. Ragland и A. Criss сделать заключение, что характер влияния лизоцима на выраженность и сбалансированность иммунного ответа зависит от соотношения уровней экстрацеллюлярного и внутриклеточного разрушения клеточных стенок бактерий [3]. Функционирование экстрацеллюлярного, в том числе введенного извне, лизоцима в слюне и других биологических секретах снижает количество субстрата (нерасщепленного полимерного пептидогликана клеточных стенок бактерий) для интрацеллюлярного лизоцима в макрофагах и нейтрофилах и тем самым подавляет избыточную активацию этих клеток, миграцию провоспалительных клеток и окислительный стресс [36].
Доказано, что лизоцим может непосредственно связывать и нейтрализовывать экстрацеллюлярные прооксидантные медиаторы [37].
Лизоцим не только служит важнейшим фактором врожденной иммунной защиты против бактерий, вирусов и грибов, но и обладает иммунодемпфирующим (противовоспалительным) действием. Это необходимо учитывать при принятии решения о применении лизоцим-содержащих препаратов в клинических ситуациях, когда требуется в первую очередь подавить избыточное локальное воспаление.
Заключение
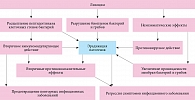
Основные векторы биологического действия лизоцима и связанные с ними фармакологические эффекты лизоцим-содержащих препаратов представлены на рисунке.
Широкая палитра биологического/фармакологического действия лизоцима является основой клинической эффективности лизоцим-содержащих препаратов при острых и хронических воспалительных заболеваниях ротоглотки и полости рта.
Включение лизоцим-содержащих препаратов в схему комплексного лечения указанных групп заболеваний имеет особую практическую ценность у детей, у которых концентрация и активность лизоцима в слюне несколько ниже, чем у подростков и взрослых [38]. Очевидно, этот факт наряду с незрелостью клеточных адаптивных реакций и возрастной недостаточностью выработки системно циркулирующего мономерного IgA и димерного секреторного IgA [39] вносит вклад в высокую восприимчивость детей к инфекциям верхних дыхательных путей, полости рта и глотки.
Бактерии-патогены полости рта и дыхательных путей уклоняются и/или подавляют функцию лизоцима [3]. Известно несколько вариантов уклонения бактерий от действия лизоцима:
- модификация пептидогликана клеточной стенки бактерий, снижающая его чувствительность к лизоциму (S. pneumoniae, S. aureus, Mycobacterium tuberculosis, St. suis, St. iniae, Enterococcus faecalis и др.);
- непосредственное подавление функции лизоцима (Pseudomonas aeruginosa, Legionella pneumophila, Neisseria spp. и др.);
- участие механизмов межклеточной химической коммуникации («чувство кворума») в формировании резистентности к лизоциму (St. pyogenes) [40].
Таким образом, целесообразно корректировать не только возрастной, но и вызванный патогенами дефицит функции лизоцима в полости рта и глотки у детей.
Среди лизоцим-содержащих препаратов по уровню доказательности выделяется препарат Лизобакт® (Босналек АО, Босния и Герцеговина), содержащий помимо лизоцима белка куриного яйца пиридоксин, наделяющий это лекарственное средство способностью предотвращать повреждение слизистой оболочки полости рта и потенцировать ее регенерацию. Наиболее авторитетная российская цитатно-аналитическая база научной литературы РИНЦ в ответ на запрос «лизобакт» в начале апреля 2018 г. выдавала 108 ссылок на научные труды с описанием либо оригинальных исследований, либо тех или иных аспектов клинического применения препарата и биологической функции лизоцима.
Доказана эффективность препарата Лизобакт® в лечении пациентов с острыми инфекциями дыхательных путей [41, 42] и реабилитации часто болеющих респираторными заболеваниями детей [43]. Особое значение приобретает использование этого лизоцим-содержащего препарата при обострениях хронических инфекций ЛОР-органов, прежде всего тонзиллитов и фарингитов, как у детей [44], так и у взрослых [45, 46]. Продемонстрирована клиническая эффективность препарата Лизобакт® у пациентов с воспалительными заболеваниями пародонта [47].
По данным ряда исследований, Лизобакт® способствует увеличению продукции секреторного IgA – важнейшей адаптивной составляющей мукозального иммунитета. Важно также, что у пациентов с острыми респираторными инфекциями, хроническими формами тонзиллита и фарингита, пародонтитом терапевтическое действие препарата коррелирует с коррекцией микробиологических сдвигов, в частности повышением уровня симбионтов/комменсалов и снижением степени колонизации полости рта и глотки патогенными и условно патогенными микробами. Это делает использование препарата Лизобакт® предпочтительным в сравнении с многими другими топическими антисептиками в рамках биоценозосберегающей стратегии при воспалительных заболеваниях ротоглотки [48] и пародонта [47].
Следует напомнить, что при назначении препарата Лизобакт® и других лизоцим-содержащих средств необходимо учитывать возможную гиперчувствительность к лизоциму как одну из причин аллергии у пациентов с сенсибилизацией к белкам куриного яйца и другие противопоказания, приведенные в инструкциях по применению. Это обеспечит не только эффективное, но и безопасное практическое использование данной плейотропной молекулы, характеризующейся рядом фармакологических свойств.
O.V. Kalyuzhin
I.M. Sechenov First Moscow State Medical University
Contact person: Oleg Vitalyevich Kalyuzhin, kalyuzhin@list.ru
The article highlights the biological properties and pharmacological effects of this phylogenetically ancient protein, some of which remain beyond the attention of physicians. Besides mechanisms of the antibacterial action of lysozyme, its antifungal, antiviral, anti-biofilm, immunomodulatory and anti-inflammatory effects are considered. In the oral cavity and pharynx, this protein provides not only innate protection against pathogenic bacteria, fungi and viruses, but also immune homeostasis. Topical application of lysozyme-containing drugs is expedient within the framework of therapeutic strategy for maintaining a healthy oral and pharyngeal microbiota, which is aimed simultaneously at suppressing the growth of pathogens in the oral cavity and pharynx and preserving the mechanisms of colonization resistance that impede persistence and recurrence of infections in these biotopes. Data on the clinical efficacy of a combination of lysozyme and pyridoxine in acute and chronic inflammatory diseases of the oropharynx and oral cavity correlating with the correction of microbiota and mucosal immunity of these biotopes are presented.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.