Диагностика дневной сонливости
- Аннотация
- Статья
- Ссылки
- English



Дневная сонливость (ДС) – состояние, характеризующееся неспособностью поддерживать достаточный уровень бодрствования в течение дня, сопровождающееся эпизодами неудержимой потребности в сне, приводящими к непреднамеренным засыпаниям. ДС может оказывать негативное влияние на качество жизни не только больного, но и членов его семьи, коллег и общество в целом. Данное состояние ассоциировано со снижением скорости психомоторных реакций, вследствие чего не только уменьшается производительность труда, но и повышается опасность для жизни самого больного и окружающих. Так, ДС становится причиной дорожно-транспортных происшествий примерно в 20% случаев [1].
Виды дневной сонливости
В настоящее время выделяют физиологическую, патологическую и субъективную сонливость [2].
Физиологическая сонливость – потребность человека в сне. Физиологическая сонливость отличается от патологической скоростью засыпания и способностью противостоять ей. Субъективная сонливость – ощущение сонливости в отсутствие таковой в реальности.
Причины дневной сонливости
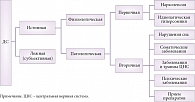
Причины развития ДС можно разделить на две группы:
- Заболевания, сопровождающиеся первичной недостаточностью систем бодрствования;
- Нарушения ночного сна, аффективные нарушения, прием некоторых лекарственных средств, а также различные неврологические и соматические заболевания (рис. 1).
Нарушения ночного сна
Самой частой причиной ДС у работающих считается синдром недостаточного сна, возникающий при регулярном ограничении длительности сна. У таких больных при обследовании не выявляют нарушений, которые могли бы привести к ДС. Они быстро засыпают, и их ночной сон качественный, однако его продолжительность ограничена в связи с различными социальными факторами. Раннее пробуждение приводит к несоответствию между потребностью в сне и его продолжительностью. При достижении достаточной продолжительности сна, например в отпуске, жалобы на ДС, как правило, отсутствуют.
Нарушения ночного сна – апноэ, синдром беспокойных ног и синдром периодических движений конечностей во сне также становятся причиной сонливости в дневное время. Синдром обструктивного апноэ сна в средней возрастной группе отмечается у 4% мужчин и 2% женщин [3]. Он чаще других первичных расстройств сна приводит к развитию ДС. Повторяющиеся эпизоды апноэ, гипопноэ и десатураций обусловливают увеличение количества электроэнцефалографических активаций (пробуждений). В результате нарушается структура сна. Он характеризуется фрагментарностью, снижением представленности глубоких стадий. Следствием хронической депривации глубоких стадий сна становятся неосвежающий сон, ДС, снижение когнитивных функций и др.
При синдроме обструктивного апноэ сна могут наблюдаться артериальная гипертензия (более выраженная в ночное время), легочная гипертензия, ожирение, сахарный диабет, снижение либидо. Синдром обструктивного апноэ сна следует заподозрить у пациентов с избыточной массой тела и резистентной к терапии артериальной гипертензией, предъявляющим жалобы на храп и остановку дыхания во сне, а также при деформации лицевого скелета и заболеваниях ЛОР-органов.
Синдром беспокойных ног характеризуется возникновением неприятных ощущений, чаще в ногах, также могут быть вовлечены другие части тела, при нахождении в состоянии покоя преимущественно в вечернее и ночное время, вынуждающих больного совершать облегчающие движения. Это нарушает засыпание и ведет к снижению общей продолжительности сна. Кроме того, в 75–80% случаев синдром беспокойных ног сочетается с синдромом периодических движений конечностей во сне, что может сопровождаться электроэнцефалографическими активациями и приводить к пробуждению больного.
Еще одна причина ДС – нарушение циркадианных ритмов. При синдроме задержки фазы сна время засыпания сдвигается на два и более часа позже принятого в данной социальной среде, при этом попытки уснуть в более раннее время не приводят к желаемому результату. Соответственно у таких пациентов утреннее пробуждение должно наступать позже, однако социальные факторы вынуждают их вставать раньше комфортного времени. Как следствие, больные жалуются на ДС в первой половине дня, снижение внимания и работоспособности. Смещение времени засыпания на два и более часа раньше желаемого или установленного называется синдромом ранней фазы сна. Последний характеризуется ДС преимущественно в вечернее время и пробуждением во второй половине ночи с невозможностью вновь заснуть. Диагноз «нарушение цикла „сон – бодрствование“» ставится на основании записей дневников больных или данных актиграфии, подтверждающих наличие сдвига привычного времени сна на более поздние или более ранние часы.
Повреждение центров бодрствования
К ДС может привести нарушение систем бодрствования. Состояние бодрствования поддерживается благодаря скоординированной работе нескольких центров: медиального парабрахиального ядра дорсальной покрышки мозга (глутаматергические нейроны), педункулопонтинного ядра (холинергические нейроны), вентральной области покрышки (дофаминергические нейроны), дорсальных и медиальных ядер шва (серотонинергические нейроны), синего пятна (норадренергические нейроны) [3]. Указанные ядра участвуют в активации таламуса, гипоталамуса, базальной области переднего мозга и мотонейронов спинного мозга и тормозят главный центр медленного сна, расположенный в вентролатеральной преоптической области. Основная роль в поддержании состояния бодрствования отводится орексинергической и гистаминергической системам, которые запускают вышеперечисленные центры бодрствования и активируют кору головного мозга.
Нарколепсия – заболевание, характеризующееся приступами непреодолимой ДС, полной или частичной утраты мышечного тонуса (катаплексией) и другими феноменами, связанными с фазой быстрого сна (фазой сна с быстрыми движениями глаз). Оно развивается при избирательном аутоиммунном поражении орексинергических нейронов латерального гипоталамуса.
Классическая клиническая картина заболевания складывается из пяти составляющих: ДС и императивных засыпаний, приступов катаплексии, гипнагогических и гипнопомпических галлюцинаций, катаплексии пробуждения (сонный паралич) и нарушения ночного сна. Полная нарколептическая пентада встречается редко и не является обязательной для постановки диагноза. Облигатным симптомом нарколепсии считается ДС.
В зависимости от наличия приступов катаплексии выделяют нарколепсию первого типа (с катаплексией) и второго типа (без катаплексии). У 90–95% больных нарколепсией первого типа определяется низкий уровень орексина в ликворе (< 110 пг/мл), что свидетельствует о поражении орексинергической системы [3]. При нарколепсии второго типа содержание орексина в ликворе не снижено, поэтому существует предположение, что это другое, отличное от нарколепсии первого типа заболевание или группа заболеваний. Патогенез нарколепсии второго типа до сих пор не установлен. К наиболее частым провоцирующим факторам относятся черепно-мозговая травма и вирусные инфекции. Если у пациентов с ДС впоследствии развиваются приступы катаплексии или снижается содержание орексина в ликворе, диагноз может быть изменен на нарколепсию первого типа.
С избыточной сонливостью днем и увеличением продолжительности ночного сна ассоциируется идиопатическая гиперсомния. В данном случае ДС должна быть подтверждена результатами множественного теста латентности сна (МТЛС) (средняя латентность ≤ 8 минут), суточной полисомнографии (общее время сна ≥ 660 минут) или актиграфии. Более чем у 30% больных длительность ночного сна превышает десять часов, при этом эффективность сна высокая – в среднем от 90 до 94% [3]. В 36–66% случаев отмечается тяжелая инерция сна (сонное опьянение). Кроме того, пациентам с идиопатической гиперсомнией дневной сон не приносит облегчения в отличие от пациентов с нарколепсией.
Другие причины
Жалобами на расстройства сна и бодрствования, в частности на затруднение засыпания, ночные пробуждения, низкое качество сна, неосвежающий сон, ДС, могут сопровождаться аффективные нарушения. Как правило, у таких больных указанные жалобы выходят на первый план, а нейропсихиатрические нарушения выявляются только после длительного общения с пациентами или их тестирования с использованием специализированных шкал. При этом на фоне терапии антидепрессантами наблюдается исчезновение не только нейропсихологической симптоматики, но и нарушений сна и бодрствования.
ДС может быть вторичной: развиться вследствие заболеваний центральной нервной системы (нейродегенеративных [4] и инфекционных заболеваний, опухолей, саркоидоза, острых нарушений мозгового кровообращения, черепно-мозговых травм, особенно при поражении гипоталамуса и ствола головного мозга); эндокринных и метаболических нарушений (гипотиреоза, печеночной энцефалопатии, хронической почечной недостаточности и др.). Кроме того, ДС может быть одним из проявлений наследственных заболеваний, таких как синдром Смита – Магениса, и миотонической дистрофии. В этом случае ДС – следствие сопутствующих нарушений дыхания во сне.
Причинами ДС также могут стать прием седативных, дофаминергических [4], нестероидных противовоспалительных средств, некоторых антибиотиков, спазмолитиков, антиаритмических средств. После отмены препарата симптомы, как правило, регрессируют. Если ДС сохраняется, рекомендуется проведение токсикологического анализа мочи и в случае отрицательных результатов дальнейшее обследование больного.
Методы диагностики
Шкалы
Эпвортская шкала сонливости (Epworth Sleepiness Scale – ESS) может применяться для диагностики ДС и оценки результатов лечения [5]. Она позволяет выявить гиперсомнию при различных заболеваниях. ESS представляет собой опросник. Пациенту предлагается оценить вероятность засыпания от 0 до 3 баллов в восьми монотонных ситуациях. При этом 0 баллов обозначает, что больной никогда не засыпает, 3 балла – существует высокая вероятность уснуть. Максимальная сумма баллов – 24 (табл. 1). Десять баллов и выше позволяют заподозрить ДС. Согласно результатам большинства исследований, такая оценка имеет самую высокую чувствительность и специфичность для диагностики ДС. В то же время ряд исследователей отмечают, что большая чувствительность соответствует 11 и 14 баллам.
Стэнфордская шкала сонливости (Stanford Sleepiness Scale – SSS) также позволяет провести оценку сонливости [6]. Пациент должен выбрать один из семи вариантов ответа, наиболее отражающий уровень сонливости непосредственно во время заполнения шкалы. К преимуществам SSS можно отнести простоту и возможность многократного повторного использования. К недостаткам – отсутствие нормативных данных и сложность сравнения результатов между пациентами.
Каролинская шкала сонливости (Karolinska Sleepiness Scale – KSS) по дизайну похожа на SSS. Однако больному предлагается выбрать уже не из семи, а из девяти утверждений, описывающих его состояние на данный момент [7]. Семь баллов и выше свидетельствуют о патологической сонливости. KSS широко применяется в клинической практике для оценки уровня сонливости у профессиональных водителей, работников нефтяной промышленности, машинистов, пилотов, а также в клинических исследованиях лекарственных средств.
Субъективная оценка, как правило, не отражает реальную выраженность ДС: часть пациентов аггравирует, другие, напротив, отрицают или уменьшают число эпизодов повышенной сонливости и императивных засыпаний. Последние могут описывать ДС как периоды снижения внимания и затруднения мышления или предъявлять жалобы на повышенную утомляемость и усталость. Известно, что ощущение ДС может нарушаться при длительной депривации сна. Поэтому при подозрении на синдром гиперсомнии может быть рекомендована беседа врача с родственником больного.
Тесты
Множественный тест латентности сна. Для объективной оценки ДС в клинической практике и научных целях применяются различные тесты. «Золотым стандартом» диагностики ДС является МТЛС [8]. Сонливость – это физиологическое состояние, предшествующее сну. Однако скорость, с которой происходит засыпание, отличается при нормальной и патологической сонливости. Показатель «время засыпания» (латентность сна) взят за основу МТЛС. Протокол исследования подразумевает от четырех до шести укладываний пациента в постель в затемненной комнате в течение дня с двухчасовыми интервалами. Во время каждого укладывания пациенту предлагается заснуть в течение 20 минут. Накануне исследования обязательно проводится ночная полисомнография для подтверждения получения достаточного времени сна, а также исключения расстройств ночного сна, которые могли бы привести к ДС. Результаты исследований показывают, что депривация сна перед МТЛС снижает латентное время сна и может привести к ложноположительным результатам.
При оценке данных учитывается среднее время засыпания и раннее начало фазы быстрого сна (в течение 15 минут после засыпания или начало сна с фазы быстрого сна). Поскольку крупные популяционные исследования с регламентированным протоколом проведения МТЛС отсутствуют, достаточной нормативной базы по указанному тесту на сегодняшний день не существует [9]. Однако установлено, что средняя латентность сна у здоровых добровольцев составляет от 10,4 ± 4,3 до 11,6 ± 5,2 минуты в зависимости от числа укладываний – четыре и пять соответственно. Учитывая, что 95% значений должно находиться в пределах двух стандартных отклонений от среднего, средняя величина латентности сна может составлять от 1,8 до 19 минут при четырех укладываниях и от 1,2 до 20 минут при пяти [9], что представляется сомнительным. Так, по данным метаанализа, средняя латентность сна 3,1 ± 2,9 минуты наблюдается, как правило, только у пациентов с нарколепсией (рис. 2). При идиопатической гиперсомнии этот показатель равен 6,2 ± 3,0 минуты [10]. Именно поэтому Американской академией медицины сна (American Academy Sleep Medicine) в качестве диагностического критерия гиперсомнии предложено ограничиться восемью минутами и менее [11]. Однако у некоторых больных гиперсомнией средняя латентность сна составляет более восьми минут. В подобных случаях требуется тщательный анализ клинической картины или проведение повторного МТЛС.
Так как МТЛС чувствителен к депривации сна, одновременно рекомендуется ведение дневников сна пациентами или выполнение актиграфии за неделю до исследования. Необходимо учитывать, что не всем пациентам достаточно шестичасового сна.
Как правило, два и более эпизода раннего начала фазы быстрого сна являются признаком нарколепсии. В то же время они могут фиксироваться и при синдроме обструктивного апноэ сна, нейродегенеративных и других заболеваниях, сопровождающихся поражением латеральных отделов гипоталамуса [12]. Следовательно, при выявлении эпизодов раннего начала фазы быстрого сна необходимо интерпретировать полученные данные с учетом клинической картины заболевания и данных ночной полисомнографии. При подозрении на нарколепсию показано также определение уровня орексина А (гипокретина 1) в ликворе. Снижение этого показателя является высокоспецифичным маркером заболевания.
Тест поддержания бодрствования (ТПБ) используется, как правило, в научных целях [10]. С его помощью оценивается способность пациента оставаться в состоянии бодрствования. ТПБ проводится в затемненной комнате. Больному, сидящему в удобном кресле, дается указание не засыпать как можно дольше, при этом запрещается заниматься деятельностью, требующей внимания, и физическими упражнениями. Средний показатель латентности сна определяется по результатам четырех тестов с интервалом между ними в два часа. Один тест длится от 40 до 60 минут (в зависимости от дизайна протокола). ТПБ применяют для оценки результатов лечения нарколепсии и синдрома обструктивного апноэ сна или диагностики ДС в качестве дополнительного метода к МТЛС. Сложность проведения данного исследования в клинической практике обусловлена отсутствием установленных границ нормы: средняя латентность сна менее восьми минут служит критерием постановки диагноза «гиперсомния», а интервал от 8 до 40 минут имеет неопределенную значимость. Необходимо отметить, что средняя латентность сна менее 19 минут – причина засыпания за рулем и возникновения дорожно-транспортных происшествий [12]. У здоровых лиц средняя латентность сна составляет 30,4 минуты.
Способность оставаться в состоянии бодрствования в течение всего времени проведения ТПБ подтверждает отсутствие гиперсомнии.
Психомоторные тесты – еще одна группа диагностических тестов. Такие тесты позволяют определить уровень сонливости по снижению способности сохранять активное внимание. Результаты психомоторных тестов могут быть ложноположительными, но не ложноотрицательными (табл. 2).
Один из наиболее часто используемых психомоторных тестов разработан D. Dinges и соавт. в 1985 г. – Psychomotor Vigilance Task (PVT) [13]. Испытуемый должен нажимать на кнопку каждый раз, когда на экране компьютера появляется светящаяся точка. Оцениваются скорость реакции и количество пропущенных точек. Результаты выполнения теста коррелируют с результатами SSS и МТЛС.
Протокол теста Oxford Sleep Resistance Test (OSLER) аналогичен протоколу ТПБ [14]. Пациент в течение 40 минут должен следить за появлением светового сигнала на экране и при его появлении нажимать на кнопку. Всего проводится четыре теста с интервалами в два часа. Испытание останавливается по истечении 40 минут или при значительном запаздывании реакции на сигнал, что свидетельствует о снижении способности поддерживать бодрствование.
Электрофизиологические методы
Актиграфия – объективный и доступный метод, который дает возможность выявить эпизоды засыпаний в дневное время, расстройства поведения в фазе быстрого сна, периодические движения конечностей во сне, нарушения циркадианных ритмов и установить общую продолжительность сна [15]. Актиграфия не требует пребывания пациента в клинике: современные приборы позволяют проводить запись в течение нескольких дней или недель. Как следствие, повышается вероятность фиксации эпизодов засыпаний. Актиграф выявляет движения и строит график суточной двигательной активности. Поэтому данные пожилых пациентов и пациентов с ограниченной физической активностью сложнее поддаются интерпретации. Актиграфия может использоваться как объективный метод диагностики, однако она не позволяет определить причины ДС, например апноэ сна.
Известно, что размер зрачков человека зависит от уровня освещенности и активности парасимпатической и симпатической систем. При засыпании парасимпатические влияния усиливаются и происходит сужение зрачков. Сонливость также приводит к снижению скорости реакции зрачков на источник света. Пупиллография использовалась в нескольких исследованиях для оценки уровня сонливости и выявления нарколепсии [16]. Несмотря на то что данный метод помогает объективизировать ДС, существуют серьезные ограничения для его применения в клинической практике. Первое ограничение – сложность исполнения. Второе – отсутствие четких критериев оценки нормальных и патологических значений.
С помощью автоматического анализа электроэнцефалограммы также можно установить уровень сонливости – электроэнцефалография, электроокулография и электромиография являются технической основой проведения МТЛС. При депривации сна увеличивается мощность спектра в дельта-диапазоне. Следовательно, это может быть критерием оценки уровня сонливости. Некоторые авторы, ссылаясь на то, что повышенная сонливость приводит к изменению реактивности центральной нервной системы, утверждают, что необходимо оценивать не электроэнцефалограмму покоя, а вызванные сенсорные потенциалы [16]. Использование данного метода ограничивается отсутствием стандартизации техники проведения исследования и нормативной базы. Кроме того, высокая степень индивидуальных различий существенно затрудняет его внедрение в клиническую практику.
Заключение
ДС относится к социально значимым расстройствам, поэтому требует пристального внимания специалистов. Активное изучение ДС позволило значительно расширить представление о причинах ее возникновения. Если пациент предъявляет жалобы на ДС, необходимо полноценно его обследовать и тщательно собрать анамнез. Первый шаг к эффективному лечению ДС – подтверждение гиперсомнии. В настоящее время существует широкий спектр субъективных и объективных инструментальных методов диагностики: шкалы, психомоторные и вегетативные тесты, электрофизиологические методы исследования. Основным методом диагностики считается МТЛС. В большинстве случаев данный тест позволяет поставить диагноз «гиперсомния» и провести ее дифференциальную диагностику. Однако иногда его бывает недостаточно, поскольку в настоящее время отсутствует полноценная нормативно-исследовательская база. Альтернативой МТЛС может стать ТПБ, однако он более сложен в проведении и интерпретации результатов. Самым простым и дешевым методом диагностики ДС являются шкалы, которые в случае необходимости можно дополнить другими методами. Приходится констатировать, что, несмотря на достаточный арсенал средств диагностики ДС, они все не идеальны и требуют дальнейшего совершенствования. Именно поэтому в сложных ситуациях необходимо применение нескольких диагностических методик.
O.V. Babkina, M.G. Poluektov, O.S. Levin
Russian Medical Academy of Postgraduate Education, Moscow
Contact person: Olga Viktorovna Babkina, med-ow@mail.ru
Many people periodically suffer from episodic excessive daytime sleepiness, but it is rarely leads to the serious consequences. In contrast, constant sleepiness seriously influences the patient’s quality of life, resulting in lack of social functioning and denial of driving. This review presents methods of estimation of daytime sleepiness considering its practical application.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.