Эффективность ведолизумаба у пациента с предшествующей терапией тремя препаратами анти-ФНО-альфа
- Аннотация
- Статья
- Ссылки
- English
Введение
Появление ингибиторов фактора некроза опухоли (ФНО) альфа кардинально изменило подход к лечению воспалительных заболеваний кишечника (ВЗК), обозначив перед врачами новые цели: достижение и поддержание беcстероидной ремиссии, профилактика осложнений ВЗК, предупреждение операций, снижение частоты госпитализаций по поводу обострения ВЗК, улучшение качества жизни. Однако часть пациентов, получающих препараты анти-ФНО-альфа, не отвечают на лечение (первичная неэффективность) или утрачивают ответ на препарат спустя время (вторичная неэффективность) [1–3]. Именно этим объясняется необходимость разработки новых методов лечения ВЗК, направленных на различные мишени, с использованием препаратов с более специфичным механизмом локального действия в органе воспаления.
Ведолизумаб – моноклональное антитело, блокирующее миграцию лейкоцитов в слизистую оболочку кишечника за счет ингибирования альфа-4-бета-7-интегрина. Препарат одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США и Европейским медицинским агентством в 2014 г., а также Министерством здравоохранения РФ в 2016 г. для лечения язвенного колита и болезни Крона умеренной и высокой активности [4, 5].
Исследования ведолизумаба
Эффективность ведолизумаба для индукции и поддержания ремиссии у пациентов с ВЗК доказана в клинических исследованиях GEMINI 1, 2 и 3 [6–11]. Кроме того, долгосрочная эффективность и безопасность препарата подтверждены результатами исследований долгосрочной безопасности (GEMINI-LTS), в которые были включены участники исследования GEMINI [10, 11]. Однако в аспекте реальной клинической практики участники клинических испытаний не являлись репрезентативными. Из всех пациентов, с которыми врачи сталкиваются в повседневной практике, только около трети могли бы соответствовать критериям включения в исследование GEMINI [12].
На сегодняшний день информация об эффективности и безопасности препарата в реальной клинической практике весьма ограниченна [12–20]. Недостаточно изучена долгосрочная эффективность ведолизумаба, поскольку лишь в трех исследованиях ее оценивали в течение года [15, 18, 20].
Сказанное подтверждает необходимость проведения дополнительных постмаркетинговых исследований для определения длительности применения, долгосрочной эффективности и безопасности препарата в условиях реальной клинической практики.
В многоцентровом международном исследовании ENEIDA, результаты которого были опубликованы в 2018 г., анализировали эффективность ведолизумаба при индукции клинической ремиссии к 14-й неделе в большой популяции пациентов с ВЗК и определяли предикторы ответа на терапию [21]. Кроме того, оценивали долгосрочную эффективность ведолизумаба, а также его безопасность в большой многоцентровой когорте пациентов с ВЗК [21].
В исследовании участвовала самая большая когорта пациентов с ВЗК, получавших ведолизумаб в реальной клинической практике. Период наблюдения также был самым продолжительным. Как показали результаты, ведолизумаб эффективен в реальной клинической практике даже в популяции пациентов с ВЗК, резистентных к предшествующей терапии. После индукционного курса две трети пациентов ответили на лечение, более 40% имели клиническую ремиссию. Определение на 14-й неделе терапии прогностических факторов наступления ремиссии позволило выявить подгруппу пациентов, у которых будет достигнут наилучший эффект. Установлено, что у пациентов с болезнью Крона, а также у пациентов с наиболее тяжелым течением болезни на исходном уровне (операции в анамнезе, высокий уровень С-реактивного белка (СРБ), высокая активность заболевания) реже наблюдается ремиссия на 14-й неделе исследования. Почти у 30% пациентов, ответивших на индукционный курс лечения, впоследствии развилась первичная неэффективность. После эскалации дозы препарата примерно у 60% пациентов ответ на терапию был восстановлен. Болезнь Крона (но не язвенный колит) и более высокий уровень СРБ после индукции служат независимыми факторами, связанными с утратой ответа на лечение.
В нескольких исследованиях с участием менее 300 пациентов в течение ограниченного периода наблюдения оценивали эффективность ведолизумаба в реальной клинической практике [12–20]. Согласно полученным результатам, около 80% пациентов ответили на лечение на 14-й неделе с учетом как ремиссии, так и ответа на терапию [12–14, 16]. Установлено, что использование препаратов анти-ФНО-альфа в анамнезе не связано с вероятностью достижения ремиссии на 14-й неделе [12–14, 16]. Кроме того, у пациентов с болезнью Крона ремиссия наблюдается реже, чем у пациентов с язвенным колитом. Это первое исследование, показавшее, что в условиях реальной клинической практики эффективность ведолизумаба у пациентов с язвенным колитом выше, чем у пациентов с болезнью Крона [21].
В большинстве исследований, основанных на популяционных данных, пациентов с болезнью Крона и пациентов с язвенной болезнью анализировали отдельно. Возможно, показатели были недостаточно высокими, чтобы продемонстрировать эту связь. Ни комбинированное лечение глюкокортикостероидами (ГКС), ни применение иммуномодуляторов не повышало ответ на лечение ведолизумабом на 14-й неделе в отличие от использования препаратов анти-ФНО-альфа. Некоторые врачи предлагают начинать лечение комбинацией ведолизумаба и ГКС для улучшения ответа на индукционный курс. Однако в исследовании ENEIDA присоединение ГКС во время индукционного курса не способствовало достижению лучших результатов. Кроме того, показано, что пациенты, получавшие ГКС во время индукции, реже достигали ремиссии на 14-й неделе. Это можно объяснить включением в исследование более тяжелых пациентов из тех, кто получал ГКС [14, 17]. В исследовании ENEIDA наблюдалась тенденция к более частому назначению ГКС более тяжелым пациентам (53, 62,7 и 67,0% при легком, среднетяжелом и тяжелом заболевании на исходном уровне соответственно; р = 0,045). Исследователи пришли к выводу, что ГКС нецелесообразно назначать во время фазы индукции пациентам с ВЗК, поскольку преимущество комбинации не доказано.
Ключевой вопрос терапии биологическими препаратами – влияние предыдущего лечения препаратами анти-ФНО-альфа на эффективность ведолизумаба. При проведении post-hoc-анализа исследований GEMINI оценивали эффективность ведолизумаба при болезни Крона и язвенном колите c учетом предыдущей терапии анти-ФНО-альфа [8, 22]. Последовательно продемонстрированы преимущества лечения ведолизумабом при индукции и поддержании клинического ответа и ремиссии как у пациентов с неэффективностью терапии анти-ФНО-альфа в анамнезе, так и у анти-ФНО-альфа-«наивных» пациентов, по сравнению с плацебо. Авторы отметили, что частота ответа и ремиссии у пациентов с болезнью Крона, не использовавших ранее препараты анти-ФНО-альфа, была выше, чем у пациентов, у которых в анамнезе имелись указания на неэффективность препаратов анти-ФНО-альфа [22]. Хорошие результаты сохранялись и на 52-й неделе. Аналогичные результаты наблюдались и у пациентов с язвенным колитом, не получавших ранее препараты анти-ФНО-альфа. У таких пациентов показатели ответа (абсолютная разница 15,5%) по сравнению с плацебо на шестой неделе были выше, чем у пациентов, ранее получавших анти-ФНО-альфа (абсолютная разница 7%). В то же время при поддерживающей терапии абсолютные различия с плацебо были одинаковы в обеих группах. При сравнении пациентов, получавших анти-ФНО-альфа-препараты, и анти-ФНО-альфа-«наивных» пациентов статистический анализ не проводился. Однако у больных, резистентных к анти-ФНО-альфа-терапии, наблюдалось более тяжелое течение болезни из-за продолжительности заболевания, более высокий уровень фекального кальпротектина, более высокий процент хирургических вмешательств, а также чаще регистрировались внекишечные проявления. Эти факторы тесно связаны с отсутствием ответа на биологические препараты, в том числе ведолизумаб.
В исследовании ENEIDA анализировали связь между неэффективностью ведолизумаба и проводимой ранее терапией анти-ФНО-альфа или более тяжелым течением заболевания [21]. Исследователи не наблюдали влияния предыдущего воздействия анти-ФНО-альфа на ранний или долгосрочный эффект (ремиссия на 14-й неделе: 57,6% пациентов, не получавших терапию анти-ФНО-альфа, 51,2% пациентов с неэффективностью одного препарата анти-ФНО-альфа, 44,0% пациентов с неэффективностью одного и более препарата анти-ФНО-альфа) [22].
В ряде исследований показан устойчивый эффект от лечения ведолизумабом в течение длительного периода времени [20]. В исследовании ENEIDA часть пациентов (приблизительно 30% в год) утрачивала ответ на лечение во время наблюдения. Частота случаев утраты ответа в нашей когорте была аналогична той, которая описана у пациентов, получавших препараты анти-ФНО-альфа после неэффективности предыдущей терапии анти-ФНО-альфа [23, 24]. Исследование GEMINI-LTS является продолжением III фазы исследования безопасности и эффективности ведолизумаба у пациентов с болезнью Крона и язвенным колитом – участников исследований C13004, GEMINI 1, 2 и 3. Недавно опубликованный промежуточный анализ данных исследования GEMINI-LTS [10, 11] показал, что частота ремиссии была стабильной на протяжении 152 недель наблюдения. Тем не менее пациенты, выбывшие из исследования, например из-за утраты ответа, не были включены в анализ. После того как это обстоятельство было принято во внимание, вновь рассчитанные показатели частоты ответа и ремиссии изменились. В зарегистрированной популяции пациентов с болезнью Крона в 71% случаев состояние ремиссии отмечалось на 52-й неделе, в 69% – на 104-й неделе, в 43% случаев – на 152-й неделе. Для пациентов с язвенным колитом эти показатели составили 74, 78 и 46% соответственно. Кроме того, такой эффект не зависел от предыдущей терапии анти-ФНО-альфа. Очень важно, что в когорте ENEIDA утрата ответа и эффективность препарата не были связаны с предыдущим использованием препаратов анти-ФНО-альфа.
В научной литературе продолжается дискуссия о том, следует ли назначать биологические препараты в комбинации с иммуномодуляторами для предотвращения утраты ответа, главным образом из-за иммуногенности. Несмотря на низкую иммуногенность ведолизумаба, в исследованиях GEMINI сопутствующие иммуномодуляторы приводили к снижению иммуногенности препарата [6, 7, 9]. Между тем в исследовании ENEIDA комбинированная терапия (ведолизумаб и иммуномодуляторы) не имела преимуществ перед ведолизумабом в качестве монотерапии как при индукции, так и в целях предотвращения утраты долгосрочного ответа [21].
Что касается безопасности, частота побочных эффектов в исследовании ENEIDA соответствовала таковой как в клинических, так и в других популяционных исследованиях [25]. Как и в других когортах, большинство пациентов могли продолжать лечение, менее 3% пациентов должны были прервать терапию ведолизумабом [21]. Наиболее распространенными побочными эффектами были инфекции (как правило, со стороны пазух носа и легких, а также желудочно-кишечные инфекции). За ними следовали инфузионные реакции и кожные проявления. Это также согласуется с более ранними результатами применения ведолизумаба [21].
Данные испытания GEMINI показали аналогичную общую частоту побочных эффектов ведолизумаба и плацебо, что также подтверждается кокрейновским обзором [26]. В исследовании ENEIDA ухудшение перианальных проявлений отмечалось у двух пациентов [21]. Подобное осложнение также описано в других популяционных когортах [12].
Исследование ENEIDA имеет несколько преимуществ перед регистрационными клиническими исследованиями. Самая большая по численности когорта пациентов с ВЗК, получавших ведолизумаб, и самое длительное наблюдение позволяют идентифицировать не описанные в популяционной когорте прогностические факторы краткосрочного ответа, эффективность препарата, а также определить долю пациентов, у которых со временем эффективность лечения утрачивается, и частоту прекращения лечения. В исследовании ENEIDA проведено сравнение между группами пациентов с язвенным колитом и болезнью Крона. В отличие от других наблюдательных исследований в исследовании ENEIDA участвовали только пациенты с активным заболеванием с целью получения более объективного стандартизированного ответа на терапию. Чтобы преодолеть потенциальную гетерогенность в клинической оценке, клиницистам было предложено рассчитать индекс Харви – Брэдшоу (для болезни Крона) и баллы по шкале Мейо (для язвенного колита) во время каждого посещения пациента. Оба индекса и их предельные значения были недавно рекомендованы организационным комитетом из 28 экспертов по ВЗК [27].
В долгосрочной перспективе часть пациентов прекращает лечение, обычно из-за утраты ответа. Эта цифра аналогична той, которая описана в когортах пациентов, резистентных к терапии анти-ФНО-альфа. Наконец, именно болезнь Крона, а не язвенный колит и более тяжелое течение заболевания ухудшают как краткосрочную, так и долгосрочную эффективность препарата. Между тем одновременное лечение иммуномодуляторами, видимо, не влияет ни на улучшение краткосрочного ответа, ни на предотвращение утраты ответа [21].
Исследователи пришли к заключению, что ведолизумаб эффективен даже в резистентной когорте пациентов с ВЗК, способствует достижению ремиссии или положительного эффекта у более чем 2/3 пациентов. На фоне применения препарата развивается минимальное количество побочных явлений [21]. В подтверждение сказанного приведем пример.
Клинический случай
Пациент А., 1986 года рождения. Диагноз язвенного колита установлен в мае 2011 г. на основании жалоб (жидкий стул до 12 раз в сутки c примесью крови и слизи) и данных колоноскопии (слизистая оболочка толстой кишки на всем протяжении резко гиперемирована, отечна; сосудистый рисунок отсутствует; складки не определяются; просвет кишки умеренно сужен за счет отека; множественные язвенные дефекты точечной и полигональной формы, покрытые фибрином; в просвете кровянистое и гноевидное содержимое; контактная кровоточивость умеренная). В соответствии с общепринятыми рекомендациями, проведена терапия преднизолоном 60 мг/сут, месалазином 4 г/сут, а также местная терапия (микроклизмы с дексаметазоном 4 мг). На фоне терапии стул стал регулярным – один раз в сутки (без примесей крови и слизи). Через два месяца после отмены преднизолона вновь отмечалось обострение заболевания – жидкий стул до десяти раз в сутки с примесью крови. Заболевание осложнилось гипоальбуминемией, железодефицитной анемией. Возобновлена терапия ГКС, проведена коррекция водно-электролитных и белково-энергетических нарушений, начата терапия иммуносупрессорами. Из-за высокой активности, непрерывного течения заболевания и формирования гормонозависимости с 15 января 2012 г. начата антицитокиновая терапия генно-инженерным биологическим препаратом (ГИБП) инфликсимабом по стандартной схеме 5 мг/кг. Пациент продолжал прием азатиоприна 150 мг/сут и месалазина 4 г/сут. На фоне проводимой терапии достигнута клинико-эндоскопическая ремиссия заболевания.
Контрольная колоноскопия от 2 апреля 2012 г.: слизистая оболочка слепой, восходящей, поперечно-ободочной кишок и дистального отдела сигмовидной кишки очагово гиперемирована. Сосудистый рисунок сглажен. Складки нормальной высоты. Слизистая оболочка остальных отделов розовая, гладкая, блестящая. Сосудистый рисунок усилен, перестроен. Единичные псевдполипозные разрастания до 0,3 см в диаметре. Контактная кровоточивость отсутствует.
С 2012 по 2015 г. на фоне терапии инфликсимабом в комбинации с иммуносупрессорами и месалазином пациент чувствовал себя удовлетворительно. Однако в декабре 2015 г. появился жидкий стул до 4–6 раз в сутки с примесью крови и слизи. Схема терапии оптимизирована за счет инфликсимаба (5 мг/кг массы тела каждые четыре недели). Несмотря на оптимизацию терапии, в течение шести месяцев сохранялся жидкий стул до четырех раз в сутки с примесью крови и слизи. Вследствие вторичной неэффективности инфликсимаба пациента перевели на другой ГИБП – препарат голимумаб. На фоне его применения зафиксирована положительная динамика – менее выраженная боль в животе, стул три-четыре раза в сутки, уменьшение примеси крови в стуле.
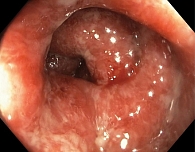
28 апреля 2016 г. выполнена контрольная ректосигмоколоноскопия: слизистая оболочка прямой, сигмовидной и нисходящей кишок гиперемирована, резко отечна. Сосудистый рисунок отсутствует. В просвете гноевидная слизь и кровь. Множественные сливные язвенные дефекты полигональной формы, некоторые из них занимают 1/3 окружности кишки. Выраженная контактная кровоточивость. Просвет этих отделов сужен за счет отека. Слизистая оболочка остальных отделов толстой кишки розовая, гладкая, блестящая с умеренной гиперемией и отеком на высоте складок в восходящей кишке. Сосудистый рисунок отчетливый. Циркулярные складки слизистой средней величины. Стенки кишки эластичные. Просвет кишки не деформирован, ее тонус сохранен. Заключение: язвенный колит, тотальное поражение. Прямая, сигмовидная и нисходящая кишки – активность процесса высокая (индекс Мейо – 8 баллов). Правые отделы – эндоскопическая ремиссия.
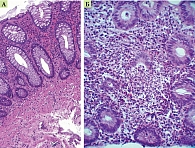
Гистологическое заключение: фрагменты слизистой оболочки толстой кишки с диффузной густой полиморфноклеточной инфильтрацией со значительной примесью эозинофильных гранулоцитов, полиповидной гиперплазией, нарушением гистоархитектоники кишечных крипт, очаговыми поверхностными эрозиями, формированием единичных крипт-абсцессов, лимфоидными агрегатами. Морфологическая картина соответствует язвенному колиту высокой степени активности (индекс Гебса – 4,5).
На фоне продолжавшегося лечения без существенной динамики сохранялись умеренные боли в животе перед дефекацией, жидкий стул до 4–6 раз в сутки с прожилками крови. Учитывая сохранявшуюся активность язвенного колита и неэффективность двух ингибиторов ФНО-альфа, больному предложили оперативное лечение, от которого он категорически отказался. Начата терапия ГКС 120 мг/кг внутривенно, продолжена терапия иммуносупрессорами и начата терапия третьим ГИБП – адалимумабом по схеме. На фоне терапии отмечалась слабоположительная динамика, однако сохранялись умеренные боли в животе перед дефекацией, жидкий стул до четырех-пяти раз в сутки с прожилками крови. Пациент похудел на 15 кг за год.
Ввиду сохранявшейся активности язвенного колита (рис. 1 и 2), неэффективности терапии тремя ГИБП, категорического отказа от оперативного лечения принято решение о назначении ГИБП с другим механизмом действия.
До начала терапии ведолизумабом в общеклиническом анализе крови (ОАК) выявлены лейкоциты 12,2 × 109/л, палочкоядерные нейтрофилы – 14%, скорость оседания эритроцитов (СОЭ) – 25 мм/ч. Биохимический анализ крови: уровни СРБ – 101,9 мг/л, сывороточного железа – 1,6 мкм/л, ферритина – 6 мкг/л, общего белка – 58 г/л, альбумина – 28,5 г/л. Уровень фекального кальпротектина > 1800 мкг/г.
На фоне терапии в течение двух месяцев от ее начала состояние и самочувствие пациента значительно улучшились: стул регулярный один-два раза в сутки без крови и слизи. ОАК: лейкоциты – 8,3 × 109/л, палочкоядерные нейтрофилы – 3%, СОЭ – 15 мм/ч. Биохимический анализ крови: уровни СРБ – 4,9 мг/л, сывороточного железа – 17,3 мкм/л, ферритина – 44 мкг/л, общего белка – 72 г/л, альбумина – 33,5 г/л. Уровень фекального кальпротектина – 200 мкг/г.
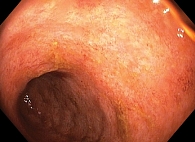
В июне 2017 г. выполнена контрольная колоноскопия: слизистая оболочка слепой, восходящей и поперечно-ободочной кишок, а также дистального отдела сигмовидной кишки очагово гиперемирована. Сосудистый рисунок сглажен. Складки нормальной высоты. Слизистая оболочка остальных отделов розовая, гладкая, блестящая. Сосудистый рисунок усилен, перестроен. Контактная кровоточивость отсутствует. Заключение: язвенный колит, ремиссия. Индекс Мейо – 1 балл (рис. 3).
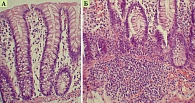
По результатам гистологического исследования также отмечалась значительная положительная динамика: активизация пролиферативных процессов с гиперплазией эпителия и усилением образования мелких и крупных фолликулов в слизистой оболочке и подслизистом слое, увеличением количества бокаловидных клеток в эпителии слизистой оболочки кишки по сравнению с исходным уровнем. Лишь в базальных отделах слизистой оболочки сохранялись небольшие фолликулоподобные скопления лимфоцитов (рис. 4).
Пациент продолжает терапию ведолизумабом 300 мг каждые восемь недель, препаратами 5-АСК, азатиоприном.
Заключение
Приведенное клиническое наблюдение демонстрирует сложности ведения пациентов с язвенным колитом. Несмотря на полный объем медикаментозной терапии, проводимой в соответствии с рекомендуемым алгоритмом [28], пациенты утрачивают ответ на терапию ГИБП. Последующее назначение ГИБП с аналогичным механизмом действия (анти-ФНО-альфа) менее эффективно, чем первое назначение. Тем не менее у пациента с резистентностью к препаратам анти-ФНО-альфа на фоне прогрессирующего и трудно контролируемого течения заболевания ведолизумаб продемонстрировал высокую эффективность и способствовал наступлению клинико-эндоскопической ремиссии в соответствии с современной концепцией лечения до достижения цели при язвенном колите [27].
Кроме того, имеющиеся данные свидетельствуют о том, что наиболее выраженный благоприятный эффект ведолизумаба наблюдается у анти-ФНО-альфа-«наивных» пациентов, что позволяет рекомендовать его в качестве первой линии биологической терапии при язвенном колите и болезни Крона умеренной и высокой активности [8, 22].
O.V. Knyazev, DM, A.V. Kagramanova, PhD, A.A. Lishchinskaya, PhD, D.S. Kulakov, A.I. Parfyonov, DM, Prof.
A.S. Loginov Moscow Clinical Scientific and Practical Center
Contact person: Oleg Vladimirovich Knyazev, oleg7@bk.ru
The article presents the results of ENEIDA multicenter international study, which evaluated vedolizumab efficacy and safety in real clinical practice in a large population of patients with inflammatory bowel diseases (IBD), and determined the predictors of response to therapy. The study allowed identifying prognostic factors of short-term response and efficacy of the drug, to determine the proportion of patients in whom treatment becomes ineffective over time, and the frequency of treatment discontinuation in patients not previously described in the population cohort. In the ENEIDA study, a comparison was made between groups of patients with ulcerative colitis and Crohn's disease. Unlike other observational studies, the ENEIDA study included only patients with active disease in order to obtain a more objective response to therapy. Based on the results of the study, it was concluded that vedolizumab is effective even in resistant patients with IBD.
On the background of its use, remission or a positive effect is observed in more than 2/3 of cases, the minimum number of side effects. The effectiveness of vedolizumab is demonstrated by the example of a patient with ulcerative colitis with three anti-TNF-alpha drugs previous therapy, which developed a secondary loss of response.
