Фармакоэкономическое исследование применения пембролизумаба и ниволумаба во второй линии терапии распространенного немелкоклеточного рака легкого
- Аннотация
- Статья
- Ссылки
- English
Цель настоящей работы – актуализировать результаты комплексного фармакоэкономического исследования ингибиторов PD-1 во второй линии терапии пациентов с распространенным НМРЛ, которые ранее получали терапию, включавшую препараты платины или (при наличии мутаций в генах EGFR или ALK) таргетные противоопухолевые препараты, и у которых рассматривается возможность проведения теста на определение уровня экспрессии PD-L1.
Методы. Сравнивали два альтернативных варианта второй линии терапии распространенного НМРЛ: пембролизумаб (у пациентов с положительной экспрессией PD-L1) или доцетаксел (у остальных пациентов) против ниволумаба (независимо от статуса PD-L1). Из-за отсутствия статистически значимых различий в эффективности данных вариантов в качестве дизайна клинико-экономического исследования была выбрана минимизация затрат. На основе результатов клинических исследований была разработана математическая модель динамики прогрессирования НМРЛ, оценены прямые медицинские расходы, связанные с использованием указанных препаратов, определена разница прямых медицинских расходов в расчете на одного пациента, а также проведен анализ «влияние на бюджет» программы обеспечения необходимыми лекарственными средствами (ОНЛС) в случае включения в программу пембролизумаба.
Результаты. Стоимость года лечения пембролизумабом/доцетакселом составляет 4 723 937 руб., что на 22,3% меньше, чем при использовании ниволумаба (6 080 353 руб.). Прямые медицинские расходы на одного пациента при использовании пембролизумаба/доцетаксела за пять лет достигают 3 031 471 руб.,
что на 20,5% меньше, чем в случае применения ниволумаба. При использовании пембролизумаба/доцетаксела расходы бюджета программы ОНЛС за три года на 3,4 млрд руб. (20,7%) меньше таковых в случае применения ниволумаба.
Цель настоящей работы – актуализировать результаты комплексного фармакоэкономического исследования ингибиторов PD-1 во второй линии терапии пациентов с распространенным НМРЛ, которые ранее получали терапию, включавшую препараты платины или (при наличии мутаций в генах EGFR или ALK) таргетные противоопухолевые препараты, и у которых рассматривается возможность проведения теста на определение уровня экспрессии PD-L1.
Методы. Сравнивали два альтернативных варианта второй линии терапии распространенного НМРЛ: пембролизумаб (у пациентов с положительной экспрессией PD-L1) или доцетаксел (у остальных пациентов) против ниволумаба (независимо от статуса PD-L1). Из-за отсутствия статистически значимых различий в эффективности данных вариантов в качестве дизайна клинико-экономического исследования была выбрана минимизация затрат. На основе результатов клинических исследований была разработана математическая модель динамики прогрессирования НМРЛ, оценены прямые медицинские расходы, связанные с использованием указанных препаратов, определена разница прямых медицинских расходов в расчете на одного пациента, а также проведен анализ «влияние на бюджет» программы обеспечения необходимыми лекарственными средствами (ОНЛС) в случае включения в программу пембролизумаба.
Результаты. Стоимость года лечения пембролизумабом/доцетакселом составляет 4 723 937 руб., что на 22,3% меньше, чем при использовании ниволумаба (6 080 353 руб.). Прямые медицинские расходы на одного пациента при использовании пембролизумаба/доцетаксела за пять лет достигают 3 031 471 руб.,
что на 20,5% меньше, чем в случае применения ниволумаба. При использовании пембролизумаба/доцетаксела расходы бюджета программы ОНЛС за три года на 3,4 млрд руб. (20,7%) меньше таковых в случае применения ниволумаба.






Введение
В 2018 г. в России было зарегистрировано 55 717 новых случаев рака трахеи, бронхов, легкого [1]. Данное злокачественное новообразование занимает первое место в структуре онкологической заболеваемости и смертности мужского населения и характеризуется крайне высокой одногодичной летальностью: 49,0% больных умирают в течение года после установления диагноза [1]. У 41% больных раком трахеи, бронхов, легкого злокачественное новообразование выявляется на последней, четвертой стадии опухолевого процесса [1], когда лечение клинически крайне сложно.
Пембролизумаб и ниволумаб – инновационные лекарственные препараты, ингибиторы PD-1, предназначенные для лечения распространенного немелкоклеточного рака легкого (НМРЛ) и характеризующиеся высокой эффективностью, доказанной в рандомизированных клинических исследованиях [2–4]. Применение указанных лекарственных средств также предусмотрено отечественными клиническими рекомендациями по диагностике и лечению рака легкого, включенными в рубрикатор Минздрава России [5].
По состоянию на 2019 г. оба лекарственных средства включены в Перечень жизненно необходимых и важнейших лекарственных препаратов, что делает их более доступными для пациентов. Вместе с тем сегодня ни один ингибитор PD-1 не входит в программу обеспечения необходимыми лекарственными средствами (ОНЛС) [6]. Пембролизумаб и ниволумаб включены в схемы лекарственной терапии, применение которых в стационарных условиях оплачивается за счет средств системы обязательного медицинского страхования с использованием клинико-статистических групп (КСГ) [7]. В результате при включении пембролизумаба и (или) ниволумаба в программу ОНЛС расходы на пребывание в стационаре могут сократиться.
Для принятия решения о включении пембролизумаба и (или) ниволумаба в программу ОНЛС необходимо проведение фармакоэкономического исследования данных препаратов в условиях российского здравоохранения. Следует отметить, что такие исследования уже проводились [8, 9], однако они не в полной мере соответствуют новым Требованиям к методологическому качеству клинико-экономических исследований лекарственного препарата и исследований с использованием анализа влияния на бюджеты бюджетной системы Российской Федерации (далее – Требования к проведению фармакоэкономических исследований) [10].
Цель настоящей работы – актуализировать проведенное в 2018 г. комплексное фармакоэкономическое исследование [8] применения ингибиторов PD-1 во второй линии терапии пациентов с распространенным НМРЛ, которые ранее получали терапию, включавшую препараты платины или (при наличии мутаций в генах EGFR или ALK) таргетные противоопухолевые препараты, и у которых возможно проведение теста на определение уровня экспрессии PD-L1, с позиций российского здравоохранения 2019 г. и с учетом новых Требований к проведению фармакоэкономических исследований.
Материал и методы
Оригинальная фармакоэкономическая модель
Для проведения фармакоэкономического анализа в настоящем исследовании была доработана методика, предложенная авторами ранее [8]. В исследовании сравнивали два альтернативных варианта второй линии терапии распространенного НМРЛ:
- пембролизумаб (для пациентов с PD-L1 ≥ 1%) 200 мг один раз в три недели1 [11] или доцетаксел (для пациентов с PD-L1 < 1%) 75 мг/м2 один раз в три недели [12] (далее – терапия с использованием пембролизумаба/доцетаксела, или вариант 1);
- ниволумаб (независимо от уровня PD-L1) 3 мг/кг один раз в две недели [13] (далее – терапия с использованием ниволумаба, или вариант 2).
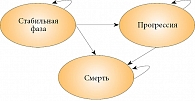
В исследовании использовали предложенную ранее модель прогрессирования НМРЛ, состоящую из трех взаимоисключающих состояний пациентов (рис. 1) [8]:
- cтабильная фаза;
- прогрессия;
- смерть.
Горизонт анализа – пять лет, шаг модели – одна неделя.
Предложенная модель [8] использовалась для моделирования исходов лечения в следующих случаях:
- Для варианта 1:
- применение пембролизумаба у пациентов с экспрессией PD-L1 ≥ 1%;
- применение доцетаксела у пациентов с экспрессией PD-L1 < 1%;
- Для варианта 2:
- применение ниволумаба у пациентов с экспрессией PD-L1 ≥ 1%;
- применение ниволумаба у пациентов с экспрессией PD-L1 < 1%.
Вероятности перехода между состояниями модели в каждом случае рассчитывались на основе данных общей выживаемости и выживаемости без прогрессирования. При этом в случаях 1а и 2б общая выживаемость и выживаемость без прогрессирования моделировались на основании данных рандомизированных клинических исследований (РКИ) KeyNote-010 [2] для группы пембролизумаба и CheckMate 017 [3] и CheckMate 057 [4] для подгруппы пациентов с экспрессией PD-L1 < 1%, получавших ниволумаб2, соответственно.
Общая выживаемость и выживаемость без прогрессирования в вариантах 1б и 2а моделировались на основании вариантов 2б и 1а соответственно с использованием модели пропорционального риска:
XB,t = (XA,t)1/HR
где Xi,t – общая выживаемость или выживаемость без прогрессирования в случае выбора варианта терапии i;
HR – отношение угроз (ОУ) применения препарата A по сравнению с препаратом B по соответствующему критерию эффективности.
ОУ смерти и прогрессирования или смерти в случае применения доцетаксела у пациентов с экспрессией PD-L1 < 1% (вариант 1б) в работе [8] соответствовало базовым результатам метаанализа эффективности применения рассматриваемых лекарственных препаратов у больных плоскоклеточным и неплоскоклеточным НМРЛ с уровнем экспрессии PD-L1 < 1% (табл. 1) [8, 14].
ОУ смерти и прогрессирования или смерти в случае применения ниволумаба у пациентов с экспрессией PD-L1 ≥ 1% (вариант 2а) в работе [8] рассчитывалось в ходе собственного непрямого сравнения эффективности данных альтернативных схем в рассматриваемой популяции пациентов, выполненного с учетом данных РКИ KeyNote-010 [2] и метаанализа [14] с использованием доцетаксела в качестве общего компаратора (табл. 1).
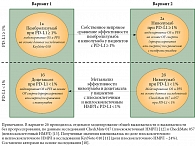
Концептуальная схема моделирования общей выживаемости и выживаемости без прогрессирования для каждого варианта модели (1а, 1б, 2а и 2б) представлена на рис. 2.
Методика для каждого случая (1а, 1б, 2а и 2б), разработанная в исследовании [8], позволяла оценить исходы лечения: среднее количество прожитых человеко-лет, среднее количество прожитых человеко-лет без прогрессирования за период моделирования, а также величину прямых медицинских расходов, связанных с ведением пациентов. При этом учитывались следующие виды прямых медицинских затрат:
- на лекарственную терапию второй линии (с использованием пембролизумаба/доцетаксела или ниволумаба);
- лечение наиболее часто встречающихся и дорогостоящих нежелательных явлений (НЯ) 3-й и 4-й степени, возникающих на фоне терапии второй линии;
- терапию третьей линии (пеметрексед, гемцитабин, винорелбин и доцетаксел);
- прочие расходы на ведение пациентов (лучевая терапия, лечение метастазов в костях, мониторинг лечения).
Все расходы учитывались с позиции российского здравоохранения 2018 г. и дисконтировались по ставке 5%.
Далее в работе [8] моделировались исходы лечения и затрат для варианта 1 (терапия с использованием пембролизумаба/доцетаксела). Для этого результаты моделирования в случаях 1а и 1б усреднялись с учетом частоты экспрессии PD-L1 ≥ 1% и PD-L1 < 1%, причем частота PD-L1 ≥ 1% считалась равной 66% [2]. Аналогичным образом проводилось усреднение для случаев 2а и 2б для моделирования исходов лечения и затрат при варианте 2 (терапия с использованием ниволумаба).
На основании результатов моделирования в исследовании [8] проводилось два фармакоэкономических анализа методами «затраты – эффективность» и «влияние на бюджет».
Подробная методика проведения исследования представлена в опубликованной работе [8].
Основные изменения в методике проведения фармакоэкономического анализа
Во-первых, согласно данным метаанализа [14] и собственного непрямого сравнения, проведенного в работе [8] (табл. 1):
- 95%-ный доверительный интервал (ДИ) для ОУ смерти (прогрессирования или смерти) в случае применения ниволумаба по сравнению с пембролизумабом у пациентов с PD-L1 ≥ 1% включает единицу;
- 95% ДИ для ОУ смерти (прогрессирования или смерти) при использовании ниволумаба по сравнению с доцетакселом у пациентов с PD-L1 < 1% также включает единицу (табл. 1).
Эффективность терапии в случае 1а сопоставима с эффективностью терапии в случае 2а, а эффективность терапии в случае 1б сопоставима с эффективностью терапии в случае 2б. Следовательно, эффективность терапии в варианте 1 (терапия с использованием пембролизумаба/доцетаксела) сопоставима с эффективностью варианта 2 (терапия с использованием ниволумаба) по критериям общей выживаемости и выживаемости без прогрессирования.
Согласно актуальной редакции Правил формирования перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи, утвержденных постановлением Правительства РФ от 28.08.2014 № 871 (редакция от 20 ноября 2018 г.) [10], в отсутствие статистически значимых различий, подтвержденных результатами клинических исследований, по эффективности и (или) безопасности между предлагаемым лекарственным препаратом и препаратом сравнения используется метод минимизации затрат.
В отличие от работы [8] в настоящем исследовании основной метод клинико-экономического исследования был изменен на минимизацию затрат. При этом эффективность ниволумаба у пациентов с экспрессией PD-L1 ≥ 1% (случай 2а) по критериям общей выживаемости и выживаемости без прогрессирования была принята равной эффективности пембролизумаба у той же группы пациентов (случай 1а), а эффективность доцетаксела у пациентов с экспрессией PD-L1 < 1% (случай 1б) по обоим критериям считалась равной эффективности ниволумаба у той же группы пациентов (случай 2б)3. Моделирование общей выживаемости и выживаемости без прогрессирования в вариантах 1а и 2б осуществлялось в соответствии с методикой, изложенной в работе [8].
Во-вторых, по сравнению с методикой, представленной в работе [8], в настоящем исследовании был исключен учет некоторых категорий расходов, которые оказались одинаковыми после принятия предпосылки о сопоставимой эффективности вариантов сравнения. В частности, не учитывались расходы на лучевую терапию, терапию метастазов в костях, амбулаторные посещения с целью мониторинга лечения. Таким образом, в настоящем исследовании принимались во внимание только расходы на лекарственную терапию второй линии (пембролизумаб/доцетаксел или ниволумаб), лечение наиболее часто встречающихся и дорогостоящих НЯ 3-й и 4-й степени, возникающих на фоне терапии второй линии, и расходы на терапию третьей линии (пеметрексед, гемцитабин, винорелбин и доцетаксел), которые различны при варианте 1 и варианте 2. Такие различия обусловлены тем, что в варианте 1 меньше пациентов получали доцетаксел в третьей линии, поскольку части из них этот препарат назначали во второй линии.
В-третьих, были актуализированы цены на лекарственную терапию по состоянию на конец 2018 г. (табл. 2). В отличие от оригинальной модели в настоящем исследовании цены на лекарственную терапию включали не только налог на добавленную стоимость (НДС) (10%), но и средневзвешенное (по численности населения) значение предельной оптовой торговой надбавки, по данным ФАС России за I квартал 2019 г. (11,84%) [15]. В остальном методика учета затрат на терапию второй и третьей линии соответствовала описанной в работе [8].
В-четвертых, в настоящем исследовании были актуализированы тарифы на оказание медицинской помощи при возникновении НЯ, в соответствии с федеральной моделью КСГ на 2019 г. Стоимость одного амбулаторного обращения считалась равной среднему финансовому нормативу затрат на одно амбулаторное обращение по поводу заболевания за счет средств обязательного медицинского страхования в 2019 г. – 1313,6 руб. Стоимость оказания помощи в стационарных условиях определялась исходя из Методических рекомендаций по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования на 2019 г. [7]. При этом в качестве базовой ставки госпитализации в дневной и круглосуточный стационар использовались значения, равные 17335,17 и 28811,52 руб. соответственно. Эти показатели определялись как 90% среднего норматива затрат на один случай госпитализации, предусмотренного в Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2019 г. [16]. Использованные коэффициенты затратоемкости госпитализаций в дневной и круглосуточный стационар и соответствующие номера клинико-статистических групп обобщены в табл. 3 [7]. В остальном методика учета затрат на лечение НЯ соответствовала описанной в работе [8].
В-пятых, в настоящем исследовании анализ влияния на бюджет программы ОНЛС проводился для периода 2020–2022 гг. (в оригинальной работе [8] горизонт анализа влияния на бюджет – 2019–2021 гг.). Методика расчета количества пациентов соответствовала описанной в работе [8]. При этом для прогнозирования численности больных НМРЛ, которые смогут получать один из вариантов лечения в случае расширения программы ОНЛС, мы дополнительно учли данные о фактической заболеваемости НМРЛ в 2017 г., согласно статистическим сборникам [17, 18]. Как и прежде, влияние на бюджет оценивали среди популяции пациентов, у которых в реальной практике рассматривается возможность применения пембролизумаба во второй линии терапии. Речь идет о пациентах с IV стадией НМРЛ в возрасте до 75 лет со статусом ECOG 0–2, ранее получавших препараты платины либо при наличии мутаций в генах EGFR или ALK таргетные противоопухолевые препараты, являющихся кандидатами на проведение теста на определение уровня экспрессии PD-L1 и имеющих право на получение льготного лекарственного обеспечения по программе ОНЛС.
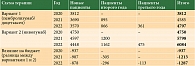
Общее количество пациентов, которые вправе претендовать на получение пембролизумаба или доцетаксела за счет средств ОНЛС в качестве терапии НМРЛ второй линии, составит в 2020 г. 1856 (пембролизумаб – 1225 пациентов, доцетаксел – 631 больной), в 2021 г. – 1886 (пембролизумаб – 1245 пациентов, доцетаксел – 641 больной), в 2022 г. – 1916 пациентов (1265 и 652 пациента соответственно). Как и в оригинальной работе [8], в настоящем исследовании влияние на бюджет определялось как разница в расходах программы ОНЛС в случае лекарственного обеспечения указанного контингента больных с использованием пембролизумаба или доцетаксела (в зависимости от уровня экспрессии PD-L1) по сравнению с лекарственным обеспечением такой же популяции больных с использованием ниволумаба (независимо от уровня экспрессии PD-L1).
В-шестых, в настоящем исследовании сначала распределялись пациенты по состояниям модели в вариантах 1 (усреднение случаев 1а и 1б по частоте экспрессии PD-L1 ≥ 1% и PD-L1 < 1%) и 2 (усреднение случаев 2а и 2б), затем рассчитывались затраты с учетом усредненных данных. Первоначальный вариант учета расходов (моделирование расходов в случаях 1а, 1б, 2а и 2б с последующим усреднением по частоте экспрессии PD-L1), использованный в работе [8], в настоящем исследовании реализован в анализе чувствительности.
Наконец, обновлен анализ чувствительности разницы в расходах на терапию одного пациента за пятилетний период, а также добавлен анализ чувствительности для влияния на бюджет при сравнении вариантов 1 (терапия с использованием пембролизумаба/доцетаксела) и 2 (терапия с использованием ниволумаба) за период 2020–2022 гг. В обоих случаях в ходе проведения однофакторного анализа чувствительности изучались колебания следующих параметров:
- цены на пембролизумаб, ниволумаб и доцетаксел в границах ±20% базовой стоимости;
- ОУ при сравнении ниволумаба и пембролизумаба по критериям общей выживаемости и выживаемости без прогрессирования для пациентов с PD-L1 ≥ 1% (в границах 95% ДИ, указанных в табл. 1);
- ОУ при сравнении доцетаксела и ниволумаба по критерию общей выживаемости и выживаемости без прогрессирования для пациентов с PD-L1 < 1% (в границах 95% ДИ, указанных в табл. 1);
- доля пациентов с PD-L1 ≥ 1% (32–100%);
- вес пациентов (60–90 кг);
- вариант моделирования результатов лечения, длительности терапии и учета расходов (исходя из доли пациентов, находящихся в разных состояниях модели, при вариантах 1 или 2 (базовый сценарий) или на основе первоначально смоделированных значений для случаев 1а, 1б, 2а и 2б с последующим усреднением по доле пациентов с наличием или отсутствием экспрессии PD-L1);
- количество больных НМРЛ, которые могут претендовать на получение пембролизумаба или доцетаксела за счет средств ОНЛС в варианте 1 в 2020, 2021 и 2022 гг.
Результаты и обсуждение
Стоимость курса лекарственной терапии
Стоимость года лечения при варианте 1 второй линии терапии распространенного НМРЛ (пембролизумаб при PD-L1 ≥ 1% или доцетаксел при PD-L1 < 1%) составит 4723937,27 руб. Это на 1346415,41 руб. (22%) меньше, чем при варианте 2 (назначение ниволумаба независимо от статуса PD-L1) (табл. 4). Такой эффект достигается за счет применения в варианте 1 менее дорогостоящего препарата – доцетаксела у больных с экспрессией PD-L1 < 1% вместо ниволумаба, который применяется в варианте 2 независимо от уровня экспрессии PD-L1.
Результаты моделирования динамики прогрессирования НМРЛ
Среднее число прожитых человеко-лет в течение периода моделирования для обоих вариантов сравнения представлено в табл. 5. В базовом варианте среднее число человеко-лет, прожитых одним пациентом, в течение периода моделирования составит 1,4 года. В том числе пациенты с экспрессией PD-L1 ≥ 1% в среднем проживут 1,5 года, с экспрессией PD-L1 < 1% – 1,3 года.
Анализ «минимизация затрат»
В сумме за пять лет прямые затраты на терапию пембролизумабом или доцетакселом составят 3 031 471 руб. на одного пациента, а для варианта с ниволумабом – 3 814 024 руб. (табл. 6). Таким образом, использование варианта 1 (пембролизумаб/доцетаксел (в зависимости от уровня экспрессии PD-L1)) на 782 552 руб., или 20,5%, дешевле варианта 2 (ниволумаб). В обоих случаях в структуре затрат доминируют расходы на основную лекарственную терапию (около 95%).
Экономия в варианте с пембролизумабом/доцетакселом обусловлена тем, что дорогостоящий лекарственный препарат используется только у тех пациентов, которые могут получить значимую клиническую пользу от него в отличие от химиотерапии. В варианте 2 иммуноонкологический лекарственный препарат (ниволумаб) получают все пациенты.
Влияние на бюджет
Если 1856–1916 больных НМРЛ будут ежегодно приступать к лекарственной терапии с использованием пембролизумаба/доцетаксела, расходы программы ОНЛС на лекарственное обеспечение (в зависимости от уровня экспрессии PD-L1) составят 3,8 млрд руб. в 2020 г., 4,6 млрд руб. – в 2021 г. и 4,8 млрд руб. – в 2022 г. (табл. 7). Если вся указанная популяция пациентов за счет средств ОНЛС будет получать лекарственную терапию ниволумабом, расходы программы составят 4,8 млрд руб. в 2020 г., 5,8 млрд руб. – в 2021 г. и 6,1 млрд руб. – в 2022 г. Таким образом, при включении пембролизумаба в программу ОНЛС ее расходы в 2020 г. окажутся меньше на 937 млн руб., в 2021 г. – на 1213 млн руб., в 2022 г. – на 1287 млн руб. Всего за трехлетний период разница в расходах достигнет 3,4 млрд руб. (-20,7%) в пользу варианта 1.
Анализ чувствительности
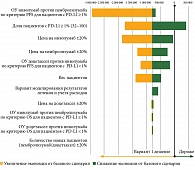
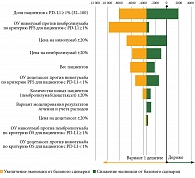
Согласно анализу чувствительности разницы в расходах на одного пациента за пять лет (рис. 3), максимальная вариативность результатов анализа «минимизация затрат» наблюдается при изменении ОУ прогрессирования или смерти на фоне применения ниволумаба по сравнению с пембролизумабом у пациентов с экспрессией PD-L1 ≥ 1%. Разница в затратах на одного пациента также зависит от частоты экспрессии PD-L1 ≥ 1%, цен на пембролизумаб и ниволумаб.
Тем не менее при изменении всех рассматриваемых параметров модели в достаточно широких границах ключевой результат настоящего исследования остается неизменным – использование пембролизумаба (у пациентов с PD-L1 ≥ 1%) или доцетаксела (у пациентов с PD-L1 < 1%) является ресурсосберегающей технологией по сравнению с применением ниволумаба (независимо от статуса PD-L1) во второй линии терапии распространенного НМРЛ. В рассмотренных сценариях расходы на одного пациента при варианте 1 выше расходов при варианте 2 только при доле пациентов с экспрессией PD-L1 ≥ 1% свыше 89,0%.
Согласно результатам анализа чувствительности для влияния на бюджет программы ОНЛС, представленного на рис. 4, максимальная вариативность наблюдается при изменении доли пациентов с PD-L1 ≥ 1%, которая отражает численность популяции пациентов, получающих пембролизумаб. Кроме того, результат анализа влияния на бюджет в существенной степени зависит от ОУ прогрессирования или смерти при использовании ниволумаба по сравнению с использованием пембролизумаба у пациентов с PD-L1 ≥ 1%, цены на лекарственные препараты, веса пациентов.
Как и прежде, колебания большинства параметров в границах заданных интервалов не повлияли на основной вывод: назначение пембролизумаба (пациентам с PD-L1 ≥ 1%) или доцетаксела (пациентам с PD-L1 < 1%) приведет к меньшим расходам программы ОНЛС по сравнению с лекарственным обеспечением такого же числа пациентов ниволумабом (независимо от статуса PD-L1). В рассмотренных сценариях экономия бюджета ОНЛС в варианте 1 по сравнению с вариантом 2 отсутствует только при доле пациентов с экспрессией PD-L1 ≥ 1% выше 88,2%.
Заключение
Фармакоэкономический анализ проведен для двух альтернативных вариантов терапии второй линии:
- пембролизумаб (у пациентов с положительной экспрессией PD-L1) и доцетаксел (у остальных пациентов);
- ниволумаб (независимо от статуса PD-L1).
По итогам исследования сделаны следующие выводы.
- Статистически значимые различия между пембролизумабом и ниволумабом (у пациентов с положительной экспрессией PD-L1), а также между ниволумабом и доцетакселом (у пациентов с отрицательной экспрессией PD-L1) по критериям общей выживаемости и выживаемости без прогрессирования отсутствуют, что предопределяет выбор дизайна клинико-экономического исследования «минимизация затрат».
- Стоимость годовой терапии с использованием варианта 1 второй линии у пациентов с распространенным НМРЛ (пембролизумаб при PD-L1 ≥ 1% или доцетаксел при PD-L1 < 1%) – 4 723 937 руб. Это на 1 356 416 руб. (22,3%) меньше стоимости годового лечения при варианте 2 (ниволумаб независимо от статуса PD-L1 – 6 080 353 руб.).
- Прямые медицинские расходы на одного пациента за пять лет, связанные с назначением пембролизумаба/доцетаксела, – 3 031 471 руб. Это на 782 552 руб., или 20,5%, меньше, чем при использовании ниволумаба (3 814 024 руб.).
- Если к лекарственной терапии, предоставляемой за счет средств программы ОНЛС, будет приступать по 1856–1916 больных НМРЛ ежегодно, расходы программы на их лекарственное обеспечение пембролизумабом/доцетакселом составят 3,8–4,8 млрд руб. в год, что на 0,9–1,3 млрд руб. меньше по сравнению с лекарственным обеспечением указанной категории пациентов ниволумабом. За три года общий размер экономии достигнет 3,4 млрд руб., или 20,7%.
1 В оригинальном исследовании [8] рассматривали режим применения пембролизумаба 2 мг/кг один раз в три недели, что соответствовало предыдущей редакции инструкции по медицинскому применению данного препарата. Вместе с тем в условиях, когда разделение упаковок между пациентами не разрешено, такое изменение практически не влияет на результаты исследования.
2 При этом проводилось отдельное моделирование общей выживаемости и выживаемости без прогрессирования, согласно данным исследования CheckMate 017 (плоскоклеточный НМРЛ) [12] и CheckMate 057 (неплоскоклеточный НМРЛ) [13]. Полученные значения взвешивались по доле плоскоклеточного и неплоскоклеточного НМРЛ (доля плоскоклеточного НМРЛ – 24% [11]).
3 Другими словами, в приведенной выше формуле во всех указанных случаях использовалось ОУ, равное единице. Иные значения ОУ (в рамках соответствующих 95% ДИ) применялись при анализе чувствительности.
N.A. Avxentyev, M.Yu. Frolov, A.S. Makarov
Scientific-Research Financial Institute of Ministry of Finance of the Russian Federation
Institute of Social Analysis and Forecasting of Russian Presidential Academy of National Economy and Public Administration
Volgograd State Medical University
Volgograd Medical Research Center
῾Association of Clinical Pharmacologists᾿ Interregional Public Organization
Contact person: Nikolay A. Avxentyev, na@nifi.ru
Lung cancer is the most common disease in the structure of cancer morbidity and mortality of the male population of Russia. Recently, new PD-1 inhibitors have become available for the treatment of patients with advanced non-small cell lung cancer (NSCLC), which allow to improve the outcomes in the second-line treatment compared with docetaxel therapy.
The Objective of this work is to update the results of a complex pharmacoeconomic study of PD-1 inhibitors in the second line of therapy in patients with advanced NSCLC who previously received therapy, including platinum drugs or (in the presence of mutations in the EGFR or ALK genes) targeted anticancer drugs, and for whom the possibility of a test to determine the level of expression of PD-L1 is being considered.
Methods. Two alternative scenarios of the second line of advanced NSCLC treatment were compared: pembrolizumab (in patients with positive expression of PD-L1) or docetaxel (in other patients) against nivolumab (regardless of the status of PD-L1). Due to the lack of statistically significant differences in the effectiveness of the discussed options, the cost minimization was chosen as the design of clinical and economic research. Based on the clinical studies data, the mathematical model of the dynamics of NSCLC progression was developed, the direct medical costs associated with the use of these drugs were estimated, the difference in direct medical costs per patient was determined, and the budget impact analysis of the program on necessary drugs provision in the case of inclusion in the program of pembrolizumab was carried out.
Results. The cost of year treatment with pembrolizumab/docetaxel is 4 723 937 RUB, which is 22.3% less than in the case of nivolumab therapy (6 080 353 RUB). Direct medical costs per patient in pembrolizumab/docetaxel scenario over five years total 3 031 471 RUB, or 20.5% lower than in the case of nivolumab therapy. For pembrolizumab/docetaxel scenario, the cost of the necessary drugs provision budget program for three years is 3.4 billion rubles (20.7%) less than in the case of nivolumab therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.