количество статей
7385
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Клиническая эффективность терапии Нурофеном при респираторных заболеваниях, сопровождающихся острым стенозирующим ларинготрахеитом, у детей
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эпидемиология и инфекции" № 1
- Аннотация
- Статья
- Ссылки
На основании собственного клинического опыта показано, что суспензия Нурофен® для детей является высокоэффективным жаропонижающим, противовоспалительным и обезболивающим средством, практически не вызывающим возникновения нежелательных побочных явлений.
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
На основании собственного клинического опыта показано, что суспензия Нурофен® для детей является высокоэффективным жаропонижающим, противовоспалительным и обезболивающим средством, практически не вызывающим возникновения нежелательных побочных явлений.
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
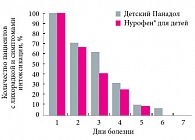
Рис. 1. Динамика лихорадки и симптомов интоксикации у больных ОРВИ с синдромом крупа на фоне лечения Нурофеном для детей и Детским Панадолом
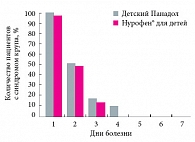
Рис. 2. Динамика симптомов стеноза гортани у больных ОРВИ с синдромом крупа на фоне лечения Нурофеном для детей и Детским Панадолом
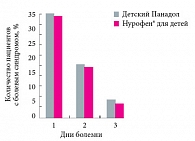
Рис. 3. Динамика болевого синдрома у больных ОРВИ со стенозом гортани и острым средним отитом на фоне лечения Нурофеном для детей и Детским Панадолом
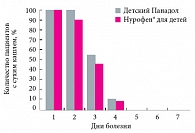
Рис. 4. Динамика сухого кашля у больных ОРВИ с синдромом крупа на фоне лечения Нурофеном для детей и Детским Панадолом
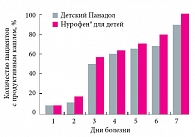
Рис. 5. Динамика появления кашля с мокротой у больных ОРВИ с синдромом крупа на фоне лечения Нурофеном для детей и Детским Панадолом
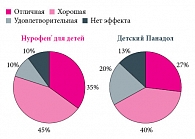
Рис. 6. Оценка эффективности терапии Нурофеном для детей и Детским Панадолом у больных ОРВИ с синдромом крупа
Введение
В структуре заболеваемости у детей доля инфекционных заболеваний составляет около 70%, а в структуре младенческой смертности – более 80%. Большая часть регистрируемой инфекционной заболеваемости (до 90%) приходится на острые респираторные вирусные инфекции (ОРВИ) и грипп. Воспалительная реакция в верхнем отделе респираторного тракта возникает в результате повреждения эпителиального пласта вирусами, бактериями и другими патогенами и презентации их антигенов макрофагальными, дендритными клетками и В-лимфоцитами, входящими в этот пласт, а также Т-лимфоцитами. В результате клеточного иммунного реагирования при ОРВИ активизируется избыточный синтез множества цитокинов и хемокинов – эндогенных пирогенов (интерлейкинов (ИЛ) ИЛ-1 альфа, ИЛ-1 бета, ИЛ-2, ИЛ-6, ИЛ-8, ИЛ-12, ИЛ-18; фактора некроза опухоли альфа (ФНО-альфа); интерферона-гамма (ИФН-гамма)), участвующих в таких реакциях организма, как лихорадка и болевой синдром.
В структуре заболеваемости у детей доля инфекционных заболеваний составляет около 70%, а в структуре младенческой смертности – более 80%. Большая часть регистрируемой инфекционной заболеваемости (до 90%) приходится на острые респираторные вирусные инфекции (ОРВИ) и грипп. Воспалительная реакция в верхнем отделе респираторного тракта возникает в результате повреждения эпителиального пласта вирусами, бактериями и другими патогенами и презентации их антигенов макрофагальными, дендритными клетками и В-лимфоцитами, входящими в этот пласт, а также Т-лимфоцитами. В результате клеточного иммунного реагирования при ОРВИ активизируется избыточный синтез множества цитокинов и хемокинов – эндогенных пирогенов (интерлейкинов (ИЛ) ИЛ-1 альфа, ИЛ-1 бета, ИЛ-2, ИЛ-6, ИЛ-8, ИЛ-12, ИЛ-18; фактора некроза опухоли альфа (ФНО-альфа); интерферона-гамма (ИФН-гамма)), участвующих в таких реакциях организма, как лихорадка и болевой синдром.
В развитии лихорадки существенную роль играет высвобождение макрофагами эндогенных пирогенов (цитокинов) ИЛ-1, ИЛ-6, ИЛ-8, ФНО-альфа и проникновение их в OVLT (organum vasculosum of the lamina terminalis – гемососудистый орган терминальной пластинки гипоталамуса) – капиллярное ложе преоптической области передней части гипофиза. Выход ИЛ-1 за пределы сосудов усиливает синтез циклооксигеназы, способствуя продукции простагландина Е (ПГЕ), циклического аденозинмонофосфата (цАМФ), накоплению Са2+. ПГЕ легко проходят барьер между OVLT и тканью мозга и воздействуют на центр терморегуляции, повышая «установочную точку» за счет усиления метаболических процессов. Уменьшается теплоотдача и увеличивается теплопродукция за счет усиления сократительного термогенеза [1–3].
Синдром лихорадки является ведущим клиническим проявлением всех инфекционных заболеваний. С теоретической точки зрения повышение температуры тела можно считать защитной реакцией, направленной на элиминацию инфекционного патогена, однако на практике такое объяснение не всегда бывает корректным. Нередко у детей на высоте температурной реакции возникают нежелательные явления в виде энцефалических реакций (судорог, потери сознания, нарушения сна, возбуждения и др.), которые могут стать причиной тяжелых последствий с нежелательным исходом, вплоть до возникновения отека и набухания головного мозга. В связи с этим далеко не бесспорным представляется распространенное мнение о том, что назначение жаропонижающих средств при инфекционных заболеваниях оправдано только при подъеме температуры тела до 39 °С и выше [1–3].
У детей с измененной реактивностью даже незначительный подъем температуры тела может явиться причиной развития нежелательных синдромов и последствий. Следовательно, с практической точки зрения представляется особенно актуальным, с одной стороны, знать механизм развития лихорадочного состояния, а с другой – уметь управлять выраженностью этих механизмов, не допуская в каждом конкретном случае их патогенного действия и нежелательного влияния на темп восстановления структуры и функции пораженных органов и тканей. Вполне очевидно, что выбор антипиретика должен основываться прежде всего на его безопасности. Безопасность антипиретиков является серьезной проблемой современной педиатрии, что связано с риском развития побочных эффектов при приеме этих препаратов. В прошлом на протяжении длительного времени использовались препараты салициловой кислоты, метамизол натрия, производные пиразолона и парааминофенола.
Синдром лихорадки является ведущим клиническим проявлением всех инфекционных заболеваний. С теоретической точки зрения повышение температуры тела можно считать защитной реакцией, направленной на элиминацию инфекционного патогена, однако на практике такое объяснение не всегда бывает корректным. Нередко у детей на высоте температурной реакции возникают нежелательные явления в виде энцефалических реакций (судорог, потери сознания, нарушения сна, возбуждения и др.), которые могут стать причиной тяжелых последствий с нежелательным исходом, вплоть до возникновения отека и набухания головного мозга. В связи с этим далеко не бесспорным представляется распространенное мнение о том, что назначение жаропонижающих средств при инфекционных заболеваниях оправдано только при подъеме температуры тела до 39 °С и выше [1–3].
У детей с измененной реактивностью даже незначительный подъем температуры тела может явиться причиной развития нежелательных синдромов и последствий. Следовательно, с практической точки зрения представляется особенно актуальным, с одной стороны, знать механизм развития лихорадочного состояния, а с другой – уметь управлять выраженностью этих механизмов, не допуская в каждом конкретном случае их патогенного действия и нежелательного влияния на темп восстановления структуры и функции пораженных органов и тканей. Вполне очевидно, что выбор антипиретика должен основываться прежде всего на его безопасности. Безопасность антипиретиков является серьезной проблемой современной педиатрии, что связано с риском развития побочных эффектов при приеме этих препаратов. В прошлом на протяжении длительного времени использовались препараты салициловой кислоты, метамизол натрия, производные пиразолона и парааминофенола.
Однако в начале 1980-х гг. появились данные о необоснованности применения (в особенности бесконтрольного) препаратов салициловой кислоты при вирусных инфекциях у детей, что может являться причиной развития жировой дегенерации печени с энцефалопатией (синдром Рея). Амидопирин также был исключен из номенклатуры лекарственных препаратов из-за своей токсичности, которая проявлялась, как и в случае метамизола натрия (анальгина), воздействием на костный мозг, вплоть до развития агранулоцитоза со смертельным исходом. Не рекомендован в качестве антипиретического лекарственного средства и нимесулид (Найз), обладающий гепатотоксичностью, которая может привести к летальному исходу [1, 4]. Накопление достоверных фактов о жаропонижающей эффективности и безопасности различных антипиретиков привело к значительному сокращению количества лекарственных средств, применяемых у детей при лихорадке.
Особенно актуальным является поиск эффективного и безопасного жаропонижающего средства для детей с отягощенным аллергическим анамнезом [1, 5]. Механизмы иммунологического реагирования у детей первых лет жизни бывают особенно выраженными при возникновении острого обструктивного (стенозирующего) ларингита (ложного крупа) на фоне гиперчувствительности дыхательных путей к инфекционным триггерным факторам, являющимся причиной острого респираторного заболевания (ОРЗ). Синдром ложного крупа может возникать при всех ОРЗ: гриппе, парагриппе, аденовирусной, респираторно-синцитиальной (РС) инфекции, риновирусной инфекции, а также при смешанной вирусно-вирусной или вирусно-бактериальной этиологии заболевания. Наиболее часто этот синдром возникает при парагриппе, а наиболее тяжело протекает при гриппе, являясь одной из главных причиной летальности детей при этой инфекции.
В патогенезе развития стеноза гортани существенное значение имеют избыточная продукция лейкотриенов и провоспалительных цитокинов на фоне накопления иммунных комплексов «иммуноглобулин E (IgE) – антиген», индуцирующих выброс биологически активных веществ (серотонина, гистамина и др.). Это способствует развитию аллергического воспаления по экссудативно-деструктивному варианту с аллергическим отеком в области гортани, сопровождающимся рефлекторным спазмом голосовой щели (стенозом гортани), болью при глотании на фоне воздействия медиаторов воспаления [6, 7]. К группе риска по развитию синдрома крупа при вирусных и вирусно-бактериальных инфекциях относят детей с атопической аномалией конституции (c атопическим дерматитом, поллинозом, пищевой аллергией), часто и длительно болеющих детей, сенсибилизированных предшествующими инфекциями или лекарственными препаратами, а также находящихся в поствакцинальном периоде.
В настоящее время Всемирной организацией здравоохранения (ВОЗ) для использования при лихорадке у детей рекомендуются только парацетамол и ибупрофен. В последнее время клиницисты все чаще отдают предпочтение ибупрофену. Данные метаанализа 17 слепых рандомизированных контролируемых исследований в педиатрии свидетельствуют о превосходстве ибупрофена над парацетамолом в отношении антипиретической, противовоспалительной и анальгезирующей активности [8]. С учетом изложенных механизмов развития основных симптомов, нам представлялось патогенетически обоснованным у больных ОРЗ с синдромом крупа назначать ибупрофен в качестве средства, направленного на угнетение синтеза простагландинов за счет снижения активности циклооксигеназы (ЦОГ) и тем самым способствующего нормализации температуры тела, анальгезирующему эффекту и уменьшению воспалительной реакции. Если парацетамол обладает только центральным жаропонижающим и анальгезирующим свойством, то ибупрофен оказывает двойное антипиретическое действие – центральное и периферическое, что обусловленно ингибированием ПГЕ в поврежденных тканях. Как результат – снижается активность воспаления, продукция цитокинов его острой фазы, в том числе эндогенного пирогена ИЛ-1, снижается продукция ПГЕ в центральной нервной системе (ЦНС) и нормализуется температура тела. При этом нет риска развития ларинго- или бронхоспазма на фоне ОРВИ [5, 9].
Мы сочли перспективным использование нестероидного противовоспалительного препарата ибупрофена у пациентов с лихорадочным состоянием на фоне ОРЗ с гиперчувствительностью дыхательных путей, проявляющейся крупом и/или бронхообструкцией и нередко сопровождающейся отитом. Ибупрофен хорошо переносится детьми и может применяться у младенцев и недоношенных детей. Препарат выпускается компанией «Бутс Хэлскэр Интернешнл» (Boots Healthcare International, Великобритания) под торговым названием «Нурофен® для детей» (Nurofen® for Children), действующее вещество (RS)-2-(4-изобутилфенил)-пропионовая кислота. Оптимальный режим дозирования в педиатрической практике достигается при приеме препарата в форме суспензии или сиропа. 1 мл суспензии содержит 20 мг ибупрофена, а также вспомогательные вещества: сироп мальтитола, глицерин, лимонную кислоту, натрия цитрат, натрия хлорид, натрия сахаринат, апельсиновый ароматизатор, ксантиновый наполнитель, полисорбат 80, домифена бромид. Суспензия дозируется с помощью прилагаемой двусторонней мерной ложки (вместимостью 2,5 и 5 мл) или мерного шприца. Целью настоящей работы явилось изучение переносимости и терапевтической эффективности Нурофена для детей при ОРВИ со стенозирующим ларинготрахеитом у детей в качестве жаропонижающего, противовоспалительного и анальгезирующего средства.
Материалы и методы исследования
В открытом рандомизированном контролируемом исследовании определяли влияние Нурофена для детей на основные клинико-лабораторные показатели у детей при ОРВИ с синдромом крупа и возможное побочное действие препарата. Под наблюдением находились 50 детей в возрасте от 6 месяцев до 12 лет с обструктивным ларингитом (ложным крупом) на фоне ОРВИ. Из исследования исключались дети с повышенной чувствительностью к ибупрофену, ацетилсалициловой кислоте или другим нестероидным противовоспалительным средствам (НПВС), а также к другим компонентам препарата; страдающие бронхиальной астмой, крапивницей, ринитом, спровоцированными приемом ацетилсалициловой кислоты (салицилатами) или другими НПВС; с заболеваниями крови: гипокоагуляцией, лейкопенией, гемофилией; язвенным поражением желудочно-кишечного тракта (ЖКТ); почечной и/или печеночной недостаточностью; снижением слуха; дефицитом глюкозо-6-фосфатдегидрогеназы.
Основную группу составили 30 детей, получавших Нурофен® для детей. Среди них ОРВИ со стенозирующим ларинготрахеитом 1-й степени стеноза была у 22 больных, 2-й степени стеноза – у 6 больных; обструктивный бронхит диагностирован у 2 детей; острый средний отит (ОСО) – у 4; конъюнктивит – у 2 детей. Группу сравнения составили 20 детей, получавших Детский Панадол. Среди них ОРВИ со стенозирующим ларинготрахеитом 1-й степени стеноза была у 14 больных; 2-й степени стеноза – у 6 детей. ОСО диагностирован у 2; конъюнктивит – у 1; атопический дерматит – у 2 детей. Нурофен® для детей назначался перорально в следующих дозировках: детям в возрасте от 6 до 12 месяцев – по 2,5 мл; от 1 до 3 лет – по 5 мл; от 4 до 6 лет – по 7,5 мл; от 7 до 9 лет – по 10 мл; от 10 до 12 лет – по 15 мл 3 раза в течение 24 часов. Разовая доза составляла 5–10 мг/кг массы тела ребенка 3–4 раза в сутки. Максимальная суточная доза не превышала 30 мг/кг массы тела ребенка в сутки. Лечение Нурофеном для детей проводилось в составе комбинированной терапии (симптоматической, антигистаминной, противовирусной и/или антибиотикотерапии). Глюкокортикоидные препараты не применялись в обеих группах.
В динамике наблюдения оценивались основные клинические проявления болезни: продолжительность лихорадки и симптомов интоксикации, ларингита со стенозом гортани, болевого синдрома при ларингите и отите, сухого кашля и продукции мокроты, а также возможные симптомы побочного действия препарата. Эффективность Нурофена для детей определялась на основании сравнительного анализа динамики купирования основных клинических симптомов заболевания в основной и контрольной группах, а также на основании результатов клинического анализа крови и мочи, по показаниям – на основании результатов рентгенологического исследования органов грудной клетки. Эффективность терапии определяли следующим образом: терапию оценивали как «отличную» – при улучшении общего состояния, исчезновении лихорадки, симптомов интоксикации, выраженных воспалительных явлений со стороны дыхательных путей и ротоглотки в первые 2–3 дня от начала приема препарата; как «хорошую» – при улучшении общего состояния, исчезновении симптомов интоксикации и катаральных явлений спустя 2–3 дня после отмены препарата; как «удовлетворительную» – при улучшении общего состояния и исчезновении симптомов респираторного заболевания более чем через 4–5 дней после отмены препарата; считали, что «нет эффекта» – в отсутствие динамики вышеперечисленных симптомов на фоне приема препарата.
Обе группы больных были сопоставимы по основным клиническим проявлениям заболевания. Большинство больных поступали в 1–2-е сутки от начала заболевания с симптомами стеноза гортани, лихорадкой выше 38 °С, из них у 87% температура тела была выше 39 °С, интоксикация была умеренной или выраженной; у 100% больных воспалительные явления в ротоглотке сопровождались выраженной гиперемией, отеком миндалин, у старших детей при этом отмечались жалобы на боль в горле при глотании и/или в ухе при наличии ОСО; у всех детей отмечался сухой грубый кашель без продукции мокроты или с незначительной продукцией. У 2 детей испытуемой группы, у которых стеноз гортани сопровождался бронхообструкцией, одышка носила смешанный и более затяжной характер.
Результаты и их обсуждение
У больных, получавших Нурофен® для детей, быстрая и стойкая нормализация температуры тела и исчезновение симптомов интоксикации ко 2-м и 3-м суткам от начала терапии отмечены у 44% и 60% соответственно, а в группе сравнения – только у 30% и 40% детей соответственно. У большинства детей прием Детского Панадола требовался каждые 3–4 часа, на фоне нового подъема температуры. В последующие 4–5 дней приема препарата мы не выявили достоверных различий в скорости купирования указанных симптомов (рис. 1). Симптомы стеноза гортани в испытуемой группе исчезали ко 2-м и 3-м суткам от начала терапии у 52% и 88% больных соответственно, к 4-м суткам – у всех больных; в то же время среди пациентов, получавших Детский Панадол, эти симптомы сохранялись у 10% детей и полностью исчезали к 5-м суткам терапии (рис. 2). При этом жалобы на боль в ротоглотке и ухе у пациентов, получавших Нурофен® для детей, ко 2-м суткам терапии исчезали у 90% больных, а в группе сравнения – только у 30% детей (рис. 3).
Исчезновение сухого кашля, обусловленное эффектом разжижения мокроты, у детей испытуемой группы наблюдалось раньше, чем у пациентов контрольной группы, – со 2-х суток лечения. С 3–4-х суток достоверных различий в характере кашля (сухой или влажный продуктивный) между группами не выявили (рис. 4 и 5). В итоге эффективность терапии был оценена как «отличная» и «хорошая» у 80% детей, получавших Нурофен® для детей, и у 67% детей, получавших Детский Панадол (рис. 6). Ни у кого из пациентов, получавших Нурофен® для детей, не отмечалось возникновения нежелательных побочных явлений, тогда как у 3 детей из числа получавших Детский Панадол появилась аллергическая экзантема, которая исчезла сразу после парентерального введения антигистаминного препарата Супрастина. Прием Детского Панадола к моменту появления аллергической реакции отменялся в связи со снижением или нормализацией температуры тела. Ни один из наблюдавшихся пациентов на фоне приема Нурофена для детей или Детского Панадола не был исключен из исследования. Не было зарегистрировано и отказов больных или их представителей от дальнейшего приема препарата.
Заключение
Полученные нами результаты, указывающие на более быстрое развитие и более выраженное жаропонижающее, противовоспалительное и аналгезирующее действие ибупрофена в сравнении с парацетамолом у детей при ОРВИ со стенозом гортани и отитом, полностью согласуются с данными, опубликованными S.M. Lesko и A.A. Mitchell [8, 10]. Нурофен® для детей хорошо переносится, не вызывая побочных нежелательных эффектов, в то время как на фоне приема Детского Панадола у части детей отмечалась аллергическая сыпь. Это полностью совпадает с данными литературы, свидетельствующими о том, что, в отличие от парацетамола, ибупрофен не образует токсичные метаболиты [8, 10]. Препарат метаболизируется в печени, быстро выводится из плазмы с относительно коротким периодом полувыведения, составляющим около 2 часов. Менее 10% препарата выводится в неизмененном виде с мочой. Экскреция метаболитов с мочой завершается в течение 24 часов с момента приема последней дозы и находится в линейной зависимости от величины дозы. Его терапевтический индекс примерно в 4 раза выше, чем у парацетамола [11].
Результаты проведенного исследования позволяют считать суспензию Нурофен® для детей высокоэффективным жаропонижающим, противовоспалительным и обезболивающим средством. Таким образом, данные литературных источников, подтвержденные собственным клиническим опытом, позволяют сделать следующие выводы:
Особенно актуальным является поиск эффективного и безопасного жаропонижающего средства для детей с отягощенным аллергическим анамнезом [1, 5]. Механизмы иммунологического реагирования у детей первых лет жизни бывают особенно выраженными при возникновении острого обструктивного (стенозирующего) ларингита (ложного крупа) на фоне гиперчувствительности дыхательных путей к инфекционным триггерным факторам, являющимся причиной острого респираторного заболевания (ОРЗ). Синдром ложного крупа может возникать при всех ОРЗ: гриппе, парагриппе, аденовирусной, респираторно-синцитиальной (РС) инфекции, риновирусной инфекции, а также при смешанной вирусно-вирусной или вирусно-бактериальной этиологии заболевания. Наиболее часто этот синдром возникает при парагриппе, а наиболее тяжело протекает при гриппе, являясь одной из главных причиной летальности детей при этой инфекции.
В патогенезе развития стеноза гортани существенное значение имеют избыточная продукция лейкотриенов и провоспалительных цитокинов на фоне накопления иммунных комплексов «иммуноглобулин E (IgE) – антиген», индуцирующих выброс биологически активных веществ (серотонина, гистамина и др.). Это способствует развитию аллергического воспаления по экссудативно-деструктивному варианту с аллергическим отеком в области гортани, сопровождающимся рефлекторным спазмом голосовой щели (стенозом гортани), болью при глотании на фоне воздействия медиаторов воспаления [6, 7]. К группе риска по развитию синдрома крупа при вирусных и вирусно-бактериальных инфекциях относят детей с атопической аномалией конституции (c атопическим дерматитом, поллинозом, пищевой аллергией), часто и длительно болеющих детей, сенсибилизированных предшествующими инфекциями или лекарственными препаратами, а также находящихся в поствакцинальном периоде.
В настоящее время Всемирной организацией здравоохранения (ВОЗ) для использования при лихорадке у детей рекомендуются только парацетамол и ибупрофен. В последнее время клиницисты все чаще отдают предпочтение ибупрофену. Данные метаанализа 17 слепых рандомизированных контролируемых исследований в педиатрии свидетельствуют о превосходстве ибупрофена над парацетамолом в отношении антипиретической, противовоспалительной и анальгезирующей активности [8]. С учетом изложенных механизмов развития основных симптомов, нам представлялось патогенетически обоснованным у больных ОРЗ с синдромом крупа назначать ибупрофен в качестве средства, направленного на угнетение синтеза простагландинов за счет снижения активности циклооксигеназы (ЦОГ) и тем самым способствующего нормализации температуры тела, анальгезирующему эффекту и уменьшению воспалительной реакции. Если парацетамол обладает только центральным жаропонижающим и анальгезирующим свойством, то ибупрофен оказывает двойное антипиретическое действие – центральное и периферическое, что обусловленно ингибированием ПГЕ в поврежденных тканях. Как результат – снижается активность воспаления, продукция цитокинов его острой фазы, в том числе эндогенного пирогена ИЛ-1, снижается продукция ПГЕ в центральной нервной системе (ЦНС) и нормализуется температура тела. При этом нет риска развития ларинго- или бронхоспазма на фоне ОРВИ [5, 9].
Мы сочли перспективным использование нестероидного противовоспалительного препарата ибупрофена у пациентов с лихорадочным состоянием на фоне ОРЗ с гиперчувствительностью дыхательных путей, проявляющейся крупом и/или бронхообструкцией и нередко сопровождающейся отитом. Ибупрофен хорошо переносится детьми и может применяться у младенцев и недоношенных детей. Препарат выпускается компанией «Бутс Хэлскэр Интернешнл» (Boots Healthcare International, Великобритания) под торговым названием «Нурофен® для детей» (Nurofen® for Children), действующее вещество (RS)-2-(4-изобутилфенил)-пропионовая кислота. Оптимальный режим дозирования в педиатрической практике достигается при приеме препарата в форме суспензии или сиропа. 1 мл суспензии содержит 20 мг ибупрофена, а также вспомогательные вещества: сироп мальтитола, глицерин, лимонную кислоту, натрия цитрат, натрия хлорид, натрия сахаринат, апельсиновый ароматизатор, ксантиновый наполнитель, полисорбат 80, домифена бромид. Суспензия дозируется с помощью прилагаемой двусторонней мерной ложки (вместимостью 2,5 и 5 мл) или мерного шприца. Целью настоящей работы явилось изучение переносимости и терапевтической эффективности Нурофена для детей при ОРВИ со стенозирующим ларинготрахеитом у детей в качестве жаропонижающего, противовоспалительного и анальгезирующего средства.
Материалы и методы исследования
В открытом рандомизированном контролируемом исследовании определяли влияние Нурофена для детей на основные клинико-лабораторные показатели у детей при ОРВИ с синдромом крупа и возможное побочное действие препарата. Под наблюдением находились 50 детей в возрасте от 6 месяцев до 12 лет с обструктивным ларингитом (ложным крупом) на фоне ОРВИ. Из исследования исключались дети с повышенной чувствительностью к ибупрофену, ацетилсалициловой кислоте или другим нестероидным противовоспалительным средствам (НПВС), а также к другим компонентам препарата; страдающие бронхиальной астмой, крапивницей, ринитом, спровоцированными приемом ацетилсалициловой кислоты (салицилатами) или другими НПВС; с заболеваниями крови: гипокоагуляцией, лейкопенией, гемофилией; язвенным поражением желудочно-кишечного тракта (ЖКТ); почечной и/или печеночной недостаточностью; снижением слуха; дефицитом глюкозо-6-фосфатдегидрогеназы.
Основную группу составили 30 детей, получавших Нурофен® для детей. Среди них ОРВИ со стенозирующим ларинготрахеитом 1-й степени стеноза была у 22 больных, 2-й степени стеноза – у 6 больных; обструктивный бронхит диагностирован у 2 детей; острый средний отит (ОСО) – у 4; конъюнктивит – у 2 детей. Группу сравнения составили 20 детей, получавших Детский Панадол. Среди них ОРВИ со стенозирующим ларинготрахеитом 1-й степени стеноза была у 14 больных; 2-й степени стеноза – у 6 детей. ОСО диагностирован у 2; конъюнктивит – у 1; атопический дерматит – у 2 детей. Нурофен® для детей назначался перорально в следующих дозировках: детям в возрасте от 6 до 12 месяцев – по 2,5 мл; от 1 до 3 лет – по 5 мл; от 4 до 6 лет – по 7,5 мл; от 7 до 9 лет – по 10 мл; от 10 до 12 лет – по 15 мл 3 раза в течение 24 часов. Разовая доза составляла 5–10 мг/кг массы тела ребенка 3–4 раза в сутки. Максимальная суточная доза не превышала 30 мг/кг массы тела ребенка в сутки. Лечение Нурофеном для детей проводилось в составе комбинированной терапии (симптоматической, антигистаминной, противовирусной и/или антибиотикотерапии). Глюкокортикоидные препараты не применялись в обеих группах.
В динамике наблюдения оценивались основные клинические проявления болезни: продолжительность лихорадки и симптомов интоксикации, ларингита со стенозом гортани, болевого синдрома при ларингите и отите, сухого кашля и продукции мокроты, а также возможные симптомы побочного действия препарата. Эффективность Нурофена для детей определялась на основании сравнительного анализа динамики купирования основных клинических симптомов заболевания в основной и контрольной группах, а также на основании результатов клинического анализа крови и мочи, по показаниям – на основании результатов рентгенологического исследования органов грудной клетки. Эффективность терапии определяли следующим образом: терапию оценивали как «отличную» – при улучшении общего состояния, исчезновении лихорадки, симптомов интоксикации, выраженных воспалительных явлений со стороны дыхательных путей и ротоглотки в первые 2–3 дня от начала приема препарата; как «хорошую» – при улучшении общего состояния, исчезновении симптомов интоксикации и катаральных явлений спустя 2–3 дня после отмены препарата; как «удовлетворительную» – при улучшении общего состояния и исчезновении симптомов респираторного заболевания более чем через 4–5 дней после отмены препарата; считали, что «нет эффекта» – в отсутствие динамики вышеперечисленных симптомов на фоне приема препарата.
Обе группы больных были сопоставимы по основным клиническим проявлениям заболевания. Большинство больных поступали в 1–2-е сутки от начала заболевания с симптомами стеноза гортани, лихорадкой выше 38 °С, из них у 87% температура тела была выше 39 °С, интоксикация была умеренной или выраженной; у 100% больных воспалительные явления в ротоглотке сопровождались выраженной гиперемией, отеком миндалин, у старших детей при этом отмечались жалобы на боль в горле при глотании и/или в ухе при наличии ОСО; у всех детей отмечался сухой грубый кашель без продукции мокроты или с незначительной продукцией. У 2 детей испытуемой группы, у которых стеноз гортани сопровождался бронхообструкцией, одышка носила смешанный и более затяжной характер.
Результаты и их обсуждение
У больных, получавших Нурофен® для детей, быстрая и стойкая нормализация температуры тела и исчезновение симптомов интоксикации ко 2-м и 3-м суткам от начала терапии отмечены у 44% и 60% соответственно, а в группе сравнения – только у 30% и 40% детей соответственно. У большинства детей прием Детского Панадола требовался каждые 3–4 часа, на фоне нового подъема температуры. В последующие 4–5 дней приема препарата мы не выявили достоверных различий в скорости купирования указанных симптомов (рис. 1). Симптомы стеноза гортани в испытуемой группе исчезали ко 2-м и 3-м суткам от начала терапии у 52% и 88% больных соответственно, к 4-м суткам – у всех больных; в то же время среди пациентов, получавших Детский Панадол, эти симптомы сохранялись у 10% детей и полностью исчезали к 5-м суткам терапии (рис. 2). При этом жалобы на боль в ротоглотке и ухе у пациентов, получавших Нурофен® для детей, ко 2-м суткам терапии исчезали у 90% больных, а в группе сравнения – только у 30% детей (рис. 3).
Исчезновение сухого кашля, обусловленное эффектом разжижения мокроты, у детей испытуемой группы наблюдалось раньше, чем у пациентов контрольной группы, – со 2-х суток лечения. С 3–4-х суток достоверных различий в характере кашля (сухой или влажный продуктивный) между группами не выявили (рис. 4 и 5). В итоге эффективность терапии был оценена как «отличная» и «хорошая» у 80% детей, получавших Нурофен® для детей, и у 67% детей, получавших Детский Панадол (рис. 6). Ни у кого из пациентов, получавших Нурофен® для детей, не отмечалось возникновения нежелательных побочных явлений, тогда как у 3 детей из числа получавших Детский Панадол появилась аллергическая экзантема, которая исчезла сразу после парентерального введения антигистаминного препарата Супрастина. Прием Детского Панадола к моменту появления аллергической реакции отменялся в связи со снижением или нормализацией температуры тела. Ни один из наблюдавшихся пациентов на фоне приема Нурофена для детей или Детского Панадола не был исключен из исследования. Не было зарегистрировано и отказов больных или их представителей от дальнейшего приема препарата.
Заключение
Полученные нами результаты, указывающие на более быстрое развитие и более выраженное жаропонижающее, противовоспалительное и аналгезирующее действие ибупрофена в сравнении с парацетамолом у детей при ОРВИ со стенозом гортани и отитом, полностью согласуются с данными, опубликованными S.M. Lesko и A.A. Mitchell [8, 10]. Нурофен® для детей хорошо переносится, не вызывая побочных нежелательных эффектов, в то время как на фоне приема Детского Панадола у части детей отмечалась аллергическая сыпь. Это полностью совпадает с данными литературы, свидетельствующими о том, что, в отличие от парацетамола, ибупрофен не образует токсичные метаболиты [8, 10]. Препарат метаболизируется в печени, быстро выводится из плазмы с относительно коротким периодом полувыведения, составляющим около 2 часов. Менее 10% препарата выводится в неизмененном виде с мочой. Экскреция метаболитов с мочой завершается в течение 24 часов с момента приема последней дозы и находится в линейной зависимости от величины дозы. Его терапевтический индекс примерно в 4 раза выше, чем у парацетамола [11].
Результаты проведенного исследования позволяют считать суспензию Нурофен® для детей высокоэффективным жаропонижающим, противовоспалительным и обезболивающим средством. Таким образом, данные литературных источников, подтвержденные собственным клиническим опытом, позволяют сделать следующие выводы:
- Нурофен® для детей оказывает более выраженное и быстро развивающееся в сравнении с Детским Панадолом жаропонижающее, обезболивающее и противовоспалительное действие у детей при ОРВИ, сопровождающихся стенозом гортани, острым средним отитом и обструктивным бронхитом;
- Нурофен® для детей является безопасным высокоэффективным препаратом, который приносит облегчение ребенку, улучшает его самочувствие, ускоряет сроки выздоровления и сокращает время госпитализации при ОРВИ со стенозирующим ларинготрахеитом;
- Нурофен® для детей целесообразно применять при ОРВИ, сопровождающихся стенозирующим ларинготрахеитом и отитом, наряду с этиотропной терапией в качестве патогенетического жаропонижающего, противовоспалительного и обезболивающего средства и рекомендовать его для широкого использования в педиатрической практике у детей с отягощенным аллергоанамнезом.
NB: Нурофен® для детей (Nurofen® for Children)
- Действующее вещество – (RS)-2-(4-изобутилфенил)-пропионовая кислота.
- Оказывает двойное антипиретическое действие – центральное и периферическое, что обусловленно ингибированием ПГЕ в поврежденных тканях.
- Хорошо переносится детьми и может применяться у младенцев и недоношенных детей.
- Оптимальный режим дозирования в педиатрической практике достигается при приеме препарата в форме суспензии или сиропа.
- Терапевтический индекс примерно в 4 раза выше, чем у парацетамола.
- Метаболизируется в печени, быстро выводится из плазмы с относительно коротким периодом полувыведения, составляющим около 2 часов.
1. Коровина Н.А., Заплатников А.Л., Захарова И.Н. Лихорадка у детей. Рациональный выбор жаропонижающих лекарственных средств. Руководство для врачей. М., 2000. 67 с.
2. Геппе Н.А., Зайцева О.В. Представления о механизмах лихорадки у детей и принципах жаропонижающей терапии // РМЖ. 2003. Т. 11. № 1 (173). С. 31–37.
3. Ветров В.П., Длин В.В., Османов И.М. и др. Рациональное использование антипиретиков в детском возрасте. Пособие для врачей / Под ред. А.Д. Царегородцева. М.: Московский НИИ педиатрии и детской хирургии, 2005. 25 с.
4. Saha K. Use of nimesulide in Indian children must be stopped // BMJ. 2003. Vol. 326. № 7391. P. 713.
5. Зайцева О.В. Лихорадка у детей с аллергическими реакциями и заболеваниями // Лечащий врач. 2003. № 3. С. 48–52.
6. Студеникин М.Я., Корюкина И.П., Каплин В.Н. Клиника, диагностика, лечение и профилактика острых и рецидивирующих стенозов верхних дыхательных путей у детей. Пермь, 1991.
7. Кладова О.В. Иммунопатогенез, клиника, лечение рецидивирующего крупа у детей: Автореферат дисс. … докт. мед. наук. М., 2003. 55 с.
8. Lesko S.M., Mitchell A.A. An assessment of the safety of pediatric ibuprofen. A practitioner-based randomized clinical trial // JAMA. 1995. Vol. 273. № 12. P. 929–933.
9. Perrott D.A., Piira T., Goodenough B., Champion G.D. Efficacy and safety of acetaminophen vs ibuprofen for treating children's pain or fever: a meta-analysis // Arch. Pediatr. Adolesc. Med. 2004. Vol. 158. № 6. P. 521–526.
10. Lesko S.M. The safety of ibuprofen suspension in children // Int. J. Clin. Pract. Suppl. 2003. № 135. P. 50–53.
11. Kelley M.T., Walson P.D., Edge J.H. et al. Pharmacokinetics and pharmacodynamics of ibuprofen isomers and acetaminophen in febrile children // Clin. Pharmacol. Ther. 1992. Vol. 52. № 2. P. 181–189.
Новости на тему
22.02.2024
Отправить статью по электронной почте
Ваш адрес электронной почты:
На основании собственного клинического опыта показано, что суспензия Нурофен® для детей является высокоэффективным жаропонижающим, противовоспалительным и обезболивающим средством, практически не вызывающим возникновения нежелательных побочных явлений.
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Суспензия Нурофен® для детей оказывает более выраженное и быстрое в сравнении с Детским Панадолом действие у пациентов с острыми респираторными вирусными заболеваниями, сопровождающимися стенозом гортани, острым средним отитом и обструктивным бронхитом.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
