Клинико-иммунологическая эффективность и целесообразность использования иммунотропной терапии при герпетической инфекции у детей
- Аннотация
- Статья
- Ссылки
- English


Разработка новых стратегий борьбы с герпетической инфекцией – одна из приоритетных задач современного мирового медицинского сообщества. При этом основой ряда профилактических и терапевтических стратегий борьбы с вирусом простого герпеса (ВПГ) является улучшение локального врожденного и адаптивного антигерпетического иммунитета слизистых оболочек [1]. В этом отношении клинический и диагностический интерес представляют исследования инфицирования вирусами семейства Herpesviridae (цитомегаловирус (ЦМВ), ВПГ), отличающимися различными механизмами ускользания от иммунного надзора [2], широким распространением и высокой частотой передачи от матери ребенку [3, 4].
Врожденный иммунитет играет существенную роль в патогенезе ВПГ-инфекции, являясь первой линией обороны от антигенов вируса за счет гуморальных (система комплемента, цитокины, хемокины) и клеточных (фагоциты, NK-лимфоциты, гамма-дельта-T-клетки) факторов, обеспечивающих условия для реализации адаптивного противовирусного иммунитета [5, 6]. При этом цитокины оказывают противовирусный эффект либо непосредственно через рецепторы, либо опосредованно через иммунотропные эффекты других структур врожденного иммунитета.
В ряде клинических и экспериментальных исследований продемонстрирована эффективность цитокиновой (интерфероновой) терапии в отношении герпетической инфекции как эффективного средства для подавления вирусной инфекции и распространения ВПГ 1-го типа [7].
Кроме того, фагоцитирующие клетки врожденного иммунитета оказывают антигерпетическое действие. Так, в первые часы после заражения активируются функции макрофагов (фагоцитарная, цитотоксическая, секреторная и антигенпрезентирующая) [8], тогда как нейтрофилы играют ключевую роль в рекрутировании Т- и B-лимфоцитов и контроле вирусной репликации при ВПГ 1-го и 2-го типов некоторых слизистых оболочек [9].
Исходя из сказанного одним из перспективных подходов к оптимизации базисной терапии герпесвирусных инфекций считается включение в нее иммуномодуляторов направленного действия, способствующих усилению функциональной активности фагоцитов как основной популяции клеток врожденного иммунитета. Перспективными корректорами дефектов функциональной активности клеток врожденного иммунитета (нейтрофильных гранулоцитов, моноцитарно-макрофагальных клеток) признаны агонисты их рецепторов в виде синтетических и природных минимальных биологически активных фрагментов (МБАФ) патоген-ассоциированных молекул. В частности, речь идет о единственном зарегистрированном в России в качестве лекарственного препарата синтетического МБАФ глюкозаминилмурамилдипептида (ГМДП) иммуномодуляторе Ликопиде [10]. ГМДП представляет собой МБАФ пептидогликана клеточной стенки всех известных бактерий [11]. Его основной точкой приложения являются фагоцитирующие клетки [12, 13], активация которых происходит при взаимодействии ГМДП и специфических внутриклеточно расположенных NOD2-рецепторов с последующим синтезом провоспалительных цитокинов [14]. Таким образом, основные механизмы действия ГМДП заключаются в увеличении экспрессии HLA-DR антигенов, усилении поглощения микроорганизмов и завершенности фагоцитарного акта за счет повышения уровня лизосомальных ферментов и образования активных форм кислорода, увеличении продукции провоспалительных цитокинов (интерлейкинов 1-бета и 12, фактора некроза опухоли альфа, колониестимулирующего фактора), а также усилении цитотоксичности по отношению к вирус-инфицированным и опухолевым клеткам. Об эффективности Ликопида в терапии герпесвирусных инфекций у детей свидетельствуют накопленные к настоящему времени данные клинико-лабораторных наблюдений.
Показано, что комплексная терапия детей с респираторно-герпетическим инфицированием, включающая иммуномодулятор Ликопид, интерферон (Виферон) и индуктор интерферона (Циклоферон), позволяет не только оптимизировать метаболизм лимфоцитов в условиях инфекционного стресса, получить достоверные доказательства клинической эффективности такого лечения, но и разработать дифференцированный подход к назначению указанных иммунотропных препаратов [15]. В частности, при неосложненных формах острой респираторной вирусной инфекции (ОРВИ) на ранних сроках заболевания показано стартовое использование Виферона. У больных с нарушениями в неврологическом статусе, неоднократно получавших терапию Вифероном и переносящих неосложненные формы ОРВИ или ОРВИ с бронхитами, целесообразно применение Циклоферона. Больным детям, госпитализированным на поздних сроках от начала заболевания, переносящим осложненные формы ОРВИ (пневмонии), прошедшим повторные курсы антибиотикотерапии и предрасположенным к формированию вторичной бактериальной инфекции, показан иммуномодулятор Ликопид. Следует также отметить, что включение в базисную терапию Ликопида, равно как Виферона и Циклоферона, обеспечивает «мягкую» нормализацию гормонального фона во всех группах пациентов с разным уровнем метаболической активности лимфоцитов [15]. При ОРВИ на фоне герпеса, осложненных пневмониями, отмечался положительный эффект при сочетанном использовании Ликопида и Циклоферона и в меньшей степени – при использовании Виферона. Это позволило сделать вывод, что при осложненном течении ОРВИ во избежание повторных бактериальных осложнений целесообразно применение Ликопида.
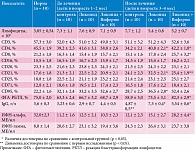
При поиске клинико-лабораторных критериев для дифференцированной терапии детей раннего возраста с перинатальной герпесвирусной инфекцией обоснована необходимость иммуномодулирующей терапии. При оценке иммунного статуса у пациентов было выявлено увеличение относительного содержания клеток с маркерами активации (CD71, CD95) и концентрации интерферона (ИФН) гамма, а также снижение относительной доли лимфоцитов CD3+, CD4+, CD8+ и концентрации ИФН-альфа. Это позволило не только обосновать диспансерное наблюдение в течение первого года жизни за такими пациентами, но и определить дифференцированный подход к иммуномодулирующей терапии [16]. В частности, установлено, что использование Ликопида в составе базисной терапии стабилизирует преимущественно гуморальный иммунный ответ пациентов, тогда как его сочетание с Вифероном оказывает нормализующее действие на клеточно-опосредованный иммунитет (см. таблицу).
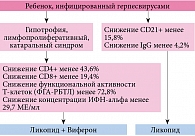
В основу дифференцированного подхода к иммунотерапии детей, инфицированных герпесвирусами и имеющих клинические признаки гипотрофии, лимфопролиферативного и катарального синдрома, легли лабораторные критерии лимфоцитов CD21+ (менее 15,81%) и концентрация IgG (менее 4,2 г/л) (рис. 1).
Достоверную клинико-иммунологическую эффективность сочетанной терапии Ликопидом и рекомбинантным ИФН-альфа (Вифероном) у детей с ассоциированными респираторными и герпетическими вирусными инфекциями продемонстрировали результаты исследования, проведенного в 2014 г. [17].
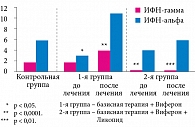
Наряду с клинической эффективностью (сокращение частоты ОРВИ, увеличение длительности клинически благополучного периода, уменьшение количества детей с рецидивами ВПГ-инфекции) зафиксированы достоверные иммунотропные эффекты сочетанной базисной традиционной терапии с использованием иммуномодулятора Ликопида в виде нормализации уровня ИФН-альфа (рис. 2), а также числа активно фагоцитирующих нейтрофильных лейкоцитов, их поглотительной, переваривающей способности и усиления резервной NADPH-оксидазной активности нейтрофильных гранулоцитов (рис. 3).
По мнению авторов, включение в программу комбинированной интерфероно- и иммунотерапии иммуномодулирующей терапии Ликопидом при наличии преобладающего дефектного функционирования нейтрофильных гранулоцитов у детей с ассоциированными возвратными респираторными и различными герпетическими вирусными инфекциями имеет существенные преимущества, связанные с эффективной коррекцией выявленных нарушений в системе нейтрофильных гранулоцитов – важных клеточных факторов врожденного иммунитета, являющихся весомым компонентом клеточной иммунной реакции против вирус-инфицированных клеток в ранней фазе вирусной инфекции [5]. Необходимо отметить, что выраженная клинико-иммунологическая эффективность последовательной терапии иммуномодулятором Ликопид на фоне стандартной базисной терапии (Изопринозин, интерферонотерапия) подтверждена указанными исследователями и у взрослых пациентов, страдающих хроническим упорно-рецидивирующим орофациальным герпесом [18].
В публикациях приводятся данные об использовании Ликопида у детей с выявленной предрасположенностью к бактериальным инфекциям и инфицированных вирусом Эпштейна – Барр для предотвращения иммунологической дисфункции и негладкого течения периода реконвалесценции [19]. У пациентов, получавших иммунотропную терапию Ликопидом, отмечались купирование астеновегетативного синдрома (76,9%), достоверное снижение содержания атипичных мононуклеаров в крови (с 9,1 ± 1,2% до 1,0 ± 0,5%), нормализация уровня содержания ИФН-гамма (снижение в 1,4 раза). При наблюдении в течение года за больными, получавшими Ликопид в периоде ранней реконвалесценции, было установлено, что частота интеркуррентных заболеваний у них была в три раза ниже, чем в группе контроля.
Клинические эффекты комплексного этиотропного лечения, включающего иммуномодулятор Ликопид в сочетании с иммунозаместительной терапией (Иммуновенин) у новорожденных и детей грудного возраста с инфекцией, вызванной ВПГ 1-го и 2-го типов, состоят в значимом сокращении длительности конъюгационной желтухи, везикулярной сыпи, лимфоаденита и частоты ОРВИ, увеличения размеров печени и гипотрофии [20]. Выявлены отчетливые иммуномодулирующие эффекты комплексной иммунотропной терапии, характеризующиеся достоверно более высоким содержанием относительного и абсолютного количества Т-лимфоцитов (CD3+, CD8+) и снижением относительного количества В-лимфоцитов (CD20+) через три месяца после окончания курса лечения [20].
Выявленная высокая фармакоэкономическая эффективность Ликопида в терапии вирусного гепатита у детей с врожденной ЦМВ-инфекцией основана на достоверных данных о сокращении длительности периода активности заболевания, длительности противовирусной терапии, быстром улучшении состояния, снижении потребности в применении глюкокортикоидных гормонов, сочетающихся с выраженным иммуномодулирующим действием иммуномодулятора (устранение глубоких дефектов продукции ИФН-гамма, восстановление фагоцитарной функции лейкоцитов, содержания цитотоксических CD8+ Т-лимфоцитов, а также В-клеток (CD19+) с нормализацией продукции ими сывороточного IgG (рис. 4) [21].
Таким образом, отечественный иммуномодулятор Ликопид, представляющий собой активный фрагмент бактериальных клеточных стенок, ответственный за иммуностимулирующий эффект целых бактерий, является природным регулятором иммунитета, выработанным в процессе эволюции. Препарат характеризуется комплексным воздействием на иммунную систему организма, стимулирует функциональную активность фагоцитирующих клеток, усиливает пролиферацию Т- и В-лимфоцитов. Высокая клинико-иммунологическая эффективность Ликопида в составе комплексной терапии герпетических инфекций у детей обуславливает целесообразность его использования для потенцирования защитных сил организма в реализации иммунотропной стратегии борьбы с герпетическими инфекциями.
N.V. Kolesnikova, T.M. Andronova
Kuban State Medical Academy
CJSC Peptek, M.M. Shemyakin – Yu.A. Ovchinnikov Institute of Bioorganic Chemistry
Contact person: Natalya Vladislavovna Kolesnikova, troickaya@rambler.ru
Preventive and therapeutic strategies of fight against herpesvirus infection are based on improving local innate and adaptive immunity in mucosae. Due to this, targeted immunomodulators facilitating enhanced functional activity of phagocytes as the main innate cell type is considered as an important approach for optimizing basal therapy. In connection with this, it is promising to use receptor agonists such as synthetic and natural minimum biologically active fragments (MBAF) from pathogen-associated molecular patterns, particularly MBAF glucosaminylmuramyl dipeptide-containing Licopid, a standalone domestic immunomodulator registered in Russia. Here we review results of clinical and laboratory observations aimed at using Licopid in therapy of herpesvirus infection in children (respiratory herpes infection, complicated acute respiratory viral infections, perinatal herpesvirus infection, persistent-recurrent orofacial herpes, Epstein – Barr virus, congenital cytomegalovirus infection). The data obtained evidence about high clinical and immunological efficacy of the drug and rationale for its use to potentiate body defense system as immunotropic strategy of fight against herpesvirus infection in children.
