Консервативные тенденции в стратегии преодоления бесплодия у пациенток с генитальным эндометриозом
- Аннотация
- Статья
- Ссылки
- English


Введение
Бесплодие – одно из основных, а часто единственное клиническое проявление наружного генитального эндометриоза. Достижение беременности при данной патологии представляет собой одну из наиболее трудных задач в гинекологической практике. Это связано с высокой распространенностью наружного генитального эндометриоза, его хроническим течением, многофакторностью нарушений репродуктивной функции [1].
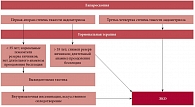
Специалистам хорошо известна основная парадигма лечения наружного генитального эндометриоза – комбинированный подход, включающий в себя хирургическое вмешательство и гормональную терапию (рисунок). В течение последних лет на основании ряда клинических и экспериментальных исследований было сформулировано несколько важных с практической точки зрения позиций, связанных с преодолением бесплодия:
- функциональный подход на этапе первого хирургического вмешательства, заключающийся в максимально бережном отношении к овариальному резерву;
- нецелесообразность повторных операций;
- своевременное применение вспомогательных репродуктивных технологий, в том числе экстракорпорального оплодотворения (ЭКО);
- назначение гормональной терапии адъювантного (перед ЭКО) и противорецидивного характера.
Эндоскопический этап до настоящего времени остается золотым стандартом диагностики большинства форм заболевания.
Хирургические методы лечения эндометриоза
Каковы основные задачи хирургического вмешательства при эндометриозе? Целесообразно выделить диагностическую и лечебную составляющие операции. Во время диагностического этапа оценивается степень тяжести наружного генитального эндометриоза и проходимость маточных труб. Степень тяжести заболевания в настоящее время, как правило, определяется по классификации Американского общества репродуктивной медицины (American Society for Reproductive Medicine, 1997), основанной на оценке распространенности гетеротопических очагов на брюшине малого таза и степени их инвазии в подлежащие ткани [2]. Именно от степени тяжести наружного генитального эндометриоза зависят прогноз наступления беременности и дальнейшая тактика преодоления бесплодия [3].
В большинстве случаев во время лапароскопии проводятся манипуляции, связанные с иссечением или коагуляцией очагов эндометриоза, удалением эндометриом, что позволяет частично восстановить анатомию органов малого таза. Основанием для выполнения операционной (а не только диагностической) лапароскопии являются результаты немногочисленных исследований. Так, согласно данным метаанализа, проведенного в 2010 г. (основан на результатах двух рандомизированных контролируемых исследований), коагуляция очагов наружного генитального эндометриоза первой-второй степени тяжести может увеличить шансы самостоятельного зачатия и родов [4, 5]. Рандомизированные контролируемые исследования, подтверждающие эффективность хирургического лечения наружного генитального эндометриоза третьей-четвертой степени тяжести в отношении наступления спонтанной беременности, отсутствуют. Имеется несколько проспективных когортных исследований, в которых показана эффективность операционной лапароскопии по сравнению с диагностической в преодолении бесплодия [6, 7]. В связи с этими обстоятельствами в национальных и европейских рекомендациях отмечена целесообразность выполнения операционной лапароскопии с целью преодоления бесплодия при наружном генитальном эндометриозе первой-второй степени тяжести. При тяжелых формах заболевания данная рекомендация не столь определенна (табл. 1).
Почему так осторожно относятся к выполнению оперативного вмешательства при наружном генитальном эндометриозе? Безусловно, важнейшая задача при хирургическом лечении эндометриоза – сохранить овариальный резерв. Это особенно актуально при билатеральном поражении яичников [8]. Функциональный подход, бережное отношение к ткани яичника считаются основными принципами эндоскопии при наружном генитальном эндометриозе, поскольку могут снизить репродуктивные риски оперативного вмешательства [9, 10]. Это касается, например, способа или метода хирургического воздействия. Так, в некоторых исследованиях показано, что эксцизия капсулы эндометриомы менее травматична по сравнению с диатермоаблацией и не только увеличивает в последующем частоту наступления беременности, но и снижает частоту рецидива эндометриомы [11].
В отношении оценки овариального резерва наиболее информативными считаются два показателя:
- число антральных фолликулов в обоих яичниках при ультразвуковом исследовании (проводится на второй-третий день менструального цикла);
- содержание антимюллерова гормона в сыворотке крови (исследование может выполняться в любой день цикла, поскольку уровень антимюллерова гормона меняется в течение менструального цикла незначительно).
Что касается такого показателя овариального резерва, как базальный уровень фолликулостимулирующего гормона в сыворотке крови (второй-третий день цикла), то его повышение (более 12 мМЕ/л), сначала периодическое, затем стойкое, свидетельствует о значительном снижении овариального резерва, развитии гипергонадотропной недостаточности яичников. У таких пациенток отмечается также укорочение менструального цикла. В этом случае большей эффективностью будут обладать протоколы с использованием донорских ооцитов, поскольку если при стимуляции собственных яичников и будут получены ооциты, а затем эмбрионы, их «качество» будет крайне низким, а результативность протокола будет стремиться к нулю.
Известно, что в физиологических условиях овариальный резерв снижается с возрастом (наиболее интенсивно после 37 лет). Часто преждевременное, значительное («драматическое») уменьшение резерва вызвано оперативными вмешательствами, в том числе по поводу эндометриоза. Именно поэтому чрезвычайно важно знать уровень антимюллерова гормона до операции. При уровне антимюллерова гормона, свидетельствующем о снижении овариального резерва, – менее 1,0 нг/мл – нужно оценить риски предстоящей операции. Более того, целесообразно поставить вопрос о необходимости и эффективности самой операции в плане преодоления бесплодия, возможности перехода на методы вспомогательной репродукции (попытка ЭКО, криоконсервация ооцитов с целью их использования в будущем). Эффективность протоколов ЭКО при уровне антимюллерова гормона менее 0,5 нг/мл низкая (частота беременности на цикл составляет менее 10%), и в этом случае женщины должны быть информированы о перспективах программы с использованием ооцитов донора.
После операции также важно оценить состояние овариального резерва. Согласно данным H.J. Chang и соавт. (2010), определять уровень антимюллерова гормона целесообразно через несколько месяцев, поскольку в течение первых недель после операции возможно «ложное» снижение уровня антимюллерова гормона, обусловленное временным нарушением фолликулогенеза и снижением количества преантральных и малых антральных фолликулов в связи с операционной травмой, воспалением, формированием гематомы, нарушением кровообращения [12]. У оперированных больных определение числа антральных фолликулов имеет меньшую диагностическую ценность в плане оценки овариального резерва [13].
С позиций риска снижения овариального резерва остается спорной необходимость повторных операций, в том числе перед протоколом ЭКО. Более того, как правило, они сложнее в техническом плане и имеют большую частоту осложнений. Исследования по оценке эффективности повторного хирургического вмешательства единичны и проведены на небольших выборках больных [5].
Наиболее остро вопрос о повторной операции стоит при рецидиве эндометриомы. Исследований, посвященных данному вопросу, мало, и результаты их достаточно противоречивы [14–17]. Хирургическое вмешательство в этом случае может быть выполнено с целью улучшения доступа к фолликулам при трансвагинальной пункции в последующем протоколе ЭКО. Кроме того, показаниями для оперативного лечения больных с эндометриомами (при наличии уже установленного ранее диагноза наружного генитального эндометриоза) могут стать болевой синдром, быстрое увеличение размеров образования, ультразвуковые признаки малигнизации опухоли, а также риск больших размеров образования [18]. В случае уже ранее установленного с помощью лапароскопии диагноза эндометриоза, при небольшом диаметре эндометриомы (≤ 3–4 см), отсутствии быстрого роста, хорошей визуализации интактных зон яичника оперативное вмешательство нецелесообразно. Согласно рекомендациям Американского общества репродуктивной медицины (2006), при наружном генитальном эндометриозе третьей-четвертой степени тяжести использование вспомогательных репродуктивных технологий представляется более эффективным в сравнении с повторной операцией [19].
Гормональная терапия эндометриоза
Согласно современным представлениям обсуждаются несколько вариантов гормональной терапии наружного генитального эндометриоза у больных с бесплодием:
- эмпирическая (у больных с подозрением на наружный генитальный эндометриоз, перед выполнением первого оперативного вмешательства);
- адъювантная после операции;
- адъювантная перед протоколом ЭКО;
- противорецидивная (для профилактики рецидива) – при изменении репродуктивных планов, «откладывании» планирования беременности по тем или иным причинам.
Эмпирическая гормональная терапия
Назначение медикаментозного лечения до операции у больных с бесплодием не рекомендовано, так как нет убедительных данных, подтверждающих ее эффективность. Эмпирическая гормональная терапия показана прежде всего женщинам с дисменореей и болевым синдромом. Однако некоторые авторы считают, что назначение гормональных средств целесообразно в период ожидания оперативного лечения при наличии болевого синдрома и бесплодия, возможно обусловленных эндометриозом [20].
В качестве средств первой линии эмпирического гормонального лечения болевого синдрома сейчас рекомендуются комбинированные оральные контрацептивы и прогестины [20, 21]. Комбинированные оральные контрацептивы назначают подросткам, а также молодым пациенткам, не планирующим беременность и нуждающимся в надежной контрацепции. При планировании беременности, а также в случае установленного диагноза бесплодия, вероятно, лучше использовать более эффективные средства (прогестины, агонисты гонадотропин-рилизинг-гормона).
Адъювантная (послеоперационная) гормональная терапия
Принципы послеоперационного ведения больных с наружным генитальным эндометриозом, бесплодием и возможностью планирования естественного зачатия в разных странах выработаны с учетом результатов национальных исследований в этой области. Отечественные позиции отражены в клинических рекомендациях, изданных в 2013 г. Российским обществом акушеров-гинекологов [22]. Необходимость гормональной терапии эндометриоза после операции объясняется тем, что невозможно полностью хирургически удалить гетеротопии (невизуализируемые, труднодоступные очаги). Кроме того, выполнение оперативного вмешательства не обеспечивает блокирование множества механизмов развития бесплодия при эндометриозе (нарушение функции яичников, рецептивности эндометрия, состава перитонеальной жидкости и влияние ее на гаметы и эмбрион и др.). Иными словами, комбинированный подход – это лечение болезни, а не лечение отдельного ее симптома. Назначение супрессивной терапии, в частности агонистов гонадотропин-рилизинг-гормона, позволяет достичь оптимальной для лечения эндометриоза концентрации эстрадиола в крови больных – 20–40 пг/мл (так называемое терапевтическое окно) [23]. Еще одним веским аргументом в пользу комбинированного подхода можно считать тот факт, что наружный генитальный эндометриоз является фактором риска акушерских осложнений [20]. Тем не менее согласно рекомендациям некоторых национальных и европейских профессиональных сообществ по преодолению бесплодия при эндометриозе, базирующимся на результатах нескольких рандомизированных контролируемых исследований и систематического обзора [24], послеоперационная гормональная терапия с целью лечения бесплодия не увеличивает шансы наступления беременности, может стать причиной «отсрочки» оптимального времени планирования беременности (табл. 2).
В последние годы появляется все больше научно-практических фактов, подтверждающих целесообразность комбинированного подхода. Так, данные российского клинического исследования показали, что применение трипторелина 3,75 мг один раз в 28 дней внутримышечно (агонист гонадотропин-рилизинг-гормона, торговое название Диферелин®) в течение шести месяцев после лапароскопии привело к наступлению беременности у 52,1% женщин с первой-второй степенью тяжести наружного генитального эндометриоза и у 39,8% женщин с эндометриозом третьей-четвертой степени тяжести. При этом у пациенток без медикаментозного лечения в результате выжидательной тактики удалось восстановить репродуктивную функцию только в 29,3% случаев. В большинстве случаев беременность наступила в первые шесть – восемь месяцев после проведенного лечения [25]. Согласно результатам российского открытого многоцентрового исследования, агонист гонадотропин-рилизинг-гормона (Диферелин®) подтвердил свою эффективность в отношении уменьшения размеров эндометриоидных очагов, устранении основных симптомов заболевания. При этом не было ни одного случая необходимости назначения add-back терапии. Нежелательные явления в виде приливов отметили только 11,3% пациенток [26].
Согласно данным X.H. Yang и соавт. (2014), частота наступления беременности у больных после двусторонней лапароскопической цистэктомии и последующего назначения в течение трех месяцев агониста гонадотропин-рилизинг-гормона в полтора раза превышала таковую у больных без гормонального лечения (57,1 и 36,8% соответственно) [27].
Некоторые специалисты заблуждаются, считая, что агонисты гонадотропин-рилизинг-гормона негативно влияют на овариальный резерв. Согласно результатам ряда исследований, агонисты гонадотропин-рилизинг-гормона не только не снижают функциональные возможности яичников, но и являются фармакологическим средством защиты овариального резерва. Так, проведение химиотерапии на фоне симультанного использования агониста гонадотропин-рилизинг-гормона у больных со злокачественными опухолями снижало частоту развития синдрома преждевременного истощения яичников [28, 29]. Это обусловлено ослаблением кровоснабжения яичников, уменьшением пула растущих фолликулов, наиболее чувствительных к действию химиотерапевтических препаратов, ингибированием апоптоза клеток, увеличением содержания в яичниках сфингозин-1-фосфата, влияющего на процессы пролиферации и ангиогенеза.
Гормональная терапия перед протоколом ЭКО
Своевременность использования методов вспомогательных репродуктивных технологий, в том числе ЭКО, является важным постулатом стратегии преодоления бесплодия у больных с наружным генитальным эндометриозом. ЭКО показано пациенткам в следующих случаях:
- наружный генитальный эндометриоз третьей-четвертой степени тяжести;
- старший репродуктивный возраст;
- сниженный овариальный резерв;
- длительный анамнез преодоления бесплодия;
- нарушение проходимости маточных труб;
- наличие мужского фактора бесплодия (значительные отклонения в параметрах спермограммы).
Известно, что ЭКО позволяет преодолеть такие причины бесплодия, как нарушения анатомии органов малого таза и функции яичников, негативное воздействие перитонеальной жидкости у больных с наружным генитальным эндометриозом (увеличение количества макрофагов, Т-лимфоцитов, интерлейкина 1) на гаметы, процесс оплодотворения и ранние этапы развития эмбриона [30]. Однако слабым звеном здесь по-прежнему остается нарушение рецептивности эндометрия. Известно, что при наружном генитальном эндометриозе в эутопическом эндометрии наблюдается сложное сочетание патологических ассоциаций как на микроскопическом (снижение развития пиноподий), так и на молекулярном уровне (снижение экспрессии НОХА-10, интегрина альфа-v-бета-3, L-cелектина, муцина MUC 1, лейкемия ингибирующего фактора, экспрессии ароматазы цитохрома Р450, а также нарушение соотношения изоформ прогестероновых и эстрогеновых рецепторов) [30]. В частности уменьшается соотношение прогестероновых рецепторов типа B/A и увеличивается соотношение эстрогеновых рецепторов бета/альфа, что обеспечивает так называемую прогестероновую резистентность эндометрия [18].
Какие в настоящее время существуют реальные практические пути оптимизации рецептивных свойств эндометрия у больных с наружным генитальным эндометриозом? В некоторых исследованиях показано, что гормональная терапия в течение трех – шести месяцев до протокола ЭКО может приводить к повышению его эффективности [31]. Доказана эффективность использования с этой целью агонистов гонадотропин-рилизинг-гормона. Хорошо известно, что агонисты гонадотропин-рилизинг-гормона вызывают десенситизацию гипофиза и подавляют продукцию гипофизарных гонадотропинов, что в свою очередь ведет к прекращению селекции и роста доминантного фолликула и созданию в организме женщины состояния выраженной гипоэстрогенемии. Это является одним из факторов, способствующих подавлению роста гетеротопических очагов. Однако положительные эффекты агонистов гонадотропин-рилизинг-гормона связаны не только с его центральным действием. Препараты данной группы снижают также концентрацию тканевых ингибиторов металлопротеиназы 1, выработку медиаторов воспаления (интерлейкина 1-бета, сосудистого эндотелиального фактора роста), которые играют важную роль в способности к инвазии эндометриоидных гетеротопий, их пролиферативной активности, усиливают апоптоз (увеличивают экспрессию проапоптотических протеинов Bax and FasL и снижают экспрессию антиапоптотического протеина Bcl-2) [32]. Значительный интерес представляют работы, показывающие увеличение экспрессии интегрина альфа-v-бета-3 в эутопическом эндометрии после применения препаратов агониста гонадотропин-рилизинг-гормона у больных с наружным генитальным эндометриозом в течение трех месяцев. Известно, что интегрин альфа-v-бета-3 экспрессируется на поверхности эпителиальных клеток эндометрия и трофобласте [33]. Частота родов после ЭКО значительно выше у пациентов с положительной экспрессией интегрина альфа-v-бета-3 в эндометрии (38 против 7%, p < 0,05).
Полученные к настоящему времени сведения послужили основанием для включения в национальные профессиональные рекомендации по лечению эндометриоза агонистов гонадотропин-рилизинг-гормона в качестве средств гормональной подготовки больных к протоколу ЭКО (в течение трех – шести месяцев до вступления в протокол) (табл. 2).
Противорецидивная гормональная терапия
Эндометриоз – это хроническое и рецидивирующее заболевание. По разным оценкам, после хирургического лечения частота рецидивов эндометриоза в течение пяти лет составляет от 11 до 32% [34]. Именно поэтому необходимо предусмотреть возможность долговременного лечения с целью предупреждения рецидива заболевания. При этом следует учитывать длительный характер терапии, удобство режима приема препаратов и их стоимость, быстрое восстановление фертильности после прекращения лечения [34]. К настоящему времени получены данные об эффективности применения в этом качестве комбинированных оральных контрацептивов (в непрерывном режиме), агонистов гонадотропин-рилизинг-гормона, прогестинов [35].
Заключение
Таким образом, преодоление бесплодия у больных с эндометриозом представляет собой комплексную проблему, успех решения которой определяется эффективным взаимодействием гинекологов общей практики, отделений оперативной гинекологии и репродуктологов, конструктивным информированным диалогом с супружеской парой. Рассматривая эндометриоз как заболевание, угрожающее реализации репродуктивных планов женщины, следует минимизировать риски на каждом из этапов лечения. Одной из основных задач является ранняя диагностика, основанная на тщательном сборе анамнеза, использовании дополнительных неинвазивных методов исследования. При хирургическом лечении функциональный подход и бережное отношение к ткани яичника может снизить репродуктивные риски оперативного вмешательства. Гормональная терапия должна проводиться по показаниям в зависимости от симптомов, возраста, овариального резерва и репродуктивных планов пациентки. Важно оценивать шансы наступления беременности и своевременно обращаться к вспомогательным репродуктивным технологиям.
Conservative Tendencies in Strategy for Overcoming Infertility in Patients with Genital Endometriosis
I.Yu. Kogan, D.A. Gerkulov, A.M. Gzgzyan
D.O. Ott Research Institute of Obstetrics, Gynecology and Reproductology
Contact person: Igor Yuryevich Kogan, ikogan@mail.ru
Here we discuss medicated and surgical methods used to treat infertility caused by genital endometriosis. It is emphasized that during surgical treatment a functional approach and careful attitude to ovarian tissues allowing to lower reproductive risks of surgical intervention are required. Hormone therapy must be applied according to indications depending on symptoms, age, ovarian reserve and reproductive life plans of a patient. Importantly, changes of pregnancy must be estimated, and assisted reproductive technologies to be used in due time.
