Коррекция дислипидемии у пациентов с сахарным диабетом 2 типа после перенесенного острого коронарного синдрома как ключевой фактор улучшения прогноза. Роль ингибиторов PCSK9
- Аннотация
- Статья
- Ссылки
- English
Анализ результатов исследования ODYSSEY OUTCOMES показал, что терапия ингибитором PCSK9 алирокумабом у пациентов с сахарным диабетом, перенесших острый коронарный синдром, ассоциировалась со снижением относительного и абсолютного рисков развития больших сердечно-сосудистых событий, таких как инфаркт миокарда, ишемический инсульт, смерть от ишемической болезни сердца или нестабильная стенокардия, потребовавшая госпитализации (ОР 0,84, 95% ДИ 0,74–0,97, абсолютное снижение риска – 2,3). Длительная терапия алирокумабом (медиана – 2,8 года) не влияла негативно на гликемический профиль как у пациентов с сахарным диабетом, так и у пациентов без диабета и не приводила к увеличению частоты впервые выявленного диабета.
Анализ результатов исследования ODYSSEY OUTCOMES показал, что терапия ингибитором PCSK9 алирокумабом у пациентов с сахарным диабетом, перенесших острый коронарный синдром, ассоциировалась со снижением относительного и абсолютного рисков развития больших сердечно-сосудистых событий, таких как инфаркт миокарда, ишемический инсульт, смерть от ишемической болезни сердца или нестабильная стенокардия, потребовавшая госпитализации (ОР 0,84, 95% ДИ 0,74–0,97, абсолютное снижение риска – 2,3). Длительная терапия алирокумабом (медиана – 2,8 года) не влияла негативно на гликемический профиль как у пациентов с сахарным диабетом, так и у пациентов без диабета и не приводила к увеличению частоты впервые выявленного диабета.


Введение
Взаимосвязь между сахарным диабетом (СД) и сердечно-сосудистыми заболеваниями (ССЗ) была продемонстрирована уже в Фрамингемском исследовании – по данным 20-летнего наблюдения, риск последних у пациентов с СД был в два-три раза выше, чем у пациентов без диабета [1]. K. Gu и соавт. (1998) установили, что медиана продолжительности жизни у пациентов с диабетом в возрасте от 55 до 64 лет, а также у пациентов в возрасте от 65 до 74 лет на восемь и четыре года (соответственно) меньше, чем у пациентов без диабета [2]. Анализ причин смерти 1099 пациентов с СД, участвовавших в международном исследовании сосудистых заболеваний при диабете Всемирной организации здравоохранения (ВОЗ), показал, что ССЗ – наиболее распространенная причина смерти больных СД. При СД 1 типа на их долю в структуре смертности приходится 44%, при СД 2 типа – 52% [3]. Эти данные были неоднократно подтверждены результатами других исследований. Метаанализ результатов 102 проспективных исследований, включавших 698 782 пациентов, у которых регистрировали сердечно-сосудистые события, продемонстрировал, что у пациентов с СД 2 типа в два-четыре раза повышен риск ишемической болезни сердца (ИБС), ишемического инсульта и в 1,5–3,6 раза – сердечно-сосудистой смерти [4]. Поэтому длительное время СД рассматривали как эквивалент ССЗ в отношении риска сердечно-сосудистых событий [5]. Так, согласно результатам финского семилетнего популяционного исследования, частота инфаркта миокарда (ИМ) у пациентов с СД 2 типа статистически значимо не отличалась от таковой у пациентов без диабета, но с ИМ в анамнезе – 20,2 против 18,8%. При этом частота ИМ у пациентов с СД 2 типа и ранее перенесенным ИМ за семь лет наблюдения достигла 45,0% [6].
В настоящее время считается, что при оценке риска развития ССЗ у пациентов с диабетом необходимо учитывать значительную гетерогенность этой группы больных и наличие других неблагоприятных факторов [7, 8]. Наличие последних существенно увеличивает сердечно-сосудистый риск у пациентов с СД по сравнению с пациентами без диабета [7]. Основные факторы сердечно-сосудистого риска у пациентов с СД 2 типа (n = 3055) изучали в исследовании UKPDS. Длительное наблюдение (медиана – 7,9 года) показало, что наибольшее влияние на развитие ИБС оказывало повышение уровня холестерина липопротеинов низкой плотности (ХС ЛПНП), снижение уровня холестерина липопротеинов высокой плотности (ХС ЛПВП), повышение систолического артериального давления, гипергликемия и курение [9].
Согласно российским и европейским рекомендациям по коррекции дислипидемии, большинство пациентов с СД без дополнительных неблагоприятных факторов относятся к группе высокого риска развития ССЗ, а при наличии признаков поражения органов-мишеней, например почек (протеинурия), или как минимум одного из факторов риска, например курения, артериальной гипертензии или дислипидемии, – к группе очень высокого риска [10, 11]. В случае верифицированного ССЗ – в анамнезе ИБС, ИМ, острый коронарный синдром (ОКС), ишемический инсульт или атеросклеротическое поражение периферических артерий – пациенты также подпадают под категорию очень высокого риска [10, 11]. В то же время, согласно американским рекомендациям по коррекции дислипидемии, пациентов с СД и ССЗ следует относить к группе экстремально высокого риска [12].
У пациентов, перенесших ОКС и имеющих СД, более высокий риск повторных сердечно-сосудистых событий по сравнению с пациентами без СД. По данным шведского национального регистра, у 97 254 пациентов, госпитализированных с ИМ с июля 2006 г. по июнь 2011 г. и выписанных из клиники, частота встречаемости СД составила 23,2%. При этом СД ассоциировался с увеличением кумулятивного риска повторного ИМ, инсульта или сердечно-сосудистой смерти в течение года (отношение рисков (ОР) 1,37 при 95%-ном доверительном интервале (ДИ) 1,34–1,40, p < 0,001) [13].
Ключевым фактором снижения сердечно-сосудистого риска у таких пациентов является липидоснижающая терапия. Так, всем пациентам с СД и ССЗ помимо изменения образа жизни рекомендована высокоинтенсивная терапия статинами, а при недостижении целевого уровня ХС ЛПНП (1,8 ммоль/л и ниже) – дополнительная липидоснижающая терапия, включащая эзетимиб или ингибиторы пропротеиновой конвертазы субтилизин/кексин 9 типа (PCSK9) [14].
Согласно российским рекомендациям по диагностике и коррекции нарушений липидного обмена VI пересмотра, у пациентов, относящихся к группе очень высокого риска развития ССЗ, включая пациентов с СД 2 типа и ССЗ, а также пациентов с СД 2 типа старше 40 лет без ССЗ, но при наличии других неблагоприятных факторов риска или признаков поражения органов-мишеней, целевой уровень ХС ЛПНП должен составлять менее 1,5 ммоль/л [11]. В рекомендациях, разработанных экспертами Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологов, для пациентов с СД и ССЗ (группа экстремально высокого риска) установлены еще более низкие целевые значения ХС ЛПНП – менее 55 мг/дл (примерно 1,4 ммоль/л) [12]. Результаты последних исследований свидетельствуют, что у пациентов с СД, перенесших ОКС, более интенсивная липидоснижающая терапия (применение высоких доз статинов в комбинации с эзетимибом) ассоциировалась с большим снижением риска повторных сердечно-сосудистых событий, чем у пациентов без СД. В исследовании IMPROVE-IT из 18 144 пациентов с ОКС 27% был поставлен диагноз СД. За семь лет наблюдения вероятность достижения событий комбинированной первичной конечной точки: сердечно-сосудистая смерть, нефатальный ИМ или инсульт, нестабильная стенокардия (НС), потребовавшая госпитализации или коронарной реваскуляризации, у пациентов с СД составила 45,51% на фоне терапии симвастатином в дозе 40 мг/сут, в то время как у пациентов без диабета – 30,84%. Назначение более интенсивной липидоснижающей терапии (симвастатин 40 мг/сут в комбинации с эзетимибом 10 мг/сут) привело к снижению кумулятивной частоты событий у пациентов с СД до 40,04% (ОР 0,86 (95% ДИ 0,78–0,94), p = 0,02), у пациентов без СД – до 30,16% [15].
В реальной клинической практике очень мало пациентов достигают целевых значений липидов. По данным наблюдательного исследования EUROASPIRE, только у 37% пациентов с СД, перенесших ОКС, ХС ЛПНП достигал целевых значений – менее 1,8 ммоль/л [16]. Поэтому у пациентов, не достигающих целевого уровня ХС ЛПНП на фоне высокоинтенсивной терапии статинами, должна быть рассмотрена возможность назначения дополнительной липидоснижающей терапии [14].
В настоящее время доступно несколько групп препаратов, которые могут применяться в комбинации со статинами для усиления гиполипидемического эффекта при недостижении целевых значений ХС ЛПНП, а также в случае непереносимости статинов. К таковым следует отнести ингибиторы абсорбции холестерина (эзетимиб), секвестранты желчных кислот, никотиновую кислоту (ниацин), фибраты, а также моноклональные антитела к PCSK9 [17]. Необходимо отметить, что доказательства улучшения прогноза у пациентов с СД и ССЗ до недавнего времени были доступны только для эзетимиба [15]. Результаты клинических исследований ниацина и фенофибрата не подтвердили значимого снижения частоты сердечно-сосудистых событий у пациентов с СД, хотя и позволили выдвинуть предположение о некотором положительном влиянии фенофибрата у пациентов с очень высоким уровнем триглицеридов (ТГ) [18–21]. В то же время недавно опубликованные результаты исследования ODYSSEY OUTCOMES продемонстрировали уменьшение сердечно-сосудистого риска на фоне терапии одним из ингибиторов PCSK9 алирокумабом в сочетании со статинами у пациентов, перенесших ОКС за 1–12 месяцев до рандомизации [22].
Механизм действия и эффекты
Влияние PCSK9 на концентрацию ХС ЛПНП обусловлено его способностью связываться с рецепторами ЛПНП и вызывать их деградацию.
Рецепторы ЛПНП выводят из системного кровотока циркулирующие ЛПНП. На поверхности гепатоцитов ЛПНП связываются со своими рецепторами и образуют комплекс, который поглощается клеткой. После этого рецептор ЛПНП возвращается на поверхность клетки. Данный процесс может повторяться до 150 раз [23]. Уменьшение количества рецепторов ЛПНП вследствие их связывания с PCSK9 приводит к повышению концентрации ХС ЛПНП в крови [24].
Открытие данного механизма определило разработку новой группы лекарственных средств – ингибиторов PCSK9.
В Российской Федерации доступно два лекарственных препарата ингибиторов PCSK9 – алирокумаб и эволокумаб.
Алирокумаб был зарегистрирован в 2017 г. под торговым наименованием Пралуэнт. Препарат выпускается в виде раствора для подкожного введения в дозах 75 и 150 мг/мл.
Алирокумаб представляет собой полностью человеческое моноклональное антитело (IgGl), мишенью которого является PCSK9. Алирокумаб ингибирует связывание циркулирующей в крови PCSK9 с рецепторами ЛПНП, что приводит к увеличению количества этих рецепторов и активному выведению циркулирующих ЛПНП из системного кровотока [25].
При проведении генетических исследований M. Abifadel и соавт. (2003) обнаружили мутации в гене PCSK9, приводящие к повышению функции фермента и развитию гиперхолестеринемии, наследуемой по аутосомно-доминантному типу [26]. Указанные мутации ассоциировались с высоким уровнем ХС ЛПНП и повышенным риском развития ССЗ [27, 28]. Позже были выявлены другие мутации этого гена, которые обусловливали снижение функциональной активности PCSK9, низкий уровень ХС ЛПНП и риск развития ССЗ [29–31]. Выраженное снижение активности PCSK9 у здоровых субъектов с такими мутациями сопровождалось снижением концентрации ХС ЛПНП до 14 мг/дл (0,36 ммоль/л) без каких-либо видимых негативных последствий для здоровья [30, 32].
Рецепторы ЛПНП также связывают богатые ТГ ремнантные липопротеины очень низкой плотности (ЛПОНП) и липопротеины промежуточной плотности (ЛППП). Поэтому при терапии ингибиторами PCSK9 наблюдается также снижение концентрации этих ремнантных липопротеинов. Доказательством служит уменьшение аполипопротеина В, холестерина липопротеинов, не являющихся липопротеинами высокой плотности (ХС ЛПнеВП) и ТГ [33]. Кроме того, отмечается снижение уровня липопротеина (а), несмотря на то что рецепторы ЛПНП обладают низким сродством к нему. Точный механизм данного эффекта пока не установлен [25].
Рассмотренные выше эффекты представляются очень важными для пациентов с СД 2 типа, пациентов с СД 1 типа и недостаточным контролем гликемии, у которых развивается дислипидемия, характеризующаяся снижением печеночного клиренса богатых ТГ липопротеинов, увеличением синтеза ЛПОНП в печени и образованием хиломикронов в кишечнике [34]. При этом типе дислипидемии, так называемой диабетической или смешанной дислипидемии, увеличивается концентрация ХС ЛПнеВП, ТГ и мелких плотных частиц ХС ЛПНП [34, 35].
Эффективность алирокумаба изучали в серии плацебоконтролируемых и эзетимибконтролируемых исследований как в виде монотерапии, так и в составе комбинированной липидоснижающей терапии. Их участниками были пациенты с дислипидемией, включая семейную гиперхолестеринемию, пациенты с умеренным, высоким и очень высоким сердечно-сосудистым риском, а также пациенты с непереносимостью статинов [36–47]. Выраженный гиполипидемический эффект развивался в течение 15 дней после первого введения алирокумаба, достигая максимума к четвертой неделе. При этом он сохранялся на протяжении всего периода лечения. Совокупный анализ результатов десяти рандомизированных клинических исследований фазы III ODYSSEY свидетельствует, что через 24 недели после начала терапии у пациентов с дислипидемией, получавших алирокумаб в дополнение к высокоинтенсивной терапии статинами или в виде монотерапии, уровень ХС ЛПНП и аполипопротеина В был ниже, чем в группах, получавших эзетимиб или плацебо в дополнение к высокоинтенсивной терапии статинами или в виде монотерапии (p < 0,0001) [45]. При этом достигнутый эффект сохранялся в течение всего периода лечения (до 78 недель по результатам исследования ODYSSEY LONG TERM) [47]. Через 24 недели терапии алирокумабом более 70% пациентов достигли целевых значений ХС ЛПНП и аполипопротеина В (p ≤ 0,0001 по сравнению с контрольной группой) [45].
Субанализ подгрупп пациентов, принимавших участие в клинических исследованиях фазы III, показал, что эффекты алирокумаба в отношении снижения ХС ЛПНП у пациентов с СД и без такового практически не различались [48–50]. Аналогичные результаты получены и в отношении пациентов с предиабетом [51].
Согласно результатам недавно опубликованного совокупного анализа по подгруппам пациентов с СД и ССЗ, принимавших участие в девяти клинических исследованиях алирокумаба, через 24 недели терапии алирокумабом и статинами уровень ХС ЛПНП снизился на 61,5% (алирокумаб 150 мг) и 48,7% (алирокумаб 75 мг с возможностью повышения до 150 мг) соответственно. При этом прием эзетимиба и статинов приводил к снижению ХС ЛПНП только на 20,6%. На фоне терапии алирокумабом у пациентов с СД и ССЗ также наблюдалось статистически значимое снижение ХС ЛПнеВП, аполипопротеина В и липопротеина (а) [49].
Два исследования алирокумаба – ODYSSEY DM-INSULIN и DM-DYSLIPIDEMIA проводили с участием пациентов с СД. Основной целью исследования ODYSSEY DM-INSULIN была оценка эффективности и безопасности одновременной терапии двумя биологическими препаратами у пациентов с СД 1 и 2 типов, гиперхолестеринемией и высоким сердечно-сосудистым риском. В частности, в него были включены 76 пациентов с СД 1 типа и 441 пациент с СД 2 типа. Все они получали инсулин и, несмотря на стабильную терапию максимально переносимыми дозами статинов, имели уровень ХС ЛПНП при включении в исследование ≥ 70 мг/дл (1,8 ммоль/л). Кроме того, у пациентов отмечался как минимум один дополнительный фактор сердечно-сосудистого риска или ССЗ. Пациенты были рандомизированы на две группы терапии: алирокумабом в дозе 75 мг один раз в две недели с возможностью увеличения дозы до 150 мг или плацебо. Длительность терапии составляла 24 недели. На фоне лечения алирокумабом концентрация ХС ЛПНП у пациентов с СД 2 типа снизилась на 49,0 ± 2,7%, у пациентов с СД 1 типа – на 47,8 ± 6,5% по сравнению с получавшими плацебо (p < 0,0001 для обеих групп). Наблюдалось также статистически значимое снижение уровней ХС ЛПнеВП, аполипопротеина В и липопротеина (а). В конце исследования 76,4 и 70,2% пациентов с СД 2 и 1 типов соответственно достигли целевых значений ХС ЛПНП < 70 мг/дл (1,8 ммоль/л). На протяжении всего исследования уровни гликированного гемоглобина (HbA1c) и глюкозы плазмы натощак (ГПН) оставались неизменными. Частота нежелательных реакций была одинаковой у получавших алирокумаб и плацебо [52]. В исследовании ODYSSEY DM-DYSLIPIDEMIA сравнивали эффективность и безопасность алирокумаба и традиционной липидоснижающей терапии (эзетимиба, фенофибрата, омега-3 ненасыщенных жирных кислот, никотиновой кислоты) при их добавлении к статинам в максимально переносимых дозах. В исследовании приняли участие 413 пациентов с СД 2 типа и дислипидемией смешанного типа, имеющих исходные показатели ХС ЛПнеВП ≥ 2,59 ммоль/л и ТГ ≥ 1,70 ммоль/л, но < 5,65 ммоль/л. Первичным параметром оценки стал уровень ХС ЛПнеВП. Через 24 недели терапии у пациентов, получавших алирокумаб, уровень ХС ЛНнеВП был на 32,5% ниже, чем у пациентов, получавших стандартную терапию (p < 0,0001). Дизайн исследования предусматривал повышение дозы алирокумаба с 75 до 150 мг при сохранении уровня ХС ЛПнеВП ≥ 2,59 ммоль/л через восемь недель лечения. Необходимо отметить, что через 24 недели 63,3% пациентов в группе алирокумаба продолжили получать препарат в дозе 75 мг один раз в две недели. В группе алирокумаба по сравнению с получавшими традиционную липидоснижающую терапию также статистически значимо снизились концентрации ХС ЛПНП – на 24,6%, аполипопротеина В – на 32,3%, общего ХС – на 24,6%. Частота нежелательных явлений между группами не различалась. В ходе исследования не было зарегистрировано каких-либо эффектов в отношении уровня HbA1c или изменения гипогликемической терапии [53].
Несмотря на доказательства эффективности алирокумаба при дислипидемии, до настоящего времени было недостаточно данных о его влиянии на долгосрочный прогноз, что особенно важно для пациентов с СД и высоким сердечно-сосудистым риском.
Вторичный анализ результатов исследования ODYSSEY LOGN TERM, в котором принимали участие пациенты с высоким сердечно-сосудистым риском, в том числе 34% пациентов с СД, позволил предположить, что препарат способен улучшать прогноз у данной категории пациентов. Так, в группе алирокумаба кумулятивная частота больших сердечно-сосудистых событий (Major Adverse Cardio-vascular Events – MACE), в частности смерти от ИБС, нефатального ИМ или нефатального ишемического инсульта, НС, потребовавшей госпитализации, была ниже, чем в группе плацебо (ОР 0,52 (95% ДИ 0,31–0,90), p = 0,02) [47].
Обзор исследования ODYSSEY OUTCOMES
Исследование ODYSSEY OUTCOMES проводили с целью изучить влияние длительной терапии алирокумабом на частоту возникновения больших сердечно-сосудистых событий (ИМ, ишемического инсульта, смерти от ИБС, НС, потребовавшей госпитализации) у пациентов после перенесенного ОКС. Вторичными целями исследования стали оценка безопасности и переносимости алирокумаба, его влияния на уровни липидов, выработку антител к алирокумабу.
В исследовании приняли участие 18 924 пациента 40 лет и старше, перенесших ОКС (ИМ с подъемом ST, ИМ без подъема ST или нестабильная стенокардия) в течение последнего года, но не менее одного месяца до рандомизации.
До назначения алирокумаба или плацебо пациенты начинали получать высокоинтенсивную терапию статинами (аторвастатин в дозе 40/80 мг, или розувастатин в дозе 20/40 мг, или один из этих препаратов в максимально переносимой дозе).
Дизайн исследования допускал добавление к терапии нестатиновых липидоснижающих препаратов.
В исследование включали только тех пациентов, у которых, несмотря на интенсивную терапию статинами, уровень липидов превышал целевые значения. Обязательным для включения было соответствие по меньшей мере одному из следующих критериев: ХС ЛПНП ≥ 70 мг/дл (≥ 1,81 ммоль/л), или аполипопротеин B ≥ 80 мг/дл (≥ 0,8 г/л), или ХС ЛПнеВП ≥ 100 мг/дл (≥ 2,59 ммоль/л).
Пациенты в двойном слепом режиме получали алирокумаб или плацебо каждые две недели в дополнение к статинам на протяжении всего периода лечения.
Алирокумаб вводили подкожно, начальная доза составляла 75 мг. В дальнейшем, в зависимости от достижения и поддержания целевого уровня ХС ЛПНП 0,65–1,3 ммоль/л, было предусмотрено заслепленное титрование дозы до 150 мг, а при достижении нижней границы целевых значений – снижение дозы или перевод пациента на плацебо.
Медиана длительности лечения составила 2,8 года. У 44% пациентов терапия алирокумабом продолжалась более трех лет.
Преждевременно лечение прекратили 14,2% пациентов в группе алирокумаба и 15,8% в группе плацебо, 7,7% пациентов были переведены с алирокумаба на плацебо (два последующих значения ХС ЛПНП < 0,39 ммоль/л). На фоне терапии алирокумабом уровень ХС ЛПНП уменьшился на 62,7% через четыре месяца, на 61,0% через 12 месяцев и на 54,7% через 48 месяцев (по сравнению с применением плацебо). Крупные сердечно-сосудистые события были зарегистрированы у 9,5% пациентов в группе алирокумаба и 11,1% пациентов в группе плацебо. За весь период наблюдения снижение относительного риска наступления событий комбинированной первичной конечной точки, рассчитанное на основании кумулятивной частоты, на фоне терапии алирокумабом составило 15% (ОР 0,85 (95% ДИ 0,78–0,93), p < 0,001). Общая смертность была ниже в группе алирокумаба – 3,5 против 4,1% в группе плацебо (ОР 0,85 (95% ДИ 0,73–0,98), р = 0,03) [54]. Преимущество алирокумаба было наиболее выраженным у пациентов с исходным уровнем ХС ЛПНП более 2,6 ммоль/л. В этой группе в отличие от группы плацебо наблюдалось снижение относительного риска больших сердечно-сосудистых событий на 24% (снижение абсолютного риска на 3,4%), а риска смерти от любых причин – на 29% (снижение абсолютного риска на 1,7%). Частота нежелательных реакций была сопоставимой в обеих группах, за исключением реакций в месте инъекции. Последние чаще отмечались при введении алирокумаба – 3,8 против 2,1% [22].
Субанализ данных исследования ODYSSEY OUTCOMES
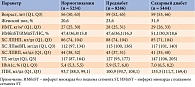
Из 18 924 пациентов, включенных в исследование ODYSSEY OUTCOMES, более чем у 60% наблюдались нарушения углеводного обмена: 5444 (28,8%) пациента с СД и 8246 (43,6%) – с предиабетом (табл.).
Диагноз СД 1 или 2 типа подтверждали на основании данных анамнеза, получения терапии гипогликемическими препаратами и лабораторных параметров (HbA1c ≥ 6,5%, два последовательных значения ГПН ≥ 7,0 ммоль/л). Предиабет устанавливали исходя из значений HbA1c ≥ 5,7 и < 6,5% или двух последовательных значений ГПН > 5,6 ммоль/л, но не более 7,0 ммоль/л. Диагноз «впервые выявленный сахарный диабет» устанавливали на основании одного или более критериев: как минимум два измерения HbA1c ≥ 6,5%, как минимум два измерения ГПН ≥ 7 ммоль/л, зарегистрированные нежелательные явления, указывающие на впервые выявленный СД 1 или 2 типа, начало терапии противодиабетическими препаратами после подтверждения диагноза СД заслепленной панелью экспертов.
При рандомизации группы алирокумаба и плацебо были сбалансированы по характеристикам внутри каждой страты, выделенной в зависимости от гликемического статуса (нормогликемия, предиабет, СД). Медиана HbA1c у пациентов с СД составляла 7,0% (межквартильный размах 6,5–8,2%), с предиабетом – 5,9% (5,7–6,0%) и с нормогликемией – 5,4% (5,3–5,5%).
Пациенты с нарушениями углеводного обмена были более старшего возраста (медиана – 59 лет) по сравнению с лицами с нормогликемией (медиана – 56 лет). Эта группа отличалась большей долей женщин и немного большим индексом массы тела (ИМТ). Исходные значения показателей липидного обмена представлены в таблице.
На фоне терапии алирокумабом динамика показателей липидного профиля у пациентов с СД и предиабетом не отличалась от пациентов с нормогликемией. Через 16 недель от начала лечения у получавших алирокумаб наблюдалось выраженное снижение ХС ЛПНП на 64–65%, уменьшение ХС ЛПнеВП на 54%, ТГ на 14–16% и незначительное повышение ХС ЛПВП на 7–8% (рис. 1).
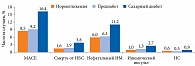
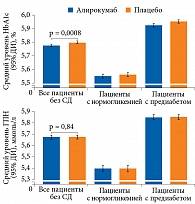
Несмотря на продолжавшуюся высокоинтенсивную терапию статинами и другими препаратами, влияющими на прогноз, больные СД имели более высокий сердечно-сосудистый риск. В группе плацебо кумулятивная частота больших сердечно-сосудистых событий у пациентов с СД достигала 16,4%, в то время как у пациентов с предиабетом и нормогликемией – 9,2 и 8,5% соответственно (p < 0,0001). Частота отдельных компонентов первичной конечной точки – смерти от ИБС, нефатального ИМ и инсульта у пациентов с СД практически в два раза превышала таковую у лиц с нормогликемией или предиабетом (рис. 2). Терапия алирокумабом у пациентов с СД сопровождалась снижением относительного и абсолютного риска достижения комбинированной первичной конечной точки (ОР 0,84 (95% ДИ 0,74–0,97), абсолютное снижение риска на 2,3%). Необходимо подчеркнуть, что сокращение относительного риска в данной группе не отличалось от групп без СД. В то же время в отношении уменьшения абсолютного риска больших сердечно-сосудистых событий группа СД превосходила группу без диабета (рис. 3). Терапия алирокумабом не оказывала значимого влияния на ГПН, однако у пациентов без СД, то есть с нормогликемией или предиабетом, отмечался более низкий средний уровень HbA1c по сравнению с получавшими плацебо (p = 0,0008) (рис. 4). Ухудшение течения СД или развитие его осложнений было зарегистрировано у 18,8% пациентов в группе алирокумаба и 21,2% в группе плацебо. Частота впервые выявленного СД статистически значимо не различалась между группами алирокумаба и плацебо и составила 9,6 и 10,1% соответственно [55].
Данные о безопасности
В исследовании ODYSSEY OUTCOMES пациенты хорошо переносили длительную терапию алирокумабом. В ходе исследования не было выявлено различий по частоте развития нежелательных реакций между группами алирокумаба и плацебо, за исключением реакции в месте введения препарата, которая в большинстве случаев носила легкий характер и разрешалась самостоятельно.
Среди наиболее частых отклонений лабораторных показателей – повышение уровней аланинаминотрансферазы, аспартатаминотрансферазы, креатинфосфокиназы и общего билирубина. Однако эти изменения регистрировали с одинаковой частотой в обеих группах. У 0,7% пациентов в группе алирокумаба и 0,4% пациентов в группе плацебо была выявлена положительная реакция на антитела к алирокумабу, нейтрализующие антитела отмечались у 0,5% и менее 0,1% пациентов соответственно [22].
По данным совокупного анализа безопасности 14 исследований, общая частота нежелательных явлений, серьезных нежелательных явлений, а также преждевременного прекращения лечения вследствие развития нежелательных явлений, связанных с приемом алирокумаба, не отличалась от таковой при использовании плацебо или эзетимиба. Алирокумаб ассоциировался с более высокой частотой развития реакций в месте введения препарата (7,4 по сравнению с 5,3% в группе плацебо и 3,1 по сравнению с 2,3% в группе эзетимиба) и кожного зуда (1,3 по сравнению с 0,4% в группе плацебо и 0,9 по сравнению с 0,5% в группе эзетимиба). Частота побочных эффектов со стороны опорно-двигательного аппарата, нервной системы, офтальмологических, нейрокогнитивных нарушений, изменений со стороны печени или связанных с СД и его осложнениями была одинаковой в группах алирокумаба, эзетимиба и плацебо [56].
Субанализ по подгруппам пациентов с СД, принимавших участие в исследованиях алирокумаба, не выявил значимых различий в профиле безопасности препарата (по сравнению с пациентами без СД) [48, 50, 57]. В исследовании ODYSSEY DM-INSULIN у больных СД 1 и 2 типов с высоким сердечно-сосудистым риском и получавших инсулин, а также в исследовании ODYSSEY DM-DYSLIPIDEMIA у пациентов с СД 2 типа и смешанной дислипидемией алирокумаб не увеличивал общую частоту нежелательных реакций и не оказывал значимого влияния на уровни HbA1c и ГПН [52, 53].
Кроме того, в нескольких субанализах клинических исследований установлено, что частота реакций в месте инъекции после введения алирокумаба у пациентов с СД была ниже, чем у пациентов без СД [48, 50, 57].
Результаты нескольких генетических исследований позволяют предположить, что наличие мутации, ассоциирующейся с уменьшением активности PCSK9 и низкими значениями ХС ЛПНП, как и терапия статинами, может ассоциироваться с небольшим, но статистически значимым повышением риска развития СД [58–60]. Однако доступные на сегодняшний день данные клинических исследований алирокумаба, а также другого ингибитора PCSK9 – эволокумаба не подтверждают этого предположения [61].
H.M. Colhoun и соавт. (2016) провели объединенный анализ данных, полученных в отношении 4974 пациентов, принимавших участие в десяти клинических исследованиях алирокумаба длительностью от 24 до 104 недель. Большинство пациентов во время исследования принимали статины в максимально переносимых дозах. Исходно 30,7% из них страдали СД, 39,6% соответствовали критериям предиабета и 29,7% имели нормогликемию. Авторы исследования проанализировали зарегистрированные на фоне терапии алирокумабом нежелательные реакции, а также динамику HbA1c и ГПН и пришли к выводу, что частота впервые выявленного СД у пациентов, получавших алирокумаб, статистически значимо не отличалась от частоты впервые выявленного СД у получавших плацебо или эзетимиб [62].
В исследовании FOURIER изучали влияние ингибитора PCSK9 эволокумаба на частоту сердечно-сосудистых событий у 27 564 пациентов с ИБС, не достигших целевых значений ХС ЛПНП на терапии статинами. Эффективность эволокумаба не зависела от наличия или отсутствия СД, а частота зарегистрированных случаев впервые выявленного СД была сопоставимой у пациентов, получавших в течение 36 месяцев эволокумаб или плацебо (ОР 1,05 (95% ДИ 0,94–1,17)) [63].
Анализ результатов исследования ODYSSEY OUTCOMES не выявил каких-либо фактов, указывающих на увеличение риска развития СД, частота впервые выявленного СД не различалась между группами алирокумаба и плацебо (ОР 1,00 (95% ДИ 0,89–1,11)), а уровень HbA1c у пациентов без диабета, получавших алирокумаб, был ниже, чем в группе плацебо [55].
Существует предположение, что увеличение частоты развития СД у субъектов с генетически обусловленным снижением активности PCSK9 в отличие от пациентов, принимающих ингибиторы PCSK9, связано с внутриклеточными механизмами действия фермента, которые еще мало изучены. Моноклональные антитела ингибируют только внеклеточную PCSK9, циркулирующую в крови [61].
Заключение
Результаты клинических исследований доказывают высокую эффективность ингибиторов PCSK9 в отношении снижения и поддержания целевого уровня ХС ЛПНП у пациентов с СД и дислипидемией при их назначении в дополнение к максимально переносимым дозам статинов. Ингибиторы PCSK9 хорошо переносятся и не оказывают негативного влияния на контроль гликемии у пациентов с СД, а также не увеличивают риск развития СД.
Недавно опубликованные результаты исследования ODYSSEY OUTCOMES продемонстрировали эффективность ингибитора PCSK9 алирокумаба в отношении предупреждения повторных ишемических сердечно-сосудистых осложнений у пациентов, перенесших ОКС. Преимущества терапии алирокумабом были более выраженными у пациентов с СД.
Исходя из сказанного выше, можно сделать вывод, что возможности для улучшения прогноза у этой категории больных расширяются.
A.M. Mkrtumyan
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
A.S. Loginov Moscow Clinic Scientific Center
Contact person: Ashot Musaelovich Mkrtumyan, vagrashot@mail.ru
Patients with diabetes mellitus who have suffered acute coronary syndrome have a very high risk of recurrent cardiovascular events, despite evidence-based prognosis-modifying treatment, including the maximum tolerated doses of statins. The results of clinical studies have demonstrated the high efficacy of PCSK9 inhibitors in reducing and maintaining the target level of low-density lipoprotein cholesterol in patients with diabetes and dyslipidemia who were unable to reach the goals of lipid-lowering treatment with maximum tolerated doses of statins. An analysis of the results from a recently published ODYSSEY OUTCOMES trial showed that treatment with PCSK9 inhibitor alirocumab in patients with diabetes who suffered an acute coronary syndrome decreased the relative and absolute risk of major cardiovascular events such as myocardial infarction, ischemic stroke, death from coronary heart disease or unstable angina, requiring hospitalization (RR 0.84, 95% CI 0.74–0.97, absolute risk reduction - 2.3). Long-term therapy with alirocumab (median duration of treatment 2.8 years) was well tolerated and didn’t have any negative impact on the glycemic profile in patients with diabetes mellitus as well as in patients without diabetes and did not lead to an increase in the frequency of newly diagnosed diabetes.
