Оптимальная терапия сахарного диабета: цена вопроса и вопрос цены. VIII Всероссийский диабетологический конгресс «Сахарный диабет – пандемия XXI века». Сателлитный симпозиум компании «Такеда»
- Аннотация
- Статья
- Ссылки
В рамках симпозиума, состоявшегося при поддержке компании «Такеда» (Москва, 28 февраля 2018 г.), ведущие российские и зарубежные специалисты в области диабетологии обсудили методы терапии СД 2 типа, предложенные в последних рекомендациях и руководствах по оказанию помощи таким пациентам, сравнили эффективность и безопасность разных классов сахароснижающих препаратов, проанализировали возможность интенсификации терапии с помощью фиксированной комбинации ингибитора дипептидилпептидазы 4 алоглиптина и метформина. Председателем мероприятия выступила директор Института диабета ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения РФ, академик Российской академии наук, профессор Марина Владимировна ШЕСТАКОВА.
В рамках симпозиума, состоявшегося при поддержке компании «Такеда» (Москва, 28 февраля 2018 г.), ведущие российские и зарубежные специалисты в области диабетологии обсудили методы терапии СД 2 типа, предложенные в последних рекомендациях и руководствах по оказанию помощи таким пациентам, сравнили эффективность и безопасность разных классов сахароснижающих препаратов, проанализировали возможность интенсификации терапии с помощью фиксированной комбинации ингибитора дипептидилпептидазы 4 алоглиптина и метформина. Председателем мероприятия выступила директор Института диабета ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения РФ, академик Российской академии наук, профессор Марина Владимировна ШЕСТАКОВА.


Комбинированная терапия сахарного диабета 2 типа: в какой последовательности и какими препаратами
Профессор, руководитель отделения диабетологии, эндокринологии и метаболических заболеваний, IRCCS Центра кардиологии Монзино (Милан, Италия) Стефано ДЖЕНОВЕЗЕ отметил, что сахарный диабет (СД) 2 типа в последние годы приобрел характер эпидемии. В связи с этим многочисленные исследования сосредоточены на поиске эффективных методов и средств его лечения.
Современная стратегия терапии предполагает как изменение образа жизни, так и медикаментозное воздействие. Последнее прежде всего направлено на уменьшение инсулинорезистентности, восстановление секреции инсулина, устранение липотоксичности и снижение глюкозотоксичности. С этой целью применяются разные группы препаратов. Их назначают как для моно-, так и для комбинированной терапии.
Несмотря на большой пул лекарственных средств, не всегда удается добиться контроля заболевания. Недостаточная эффективность лечения объясняется клинической инертностью, то есть неспособностью интенсифицировать терапию тогда, когда это клинически целесообразно. Причин инертности может быть несколько: переоценка оказанной помощи, отсутствие знаний и опыта в достижении терапевтических целей, недостаточная приверженность пациентов лечению и многое другое1.
В то же время известно, что своевременная интенсификация терапии СД 2 типа позволяет улучшить гликемический контроль и таким образом снизить риск развития осложнений.
По данным ряда авторов, раннее вмешательство может способствовать достижению целевых значений гликированного гемоглобина (HbA1c)2.
В британском проспективном исследовании диабета UKPDS, в котором принимали участие пациенты с впервые выявленным СД 2 типа, были продемонстрированы преимущества интенсивного контроля гликемии. Он оказался надежным методом профилактики диабетических осложнений, в том числе сердечно-сосудистых. Риск развития заболеваний, обусловленных макро- и микрососудистыми осложнениями диабета, был ниже именно у тех пациентов, у которых был достигнут лучший контроль гликемии3. Эти результаты в дальнейшем подтвердились результатами исследований ACCORD4 и ADVANCE5. Использование методов интенсивной сахароснижающей терапии способствовало снижению уровня HbA1c, благодаря этому уменьшился риск микро- и макрососудистых осложнений. Интенсивная терапия даже при использовании старых групп сахароснижающих препаратов (инсулина, препаратов сульфонилмочевины (ПСМ), метформина) способна снизить частоту нефатального инфаркта миокарда, патологий коронарных артерий, инсульта и микрососудистых патологий. Однако при использовании инсулина, ПСМ не отмечено эффекта в отношении смертности.
По мнению профессора С. Дженовезе, в международных алгоритмах лечения СД 2 типа Американской диабетической ассоциации (American Diabetes Association – ADA) и Европейской ассоциации по изучению диабета (European Association for the Study of Diabetes – EASD) недооценена роль в снижении уровня HbA1c у больных СД 2 типа новых препаратов – ингибиторов дипептидилпептидазы 4 (ДПП-4) и агонистов рецепторов глюкагоноподобного пептида (ГПП-1). На сегодняшний день уникальные свойства и большой терапевтический потенциал инкретин-направленной терапии в регуляции углеводного обмена доказан результатами многочисленных исследований6.
Далее докладчик перечислил качества идеального препарата: «Этот препарат должен быть эффективным, безопасным, обладать другими клиническими преимуществами. На фоне его применения риск развития нежелательных реакций должен быть минимальным или отсутствовать. Препарат должен обладать оптимальным соотношением цены и эффективности». Ингибиторы ДПП-4 соответствуют этим критериям в полной мере. Их можно считать оптимальными препаратами для персонифицированной терапии СД 2 типа.
Ингибиторы ДПП-4 регулируют секрецию глюкагона в глюкозозависимом режиме. Доказано их протективное воздействие на массу и функцию бета-клеток. Среди негликемических эффектов препаратов данного класса следует отметить влияние на артериальное давление, липиды, факторы воспаления, эндотелий, кардиомиоциты7.
Ингибиторы ДПП-4 обеспечивают устойчивый гликемический контроль без риска гипогликемий и увеличения массы тела. Их отличают удобство приема, возможность комбинации с другими пероральными сахароснижающими препаратами, долгосрочность эффекта, положительное влияние на течение СД и клинические исходы.
Алоглиптин – высокоселективный ингибитор ДПП-4, который позволяет увеличить секрецию инсулина и снизить секрецию глюкагона, улучшить эффект инкретинов8. Препарат можно применять как в виде моно-, так и в виде комбинированной терапии.
Добавление алоглиптина к пиоглитазону, глибенкламиду или инсулину сопровождается значимым снижением уровня HbA1c по сравнению с добавлением плацебо. На фоне терапии алоглиптином в сочетании с другими сахароснижающими препаратами отмечается низкая частота эпизодов гипогликемий9–11.
Интенсификация монотерапии метформином с помощью алоглиптина в дозах 12,5 и 25,0 мг также способствовала большему снижению уровня HbA1c12.
В многоцентровом рандомизированном сравнительном исследовании эффективности алоглиптина и ПСМ глипизида при их комбинации с метформином установлено, что у пациентов с СД 2 типа и неудовлетворительным контролем на монотерапии метформином добавление алоглиптина обеспечивает более выраженный и устойчивый гликемический контроль без риска гипогликемий в течение двух лет13.
Преимущество ингибиторов ДПП-4 перед ПСМ заключается прежде всего в их нейтральном воздействии на массу тела и низком риске гипогликемических состояний.
Для сравнения эффективности ингибиторов ДПП-4 (алоглиптина, линаглиптина, саксаглиптина, ситаглиптина и вилдаглиптина) в комбинации с метформином и ПСМ при лечении пациентов с неконтролируемым СД 2 типа проведен ряд исследований. Применение алоглиптина в дозе 25,0 мг в комбинации с метформином в течение 104 недель привело к значимому снижению уровня HbA1c в отсутствие эпизодов гипогликемий по сравнению с применением ПСМ. При использовании ПСМ риск развития гипогликемий повышался в несколько раз14.
В ряде работ продемонстрировано плейотропное влияние ингибиторов ДПП-4 на сердечно-сосудистую систему. Выделяют прямые и опосредованные эффекты, среди которых – изменение сердечно-сосудистых факторов риска, защита миокарда от ишемии, артериальная вазодилатация.
Недавно опубликованы результаты исследования о влиянии алоглиптина на толщину комплекса «интима – медиа» (ТКИМ). Терапия алоглиптином по сравнению со стандартной терапией сопровождалась замедлением прогрессирования ТКИМ сонных артерий у пациентов с СД 2 типа без сердечно-сосудистых заболеваний15.
Особого внимания заслуживают результаты крупного исследования EXAMINE16.
Исследование EXAMINE – мультицентровое рандомизированное двойное слепое исследование сердечно-сосудистой безопасности алоглиптина у больных СД 2 типа, завершившееся в 2013 г. Особенностью дизайна было участие пациентов с СД 2 типа и очень высоким сердечно-сосудистым риском. В исследование включали лиц старше 18 лет, перенесших острый коронарный синдром за 15–90 дней до рандомизации и получавших любую сахароснижающую терапию, за исключением агонистов рецепторов ГПП-1 и ингибиторов ДПП-4.
В ходе исследования к исходной сахароснижающей терапии в двойном слепом режиме добавлялся алоглиптин (n = 2701) или плацебо (n = 2679). Сердечно-сосудистую терапию обе группы продолжали получать в соответствии с рекомендациями.
Конечными первичными точками в исследовании были сердечно-сосудистая смерть, нефатальный инфаркт миокарда, нефатальный инсульт.
Результаты исследования EXAMINE позволили сделать следующие выводы.
Частота развития событий первичной конечной точки в группе алоглиптина была сопоставима с частотой таковых в группе плацебо. Отношение рисков для каждого компонента первичной конечной точки было сопоставимо с отношением риска для их совокупности.
Анализ результатов по основной вторичной конечной точке (комбинация событий первичной конечной точки и экстренной реваскуляризации в связи с нестабильной стенокардией) не показал достоверных различий между группами. На фоне терапии аглоглиптином по сравнению с применением плацебо не отмечено повышения риска сердечно-сосудистой смерти и смерти от всех причин. Не выявлено также влияния уровня NT-pro-BNP на частоту госпитализаций по причине сердечной недостаточности. Применение алоглиптина не сопровождалось ни развитием новых случаев сердечной недостаточности, ни ухудшением ее течения.
В обсервационном исследовании с участием 35 тыс. пациентов с СД 2 типа сравнивали эффективность и безопасность ПСМ и ингибиторов ДПП-4 в комбинации с метформином. Оценивалась связь сахароснижающей терапии с основными неблагоприятными сердечно-сосудистыми событиями и смертью от всех причин. Риск развития нежелательных сердечно-сосудистых событий и смерти был выше у больных, принимавших ПСМ, чем у пациентов, получавших метформин и ингибиторы ДПП-417.
Таким образом, алоглиптин продемонстрировал кардиологическую безопасность у пациентов с СД 2 типа с очень высоким сердечно-сосудистым риском без увеличения риска развития других нежелательных явлений.
Далее докладчик акцентировал внимание аудитории на проблеме гипогликемии у больных СД 2 типа.
Гипогликемия признана основной причиной госпитализаций, макро- и микрососудистых осложнений, комы, смерти больных СД.
По данным многочисленных исследований, алоглиптин имеет благоприятный профиль безопасности у пациентов с СД 2 типа, в том числе у пожилых пациентов. Ретроспективный анализ результатов лечения пероральными сахароснижающими препаратами свидетельствует, что при включении в схему терапии алоглиптина частота гипогликемических состояний была низкой как у пациентов моложе 65 лет, так и у больных старше 65 лет18.
По словам профессора С. Дженовезе, ингибиторы ДПП-4 являются перспективными препаратами для лечения СД 2 типа. Они не только отличаются эффективностью и безопасностью, но и имеют дополнительные преимущества, прежде всего уникальный механизм действия, негликемические эффекты и разумное соотношение цены и качества. Благодаря дополнительным механизмам действия ингибиторы ДПП-4, в частности алоглиптин, могут назначаться в комбинации с метформином на ранних этапах лечения СД 2 типа с целью своевременной оптимизации терапии, поддержания гликемического контроля на долгосрочной основе и снижения риска развития осложнений.
Достижение цели: как соблюсти баланс
По словам д.м.н., заведующего отделением диабетической стопы ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, профессора Гагика Радиковича ГАЛСТЯНА, лечение пациентов с СД в первую очередь направлено на увеличение продолжительности жизни, повышение ее качества, предупреждение развития или прогрессирования поздних осложнений заболевания.
Поздние осложнения диабета, такие как ретинопатия, нефропатия, синдром диабетической стопы, ишемическая болезнь сердца, полинейропатия, являются главной причиной инвалидизации и смерти больных СД.
Сахарный диабет является одним из наиболее ресурсоемких заболеваний.
Оценка затрат на лечение больных СД – важный вопрос диабетологии. Расходы на лечение пациентов с СД подразделяются на прямые и непрямые.
В прямые траты входит стоимость лечения СД и его осложнений, скрининга поздних осложнений заболевания, лечения заболеваний, ассоциированных с СД (ожирение, опухоли и др.). При этом на поздних стадиях затраты на лечение возрастают.
К непрямым расходам относится оплата временной нетрудоспособности. Учитывают также снижение производительности труда, полную утрату трудоспособности, раннюю инвалидизацию и смерть. Непрямые траты могут занимать большую долю в конечной стоимости лечения19.
По данным Международной федерации диабета (International Diabetes Federation – IDF) за 2017 г., 12% глобальных расходов здравоохранения приходятся на лечение СД (727 млн долларов). Значительная их часть связана с лечением сердечно-сосудистой патологии. Так, в США 20% койко-дней в стационарах и 15% визитов к врачу обусловлены сердечно-сосудистыми заболеваниями. 64% пациентов с диабетической ретинопатией испытывают ограничения в повседневной активности по сравнению с 37% больных без ретинопатии. Основные расходы, связанные с ретинопатией, обусловлены утратой работоспособности и затратами на лиц, осуществляющих уход за такими больными.
По данным экспертов IDF, СД 2 типа – одна из основных причин развития почечной недостаточности. Расходы на пациентов с хронической болезнью почек на диализе в 2,8 раза выше, чем на пациентов с хронической болезнью почек до диализа20.
Экономический анализ ежегодных расходов во Франции на пациентов с СД, получающих сахароснижающую терапию, продемонстрировал, что сумма общих расходов составляет 17,7 трлн евро. При этом 2,5 трлн евро приходится на лечение и профилактику осложнений СД, 4,2 трлн – на лечение его поздних осложнений21.
Российскими специалистами была предпринята попытка оценить долю расходов на лекарственную терапию пациентов с СД – как основного заболевания, так и его осложнений. В этот анализ не включались расходы на обследование и скрининг осложнений. Установлено, что большая часть затрат связана с лечением осложнений, прямыми немедицинскими и непрямыми расходами. Затраты на лечение пациентов, у которых развились осложнения СД, превосходят затраты на лечение пациентов без осложнений. В случае СД 2 типа величина расходов различается в три раза22.
Контроль над экономическим бременем СД и сдерживание его роста можно обеспечить с помощью предотвращения развития осложнений вследствие назначения адекватной сахароснижающей терапии.
Последнее десятилетие ознаменовалось бурным развитием новых методов фармакотерапии. Сегодня на фармацевтическом рынке представлено 11 групп сахароснижающих препаратов. Важно отметить, что новые классы сахароснижающих препаратов (ингибиторы ДПП-4, агонисты рецепторов ГПП-1) характеризуются низким риском гипогликемических состояний, иначе влияют на течение СД, ассоциированного с избыточной массой тела или ожирением, по сравнению с такими классами препаратов, как ПСМ, глиниды, глитазон.
Результаты ретроспективного анализа базы данных Германии продемонстрировали изменения в подходах к лечению СД 2 типа с 2006 по 2014 г. Авторы исследования изучали динамику назначения сахароснижающих препаратов старого и нового поколения. Среди новых препаратов преимущественно назначались ингибиторы ДПП-4 и агонисты рецепторов ГПП-1, среди старых препаратов – ПСМ, глиниды, глитазон. К 2014 г. доля больных, получавших новые пероральные сахароснижающие препараты, возросла по сравнению с 2010 г. (7,2%) и составила 17,6%. Неизменными остались расходы на инсулинотерапию, сократились расходы на старые препараты и увеличились – на новые. Достоверно повысилось количество больных с уровнем HbA1c менее 6,5%. Кроме того, отмечено увеличение времени между назначением первого перорального сахароснижающего препарата и началом инсулинотерапии. Это не самый объективный критерий оценки качества лечения больных. Тем не менее назначение инсулина ассоциируется с дополнительными расходами и бременем для самого пациента, поскольку лечение связано с большими рисками развития гипогликемических эпизодов.
Результаты исследования показали, что более частое назначение новых сахароснижающих препаратов сопряжено с увеличением затрат на лечение и вместе с тем сопровождается снижением уровня HbA1c, частоты макрососудистых осложнений и увеличением времени до начала инсулинотерапии23.
Необходимо отметить, что в разных странах стандартизированный подход к терапии больных СД 2 типа значительно различается. Так, в странах Северной Европы в качестве первой линии терапии больным СД 2 типа в дебюте рекомендованы изменение образа жизни и метформин. В Дании и Финляндии препаратами второй линии являются ингибиторы ДПП-4 и агонисты рецепторов ГПП-1 (в Финляндии стоимость препарата не является определяющей при выборе терапии), в Норвегии и Швеции лидируют базальный инсулин и ПСМ.
При назначении сахароснижающей терапии лицам пожилого возраста акцент делается на применении наиболее безопасных препаратов. Так, в Финляндии для второй линии терапии больным СД 2 типа пожилого возраста показаны ингибиторы ДПП-4, глиниды, при симптоматической гипергликемии – инсулин24.
Результаты исследования, проведенного в США, также свидетельствуют об изменении подходов к лечению. Так, с 2005 по 2016 г. увеличилось использование в качестве препарата первой линии метформина (с 60 до 77%), инсулина (с 8 до 10%), новых пероральных сахароснижающих препаратов (до 4%). При этом сократилось назначение ПСМ (с 20 до 8%), глитазонов (с 11 до 1%). В отношении препаратов второй линии по-прежнему сохраняют лидерство ПСМ. Однако их применение сократилось с 60 до 46%. Использование инсулина в качестве препарата второй линии увеличилось с 7 до 17%, ингибиторов ДПП-4 – с 0,4 до 21%, ингибиторов натрий-глюкозного котранспортера 2 типа – до 17% (практически в два раза). К 2017 г. доля новых сахароснижающих препаратов в терапии СД 2 типа достигла 34%25.
Профессор Г.Р. Галстян отметил, что согласно данным реальной клинической практики наиболее вероятной причиной снижения потенциала сахароснижающих препаратов является низкая приверженность пациентов терапии.
Сравнение данных рандомизированных клинических исследований и реальной клинической практики в отношении применения разных антидиабетических препаратов свидетельствует, что агонисты рецепторов ГПП-1 и ингибиторы ДПП-4 демонстрируют примерно одинаковую эффективность. Однако в реальной практике терапия агонистами рецепторов ГПП-1 ассоциируется с более низкими показателями приверженности лечению. Скорее всего, это связано с высокой стоимостью препаратов и спектром нежелательных явлений, развивающихся на фоне такой терапии26.
Далее докладчик представил результаты ретроспективного анализа данных Федерального регистра больных СД, целью которого было сравнить фармакоэкономические показатели терапии ингибиторами ДПП-4 и ПСМ в фиксированной комбинации с метформином. Из 140 724 историй болезни отобрано 151 720. Это пациенты, которые начиная с 2010 г. получали лечение исключительно комбинированными препаратами. Средний возраст больных составил 68 лет, средняя длительность СД 2 типа – девять лет.
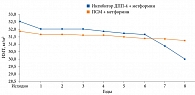
Оценивали также связь между индексом массы тела (ИМТ) пациентов и выбором препарата. Комбинация ингибитора ДПП-4 и метформина назначалась пациентам с большим ИМТ, поскольку препарат характеризуется нейтральным влиянием на массу тела. Терапия данной комбинацией способствовала снижению ИМТ у больных СД 2 типа.
С течением времени этот показатель в указанной когорте оставался неизменным.
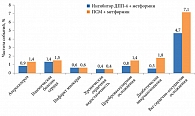
В группе пациентов, получавших ПСМ и метформин, зафиксирована более высокая частота сердечно-сосудистых осложнений по сравнению с больными, принимавшими ингибиторы ДПП-4 и метформин (рис. 1 и 2).
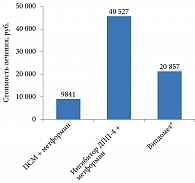
Один из важных параметров, оцениваемых в ходе исследования, – общие расходы на лечение одного пациента с СД 2 типа в год. Расчет всех трат дает реальное представление о расходах государства, понесенных в зависимости от выбранного вида терапии. Годовая стоимость терапии ПСМ и метформином составила 9841 руб., ингибитором ДПП-4 и метформином – 40 527 руб.
Четырехкратная разница в стоимости лекарственного средства в будущем покроется за счет уменьшения расходов на лечение осложнений и их последствий.
Лечение препаратом Випдомет (алоглиптин + метформин) обойдется в 20 857 руб./год. Терапия комбинацией ингибитора ДПП-4 и метформина с более конкурентной ценой за упаковку (Випдомет®) становится более экономически целесообразной.
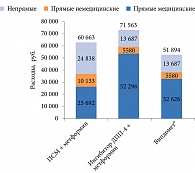
Общие годовые расходы на одного пациента, получающего Випдомет®, составили 51 894 руб., ПСМ и метформин – 60 663 руб., ингибитор ДПП-4 и метформин – 71 563 руб. (рис. 3 и 4).
Подводя итог, профессор Г.Р. Галстян подчеркнул, что анализ национальных регистров, базирующихся на данных реальной клинической практики, показывает, что применение новых классов сахароснижающих препаратов связано с улучшением контроля гликемии и тенденцией к снижению частоты хронических осложнений СД 2 типа. Применение при СД 2 типа ингибиторов ДПП-4 отличается лучшей приверженностью лечению по сравнению с использованием ПСМ и агонистов рецепторов ГПП-1.
Необходимы дальнейшие усилия по оптимизации расходов на лечение пациентов с СД 2 типа, прежде всего за счет предупреждения развития острых и хронических осложнений.
Заключение
Последние годы в мировой клинической практике все большую популярность приобретают новые классы сахароснижающих препаратов и новые подходы к терапии, в частности использование фиксированных комбинаций. Это позволяет не только воздействовать на несколько патогенетических звеньев СД 2 типа, повышать безопасность и приверженность лечению, но и снижать его стоимость.
Фиксированная комбинация метформина и ингибитора ДПП-4 алоглиптина (Випдомет®, компания «Такеда») воздействует на основные патогенетические механизмы развития СД 2 типа. К клиническим преимуществам сочетанного использования алоглиптина и метформина относятся потенцирование и усиление сахароснижающего эффекта, низкий риск гипогликемий, нейтральное воздействие на массу тела. Алоглиптин обладает сердечно-сосудистой безопасностью у больных СД 2 типа, в том числе из группы высокого риска.
Доза препарата Випдомет® должна подбираться индивидуально, исходя из текущих результатов лечения.
