Препараты сульфонилмочевины в современных алгоритмах ведения больных сахарным диабетом 2 типа
- Аннотация
- Статья
- Ссылки
В обзоре представлена эволюция взглядов на методы достижения гликемического контроля у больных сахарным диабетом (СД) 2 типа, описаны алгоритмы лечения пациентов с СД 2 типа согласно последним рекомендациям IDF и РАЭ.
Современная стратегия сахароснижающей терапии основывается на достижении индивидуализированных целей гликемического контроля, устанавливаемых с учетом возраста пациента, наличия у него сопутствующих заболеваний и других факторов, и предъявляет к сахароснижающим препаратам высокие требования не только в отношении их эффективности, но и профиля безопасности.
Авторы обсуждают место глибенкламида в современных схемах лечения пациентов с СД 2 типа в качестве моно- и комбинированной терапии с точки зрения эффективности в отношении коррекции углеводного обмена и отсутствия/минимизации риска развития гипогликемических состояний, увеличения веса и негативного влияния на сердечно-сосудистую систему.
На основании данных доказательной медицины показано, что применение глибенкламида в микронизированной форме (препарат Манинил®) является эффективным, препарат обладает высоким профилем безопасности при корректной тактике лечения и может также назначаться пожилым пациентам с наличием сопутствующих заболеваний.
В обзоре представлена эволюция взглядов на методы достижения гликемического контроля у больных сахарным диабетом (СД) 2 типа, описаны алгоритмы лечения пациентов с СД 2 типа согласно последним рекомендациям IDF и РАЭ.
Современная стратегия сахароснижающей терапии основывается на достижении индивидуализированных целей гликемического контроля, устанавливаемых с учетом возраста пациента, наличия у него сопутствующих заболеваний и других факторов, и предъявляет к сахароснижающим препаратам высокие требования не только в отношении их эффективности, но и профиля безопасности.
Авторы обсуждают место глибенкламида в современных схемах лечения пациентов с СД 2 типа в качестве моно- и комбинированной терапии с точки зрения эффективности в отношении коррекции углеводного обмена и отсутствия/минимизации риска развития гипогликемических состояний, увеличения веса и негативного влияния на сердечно-сосудистую систему.
На основании данных доказательной медицины показано, что применение глибенкламида в микронизированной форме (препарат Манинил®) является эффективным, препарат обладает высоким профилем безопасности при корректной тактике лечения и может также назначаться пожилым пациентам с наличием сопутствующих заболеваний.

Сахарный диабет (СД) 2 типа – одно из наиболее распространенных заболеваний. В настоящее время, по данным Международной диабетической федерации (International Diabetes Federation, IDF), сахарным диабетом в мире болеют более 366 млн человек, а к 2030 г. эта цифра может превысить 552 млн человек, в основном за счет больных СД 2 типа.
СД 2 типа – хроническое прогрессирующее заболевание с развитием специфических сосудистых осложнений (микроангиопатий) и быстрым прогрессированием атеросклероза, что повышает смертность от сердечно-сосудистых заболеваний в 4–5 раз по сравнению с общей популяцией [1–4]. При этом в 80% случаев причиной смерти больных СД 2 типа являются атеросклеротические поражения коронарных, церебральных и периферических сосудов [5].
В структуре причин смерти больных СД доля смертей, обусловленных атеросклерозом, превышает таковую от всех других причин, вместе взятых [5]. Согласно современным представлениям, такое выраженное поражение сосудистого русла происходит под влиянием гипергликемии, которая наряду с повышенным уровнем общего холестерина и артериального давления является фактором риска сердечно-сосудистой летальности [6].
Широко известные результаты крупномасштабного проспективного исследования UKPDS (United Kingdom Prospective Diabetes Study – Проспективное исследование сахарного диабета в Великобритании), показавшие роль неудовлетворительного гликемического контроля в прогрессировании диабетических сосудистых осложнений и подтвержденные в дальнейшем данными многочисленных рандомизированных исследований [7–14], стали основой Международного консенсуса по лечению СД 2 типа, провозгласившего достижение уровня HbA1c < 6,5% как конечную цель в лечении СД 2 типа. Однако интенсивная сахароснижающая терапия связана с риском развития гипогликемических состояний и увеличения массы тела, что приводит к повышению летальности по причине острых сосудистых катастроф.
Согласно результатам последних рандомизированных исследований, эпизоды гипогликемии выявлялись чаще при интенсивном лечении по сравнению со стандартной терапией: ACCORD (Action to Control CardiOvascular Risk in Diabetes – Исследование по контролю риска развития сердечно-сосудистых заболеваний при сахарном диабете 2 типа): частота эпизодов гипогликемии составила 16,2% против 5,1% соответственно; VADT (Veterans Affairs Diabetes Trial – Исследование сахарного диабета у ветеранов войн США): 21,2% против 9,9%; ADVANCE (Action in Diabetes and Vascular disease: preterAx and diamicroN-MR Controlled Evaluation – Действие при диабете и сосудистой болезни: контролируемая оценка Претеракса и Диамикрона MR): 2,7% против 1,5%. Повышение частоты гипогликемий сопровождалось увеличением общей летальности на 22% (исследование АССORD) и повышением частоты сердечно-сосудистых событий в последующие 3 месяца после тяжелой гипогликемии у пожилых людей (исследование VADT) [15, 16].
В ходе крупных исследований было также показано, что риск острой сердечно-сосудистой летальности повышается на фоне интенсивной сахароснижающей терапии, направленной на достижение целевого уровня HbA1c < 6,5%. В исследования ACCORD, ADVANCE и VADT были включены около 24 000 пациентов с большим «стажем» СД 2 типа, которые были рандомизированы в группы стандартного и интенсивного гликемического контроля для достижения уровня HbA1c менее 7,5% [15, 16, 17]. Средний уровень HbA1c в группе интенсивного контроля в исследованиях ACCORD, ADVANCE и VADT составил 6,4%, 6,5% и 6,9% по сравнению с 7,5%, 7,3% и 8,5% в группе стандартного контроля.
В этих исследованиях строгий гликемический контроль не снижал риск развития сердечно-сосудистых осложнений, и ни в одном из них не было отмечено положительного влияния интенсивной сахароснижающей терапии на частоту сердечно-сосудистых событий и смертность. Более того, исследование ACCORD было досрочно прервано в связи с повышенной смертностью среди пациентов, получавших интенсивную сахароснижающую терапию. Частота смерти от сердечно-сосудистых заболеваний была выше в группе интенсивного контроля по сравнению с группой стандартного контроля (2,6% против 1,8%).
Эти данные послужили основанием для пересмотра алгоритма ведения пациентов с СД, согласно которому интенсивная сахароснижающая терапия рекомендовалась для достижения целевого уровня гликемии. По последним рекомендациям Американской диабетической ассоциации (American Diabetes Association, ADA) и Европейской ассоциации по изучению диабета (European Association for the Study of Diabetes, EASD), целевой уровень HbA1c с учетом ожидаемого снижения частоты развития осложнений составляет < 7%, а уровень HbA1c ≥ 7% является сигналом к изменению сахароснижающей терапии [18].
Согласно рекомендациям IDF (2011), тактика достижения целевого уровня гликемии (HbA1c < 7%) на первом этапе терапии включает все мероприятия, касающиеся изменения образа жизни. Известно, что изменение образа жизни, направленное на снижение массы тела и расширение физической активности, позволяет достичь целевого уровня гликемии менее чем у 30% пациентов с впервые выявленным СД 2 типа [7].
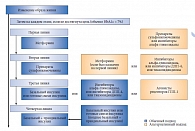
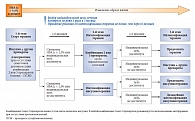
В связи с этим наряду с модификацией образа жизни предлагается поэтапное включение в терапию сахароснижающих препаратов (ССП) и рассматриваются четыре линии медикаментозной терапии с выбором обычного или альтернативного подхода (рис. 1) [19]. В качестве препарата первой линии рекомендуется (IDF, 2011) назначать метформин, учитывая его влияние на снижение уровня гликемии, отсутствие прибавки массы тела, низкий риск развития гипогликемических состояний, обычно хорошую переносимость и относительно низкую стоимость. Метформин остается наиболее изученным с точки зрения эффективности и профиля безопасности препаратом при монотерапии.
Максимальная сахароснижающая активность метформина отмечается при дозе 2000–2500 мг/сутки, которую рекомендуется достигать методом титрования, увеличивая дозировку на 500 мг каждую неделю (для уменьшения побочных явлений со стороны желудочно-кишечного тракта). Препараты сульфонилмочевины (ПСМ) должны назначаться пациентам с СД 2 типа в качестве препаратов второй линии, если на фоне монотерапии метформином не достигается целевой уровень HbA1c. В качестве препаратов третьей и четвертой линий рассматриваются различные варианты инсулинотерапии. Такие препараты, как ингибиторы дипептидилпептидазы 4-го типа (ДПП-4), ингибиторы альфа-гликозидазы, производные тиазолидиндионов (ТЗД) или агонисты глюкагоноподобного пептида 1 (ГПП-1), на сегодняшний день (пока не опубликованы результаты проспективных исследований) являются альтернативными препаратами для лечения СД 2 типа [18].
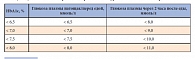
В 2011 г. эксперты Российской ассоциации эндокринологов (РАЭ) предложили установить индивидуальные цели сахароснижающей терапии по уровню НbА1с в зависимости от возраста пациента, ожидаемой продолжительности жизни, риска развития гипогликемических состояний и наличия/отсутствия тяжелых осложнений (табл. 1, 2) [20, 21]. Предложены схемы старта и интенсификации сахароснижающей терапии в зависимости от исходного уровня HbA1c [20, 21]. Во всех случаях рекомендуется определить индивидуальное целевое значение HbA1c для каждого пациента и, исходя из клинической ситуации, выбрать оптимальный вариант медикаментозной терапии.
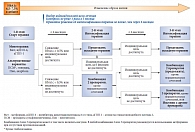
При исходном уровне НbА1с 6,5–7,5% рекомендуется начинать лечение с монотерапии препаратами с минимальным риском развития гипогликемии (метформин, ингибиторы ДПП-4, агонисты ГПП-1) (рис. 2) [20, 21]. При непереносимости или противопоказаниях к препаратам первого ряда рекомендуются альтернативные варианты терапии (ПСМ, глиниды, ТЗД, ингибиторы альфа-гликозидазы). В связи с риском развития гипогликемических состояний ПСМ при исходном уровне НbА1с 6,5–7,5% не являются средствами первого ряда, поэтому назначение ПСМ при данном уровне НbА1с целесообразно в отсутствие избыточной массы тела (что свидетельствует о сниженной секреции инсулина) либо при наличии противопоказаний или непереносимости препаратов первого ряда.
Терапия считается эффективной в случае достижения индивидуальных целей гликемии или снижения уровня НbА1с более чем на 0,5% от исходного за 6 месяцев наблюдения. Изменение терапии при недостаточной ее эффективности на каждом этапе рекомендуется осуществлять не позже, чем через 6 месяцев от начала лечения, а в случае ухудшения самочувствия пациента – раньше [20, 21]. При интенсификации терапии на втором этапе назначаются комбинации двух препаратов, обладающих взаимодополняющим механизмом действия. Наиболее рациональными признаны комбинации «метформин + ингибитор ДПП-4», «метформин + агонист ГПП-1», «метформин + ПСМ или глинид», которые уменьшают инсулинорезистентность и стимулируют секрецию инсулина.
Возможно назначение фиксированных комбинаций двух различных препаратов, в частности, зарегистрированных к применению в России готовых комбинаций («метформин + ПСМ», «метформин + ингибитор ДПП-4»). При недостаточной эффективности двойной терапии (при использовании в максимальной дозировке) следующим этапом является назначение тройной комбинации ССП или инсулинотерапии. Могут быть использованы различные сочетания препаратов (в том числе инсулин), кроме нерациональных комбинаций. Метформин продолжает являться основой лечения на данном этапе, вторым и третьим может быть препарат инкретинового ряда (ингибитор ДПП-4 или агонист ГПП-1), ПСМ или глинид, в отдельных случаях – ТЗД [20, 21]. Если применение тройной комбинации ССП является недостаточно эффективным, согласно Российским рекомендациям по проведению инсулинотерапии, необходимо проведение инсулинотерапии [22].
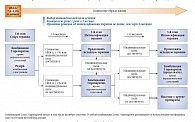
При исходном уровне НbА1с 7,6–9,0% (рис. 3) [20, 21] рекомендуется начать лечение с комбинации двух ССП, воздействующих на разные механизмы развития СД 2 типа. Наиболее рациональным является сочетание метформина (снижающего инсулинорезистентность) и препаратов, стимулирующих секрецию инсулина либо за счет непосредственного воздействия на бета-клетки (ПСМ, глиниды и агонисты ГПП-1), либо опосредованно – за счет блокады расщепления нативного ГПП-1 (ингибиторы ДПП-4). Двойная комбинация СПП, воздействуя на оба патогенетических звена развития СД 2 типа (инсулинорезистентность и неадекватную секрецию инсулина), обеспечивает адекватный контроль гликемии натощак и после еды и приводит к быстрому достижению индивидуальной цели лечения.
По данным многочисленных исследований, одновременное назначение препаратов с различным механизмом действия обеспечивает значимое снижение HbA1c не только за более короткие сроки, но и в меньших дозировках [23–25]. Эффективным считается темп снижения НbA1c > 1,0% за 6 месяцев наблюдения. Пациентам, входящим в группу высокого риска развития гипогликемических состояний, а также имеющим избыточную массу тела или ожирение, целесообразно назначение комбинаций метформина с ингибитором ДПП-4 или агонистом ГПП-1. Больным с выраженной декомпенсацией углеводного обмена (НbА1с > 8,5%) рекомендуется назначение комбинации метформина с ПСМ или инсулином [20, 21]. В отсутствие достижения индивидуальных целей гликемического контроля или при снижении уровня НbА1с менее чем на 1,0% от исходного за 6 месяцев наблюдения на втором этапе необходимо назначение комбинации трех препаратов, одним из которых может быть инсулин.
В любой тройной комбинации рекомендуется применение метформина (в отсутствие противопоказаний). Если комбинированная тройная терапия в течение 6 месяцев оказалась недостаточно эффективной, рекомендуется начать инсулинотерапию – сначала в фоновом, а затем и фоново-болюсном режиме, при переходе к которому необходимо отменить препараты, стимулирующие секрецию инсулина [20, 21]. Исходный уровень HbA1c > 9% предполагает наличие глюкозотоксичности, для устранения которой необходимо назначение инсулинотерапии (или комбинации инсулина с ССП) (рис. 4) [20, 21]. В редких случаях, когда при исходном уровне HbA1c > 9% отсутствуют выраженные клинические симптомы декомпенсации заболевания, можно начать лечение с альтернативного варианта с назначением комбинации двух или трех ССП.
Основой такой комбинации являются ПСМ как средства, наиболее эффективно повышающие секрецию эндогенного инсулина [20, 21]. Если в течение 6 месяцев инсулинотерапии достигнуты индивидуальные цели гликемического контроля или уровень НbА1с снизился > 1,5%, то возможен переход на комбинацию двух или трех ССП с отменой инсулинотерапии. В любой комбинации двух или трех препаратов рекомендуется использование метформина (в отсутствие противопоказаний). Если же за 6 месяцев терапии цель не достигнута или уровень НbА1с снизился < 1,5%, то терапию инсулином необходимо интенсифицировать в соответствии с Российскими клиническими рекомендациями «Оптимизация и интенсификация инсулинотерапии при сахарном диабете 2 типа» [22].
Таким образом, применение ПСМ в лечении СД 2 типа прочно сохраняет свои позиции в современной стратегии сахароснижающей терапии. Одним из наиболее известных и широко применяемых препаратов данного класса по-прежнему является глибенкламид, внедренный в клиническую практику еще в 1969 г. Глибенкламид, известный у нас в стране под торговым наименованием Манинил® (компания «Берлин-Хеми АГ», Германия), включен в современные алгоритмы сахароснижающей терапии как наиболее эффективный по своей гипогликемической активности препарат, а также благодаря таким характеристикам, как удобство применения (не чаще 1–2 раз в день), отсутствие клинически значимых (за исключением гипогликемии) побочных эффектов и невысокая стоимость.
Манинил® (глибенкламид) как препарат, играющий важную роль в оптимизации фармакотерапии СД 2 типа, неоднократно удостаивался международных премий. Значение глибенкламида, в частности его микронизированной формы, для мировой диабетологии было по достоинству оценено престижной фармацевтической премией имени Г. Крейтцфельдта в 2010 г. В 2012 г. Международное общество профилактической медицины впервые учредило номинацию «Профилактическое лекарственное средство» и присудило премию препарату Манинил®. Препарат, достойный присуждения премии, должен удовлетворять следующим критериям: обладать значительным терапевтическим и профилактическим потенциалом при СД 2 типа и его осложнениях, что должны подтверждать результаты большого числа доказательных исследований; должен быть представлен в современной лекарственной форме; обладать высоким профилем безопасности и хорошей переносимостью; быть пригодным для использования в комбинации с другими ССП или инсулином; быть пригодным для назначения пациентам пожилого возраста и иметь приемлемый фармакоэкономический профиль. Все эти характеристики присущи препарату Манинил®.
Основным механизмом сахароснижающего действия производных сульфонилмочевины является стимуляция секреции инсулина за счет связывания со специфическими рецепторами плазматической мембраны бета-клеток поджелудочной железы, интегрированными в структуру аденозинтрифосфат(АТФ)-зависимых К+-каналов. В настоящее время роль АТФ-зависимых К+-каналов в процессе регуляции инсулиновой секреции считается ключевой. Схематически этот процесс выглядит следующим образом: при поступлении глюкозы в бета-клетку повышается внутриклеточная концентрация АТФ, в результате чего закрываются АТФ-зависимые К+-каналы, происходит деполяризация мембраны, открываются вольтажзависимые Са2+-каналы, и ионы Са2+ входят в клетку. Вследствие повышения внутриклеточной концентрации ионов кальция происходит сокращение внутриклеточных миофибрилл и секреция инсулина, синтезированного ранее и накопленного в бета-клетке.
Благодаря тому, что ПСМ повышают чувствительность бета-клеток поджелудочной железы к глюкозозависимому инсулинотропному полипептиду (ГИП), стимуляция секреции инсулина происходит в зависимости от уровня гликемии, вследствие чего восстанавливается нормальная кривая инсулиновой секреции (1-я фаза), необходимая для снижения постпрандиальной гликемии. Неодинаковая аффинность ПСМ к специфическим рецепторам бета-клеток поджелудочной железы обусловливает их различную сахароснижающую активность. Чем выше сродство препарата к рецептору, тем длительнее его ингибирующее влияние на АТФ-зависимые К+-каналы и тем сильнее стимулируется секреция инсулина за счет поступления в бета-клетки ионов Са2+.
Среди всех ПСМ наиболее выраженным эффектом обладает глибенкламид. Высокая сахароснижающая активность глибенкламида объясняется особенностями его химической структуры – наличием не только сульфонилмочевинной, но и бензамидной группировки. Соединяясь с двумя связывающими местами рецепторов бета-клеток поджелудочной железы, глибенкламид наиболее быстро и мощно способствует закрытию АТФ-зависимых К+-каналов, стимулирует деполяризацию мембраны, повышение уровня внутриклеточного Са2+ и секрецию инсулина. Благодаря мощному сахароснижающему действию, отличающему глибенкламид от всех других имеющихся в настоящее время ПСМ, препарат, по мнению многих авторов, по-прежнему остается «золотым стандартом» пероральной сахароснижающей терапии. Практически во всех исследованиях, изучающих различные подходы к лечению СД 2 типа, активность сахароснижающих средств сравнивают с активностью глибенкламида.
Многочисленные рандомизированные исследования доказали клиническую эффективность глибенкламида в поддержании гликемического контроля. Одно из крупномасштабных исследований – UKPDS, в котором участвовали 4279 пациентов с впервые выявленным СД 2 типа, – показало, что через 3 года терапии цели гликемического контроля (гликемия < 7,8 ммоль/л и HbA1c < 7,0%) были достигнуты у 47% пациентов, получавших терапию глибенкламидом или инсулином, и у 44% пациентов, получавших метформин [7]. Проведенный A. Gangji и соавт. метаанализ 20 исследований, в которых глибенкламид сравнивали с другими ПСМ и секретагогами, подтвердил самую высокую эффективность глибенкламида по сравнению с другими ПСМ [26]. Исследование ADOPT (A Diabetes Outcome Progression Trial – Исследование исходов прогрессирующего диабета), включавшее 4127 пациентов, которые получали росиглитазон, метформин и глибенкламид в течение 4 лет, также продемонстрировало наибольшую сахароснижающую активность глибенкламида в течение 1-го года терапии и наиболее значимое снижение риска сердечно-сосудистых осложнений [9].
Критерием эффективности любого сахароснижающего препарата является не только достижение и поддержание адекватного гликемического контроля, но и способность препарата предупреждать макро- и микрососудистые осложнения СД, от которых погибают большинство больных. Глибенкламид можно считать самым изученным препаратом среди ПСМ 2-го поколения, поскольку во всех крупных многоцентровых исследованиях, посвященных лечению СД 2 типа и развитию его осложнений, участвовали группы пациентов, которые принимали глибенкламид. В ходе исследования UKPDS было продемонстрировано, что длительное применение глибенкламида приводит к значительному снижению риска развития микрососудистых осложнений [7].
По завершении исследования UKPDS часть пациентов была включена в дальнейшее наблюдение длительностью 10 лет, в результате чего появилась возможность проследить эффекты интенсивной сахароснижающей терапии в течение 20 лет после первичной диагностики СД 2 типа. В группе приема ПСМ или инсулинотерапии частота микрососудистых осложнений СД к моменту окончания периода наблюдения достоверно снизилась на 24%, частота инфаркта миокарда – на 15%, смертность от других причин – на 13% [13]. В исследовании ADOPT отмечалось снижение частоты сердечно-сосудистых осложнений в группе глибенкламида в 2,2 раза по сравнению с группой росиглитазона [9]. Таким образом, доказано, что прием ПСМ, в частности глибенкламида, в течение длительного времени снижает риск развития микро- и макрососудистых осложнений СД 2 типа.
Аспекты сердечно-сосудистой безопасности сахароснижающих средств и возможности снижения сердечно-сосудистого риска путем оптимизации терапии СД 2 типа были и остаются темами дискуссий и научного поиска. В середине 70-х годов прошлого столетия появились публикации, свидетельствовавшие о повышении сердечно-сосудистой смертности при применении ПСМ 1-го поколения, в частности толбутамида [16]. В те же годы начали проводить исследования по изучению профиля безопасности глибенкламида, результаты которых носили противоречивый характер. Некоторые авторы опровергали предположения о высоком риске сосудистых катастроф при приеме глибенкламида, другие указывали на его кардиотоксичность. Это, скорее всего, обусловлено различиями в методологии проведения исследований.
В тех исследованиях, где было показано негативное влияние глибенкламида на сердечно-сосудистую систему, препарат вводили в высоких дозах внутрикоронарно или внутривенно, что, безусловно, нельзя сравнивать с пероральным приемом при СД 2 типа. Этот вопрос был закрыт после публикаций результатов UKPDS [7], показавших отсутствие через 10 лет лечения заметной разницы в отношении сердечно-сосудистой заболеваемости и смертности между группами больных, получавших лечение инсулином, глибенкламидом или хлорпропамидом. Активная дискуссия возобновилась в середине 1990-х гг., когда были клонированы АТФ-зависимые К+-каналы и доказана гетерогенность рецепторов к ПСМ (SUR) в бета-клетке (SUR1) и в кардиомиоцитах и гладкомышечных клетках сосудистой стенки (SUR2A и SUR2B).
Было высказано мнение о том, что в связи с наличием в структуре глибенкламида сульфонилмочевинной и бензамидной группировок препарат может обладать кардиотоксическим эффектом, так как в эксперименте он блокирует активность АТФ-зависимых К+-каналов не только бета-клеток поджелудочной железы, но и кардиомиоцитов, связываясь с SUR2А, содержащим только бензамидные связывающие места. Длительная блокада К+-АТФ-каналов кардиомиоцитов высокими дозами ПСМ в условиях эксперимента с моделированием ишемии миокарда усугубляла нарушения обмена калия в кардиомиоцитах. Теоретически это могло бы отрицательно влиять на исходы инфаркта миокарда у больных СД 2 типа [27, 28]. Однако кардиотропность глибенкламида не подтвердилась in vivo: установлено, что кардиомиоцит имеет существенно более низкую чувствительность к ПСМ, чем бета-клетка [29–31]. Эта гипотеза не подтвердилась и в клинических исследованиях.
В проспективном исследовании LAMBDA (The LAngendreer Myocardial infarction and Blood glucose in Diabetic patients Assessment – Лангендрерское исследование острого инфаркта миокарда и уровня глюкозы крови у пациентов с сахарным диабетом) было показано, что предшествующий прием глибенкламида, как и всех остальных ПСМ, не оказывает отрицательного влияния на уровень выживаемости больных с СД 2 типа после перенесенного инфаркта миокарда [32]. В другом исследовании ретроспективно оценивалась летальность от инфаркта миокарда у 386 пациентов с СД 2 типа, которые до инфаркта получали ПСМ 2-го поколения (n = 120), инсулин (n = 180) или немедикаментозное лечение (n = 86). После исключения таких факторов, как возраст, пол, сердечная недостаточность, длительность СД, почечная дисфункция, проведение реваскуляризации миокарда, оказалось, что на фоне приема ПСМ летальность от инфаркта миокарда была достоверно ниже, чем в группе инсулинотерапии (относительный риск 0,41; 95% доверительный интервал (ДИ) 0,21–0,80; р = 0,009) [33].
Результаты ретроспективного метаанализа, в котором изучалось влияние монотерапии различными ПСМ на летальность среди 11 141 пациентов с СД 2 типа, не выявили достоверной разницы в риске общей летальности между пациентами, получавшими монотерапию глибенкламидом (n = 4279), глипизидом (n = 4325) или глимепиридом (n = 2537) [34]. В дальнейшем прицельному изучению с точки зрения сердечно-сосудистой безопасности подвергались все новые сахароснижающие средства. Проведено немало специальных исследований, посвященных оценке сердечно-сосудистых исходов на фоне лечения СД 2 типа различными ПСМ, однако кардиотоксичность этого класса препаратов или отдельных его представителей не подтвердилась.
Так, в систематический обзор 2008 г., посвященный проблеме долгосрочных сердечно-сосудистых исходов пероральной сахароснижающей терапии, включены результаты анализа данных 40 контролируемых исследований, в которых регистрировались сердечно-сосудистые события (в основном инфаркты миокарда и инсульты) у пациентов с СД 2 типа, получавших ПСМ 2-й генерации, бигуаниды, ТЗД или меглитиниды. Статистический анализ не выявил взаимосвязи приема ССП с повышением частоты смертельных и несмертельных сердечно-сосудистых событий, а также общей смертности [35]. В 2010 г. был представлен анализ литературных данных о частоте сердечно-сосудистых осложнений на фоне терапии СД 2 типа секретагогами, в том числе ПСМ. В трех рандомизированных контролируемых исследованиях с общим числом пациентов 2822 и длительностью наблюдения от 1 до 10 лет, в которых оценивался риск сердечно-сосудистых осложнений у пациентов с СД 2 типа, авторы не выявили статистически значимых различий между группами больных, получавших монотерапию глибенкламидом и другими секретагогами (хлорпропамидом, репаглинидом и глимепиридом) [36].
Кроме того, в отношении глибенкламида был показан его достаточно выраженный антиаритмический эффект. Это свойство напрямую связано с мягким действием препарата на АТФ-зависимые К+-каналы (блокада затрагивает порядка 10% каналов) и способностью предотвращать чрезмерную потерю ионов К+ клетками миокарда в условиях ишемии. Это свойство отличает глибенкламид от других ПСМ, которые практически не связываются с рецепторами в миокарде. Антиаритмический эффект глибенкламида очень важен для пациентов с СД 2 типа в остром периоде инфаркта миокарда, поскольку одной из основных причин смерти этой категории больных является желудочковая аритмия и, в частности, фибрилляция желудочков, связанная со снижением внутриклеточного содержания ионов К+. В клинических исследованиях получены доказательства того, что у пациентов с СД 2 типа, которые принимали глибенкламид, в условиях развившейся ишемии снижается вероятность возникновения желудочковых аритмий и фибрилляции желудочков [37].
В одном из исследований регистрировали аритмические осложнения острого инфаркта миокарда у 232 пациентов с СД 2 типа. 106 больных получали глибенкламид (группа 1), 126 – другие ССП или не получали медикаментозной терапии (группа 2). Контрольную группу составили 830 больных с инфарктом миокарда без СД. Отмечено, что фибрилляция желудочков достоверно реже возникала у пациентов группы 1 (1,9%) по сравнению с группой 2 (7,9%) и контролем (9,9%) [38]. Ретроспективная оценка 56 715 историй болезни выявила, что летальность при остром инфаркте миокарда составила 12% в группе пациентов без СД и 28,1% у пациентов с СД, а частота развития фибрилляции желудочков у больных СД, получавших глибенкламид, была аналогична таковой у пациентов без СД (11,8 и 11,0% соответственно), однако была меньше, чем у пациентов, получавших гликлазид (18%) и инсулин (22,8%) [39].
Определенную точку в вопросе влияния глибенкламида на сердечно-сосудистую систему может поставить метаанализ А.S. Gangji и соавт. [26], одной из целей которого было сравнение безопасности монотерапии глибенкламидом, другими секретагогами и инсулином в отношении риска развития гипогликемии и сердечно-сосудистых событий. Авторами метаанализа, в который было включено 21 рандомизированное клиническое исследование, проводившееся в период с 1966 по 2005 г., был сделан вывод, что применение глибенкламида ассоциируется с более высокой частотой гипогликемических состояний, но не сопровождается повышением риска сердечно-сосудистых событий, смерти и увеличением массы тела к концу периода наблюдения.
Таким образом, накопленные к настоящему времени данные доказательной медицины свидетельствуют о том, что глибенкламид и другие ПСМ не увеличивают сердечно-сосудистый риск. Глибенкламид обладает скорее кардиопротекторным эффектом в условиях ишемии миокарда, поскольку его мягкое действие на АТФ-зависимые К+-каналы миокардиоцитов предотвращает чрезмерную потерю калия и, следовательно, нарушения ритма при инфаркте миокарда. Как отмечалось выше, глибенкламид обладает наибольшим сродством к АТФ-зависимым K+-каналам бета-клеток поджелудочной железы и поэтому оказывает самый мощный сахароснижающий эффект, нередко являющийся причиной развития гипогликемических состояний.
Повышенный риск развития гипогликемических состояний, как правило, связан с нарушением режима питания (пропусками приемов пищи), интенсивной физической нагрузкой, быстрым титрованием дозы глибенкламида и приемом немикронизированного глибенкламида, который обладает менее безопасным фармакокинетическим профилем. Особенностью традиционных лекарственных форм глибенкламида является медленное и постепенно нарастающее наступление сахароснижающего эффекта. Это связано с медленным всасыванием препарата и его низкой биодоступностью, что повышает вероятность развития гипогликемии в постабсорбционном периоде, особенно при приеме высоких доз (10 мг и более). Это объясняет повышенный риск отсроченной, возникающей на 4–6-м часу после приема препарата, гипогликемии.
Решить эту проблему позволяет микронизированная форма глибенкламида, которая практически вытеснила обычные формы препарата из клинической практики. Микронизированные формы (Манинил® 3,5 и Манинил® 1,75) характеризуются практически 100%-ной биодоступностью и большей эффективностью при употреблении в меньшей разовой и суточной дозе. Полное высвобождение действующего вещества происходит в течение 5 минут после растворения таблетки. Благодаря высокой биодоступности суточную дозу препарата Манинил® можно уменьшить на 30–40% по сравнению с приемом обычных таблеток глибенкламида. Период полувыведения микронизированной формы составляет 2–5 часов, а длительность сахароснижающего действия достигает 24 часов.
Благодаря оптимальной фармакокинетике для круглосуточного контроля гликемии Манинил® достаточно принимать 1–2 раза в сутки непосредственно перед приемом пищи. Пик сахароснижающего действия микронизированного глибенкламида почти полностью совпадает с фазой постабсорбционной гипергликемии, что способствует снижению риска развития гипогликемических состояний между приемами пищи – без сомнения, это весьма актуально для больных пожилого возраста. Следует помнить о необходимости постепенного, медленного титрования доз препарата. Начинать подбор дозы препарата Манинил® рекомендуется с однократного приема 1,75 мг. Дозу увеличивают не быстрее чем каждые 7–10 дней до достижения необходимого терапевтического эффекта. Не следует назначать препарат в дозе более 14 мг/сут.
Непременным условием правильности подбора дозы и профилактики развития гипогликемических состояний является строгое соблюдение пациентом низкокалорийной (при СД 2 типа с ожирением) либо изокалорийной (при нормальной массе тела) диеты. Чрезмерная стимуляция секреции инсулина при применении глибенкламида отмечается только при переедании, поскольку препарат повышает чувствительность бета-клеток поджелудочной железы к ГИП и стимулирует секрецию инсулина в соответствии с уровнем гликемии. Правильно подобранная доза препарата Манинил® на фоне корректной диетотерапии, напротив, при длительном применении обеспечивает нормализацию уровня инсулинемии благодаря восстановлению чувствительности периферических тканей к нему и устранению гипергликемии.
Частота гипогликемий на фоне лечения глибенкламидом в условиях реальной клинической практики остается невысокой. В проспективном исследовании на большой выборке больных СД 2 типа частота тяжелых гипогликемий, которые требовали внутривенного введения глюкозы или глюкагона, составила 5,6 на 1000 пациенто-лет применения глибенкламида, хотя и была выше, чем у пациентов, принимавших глимепирид [40]. Все случаи гипогликемии, как правило, имели место у пожилых больных (средний возраст – 79 лет) или пациентов с тяжелыми сопутствующими заболеваниями (снижение функции почек, сердечная недостаточность, ишемическая болезнь сердца, опухоли, церебральная ишемия, алкоголизм, деменция) [41]. В упоминавшемся выше систематическом обзоре, посвященном сравнению параметров безопасности ПСМ и других секретагогов, оценивалась частота гипогликемии у пациентов, получавших монотерапию глибенкламидом, по сравнению с монотерапией хлорпропамидом, глипизидом, глимепиридом, гликлазидом, репаглинидом и натеглинидом [36].
В 3 из 11 отобранных для анализа рандомизированных исследованиях с участием 4713 пациентов и длительностью наблюдения от 8 недель до 5 лет было показано, что частота гипогликемий на фоне терапии глибенкламидом выше по сравнению с другими сахароснижающими препаратами. Однако следует учесть, что в этих исследованиях назначался немикронизированный глибенкламид в максимальной дозе 10 мг/сут. В остальных 8 проспективных исследованиях статистически значимых отличий по частоте гипогликемий между глибенкламидом и другими секретагогами отмечено не было. В двух исследованиях при сравнении микронизированного глибенкламида с репаглинидом относительный риск гипогликемий в обеих группах был сопоставимым и составил 0,93 (95% ДИ 0,39–2,24) и 0,97 (95% ДИ 0,51–1,83) соответственно. Таким образом, при сравнении монотерапии глибенкламидом и другими секретагогами в исследованиях, выполненных независимо друг от друга разными авторами, не получено доказательств повышенного риска развития гипогликемических эпизодов на фоне терапии глибенкламидом. Применение микронизированных форм глибенкламида позволяет снизить риск этого осложнения сахароснижающей терапии.
СД 2 типа является хроническим заболеванием, при котором прогрессирует инсулиновая недостаточность и инсулинорезистентность, что приводит к развитию вторичной резистентности к ПСМ и необходимости назначения комбинированной сахароснижающей терапии или перевода на инсулинотерапию. В целом ряде исследований показана эффективность глибенкламида в комбинации с фоновой инсулинотерапией [42, 43], метформином [24, 44, 45] и ТЗД при развитии вторичной резистентности к ПСМ [46]. Проведены также исследования, свидетельствующие об эффективности и высоком профиле безопасности комбинации глибенкламида и препаратов инкретинового ряда – аналогов ГПП-1 и ингибиторов ДПП-4 [47–50]. Таким образом, глибенкламид можно комбинировать с любыми известными на сегодняшний день сахароснижающими препаратами (за исключением секретагогов и прандиального инсулина), что способствует улучшению гликемического контроля без повышения риска гипогликемических состояний благодаря возможности снижения дозы глибенкламида при комбинации различных препаратов.
Пациенты с СД 2 типа – в большинстве случаев пожилые люди с избыточной массой тела, страдающие ишемической болезнью сердца, гипертонической болезнью, имеющие высокий риск развития острого инфаркта миокарда и инсульта. Гипергликемия, как показали результаты метаанализа 20 исследований, включавших 95 783 пациентов, наблюдаемых в течение 12 лет, является таким же фактором риска развития атеросклероза и острой сердечно-сосудистой летальности, как и высокий уровень общего холестерина и артериального давления [6]. Снизить риск сердечно-сосудистой смерти можно с помощью оптимального гликемического контроля, при котором отсутствует риск развития гипогликемических состояний. С этой точки зрения применение глибенкламида в микронизированной форме является эффективным, препарат обладает высоким профилем безопасности при корректной тактике лечения и может также назначаться пожилым пациентам с наличием сопутствующих заболеваний.
Важнейшим аспектом в терапии СД 2 типа, безусловно, является фармакоэкономический вопрос, то есть выбор препарата с оптимальным соотношением стоимости, клинической эффективности и профиля безопасности. Это связано с необходимостью длительного (пожизненного) лечения СД. Немаловажным фактором является высокая заболеваемость и огромное количество пациентов, страдающих СД 2 типа. Цена социально значимых препаратов, к которым относятся пероральные сахароснижающие средства, должна быть приемлемой как для каждого конкретного пациента, так и в целом для системы здравоохранения, которая обеспечивает больных сахароснижающими препаратами за счет государственного бюджета. В этом ряду Манинил® является наиболее эффективным и доступным ПСМ.
Существуют данные о том, что стоимость 1 DDD (defined daily dose – установленная суточная доза препарата) и годичного курса лечения препаратом Манинил® 3,5 мг в 9 и 10 раз меньше стоимости терапии препаратом Амарил® 2 мг и 4 мг соответственно и в 15 раз меньше лечения препаратом Диабетон® МВ 80 мг [51]. Высокую социальную значимость глибенкламида подчеркивают и эксперты Всемирной организации здравоохранения (ВОЗ), включив его в очередной раз в перечень Основных лекарственных средств (16-я редакция списка, март 2010). Этот перечень содержит наиболее эффективные, безопасные и выгодные с фармакоэкономической точки зрения лекарственные средства для лечения социально значимых заболеваний. Следует отметить, что глибенкламид является единственным представителем ПСМ в данном списке, наряду с метформином и инсулином короткой и средней продолжительности действия. Глибенкламид включен также в список Основных лекарственных средств и в нашей стране.
Таким образом, современная стратегия сахароснижающей терапии предполагает применение комбинаций сахароснижающих препаратов, которые были бы наиболее эффективны в отношении коррекции углеводного обмена, без риска развития гипогликемических состояний, увеличения веса и негативного влияния на сердечно-сосудистую систему. Применение глибенкламида в комплексной терапии СД 2 типа на сегодняшний день прочно сохраняет свои позиции в различных алгоритмах лечения, учитывающих поставленную цель гликемического контроля, возраст пациента и наличие у него сопутствующих сердечно-сосудистых заболеваний. Применение микронизированной формы препарата Манинил® при корректном проведении терапии обеспечивает благоприятное сочетание эффективности и высокого профиля безопасности. Благодаря своему фармакоэкономическому профилю глибенкламид включен в список Основных лекарственных средств ВОЗ и РФ.
NB
Манинил® 3,5 и Манинил® 1,75 – микронизированные формы глибенкламида
- Практически 100%-ная биодоступность.
- Бóльшая эффективность при употреблении в меньшей разовой и суточной дозе, по сравнению с немикронизированным глибенкламидом.
- Полное высвобождение действующего вещества – в течение 5 минут после растворения таблетки.
- Длительность сахароснижающего действия – до 24 часов.
- Манинил® достаточно принимать 1–2 раза в сутки непосредственно перед приемом пищи.
- Включен в список основных лекарственных средств ВОЗ и РФ.
Авторы обсуждают место глибенкламида в современных схемах лечения пациентов с СД 2 типа в качестве моно- и комбинированной терапии с точки зрения эффективности в отношении коррекции углеводного обмена и отсутствия/минимизации риска развития гипогликемических состояний, увеличения веса и негативного влияния на сердечно-сосудистую систему. На основании данных доказательной медицины показано, что применение глибенкламида в микронизированной форме (препарат Манинил®) является эффективным, препарат обладает высоким профилем безопасности при корректной тактике лечения и может также назначаться пожилым пациентам с наличием сопутствующих заболеваний.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.