Принципы антибактериальной терапии и профилактики перед урологическими операциями
- Аннотация
- Статья
- Ссылки




Мультирезистентные штаммы бактерий становятся частью нормальной микрофлоры кишечника. По данным Neuhauser (2003), уровень резистентности к фторхинолонам – антибиотикам для терапии мочевой инфекции – увеличивается на 2% в год ввиду селекции мутантов во время лечения, уровня резистентности к фторхинолонам в отделениях реанимации и интенсивной терапии свыше 50%, широкого использования их в ветеринарии – вместе с мясом кур, с хлебом мы поглощаем уже резистентные бактерии. Резистентные возбудители к хинолонам обнаруживаются у здоровых взрослых в 24%, у здоровых детей – уже в 26%.
Самое печальное, о чем сейчас говорят все специалисты, – на сегодняшний день против грамотрицательных микроорганизмов нет новых антибиотиков. Поэтому, конечно, нам надо сохранять имеющиеся антибиотики и принимать меры, сдерживающие резистентность в больницах. В числе таких мер EMEA предлагает: гигиену рук – элементарное мытье и использование стерильных перчаток на 50% снижает уровень возникновения резистентных инфекций мочевых путей;
- изоляцию больных с инфекцией;
- рациональное использование антибиотиков;
- меры инфекционного контроля;
- требование от больниц сообщений об уровне госпитальной инфекции и связь их с механизмами резистентности и использованием антибиотиков;
- отказ возмещения затрат страховыми компаниями при лечении госпитальной инфекции.
Огромное значение имеет лабораторный контроль. Необходимы постоянный бактериологический мониторинг в клинике, быстрое определение резистентности у больных с высоким риском инфекции (в течение нескольких часов после поступления в клинику), детекция b-лактамаз у клинических штаммов. Проведенными в НИИ урологии исследованиями выявлена большая распространенность ферментов b-лактамаз среди микроорганизмов, выделенных от больных в урологическом стационаре: процент микроорганизмов, обладающих b-лактамазной активностью, варьировал от 36 до 75 в зависимости от видовой принадлежности возбудителя. По данным НИИ урологии (2009), ведущими возбудителями ИМП остаются Klebsiella (37,5%) и E. coli (36,8%). Для россиян это 50-80% резистентных штаммов. Сегодня существует только одна группа препаратов – карбапенемы, к которой имеется 100%-ная чувствительность этих микроорганизмов. Таким образом, карбапенемы наиболее надежны.
Госпитальные штаммы микроорганизмов характеризуются множественной лекарственной устойчивостью, что вызывает значительные трудности при лечении инфекционно-воспалительных заболеваний, возникших у больного в стационаре, особенно в послеоперационном периоде. Одним из путей снижения уровня госпитальной ИМП является использование антибактериальной профилактики перед разными вмешательствами и операциями в урологических стационарах.
Говоря о принципах антимикробной терапии в больницах или клиниках, мы подразумеваем, конечно, деэскалационную терапию. Эмпирическая стартовая терапия серьезных инфекций обязывает также взять материал на культуральное исследование. Только после этого идет назначение антибиотика широкого спектра действия для того, чтобы снизить летальность, органную недостаточность, длительность госпитализации. После получения результатов бактериологического анализа (24-72 ч) переходим на антибиотики узкого спектра действия. Противомикробная терапия инфекций носит в настоящее время преимущественно эмпирический характер. Основанием для выбора антибактериальных препаратов должны являться результаты микробиологических исследований. Совершенствование диагностических тестов по выявлению возбудителей позволит добиться максимальных результатов антибактериальной терапии у данной категории пациентов. Предлагается циклическая смена классов антибиотиков в стационаре для того, чтобы замедлить развитие резистентности. Для борьбы с антибиотикорезистентностью создаются комбинации препаратов, однако целесообразность использования комбинаций доказана не всегда. Монотерапия снижает риск как лекарственных взаимодействий, так и частоту ошибок применения препаратов, неадекватного дозирования и нежелательных побочных реакций. К тому же, что немаловажно, монотерапия обладает меньшей стоимостью.
Нарушению принципов рациональной антимикробной терапии способствует назначение повторных длительных курсов антибиотиков с их сменой особенно на более мощные. Сохранение клинических признаков инфекции к концу периода, необходимого для оценки эффективности терапии (24-72 ч), является показанием для дополнительного поиска очага инфекции в организме, а не пролонгирования антимикробной терапии.
Режимы дозирования зависят от принадлежности антибиотика к Td- либо Cd-группе. К первой относятся пенициллины, цефалоспорины, азтреонам и пр., требование к режиму дозирования которых заключается в поддержании стабильных концентраций в течение суток (длительные инфузии). Метронидазол, фторхинолоны и пр., относящиеся к Cd-группе антибиотиков, требуют создания пика концентрации и длительных интервалов между введениями.
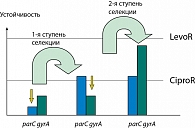
Рассмотрим механизмы ступенчатого приобретения резистентности к фторхинолонам. Так, существуют опасные зоны концентрации, в которых мутантные штаммы селективно увеличиваются. Увеличение одного резистентно мутантного типа облегчает амплификацию второго, имеющего более низкую чувствительность к препарату (рисунок 1).
При падении концентрации антибиотика увеличивается субпопуляция одноступенчатых мутантов. Сохраняя антимикробную концентрацию выше окна селекции мутации, мы сдерживаем расширение субпопуляций резистентных мутантов, тогда как при традиционном подходе (при C > MIC) мы сдерживаем выработку чувствительных патогенов (Ambrose et al., 2002). Киллинг чувствительных бактерий недостаточен, чтобы блокировать резистентные мутанты, таким образом, вследствие резистентности нет эффекта лечения.
Комбинируя антибиотики, имеющие разные мишени действия, применяя концентрации, соответствующие подходу «окна селекции мутации», мы можем проводить стратегию против мутантов (Livermore D.M., 2004), так как правильное использование антибиотиков имеет особое значение на фоне повышения резистентности грамотрицательных микроорганизмов:
- целесообразная антибиотикотерапия и профилактика;
- антибиотики с низким потенциалом в отношении дальнейшей селекции антибиотикорезистентности;
- антибиотики, не обладающие активностью в отношении P. aeruginosa, за исключением случаев, когда это необходимо, что позволит ограничить возникновение мультирезистентности P. aeruginosa;
- применение антибиотиков в течение как можно более короткого периода времени.
Этим условиям соответствует применение эртапенема (ИнванзÒ), который в условиях in vitro активен относительно широкого спектра грамположительных и грамотрицательных аэробных и анаэробных микроорганизмов. Бактерицидная активность эртапенема обусловлена угнетением синтеза клеточной стенки бактерий путем связывания эртапенема с пенициллинсвязывающими белками (ПСБ). Эртапенем устойчив к действию большинства b-лактамаз, эффективен относительно большинства штаммов микроорганизмов, вызывающих инфекционно-воспалительные заболевания в урологии. По результатам субанализа исследования OASIS II, эртапенем обладает минимальным риском развития резистентности, и внесение эртапенема в госпитальный формуляр ведет к росту чувствительности грамотрицательных бактерий к имипенему и другим антибиотикам-карбапенемам.
В урологической практике проводят профилактику развития как симптоматической урологической инфекции (острый пиелонефрит, простатит, эпидидимит, уросепсис), так и тяжелой раневой инфекции.
Риск инфицирования во время операции зависит от состояния пациента, вида хирургического вмешательства и окружающих факторов. При антибактериальной профилактике инфекционно-воспалительных осложнений урологических вмешательств, экстракорпоральной литотрипсии, трансуретральных операций, открытых операций и т.д. необходимо придерживаться двух принципов профилактики:
- первичная профилактика: предотвращение продвижения инфекции из источника вне мочевых путей (инструмент, катетер, ирригационная жидкость, кожа, слизистые, периуретральная флора);
- вторичная профилактика: снижение риска инфицирования в пределах мочевых путей (очаги инфекции в предстательной железе, почке, «биопленки» на камнях, катетерах).
Применение антибиотиков после операции не эффективно, они должны присутствовать в тканях во время вероятной контаминации, так как к концу операции микроорганизмы оказываются включенными в сгустки фибрина. Антибиотики плохо проникают в сгустки фибрина, и поэтому они должны присутствовать в тканях до момента формирования сгустков фибрина.
Назначение курсов системных антибиотиков после «чистых» и «условно чистых» операций только для прикрытия, защиты при отсутствии клинических симптомов и признаков инфекции не предотвращает развития инфекции, но способствует резистентности и нарушает принципы рациональной антимикробной терапии.
Антибактериальная профилактика перед смотровой цистоскопией или перед биопсией мочевого пузыря не показана. Перед трансуретральными операциями антибактериальная профилактика обязательна, даже при отсутствии бактериурии или данных за инфекционно-воспалительный процесс в мочевых путях перед операцией. Инфицирование возможно как во время операции (из вскрывающихся инфицированных протоков предстательной железы; нестерильного ирригационного раствора; инструментария; кожи пациента), так и после операции – установка уретрального катетера приводит к восходящему инфицированию мочевых путей.
Многие антибактериальные препараты могут применяться при предоперационной профилактике: среди них цефалоспорины II поколения; фторхинолоны; защищенные b-лактамы, фосфомицина трометамол. К препаратам группы резерва относятся защищенные аминопенициллины, цефалоспорины III-IV поколения, карбапенемы (при обсеменении мультирезистентными возбудителями) и ванкомицин (по строгим показаниям).
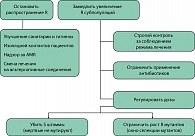
Антибактериальная профилактика является только одним из компонентов в управлении инфекцией. Необходимо строго соблюдать другие важные условия (рисунок 2), способствующие профилактике госпитальной инфекции вообще: короткий срок пребывания в больнице; короткий предоперационный период; тщательный уход за катетерами и дренажами. Важно использование «закрытой дренажной системы», строгое соблюдение санитарно-гигиенических требований – мытье рук или использование стерильных перчаток при контактировании с дренажной системой. При отсутствии факторов риска и наличии стерильной мочи необходимости в антибактериальной профилактике нет, однако при повышении ожидаемого риска (перфорация кишки во время операции, вскрытие абсцесса, карбункула почки) показано интраоперационное применение антибиотиков.
Не рекомендуют применять один и тот же антибиотик для лечения и профилактики, необходимо использовать антибиотики, создающие высокую концентрацию в моче, периодически менять препараты для антибактериальной профилактики в клинике для уменьшения селекции резистентных штаммов микроорганизмов.
