Расстройства сна и тревога
- Аннотация
- Статья
- Ссылки
- English
Определение тревоги и тревожности
Тревога – отрицательное эмоциональное состояние, неловкость, нервозность, беспокойство по поводу события с неопределенным исходом. Эти психологические симптомы часто сопровождаются физиологическими проявлениями в виде потливости, возбуждения, дрожания, головокружения, учащения сердцебиения. В отличие от эмоции страха, связанного с непосредственно воздействующей, явной и определенной угрозой целостности и существованию, тревога вызывается неопределенной, диффузной, безобъектной угрозой, направленной на социальные и личностные ценности человека, межличностные отношения, положение человека в обществе [1].
Стресс, тревога и страх отражают схожие в психологическом и физиологическом отношении состояния организма, при которых функции внимания и памяти активируются для того, чтобы обработать информацию, послужившую причиной данного эмоционального состояния, и сформировать ответную поведенческую реакцию.
Состояние тревоги может быть нормальным и повышать адаптацию, если оно возникает в редких ситуациях и продолжается недолго. Но в случаях, когда это состояние возникает часто, сохраняется на длительный срок и начинает мешать ежедневной активности (работе, учебе, взаимоотношениям), оно становится патологическим.
Если эмоция тревоги характеризует состояние субъекта в определенный момент, то тревожность как относительно устойчивая психологическая особенность может сопровождать человека всю жизнь. У таких людей состояние тревоги возникает чаще, протекает интенсивнее и имеет более низкий порог возникновения. Существуют генетические предпосылки повышенной тревожности [2], хотя ведущую роль в развитии этой личностной особенности играет влияние семьи и окружения. Отсутствие поддержки ребенка (в семье, школе, среди сверстников) формирует во взрослом возрасте тревожность, связанную со сдачей экзаменов, межличностным общением и т.д. Повышенная тревожность создает предпосылки к эмоциональным расстройствам и нарушениям адаптационных возможностей [3].
Физиология и анатомия тревоги
Согласно нейровизуализационным исследованиям, ключевым центром регуляции эмоций и эмоциональной реактивности является миндалевидное тело (амигдала). Структура амигдалы и ее функциональная активность изменяются у пациентов с тревожными расстройствами [4], а также варьируются в зависимости от личностных характеристик, затрагивающих контроль эмоций [5]. В частности, при болевом раздражении амигдала сильнее снабжается кислородом (BOLD-сигнал) у людей, которые успешнее применяют методики контроля негативных эмоций [6]. Помимо амигдалы в формировании и регуляции эмоций задействованы префронтальная кора (ПФК), кора передней поясной извилины, стриатум и гиппокамп.
Формирование эмоциональной реакции распространяется как бы снизу вверх: от вентральных нервных структур к корковым. Когнитивная переработка информации о потенциальной угрозе может привести к ингибированию эмоционального ответа в случае, если он окажется не соответствующим ситуации.
Нейрональный путь формирования чувства тревоги активируется в латеральных и латеробазальных ядрах амигдалы, в которые поступает информация о возможной опасности от органов чувств и из центров памяти. Нейроны этих ядер активируют центральное ядро амигдалы и опорное ядро краевой полосы. Они в свою очередь связаны с множеством структур гипоталамуса, центрального серого вещества и ядрами ствола головного мозга – центрами, которые обусловливают развитие реакций, направленных на противостояние предполагаемой угрозе.
Ингибирующая реакция, напротив, распространяется сверху вниз: от ПФК и гиппокампа [7, 8]. Различают произвольную и непроизвольную регуляцию эмоционального состояния. Произвольная подразумевает подавление эмоции, отвлечение внимания от информации, вызывающей тревогу, логическую переоценку информации о возможной угрозе и адекватности переживаемой эмоции. Эти механизмы осуществляются посредством дорсомедиальной и вентролатеральной областей ПФК и дорсальной корой передней поясной извилины. При высокой продуктивности мышления, восприятия, памяти люди используют телесно-ориентированные (еда, двигательная активность, занятия йогой) и интеллектуализированные (логический анализ ситуации, самоанализ) способы произвольной регуляции тревоги. При низкой – применяют речевые (вербальная агрессия, общение) и рефлексивные (внутренний диалог, самоубеждение) методы. В целом, чаще люди отдают предпочтение избегающим и пассивным способам саморегуляции в ситуации тревоги, что может привести к ее соматизации [9]. Непроизвольная регуляция эмоции тревоги включает угасание предшествующих эмоциональных реакций, ингибирование реакции автономной нервной системы и физиологической гиперактивации (через взаимодействие амигдалы и вентромедиальной ПФК [10]), автоматическое смещение внимания, автоматическую когнитивную оценку и переоценку (за счет активации ростральных отделов передней поясной извилины [11]).
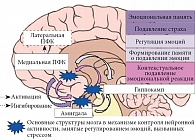
Роль гиппокампа заключается в обеспечении функции памяти, а также в непроизвольном контекстуальном подавлении эмоциональной реакции. В отличие от амигдалы, которая обрабатывает информацию о любой угрозе, дорсальный отдел гиппокампа хранит и воспроизводит информацию о ситуации, в которой возникает эта угроза. Это позволяет дифференцировать угрожающие ситуации от ситуаций с низким или средним уровнем риска. Ингибирующее действие гиппокампа на амигдалу опосредуется вентромедиальной ПФК, а в случае возобновления подавленного эмоционального ответа – дорсомедиальной ПФК (рисунок [12]) [13].
Амигдала имеет отрицательные связи с центрами области перегородки, прилежащими ядрами и вентральной областью покрышки, ответственными за положительное подкрепление. Таким образом, чувство страха вызывает снижение чувства удовольствия и наоборот. Вентральная область покрышки в свою очередь проецирует дофаминергические нейроны в другие отделы головного мозга, в том числе ПФК.
Согласно результатам магнитно-резонансных исследований функциональных связей в состоянии покоя, в норме активность амигдалы положительно коррелирует с активностью гиппокампа, островковой доли, таламуса, стриатума и медиальной лобной извилины [14] и отрицательно – с активностью верхней лобной извилины, средней лобной извилины, задней угловой, теменной и затылочной областями, которые вовлечены в процессы когнитивной переработки эмоций и ингибируют активность амигдалы.
Тревожно-аффективные расстройства (паническое расстройство, социальная тревожность, фобии, генерализованное тревожное расстройство (ГТР), посттравматическое стрессовое расстройство) связаны с ухудшением регуляции эмоционального ответа в ситуации постоянно существующей угрозы. Патогенез этих состояний обусловлен гиперактивацией или снижением порога активации амигдалы и других структур вентральной нервной системы, что проявляется повышением чувствительности к любой негативной информации. В их развитии играет роль нарушение ингибирующих влияний корковых отделов в результате снижения активности медиальной ПФК, а также нарушение связи между медиальной ПФК и амигдалой. При ГТР, паническом расстройстве, посттравматическом стрессовом расстройстве, социальной фобии особое значение приобретают ухудшение дифференцирования угрожающих и безопасных ситуаций и возобновление эмоциональной реакции после ее переоценки.
На уровне организма в целом стрессовая реакция, ассоциированная с эмоцией тревоги, активирует гипоталамо-гипофизарно-надпочечниковую систему, в результате начинают вырабатываться катехоламины, глюкокортикостероиды, готовящие организм к ответу на опасность. Острый стресс вызывает опосредуемое амигдалой высвобождение дофамина в ПФК, повышение уровня норадреналина в ПФК за счет активации амигдалой нейронов голубоватого пятна [15, 16]. Повышение уровня катехоламинов также связано с блокировкой их глиальных транспортеров глюкокортикостероидов. Чувствительные к глюкокортикостероидам клетки гиппокампа и ингибирующее действие медиальной ПФК обеспечивают обратную отрицательную связь с гипоталамо-гипофизарно-надпочечниковой системой, прекращая реакцию стресса.
Из-за того что центральную роль в механизмах стресса играет активация гипоталамо-гипофизарно-надпочечниковой системы, длительное воздействие тревоги ассоциируется с сердечно-сосудистыми заболеваниями и различными обменными нарушениями. Постоянное повышение уровня глюкокортикостероидов в крови приводит к снижению дифференциации нейронов в гиппокампе и уменьшению его объема [17]. Это в свою очередь ухудшает регуляцию гипоталамо-гипофизарно-надпочечниковой системы и способствует формированию «порочного круга», в результате происходит дальнейшее повреждение клеток. Кроме того, хронический стресс ведет к снижению выделения нейротрофического фактора мозга, необходимого для процесса дифференциации нейронов и участвующего в реализации эффектов нейромедиатора серотонина [18].
Под действием хронического стресса в клетках ПФК также возникают структурные нарушения: уменьшается количество дендритных шипиков пирамидных клеток, участвующих в формировании кратковременной памяти [19]. В других работах отмечается, что снижение количества нейронов ПФК сопровождается повышенным ростом дендритов амигдалы и еще большим усилением восходящих процессов эмоциональной реакции. Воздействие хронического стресса на нейроны гиппокампа и ПФК обусловливает снижение их регуляторных влияний на индуцированную амигдалой эмоциональную реакцию [20].
Предрасположенность к нарушениям нейрональных связей амигдалы может закладываться с детства. Разлука ребенка с матерью способствует ухудшению связей с орбитофронтальной корой, островком, гиппокампом, скорлупой, постцентральной извилиной, передней поясной извилиной [21]. Изучены гены, ассоциированные с меньшей устойчивостью связей амигдалы под влиянием внешних стрессов [22, 23]. Кроме того, выделены гены, влияющие на работу гипоталамо-гипофизарно-надпочечниковой оси и связанные с развитием тревожно-депрессивных расстройств.
Существуют гипотезы о связи между нарушением дифференциации нейронов в гиппокампе и тревожно-аффективными расстройствами, а также о реализации эффекта антидепрессантов через восстановление нейрогенеза. Подтверждена ассоциация хронического стресса с депрессией, шизофренией. У женщин среднего возраста значительный психосоциальный стресс ассоциирован с развитием болезни Альцгеймера в течение 20 лет [24], хотя механизмы развития стойкого когнитивного дефицита при хронической тревоге не изучены.
Одна из реакций на эмоцию тревоги – стартл-рефлекс (кратковременная стереотипная генерализованная двигательная реакция – вздрагивание). Эта реакция наблюдается у всех млекопитающих и имеет защитное значение. Существует обратная связь между выраженностью тревожных проявлений по шкале Бека и выраженностью стартл-рефлекса. Кроме того, притупление выраженности стартл-рефлекса коррелирует с более частыми стрессовыми событиями, длительным воздействием стрессогенного фактора, множественными психологическими и физическими травмами, часто начинающимися с раннего детства, хроническим течением заболевания и коморбидностью с депрессивными и другими тревожными расстройствами [25]. Таким образом, тяжесть и длительность течения заболевания, по-видимому, истощают нейрональные пути, ответственные не только за вегетативные реакции, но и за моторный ответ, имеющий защитное значение.
В экспериментах на животных моделях показано, что психоактивные средства, применяемые для коррекции тревожно-аффективных расстройств, снижают когнитивный дефицит [26], увеличивают дифференциацию нейронов гиппокампа [27], восстанавливают связи амигдалы с перечисленными областями [28]. В клинических исследованиях с участием пациентов с тревожно-депрессивными расстройствами установлено, что физические упражнения и антидепрессанты укрепляют функциональные связи, ответственные за внимание [29], а когнитивно-поведенческая терапия снижает гиперактивацию амигдалы [30].
Нарушения сна при генерализованном тревожном расстройстве
Расстройства сна часто сопутствуют ГТР. О нарушениях сна сообщали 64% пациентов с ГТР, при этом, по данным анамнеза, у 44–73% расстройства сна развились после дебюта ГТР, а до – только у 16–18%. Тревожное расстройство – независимый фактор риска развития инсомнии как у взрослых (отношение шансов 1,39–4,24), так и у детей (2,3–5,5) [31].
Инсомния входит в критерии диагностики ГТР согласно критериям DSM-V [3] «Тревога и волнение, обусловленные тремя из последующих шести симптомов, преобладающими на протяжении шести месяцев»:
- беспокойство или ощущение взвинченности и нахождения «на грани»;
- быстрая утомляемость;
- затрудненная концентрация или ощущение «отключки»;
- раздражительность;
- мышечное напряжение;
- нарушение сна (трудности засыпания или поддержания сна или беспокойный, невосстанавливающий сон).
Для разграничения инсомнии как проявления тревожного расстройства и как самостоятельного состояния, сопровождающегося тревогой, предлагается использовать следующие критерии. Тревога при ГТР не связана с состоянием сна, она «равномерно» распределена по времени суток, усиливается из-за определенных событий. При инсомнии тревога нарастает в вечернее время, ассоциируется с антиципацией (предчувствием) плохого сна или предполагаемыми проблемами в бодрствовании, следующими за плохим сном (дисфункциональные убеждения в отношении сна).
Структура сна больных ГТР не имеет специфических особенностей. В исследованиях выявляются частые пробуждения, увеличение времени засыпания и бодрствования в период сна, уменьшение представленности глубокого (дельта) сна. Это так называемые активационные изменения, обусловленные высоким уровнем церебральной активации, наблюдаемой и при тревоге, и собственно при инсомнии. В отличие от ГТР при депрессивном расстройстве в структуре полисомнограммы отмечается еще и уменьшение представленности фазы быстрого сна.
При ГТР для устранения тревоги назначают бензодиазепиновые анксиолитики: диазепам, лоразепам, алпразолам (уровень доказательности А) [32]. Самый распространенный в России анксиолитик с показанием к применению при различных формах тревожных расстройств – Феназепам. Бензодиазепиновые производные имеют преимущество при ГТР, сопровождающемся инсомнией, поскольку позволяют скорректировать сразу оба расстройства.
Высоким уровнем эффективности (уровень доказательности А) при ГТР обладают и препараты других групп:
- имипрамин (трициклические антидепрессанты);
- эсциталопрам, пароксетин, сертралин (ингибиторы обратного захвата серотонина);
- венлафаксин и дулоксетин (ингибиторы обратного захвата серотонина и норадреналина);
- антипсихотики (кветиапин);
- противосудорожные препараты (прегабалин).
Следует отметить, что при нарушениях сна лечение антидепрессантами должно сопровождаться приемом препаратов со снотворным действием, поскольку клинический эффект в отношении сна при приеме антидепрессантов без седативного действия развивается не сразу, а в течение двух недель. В начале антидепрессивной терапии пациент может испытывать тревогу, чтобы преодолеть усиление тревожных проявлений в первые две-три недели, можно назначить бензодиазепиновый анксиолитик, в частности Феназепам, в качестве «бензодиазепинового моста».
Депривация сна и тревога
Высокий уровень тревоги наряду с ухудшением внимания и повышением раздражительности составляют триаду нейроповеденческих последствий депривации сна, описанных W. Dement [33]. Установлена положительная корреляция между длительностью депривации и выраженностью тревоги. Метаанализ исследований последствий депривации сна продемонстрировал, что повышенный уровень тревожности (по опроснику ситуативной и личностной тревожности Спилбергера) регистрировался после полной депривации сна, но не после ограничения сна [34]. Среди других эффектов депривации сна – снижение порога чувствительности к стрессу и более выраженные стрессовые реакции, нарушение переработки информации, связанной с эмоциями (ухудшение распознавания положительных эмоций).
Нейровизуализационные исследования при депривации сна продемонстрировали снижение нейрональной активности в зоне, отвечающей за внимание (ПФК и внутритеменной борозде) и концентрацию внимания на наиболее значимом стимуле, необходимом для формирования адекватного поведенческого ответа (в островковой и медиальной фронтальной коре). Вместе с тем отмечалось усиление активности в таламусе, в котором происходит недифференцированная переработка информации, поступающей через все органы чувств [34].
Тесная взаимосвязь тревоги и депривации сна имеет серьезные последствия. Во-первых, в условиях динамичного современного мира увеличивается число случаев частичной депривации сна и диагнозов тревожных расстройств. Во-вторых, оба эти явления независимо друг от друга ассоциируются с множеством расстройств деятельности сердечно-сосудистой и эндокринной систем. Проблема связи депривации сна с тревогой важна с точки зрения профессиональной медицины. Известно, что недостаточный сон и тревога независимо друг от друга негативно влияют на способность принимать решения и другие профессиональные компетенции [35]. По результатам теста психомоторной бдительности, после депривации сна пациенты затрачивали больше времени для принятия решения и делали больше ошибок. Отсутствие ночного сна значительно повышает риск ошибок в ходе работы, что особенно опасно для людей таких профессий, как водитель, пилот, врач.
Тревога при расстройствах сна
Инсомния тесно связана с тревожными расстройствами. С одной стороны, риск развития инсомнии при тревожном расстройстве составляет 1,39–4,24. С другой стороны, инсомния увеличивает риск возникновения тревожного расстройства в 1,43–3,64 раза. Около 20% пациентов с инсомнией отмечают симптомы тревожного или депрессивного расстройства [36]. Таким образом, инсомния может возникать до тревожного расстройства и способствовать его развитию одновременно с симптомами тревоги или дебютировать уже в развернутой картине тревожного расстройства. Нарушения сна и тревожные расстройства могут долго протекать субклинически, поэтому определить, какое из состояний первично, практически невозможно. К развитию инсомнических нарушений предрасполагают такие личностные характеристики, как нейротизм, интернализация, перфекционизм, интровертированность [37]. Есть в этой взаимосвязи и положительный аспект: лечение одного из коморбидных расстройств оказывает благоприятный эффект на другое [38].
Патогенетические механизмы развития тревоги и инсомнии во многом схожи. Воздействие стресса, активируя амигдалу, помимо эмоциональной реакции запускает процесс гиперактивации, затрагивающий в том числе взаимодействие центров регуляции сна и бодрствования. При длительном течении инсомнии (больше трех месяцев) появляются функциональные и/или структурные изменения в структурах головного мозга:
- снижение орбитофронтального объема [39];
- гипометаболизм во время бодрствования в префронтальной коре с двух сторон;
- гипометаболизм в коре верхней височной извилины теменной и затылочной долей слева;
- гипометаболизм в таламусе, гипоталамусе и ретикулярной формации;
- гиперметаболизм в состоянии сна в ретикулярной формации, гипоталамусе, таламусе, амигдале, гиппокампе, медиальной префронтальной коре, коре островка и передней поясной извилины [40, 41].
Важно отметить, что эти изменения сохраняются в течение всего дня. Это приводит к объективному ухудшению кратковременной, эпизодической памяти и проблемам при решении задач у пациентов с хронической инсомнией по сравнению со здоровыми людьми [35]. Нарушение дневного функционирования при хронической инсомнии, по-видимому, вызвано дисфункцией мозговых структур, которые вовлечены в контроль эмоциональных реакций, когнитивных функций и гиперактивации (гиппокамп, ПФК) [42, 43]. Исследования показали, что выраженность симптомов когнитивного дефицита не зависит от того, сколько пациенты с хронической инсомнией спали накануне, в отличие от группы контроля, в которой ухудшение выполнения заданий на память и внимание оказалось связано с качеством сна в предыдущие ночи и дневной сонливостью в день исследования [35]. Следовательно, характер ухудшения памяти и внимания при инсомнии отличается от такового при депривации сна [44].
Тревога и беспокойство по поводу собственного сна влияют на поведение больного и приводят к формированию «порочного круга» самовозбуждения. Внимание больного концентрируется на всем, что несет потенциальную угрозу сну (собственных мыслях, настроении, окружающей обстановке), а также на последствиях бессонной ночи (усталости, сонливости, снижении работоспособности). Гиперболизация возможной угрозы ночному сну и последствий бессонной ночи приводит к самоограничительному поведению и дальнейшей фиксации внимания на инсомнии [9].
Инсомния – независимый фактор риска развития сердечно-сосудистых заболеваний и метаболических нарушений. С одной стороны, тесная связь инсомнии и тревоги обусловливает активацию гипоталамо-гипофизарно-надпочечниковой системы. С другой, уменьшение продолжительности сна, особенно медленноволнового при инсомнии, снижает ингибирующее влияние на стресс-реактивную систему.
Метод выбора лечения хронической инсомнии – когнитивно-поведенческая терапия. Ее основная цель – устранение дисфункциональных убеждений в отношении сна, поддерживающих нежелательную ночную гиперактивацию нервной системы. Кроме того, в рамках этой методики пациент обучается правильному поведению, минимизирующему риски нарушения сна (соблюдение правил гигиены сна) и увеличивающему давление сна в нужное для этого время. На фоне когнитивно-поведенческой терапии не только улучшаются показатели самого сна и уменьшается выраженность инсомнии, но и снижается выраженность тревожных и депрессивных проявлений. Так, по данным A. Harvey и соавт. (2007), у пациентов с хронической инсомнией на фоне когнитивно-поведенческой терапии достоверно снижались показатели по шкале депрессии Бека (-75%) и шкале тревоги Бека (-44%) [45].
Однако метаанализ исследований, посвященных изучению влияния когнитивно-поведенческой терапии на тревожность, демонстрирует низкий и умеренно выраженный эффект лечения [46]. Эти данные соответствуют и результатам нашего собственного исследования эффективности нелекарственных методов терапии, проведенного в отделении медицины сна Университетской клинической больницы № 3. 42 пациента с хронической инсомнией прошли двухнедельный курс лечения с применением структурированной методики, объединяющей информационно-образовательные, релаксационные методы и методы поведенческой коррекции (аналог когнитивно-поведенческой терапии). Несмотря на достоверное снижение индекса тяжести инсомнии на 27% (р = 0,0001) и уменьшение депрессивных проявлений по шкале депрессии Бека на 30% (р = 0,04), статистически значимых изменений на фоне лечения по шкале тревоги Спилбергера обнаружено не было: ситуативная тревожность снизилась на 2,9% (р = 0,58), личностная – на 0,8% (р = 0,82).
Вместе с тем высокая коморбидность инсомнии и тревожных расстройств позволяет подходить к лечению инсомнии «с другой стороны» путем уменьшения выраженности тревоги. Для этого назначают типичные и атипичные анксиолитики, антипсихотики, антидепрессанты и некоторые противоэпилептические препараты. При острой (длящейся не более трех месяцев) инсомнии эффективны селективные и неселективные агонисты ГАМКА хлорионного рецепторного комплекса. Селективные агонисты (так называемые Z-препараты: зопиклон, золпидем, залеплон), связывающиеся с альфа-субъединицей рецептора, характеризуются только снотворным эффектом. Неселективные агонисты, действующие на все подтипы ГАМКА-рецептора (содержащие субъединицы альфа 1, 2, 3, 5, 6-го типов), при острой инсомнии оказывают, наряду со снотворным, целый ряд дополнительных эффектов. При тревожных расстройствах, коморбидных инсомнии, важно, чтобы препараты обладали анксиолитическим действием. Оно реализуется за счет связывания препаратов с альфа-2- и альфа-3-субъединицами ГАМКА-рецепторов, расположенных в структурах мозга, отвечающих за обеспечение ответных реакций и генерацию эмоций (амигдала, кора полушарий, гиппокамп, полосатое тело). Применение бензодиазепиновых транквилизаторов, например Феназепама, в терапевтических дозах способствует снижению уровня тревоги на 82% [47]. Согласно данным этого же исследования, при инсомнии, коморбидной тревожному расстройству, лечение Феназепамом в течение 14 суток улучшает показатели сна на 87%. В исследовании с участием больных ишемической болезнью сердца и неврозоподобными расстройствами, получавших несколько бензодиазепиновых транквилизаторов, было показано, что по анксиолитическому эффекту (70%) Феназепам превосходил диазепам (62%) и хлордиазепоксид (49%) [48].
Клинические исследования выявили положительную корреляцию апноэ сна и тревоги: повышенная тревожность отмечается у 12–17% страдающих синдромом обструктивного апноэ сна (СОАС) [49]. Среди возможных причин повышенной тревожности при СОАС называют недостаточность медленноволнового сна, повышение уровня кортизола в крови, повреждающее гиппокамп, однако не исключается и влияние других аспектов СОАС. В частности, установлены такие предикторы повышенной тревожности, как жалобы на невосстанавливающий сон и частые ночные пробуждения [50]. Многочисленные дневные проявления СОАС (дневная сонливость, головные боли, ухудшение памяти и внимания) ухудшают качество жизни, влияя на профессиональные навыки, социальные связи, личную жизнь. Это создает предпосылки для развития тревожно-аффективных нарушений «вторичного» характера.
При проведении нейровизуализационных исследований пациентов с СОАС обнаруживается множество микроочагов ишемии в белом веществе головного мозга, обусловленных поражением сердечно-сосудистой системы [51]. Кроме того, снижается объем серого вещества лобной и теменной долей, передней поясной извилины, базальных ганглиев и гиппокампа [52]. Следует отметить, что базальные ганглии, в которых были выявлены структурные изменения, чувствительны к гипоксии. Это может служить объяснением нарушений аффективного контроля вследствие первичного ишемического поражения этих образований. По данным функциональной магнитно-резонансной томографии, у тревожных пациентов с СОАС, в отличие от пациентов с низким уровнем тревоги, наблюдается более выраженное поражение вентромедиальной ПФК, островковой коры и крючка гиппокампа [53].
На фоне СиПАП-терапии выраженность проявлений тревоги снижается через три месяца после начала лечения [54], что может объясняться упоминавшимся вторичным характером тревожных расстройств при СОАС. С одной стороны, улучшение качества сна способствует репарации повреждений базальных ганглиев, гиппокампа и ПФК, вызванных гипоксией и повышением уровня кортизола. С другой стороны, нормализация сна устраняет другие дневные симптомы СОАС, которые также вызывают тревогу.
Патогенез нарушений движений во сне остается неясным, поэтому повышенная тревожность при таких состояниях, как синдром беспокойных ног (СБН) и синдром периодических движений конечностей во сне (СПДК), считается вторичным симптомом, развивающимся как реакция на нарушение ночного сна. Анамнестические данные свидетельствуют о том, что СБН возникает раньше тревожных расстройств.
Эпидемиологические исследования выявили повышенный риск развития тревожных расстройств у пациентов с СБН (у 23,2% больных). Среди тревожных расстройств, коморбидных СБН, лидирует паническое тревожное расстройство (у 16,7% больных) [55]. Риск развития тревожно-депрессивных расстройств коррелирует с выраженностью СБН и наиболее высок у испытуемых, отмечавших проявления СБН ежедневно.
Синдром беспокойных ног и синдром периодических движений конечностей во сне отличаются высокой коморбидностью. Лишь 20% пациентов с СБН не имеют СПДК, причем у этой группы пациентов выше риск развития депрессивных и тревожных расстройств, а при полисомнографическом исследовании обнаруживается более высокий индекс спонтанных пробуждений [56]. Полисомнографическое исследование при СПДК продемонстрировало ожидаемое увеличение количества пробуждений, изменение стадий сна и представленности первой стадии сна. При этом картирование дневной электроэнцефалограммы показало повышение индекса альфа-1-активности, что совпадает с показателями электроэнцефалограммы при тревожном расстройстве. Патогенез этих изменений остается невыясненным.
Таким образом, результаты эпидемиологических исследований позволяют говорить о коморбидности тревожных расстройств и нарушений сна. Однако если в случае инсомнии роль повышенной тревожности хорошо изучена, механизм коморбидности с другими нарушениями сна требует дальнейших исследований.
M.G. Poluektov, P.V. Pchelina
I.M. Sechenov First Moscow State Medical University (Sechenovskiy University)
Contact person: Mikhail Guryevich Poluektov, polouekt@mail.ru
Anxiety is the emotion normally arising in response to a situation threatening well-being of a person. Amygdala triggers anxiety reaction by activating specific neural circuits and hypothalamic-pituitary-adrenal axis. Control of emotional response is conducted by prefrontal cortex and hippocampus. Prolonged or frequent emotion in anxiety disorders causes functional deficit in emotional regulation, impaired hippocampal neurogenesis and structural degeneration of the prefrontal cortex. Sleep disorders are similar to any illness associated to higher anxiety. But the close connectivity of centers regulating sleep and emotions determines higher comorbidity of sleep and anxiety disorders. It is known that anxiety plays part of the development of chronic insomnia. Correlations between anxiety and sleep-related movement disorders or sleep-related breathing disorders currently are under discussion.