Растительные препараты в климактерии: многообразие и разумный выбор
- Аннотация
- Статья
- Ссылки
Климактерий – период биологически запрограммированного угасания и прекращения функции яичников. Гормональные изменения, свойственные климактерию, часто сопровождаются комплексом симптомов, наиболее типичные из которых – приливы жара, повышенная потливость, нарушения сна, артериальная гипертензия, эмоциональная лабильность и др. Появление этих симптомов ведет к значительному снижению качества жизни женщины.
Для лечения патологического климакса чаще всего применяется гормональная терапия, однако назначение гормонов не всегда возможно из-за противопоказаний или категорического отказа женщин использовать эти лекарственные средства. В этих случаях выбираются препараты растительного происхождения и биологически активные добавки (БАД), оказывающие положительный терапевтический эффект и не имеющие свойственных гормональной терапии рисков [1, 2].
Женщины всего мира на протяжении столетий используют растительные экстракты для решения проблем, связанных с женским здоровьем, в том числе ассоциированных с менструальным циклом, а также для обеспечения нормального течения беременности и рождения здорового ребенка, облегчения симптомов климакса. Число случаев использования БАД женщинами в постменопаузе особенно повысилось в последнее десятилетие [3]. Так, в США и Великобритании биодобавки в постменопаузе принимают около 80% женщин, при этом 60–70% полностью удовлетворены их эффектом.
Основным действующим веществом различных фитопрепаратов и БАД, применяемых женщинами в климактерическом периоде, являются фитоэстрогены, по структуре очень близкие к эндогенным эстрогенам и представляющие собой нестероидные вещества класса полифенольных соединений. Фитоэстрогены могут вводиться в состав обогащенных продуктов (хлеб, соевое молоко) или применяться в виде таблеток. Доказательства эффективности фитоэстрогенов проистекают из двух источников: клинические наблюдения и клинические испытания. Эпидемиологические данные свидетельствуют о значительной разнице в частоте приливов жара в популяциях с высоким и низким потреблением фитоэстрогенов. Так, приливы жара отмечают только 5–10% женщин Японии, потребляющие 20–150 мг/сут фитоэстрогенов, по сравнению с 70–80% женщин Европы, где содержание фитоэстрогенов в суточном рационе не превышает 5 мг. В Японии также реже наблюдаются сердечно-сосудистые заболевания и остеопороз.
Плацебоконтролируемые клинические исследования дают противоречивые результаты [4, 5]. В большинстве из них сообщается об облегчении «приливов» после добавления в пищу фитоэстрогенов, но статистическая разница по сравнению с плацебо достигается редко. По некоторым данным, фитоэстрогены в виде БАД способны снизить выраженность и количество проявлений климактерического синдрома, в том числе приливов жара, нарушений сна, головных болей, ночной потливости [6]. Отмечена также сильная негативная корреляция уровня экскреции изофлавонов с мочой и частотой приливов жара. В ряде работ обнаружены положительные изменения цитологии влагалища. В то же время метаанализ исследований эффективности изофлавонов красного клевера не выявил достоверного снижения частоты приливов жара на фоне лечения. Аналогичный анализ эффективности изофлавонов сои дал противоречивые результаты.
Обсуждается возможность использования растительных экстрактов с эстрогеноподобным действием в качестве средства первичной и вторичной профилактики сердечно-сосудистых заболеваний. Это основано на данных о положительном влиянии фитоэстрогенов на уровень липопротеидов, функцию эндотелия и артериальное давление [7]. В США Администрация по контролю за пищевыми продуктами и медикаментами (FDA) одобрила использование пищевых продуктов и пищевых субстанций с высоким содержанием соевого белка для снижения риска сердечно-сосудистых заболеваний.
В настоящее время международные эксперты полагают, что у женщин, употребляющих «фитоэстрогены в больших количествах, особенно в составе соевых продуктов, снижается частота заболеваний сердечно-сосудистой системы, раком молочной железы и матки, а также уменьшается выраженность климактерических симптомов по сравнению с женщинами, находящимися на стандартной диете» [8]. При нерезко выраженных жалобах и у здоровых женщин в постменопаузе с профилактической целью использование этих препаратов приветствуется европейскими гинекологами [9].
К фитоэстрогенам относятся следующие классы химических соединений: флавоны, изофлавоны, куместаны, лигнаны, флавоноиды, наиболее важными считаются изофлавоны и лигнаны [10]. Изофлавоны в большом количестве содержатся в соевых бобах, горохе, других бобовых культурах, клевере; лигнаны (энтеролактон, энтеродиол) обнаруживаются в масличных семенах (например, семенах льна), отрубях, цельных зернах, овощах, бобовых и фруктах; куместаны (куместрол) – в брюссельской капусте.
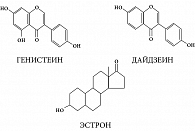
Действующими веществами наиболее изученных к настоящему времени изофлавонов являются генистеин, дайдзеин и глицитеин, структурно сходные с эстроном (рис. 1).
Изофлавоны быстро абсорбируются и метаболизируются в кишечнике, хорошо переносятся, при их употреблении не наблюдаются нежелательные явления [11]. В некоторых тканях изофлавоны вызывают проэстрогенный ответ, в других подавляют эстрогенные эффекты, что объясняется различным сродством к двум подтипам рецепторов эстрогенов (РЭ). Если аффинность эстрадиола к РЭ принять за 100%, то аффинность генистеина к РЭ-альфа составит 5%, к РЭ-бета – 36%, то есть в отношении РЭ-бета гинестеин проявляет активность, сравнимую с активностью эстрона. Исходя из этого, становится понятным, почему фитоэстрогены безопасны с точки зрения избыточной пролиферации и не требуют прогестагенного прикрытия: низкое сродство к РЭ-альфа не позволяет фитоэстрогенам осуществить ростовые функции.
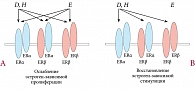
Кроме того, фитоэстрогены стимулируют в печени продукцию глобулина, связывающего половые стероиды, что приводит к снижению биологической доступности не только эстрогенов, но и андрогенов, относительный избыток которых в постменопаузе неблагоприятен ввиду кардиометаболического риска. Наконец, связываясь с РЭ, фитоэстрогены блокируют взаимодействие с рецептором эндогенного эстрадиола, поэтому, будучи намного слабее эстрадиола, фитоэстрогены оказывают антиэстрогенное или эстрогенное действие в условиях, соответственно, высокой или низкой эстрогенной насыщенности (рис. 2), в связи с чем их относят к природным селективным модуляторам РЭ.
Из-за такого селективного эстрогенного/антиэстрогенного действия в зависимости от условий эстрогенной насыщенности изофлавоны не только не оказывают пролиферативного действия, но также обладают протективным эффектом в отношении эстроген-зависимой, в том числе злокачественной, клеточной пролиферации. Ингибирующее влияние фитоэстрогенов на ангиогенез также является основанием предполагать, что они обладают противоопухолевой активностью.
Механизм действия фитоэстрогенов на вазомоторную симптоматику климактерического синдрома до конца не ясен, наиболее вероятным объяснением является их воздействие на РЭ гипоталамуса и, возможно, других структур головного мозга.
Генистеин и дайдзеин, обладая гораздо меньшей аффинностью к РЭ по сравнению с эстрадиолом, тем не менее способны оказывать биологические эффекты даже в тех количествах, которые содержат натуральные продукты. Изофлавоны соевых бобов не производят феминизирующего действия на самцов-приматов, но влияют на внутриутробное развитие самок крыс, уменьшая массу матки и яичников.
Доклинические и клинические исследования продемонстрировали улучшение липидного профиля плазмы на фоне приема изофлавонов, а также подавление процесса окисления липопротеидов низкой плотности (ЛПНП). Было также показано, что изофлавоны нормализуют реактивность сосудистой ткани у приматов с дефицитом эстрогенов. В экспериментальных исследованиях активность фитоэстрогенов в отношении РЭ-бета позволила подавить пролиферацию и миграцию гладкомышечных клеток сосудов сопоставимо с эффектом 17-бета-эстрадиола. Продемонстрировано уменьшение ригидности артериальной стенки при лечении изофлавонами женщин в постменопаузальном периоде. В экспериментальных работах на коронарных артериях генистеин и дайдзеин проявили свойства антагонистов кальция. Помимо положительного действия на климактерические симптомы и сосудистую стенку, фитоэстрогены имеют благоприятный эффект на минеральную плотность костной ткани.
Эстрогенное действие свойственно также группе макролактонов, открытых в результате исследования факта развития гиперэстрогении у свиней, которых кормили заплесневелым зерном. Действие микотоксинов заплесневелого зерна усиливал зеараленон, который с высоким сродством связывал РЭ и вызывал «утеротропный» ответ со стороны матки у крыс. В 70-х годах прошлого века зеараленон использовали для уменьшения частоты и интенсивности приливов у женщин.
Кроме перечисленных продуктов, эстрогеноподобными свойствами обладают и другие растения, например женьшень. В рандомизированном многоцентровом двойном слепом плацебоконтролируемом исследовании эффективности женьшеня была выявлена тенденция к улучшению общего самочувствия и статистически значимое улучшение по шкалам, отражающим общее состояние здоровья и наличие депрессии.
Помимо того, исследуется возможность использования в качестве фитотерапии при климактерических нарушениях алоэ вера, кава-кава и молока чертополоха. В Иране для снижения интенсивности приливов используется Glycyrrhiza glabra (корень солодки) в виде таблетированного препарата.
В Германии для лечения климактерических нейровегетативных симптомов сертифицирован клопогон кистевидный (Cimicifuga racemosa), компоненты которого также стимулируют рецепторы эстрогенов. В репродуктивном возрасте Cimicifuga racemosa пробуют назначать в циклах проведения стимуляции овуляции [12, 13]. Как средство облегчения климакса Cimicifuga racemosa используется более 100 лет. Клинические исследования демонстрирует эффективность экстракта этого растения в уменьшении частоты и силы приливов, снижении потливости, нормализации сердечного ритма, уменьшении степени тревоги и депрессии, нормализации настроения, улучшении метаболизма костной ткани. Отмечены положительные эффекты клопогона кистевидного в отношении не только вазомоторных жалоб, но и маркеров костного метаболизма [14, 15].
Популярными являются также экстракты дикого ямса, содержащего стероиды, дон ква, корня валерианы и другие [16]. Свойства их продолжают изучаться. Активный компонент дикого ямса – диосгенин является предшественником прогестерона. Несмотря на то что в организме человека нет ферментных систем, обеспечивающих конверсию диосгенина в прогестерон, прием экстракта дикого ямса имеет ряд биологических эффектов: способствует уменьшению индекса атерогенности, оказывает спазмолитическое действие, обладает вазодилатирующим эффектом.
Хотя исследования по долговременному отслеживанию вероятных побочных реакций фитотерапии проводятся редко [17, 18], токсических эффектов не наблюдалось, и фитотерапия считается относительно безопасным методом лечения. Женщины также уверены в полной безопасности длительного применения любых БАД, однако эта уверенность не имеет доказательной базы. Более того, исследования влияния фитоэстрогенов на эндометрий продемонстрировали, что пятилетнее использование изофлавонов сои приводит к достоверному увеличению частоты гиперплазии эндометрия по сравнению с плацебо [19]. Такой результат характерен для приема обогащенных пищевых продуктов, в которых сложно учесть количество вводимых в организм фитоэстрогенов. Следовательно, более безопасным вариантом является применение не обогащенных продуктов, а готовых лекарственных форм и БАД, в которых количество фитоэстрогенов строго регламентировано. Были также предприняты попытки создать синтетические изофлавоны, которые показали сходную с оригиналом эффективность. Но их использование (иприфлавон) может привести к развитию лимфопении.
Исходя из приведенных данных, можно заключить, что на сегодняшний день следует рекомендовать к использованию наиболее изученные с точки зрения положительных и негативных эффектов растительные экстракты, а именно: фитопрепараты, содержащие изофлавоны (например, изофлавоны сои), Cimicifuga racemosa, экстракт корня дикого ямса.
Очевидно, что только фитоэстрогены не способны полностью удовлетворить все направления лечения симптомов, ассоциированных с менопаузой и старением, поэтому при выборе метода негормональной коррекции возрастных проблем встает вопрос о назначении комплекса препаратов или комплексного препарата, составные части которого дополняют друг друга.
Помимо фитоэстрогенов, существует еще ряд средств, способных повлиять на течение климактерических симптомов, хотя применение многих из них основано на ничем не подтвержденных представлениях широкой публики о хорошем эффекте в отношении менопаузальных симптомов. Примером может служить использование масла вечернего первоцвета, содержащего гамма-линоленовую кислоту, исследования эффективности которой не подтвердили преимуществ по сравнению с плацебо.
Некоторые мифы о свойствах травяных препаратов используются с рекламной целью, прежде всего это относится к возможному влиянию трав на половую функцию. На самом деле действие фитопрепаратов на сексуальную сферу в период климактерия изучено слабо. Примечательно, что азиатские клиницисты не ожидают появления травяного препарата, эффективного в лечении женской сексуальной дисфункции, поскольку тысячелетний опыт восточной медицины не смог выявить такой препарат даже для восстановления более примитивной мужской сексуальности.
В то же время существуют растения с доказанным положительным эффектом в отношении симптомов, сопровождающих старение организма.
В Германии проводилось исследование эффектов экстракта зверобоя на менопаузальные симптомы и сексуальность у женщин. Были получены данные, свидетельствующие об уменьшении выраженности депрессии, что привело к субъективному повышению самооценки половой функции. Зверобой известен как препарат с антидепрессивным действием, поэтому такая характеристика его эффекта закономерна. Дополнительное положительное влияние на депрессивные симптомы должно рассматриваться при назначении фитотерапии женщинам в климактерическом периоде. Но экстракт травы зверобоя непригоден для длительного, исчисляющегося годами, применения ввиду своего множественного влияния на различные параметры гомеостаза, в частности на свертывающую систему крови. Достаточное сильное антидепрессивное действие экстрактов травы зверобоя позволяет рекомендовать его курсовое использование в течение нескольких месяцев для лечения аффективных расстройств.
Помимо зверобоя, еще целый ряд препаратов обладают антидепрессивным действием. При этом их действие более мягкое, чем у зверобоя, а значит, они могут использоваться длительное время в составе комплексных средств лечения климактерического синдрома. Например, фолиевая кислота повышает способность противостоять стрессам и депрессии, витамин В6 повышает устойчивость к стрессам. Аминокислоты D, L-фенилаланин, 5-гидрокситриптофан – мягкие антидепрессанты – увеличивают синтез эндорфинов, обладают болеутоляющими свойствами, благодаря чему нормализуют эмоциональное состояние, повышают устойчивость к стрессам [20].
Фитоэстрогены оказывают положительное влияние не только на вазомоторные и психовегетативные симптомы климакса, но и на минеральную плотность кости, однако профилактический эффект в отношении остеопоротических переломов невелик. Усилить этот эффект возможно введением дополнительных средств, улучшающих костный метаболизм, и прежде всего кальция и витамина D. Контролируемые клинические испытания установили, что у лиц пожилого возраста адекватное потребление кальция и витамина D позволяет уменьшить потерю костной ткани и снижает риск переломов позвоночника и проксимального отдела бедра.
Желательно, чтобы кальций поступал в организм в составе пищевых продуктов, но не все индивидуумы могут повысить содержание кальция таким путем. В таких случаях рекомендуется дополнительный прием кальция в виде самостоятельного препарата или в составе комплексных средств. Рекомендуемое суточное потребление кальция для женщин старше 50 лет составляет 1200 мг. В растительных препаратах, содержащих кальций, этот микроэлемент может находиться в виде разных солей, например фруктобората кальция, где бор усиливает действие фитоэстрогенов, замедляет развитие остеопороза. Вероятное дополнительное положительное действие может оказать экстракт листьев крапивы, увеличивающий синтез кальцитонина.
Одно из важных направлений сохранения женского здоровья – профилактика сердечно-сосудистых заболеваний. Диетическая коррекция: снижение общего потребления жира и насыщенных жиров, средиземноморская диета с высоким содержанием олеиновой и жирных кислот омега-3, диета с высоким содержанием фруктов, овощей, бобовых показали свою эффективность в профилактике ишемической болезни сердца. Проводятся исследования эффективности пищевых добавок в виде витаминов В6 и В12, витамина Е, фолиевой кислоты, флавоноидов в первичной и вторичной профилактике сердечно-сосудистых заболеваний у женщин.
Противоопухолевая активность некоторых травяных экстрактов обеспечивает дополнительную безопасность использования фитоэстрогенов в комплексных препаратах. Например, индол-3-карбинол (биологически активное вещество, содержащееся в овощах семейства крестоцветных) способствует нормализации метаболизма эстрогенов, блокирует пути стимуляции патологической пролиферации, тем самым оказывая противоопухолевое действие и предотвращая развитие злокачественных новообразований.
Таким образом, выбирая фитопрепарат или БАД для лечения климактерических симптомов, следует руководствоваться не только сиюминутными целями улучшения самочувствия, но и долгосрочными перспективами сохранения здоровья и проведения профилактики сердечно-сосудистых, онкологических заболеваний, а также остеопороза. В связи с этим комплексные препараты, содержащие фитоэстрогены, витамины и другие биологически активные субстанции, имеют преимущества по сравнению с монопрепаратами фитоэстрогенов.
Один из таких комплексных препаратов (БАД), Эстровэл®, разработан отечественной фармацевтической компанией «Экомир» (ТУ 9197-007-77480016-06, свидетельство гос. регистрации № 77.99.23.3.У.10113.10.09 от 29.10.2009). БАД Эстровэл® выпускается в виде таблеток, покрытых оболочкой, по 500 мг и имеет следующий состав: Cimicifuga racemosa, экстракт сои, экстракт корня дикого ямса, индол-3-карбинол, экстракт листьев крапивы, органический бор в составе фруктобората кальция, витамин Е, витамин В6, фолиевая кислота, 5-гидрокситриптофан, D, L-фенилаланин.
При наличии урогенитальных расстройств в комплексное лечение можно включать растительные препараты, тропные к мочевым путям, одним из вариантов такого воздействия является Уропрофит®. Уропрофит® апробирован в урологической клинике у больных хронической инфекцией нижних мочевых путей в перименопаузе. Значительное улучшение диуреза, наблюдаемое при приеме препарата Уропрофит®, способствует механическому удалению бактерий, что является одним из ключевых моментов лечения. Препарат способствует нормализации мочеиспускания, уменьшает риск повторных обострений хронического цистита. Повышение диуреза приводит к снижению бактериурии и тем самым – к пролонгированию безрецидивного периода. Дополнительное положительное действие при урогенитальных расстройствах оказывает витамин Е, улучшающий кровоснабжение стенок влагалища.
Не исключено также, что хорошее лечебное действие изофлавонов зависит от состава микрофлоры кишечника, которая способна превращать дайдзеин и генистеин в более активный эстроген эквол. Это предполагает дополнительный положительный эффект от применения эубиотиков, полезных, к тому же, и с позиций усиления защитных свойств слизистых оболочек.
Таким образом, планируя профилактику и коррекцию менопаузальных расстройств, следует думать о многоплановом и безопасном воздействии на организм, направленном не только на уменьшение вегетативных жалоб, но и на все составляющие процесса старения. Фитотерапия часто позволяет добиться такого многопланового воздействия при правильном подборе ее компонентов. Безусловно, ресурс травяных экстрактов в профилактике и лечении заболеваний/состояний, ассоциированных со старением, далеко не исчерпан, и дальнейшие исследования должны привести к созданию алгоритмов и схем их назначения, максимально учитывающих индивидуальные потребности пациента.
