Современный взгляд на возможности применения альфа-липоевой кислоты
- Аннотация
- Статья
- Ссылки
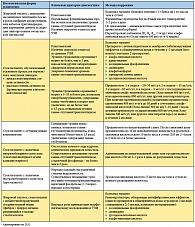
Клиническая фармакокинетика
Альфа-липоевая кислота является дисульфидным производным октановой кислоты [1]. АЛК – естественный коэнзим митохондрий мультиэнзимного комплекса, катализирующего окислительное декарбоксилирование альфа-кетокислот, таких как пируват и альфа-кетоглютарат. АЛК является мощным антиоксидантом, что определяет возможность ее терапевтического использования. Структурная формула и свойства АЛК были открыты в 1951 г., в том же году были проведены ее первые клинические испытания, применение альфа-липоевой кислоты у людей начато в 1970 г. Ранние исследования по использованию АЛК проводились на фоне недостаточного представления о механизмах ее действия и касались главным образом липидного и углеводного обмена.
Альфа-липоевая кислота является одновременно жиро- и водорастворимой, поэтому она может проникать в любые ткани организма, оказывая антиоксидантное действие не только вне, но и внутри клетки. Она также активизирует деятельность других антиоксидантов – витаминов А, С, глутатиона и коэнзима Q10. АЛК обладает уникальными свойствами, которые позволяют использовать ее для лечения и профилактики широкого спектра заболеваний, в первую очередь периферической нервной системы и мозга, поскольку нервная ткань крайне чувствительна к токсическому воздействию свободных радикалов. Традиционно АЛК используется в терапии диабетической полинейропатии. Однако токсическое действие свободных радикалов, приводящее в том числе к развитию нейропатии и одного из ее ранних проявлений – нейрогенной эректильной дисфункции, наблюдается при целом ряде других состояний, таких как сахарный диабет (СД), ожирение, старение, длительный прием лекарственных препаратов (токсическая нейропатия), метаболический синдром, метаболические заболевания печени.
Патогенетическое применение альфа-липоевой кислоты
Действие АЛК хорошо изучено у здоровых добровольцев и больных сахарным диабетом. Фармакокинетические характеристики АЛК при внутривенном введении не отличаются у здоровых людей и больных СД; выявлена линейная зависимость между концентрацией АЛК в плазме и дозой вводимого внутривенно препарата в диапазоне от 200 до 1200 мг [2]. При приеме таблеток у здоровых людей линейная зависимость концентрации АЛК в плазме от дозы препарата находилась в границах 50–600 мг. При любом способе введения через 24 ч в плазме не остается АЛК, поскольку она поступает в печень, сердце, почки, где аккумулируется, с последующей экскрецией [1].
Исследование биодоступности АЛК у здоровых людей при приеме таблеток на пустой желудок или сразу после завтрака показало, что пища значительно снижает концентрацию АЛК в плазме. В связи с этим рекомендуется прием таблеток АЛК сразу после сна за 30–45 мин до приема пищи. АЛК подвергается бета-окислительной деградации и выводится с мочой в виде метаболитов [2]. Многочисленные экспериментальные исследования продемонстрировали, что АЛК является мощнейшим антиоксидантом за счет участия в ресинтезе витамина Е, способности АЛК связывать свободные радикалы. Было высказано также предположение о том, что АЛК является антиоксидантом, защищающим сульфгидрильные группы системы транспортеров глюкозы, что, в свою очередь, приводит к повышению инсулинзависимой утилизации глюкозы [1].
Известно, что оксидативный стресс и отек из-за экстравазации плазмы, развивающиеся после травматического повреждения мозговой ткани, играют важную роль во вторичных механизмах нарушения мозговых функций. В литературе рассматривается возможность использования в этих случаях антиоксидантной терапии, включая АЛК. В эксперименте после травматического мозгового повреждения АЛК уменьшала выраженность оксидативного стресса, отек мозговой ткани и гистопатологические изменения [3]. Целый ряд антиоксидантов, включая АЛК, уменьшает активацию процессов апоптоза, обусловленную этанолом. В клиническом открытом исследовании 56 больных с алкогольной полинейропатией выявлено снижение позитивной и негативной невропатической симптоматики на фоне приема АЛК в дозе 300 мг ежедневно, причем АЛК оказалась более эффективной, чем тиамин.
В России имеется несколько препаратов альфа-липоевой кислоты, но наибольший практический опыт накоплен по препарату Эспа-липон, который одним из первых появился на российском рынке (1995) и отлично зарекомендовал себя как высокоэффективное средство. Благодаря оптимальным дозировкам, наличию пероральной и инфузионной форм выпуска, немецкому качеству и доступной цене Эспа-липон может максимально широко использоваться в современной медицине.
Клиническое применение альфа-липоевой кислоты
АЛК может использоваться при многих заболеваниях, в том числе при патологии центральной нервной системы, сопряженной с оксидативным стрессом и воспалительными изменениями. АЛК ингибирует миграцию Т-клеток в структуры центральной нервной системы. Показано, что АЛК может подавлять активность клеток, определяющих иммунный ответ путем ингибирования в них интерлейкинов и стимуляции цАМФ. В фибробластах пациентов с болезнью Альцгеймера выявлен выраженный оксидативный стресс, связанный с митохондриальной дисфункцией. В терапии болезни Альцгеймера АЛК рассматривается как один из методов нейропротекции. Нейропротекторные возможности АЛК реализуются за счет улучшения функции митохондрий. Показано, что АЛК увеличивает в головном мозге продукцию ацетилхолина за счет активации холинацетилтрансферазы и увеличения продукции ацетил-коэнзима А, уменьшает церебральный оксидативный стресс и синтез индуцибельной синтазы оксида азота, что является основой ее нейропротективного эффекта и дает возможность использования при нейродегенеративных процессах. В двух открытых клинических исследованиях 600 мг АЛК назначали больным с болезнью Альцгеймера в период от 12 до 48 месяцев и отметили замедление прогрессирования болезни при легкой степени деменции (ADAScog < 15) по сравнению с пациентами, не получавшими лечения или получавшими лечение ингибиторами ацетилхолинэстеразы [4]. АЛК также находит свое применение в гепатологии. В настоящее время отсутствуют лекарственные препараты с научно доказанным влиянием на метаболизм и выведение липидов из гепатоцитов. Однако медикаментозная терапия может существенно повлиять на последствия жирового гепатоза, а именно:
- снизить уровень перикисного окисления липидов;
- связать и инактивировать токсические субстраты в гепатоците в результате увеличения синтеза детоксикационных субстанций;
- блокировать активность мезенхимально-воспалительных реакций;
- замедлить прогрессирование фиброза [5].
Большое значение придается базисной терапии, включающей:
- прекращение действия этиологических факторов;
- полное исключение алкоголя;
- диету, богатую белками (1 г белка на 1 кг массы тела) и водорастворимыми витаминами, но бедную жирами;
- нормализацию в крови содержания глюкозы, липидов, мочевой кислоты при наличии соответствующих нарушений.
- способность снижать уровень перикисного окисления липидов (связывает свободные радикалы и свободное тканевое железо);
- участие в окислении жирных кислот и ацетата (предупреждает развитие жирового стеатоза печени);
- декарбоксилирование бета-кетокислот (энергообеспечение клетки и профилактика развития кетоацидоза);
- повышение трансмембранного транспорта глюкозы в клетку (накопление гликогена в клетке, увеличение ее энергетического баланса);
- подавление синтеза оксида азота гепатоцитами (профилактика и купирование реологических расстройств и сосудистых нарушений).
Препараты альфа-липоевой кислоты рекомендуется использовать при алкогольном и неалкогольном стеатогепатите, при жировом стеатозе для профилактики прогрессирования и развития осложнений. Лечение можно проводить в виде монотерапии и в сочетании с другими антиоксидантами и гепатопротекторами.
В настоящее время имеются единичные публикации об эффективности лечения больных с заболеваниями печени, ассоциированными с вирусом гепатита С, комбинацией Эспа-липона 300 мг 2 раза в день, силимарина 300 мг 3 раза в день и селенметионина 200 мкг 2 раза в день, принимаемой в течение года [8]. Дополнительно назначались комплекс витаминов В, С, Е и микроэлементы. К окончанию годичного курса лечения у всех пациентов было достигнуто улучшение клинических и биохимических показателей без элиминации вируса гепатита С. Данное исследование показало, что при невозможности провести адекватную противовирусную терапию (наличие побочных эффектов и противопоказаний, неэффективность проводимой ранее терапии) использование гепатопротекторов существенно улучшает качество жизни данных больных. Таким образом, учитывая широкий спектр действия по восстановлению практически всех видов обмена в гепатоците, препараты альфа-липоевой кислоты (например, Эспа-липон) должны найти широкое распространение в лечении метаболических заболеваний печени алкогольного и неалкогольного генеза.
Одно из перспективных направлений использования альфа-липоевой кислоты, которое мы широко используем в своей работе, – нейрогенная эректильная дисфункция (ЭД) на фоне ожирения и метаболического синдрома. Диагностика нейрогенной ЭД, которую можно считать ярким клиническим проявлением негативного действия окислительного стресса, приводящего к снижению секреции оксида азота (основного нейромедиатора) кавернозными нервами, достаточно проста (метод Калинченко – Роживанова). Определение нейропатии полового члена проводится с помощью прибора Тиотерм, у которого имеются два разных конца – металлический (холодный) и пластмассовый (теплый). Пациенты с нейропатией не различают разницы между холодным и теплым концом.
По данным эпидемиологических исследований, частота диабетической нейропатии (ДН) при СД варьирует от 5 до 100% в зависимости от используемых методов обследования. Различия в частоте встречаемости обусловлены использованием различных критериев диагностики ДН [9]. Согласно сложившейся точке зрения, наиболее ранней и частой формой ДН является диабетическая периферическая полинейропатия (ДПН). У 7,5% больных с впервые выявленным СД 2 типа уже имеются клинические и лабораторные проявления ДПН [9]. Однако, согласно нашим многочисленным исследованиям, наиболее ранней и частой формой ДН у мужчин с СД является эректильная дисфункция, которая значительно ухудшает качество жизни не только мужчины, но и семейной пары, а также является причиной развития депрессии, негативно влияющей и на возможность достижения копменсации углеводного обмена.
Нами исследованы клинико-эпидемиологические характеристики нейрогенных форм нарушений половой функции у мужчин, больных СД [10]. В сплошное одномоментное исследование было включено 611 больных СД (репрезентативная выборка), проживающих в различных регионах Российской Федерации. Все пациенты были анкетированы по опроснику Международного индекса эректильной функции 5 (МИЭФ-5) и Aging Male Simptoms по Heinemann. Степень компенсации углеводного обмена оценивалась по уровню гликированного гемоглобина (HbA1c) (норма – до 6,4%). Скрининг диабетической полинейропатии осуществлялся путем исследования вибрационной, температурной и тактильной чувствительности нижних конечностей (шкала NDS по Янгу и шкала TSS). Для выявления нейропатии половых органов оценивали вибрационную, тактильную и температурную чувствительность полового члена методом Калинченко – Роживанова. Для исследования гемодинамики полового члена проводилась ультразвуковая допплерография аппаратом Minimax Doppler Fono фирмы Minimax с датчиком 10 мГц. При статистической обработке данных использовали пакет прикладных программ Statistica (StatSoft Inc., США, версия 6.0).
Выявлено увеличение распространенности ЭД в старших возрастных группах. С возрастом и у мужчин, и у женщин происходит снижение секреции половых гормонов – важных эндогенных антиоксидантов, что усугубляет проявления окислительного стресса, а у ряда пациентов без сахарного диабета является ведущей причиной его возникновения. Кроме того, нами установлено, что нейрогенная форма ЭД у больных с СД 1 и 2 типов возникла раньше первых клинических проявлений дистальной диабетической нейропатии не менее чем в 37,4 и 51,9% случаев соответственно. Данная особенность позволяет использовать нейрогенную форму ЭД как ранний клинический прогностический признак развития дистальной диабетической нейропатии. Следует еще раз отметить, что сахарный диабет является не единственной причиной развития нейрогенной эректильной дисфункции. Когда определение чувствительности полового члена вошло в рутинную практику, мы стали выявлять достаточную распространенность ЭД и у мужчин без сахарного диабета. Нам удалось выделить несколько причин развития нейрогенной ЭД, на основании чего мы предлагаем следующую классификацию нейрогенной ЭД:
- Диабетическая нейрогенная ЭД.
- Травматическая нейрогенная ЭД (нередко наблюдается после операций на органах малого таза и половом члене).
- Токсическая нейрогенная ЭД (развивается на фоне приема алкоголя, длительного приема лекарственных препаратов, уремии, поражения печени, авитаминоза; нейропатия, развившаяся на фоне инфекций, системных заболеваний, аллергических заболеваний).
- Возрастная нейрогенная ЭД (развивается на фоне снижения секреции тестостерона).
Своевременное применение АЛК при нейрогенной эректильной дисфункции на фоне ожирения является профилактикой развития сосудистой эректильной дисфункции, которая достаточно трудно поддается терапии и предшествует более серьезным сосудистым катастрофам, таким как инсульт и ишемическая болезнь сердца. Оксидативный стресс, гиперхолестеринемия, активация эндотелия и адгезия моноцитов являются звеньями формирования атеросклеротического поражения сосудистой стенки.
В эксперименте доказано, что введение АЛК уменьшало размеры атеросклеротических бляшек в брюшной аорте, что сопровождалось уменьшением содержания жировых и воспалительных клеток в стенке аорты. АЛК улучшала сосудистую реакцию на ангиотензин II, ацетилхолин и инсулин, уменьшала оксидативный стресс. Применение АЛК уменьшает свободнорадикальное повреждение миоцитов вследствие оксидативного стресса при ишемии миокарда. В эксперименте назначение АЛК приводило к значительному снижению апоптоза, уменьшению перекисного окисления липидов, увеличению активности глутатиона и в митохондриях кардиомиоцитов, что препятствовало развитию необратимых нарушений сердечной функции. В исследовании ISLAND прием таблеток АЛК в дозе 300 мг в качестве монотерапии у больных с метаболическим синдромом в течение 4 недель приводил к увеличению эндотелий-зависимой вазодилатации брахиальной артерии, что сопровождалось уменьшением содержания в плазме интерлейкина-6 и активатора плазминогена-1. Таким образом, показано действие АЛК на эндотелиальную дисфункцию, реализующееся через влияние на противовоспалительные и антитромботические механизмы [11].
В пилотных исследованиях показано, что АЛК уменьшает апоптоз, связанный с оксидативным стрессом, но стимулирует процессы апоптоза в различных раковых клетках. В эксперименте на культуре клеток показано, что АЛК дозозависимо ингибирует пролиферацию клеток рака молочной железы человека и активирует в них процесс апоптоза. Аналогичные результаты были получены для клеток рака легкого, причем АЛК активирует апоптоз в раковых клетках как каспаза-независимым, так и каспаза-зависимым путем. Врачи из Нью-Мехико (США) описали случай больного раком поджелудочной железы с метастазами в печень, состояние которого улучшилось после инфузий АЛК в сочетании с приемом низких доз налтрексона. Больной был жив и хорошо себя чувствовал через 78 месяцев после первоначального описания. Цисплатин, широко используемый противораковый препарат, приводит к увеличению перекисного окисления липидов и снижению активности антиоксидантных ферментов в почечной ткани. Лечение цисплатином может стать причиной острого поражения почек, причем могут возникать необратимые нарушения фильтрации. В эксперименте показано, что АЛК уменьшает симптомы острого почечного поражения за счет уменьшения экспрессии воспалительных молекул адгезии и процессов апоптоза. Химиотерапия цисплатином и паклитакселом может вызывать поражение периферических нервов из-за нарушения функций митохондриального аппарата клеток. В эксперименте показано, что АЛК может предотвращать развитие полинейропатии, уменьшая оксидативный стресс и предохраняя митохондрии от повреждения при использовании этих препаратов [12].
Заключение
Таким образом, анализ экспериментальных и клинических исследований свидетельствует об универсальности антиоксидантного действия АЛК в сосудистом русле и цитоплазме клеточных структур различных органов. Возможность с помощью применения альфа-липоевой кислоты влиять на воспаление, апоптоз, кровоток, эндотелиальную дисфункцию, активацию нейротрансмиттеров, метаболические процессы позволяет рассматривать ее препараты как потенциальное лекарственное средство в различных областях медицины. Мы считаем, что у всех пациентов с нейрогенной эректильной дисфункцией применение альфа-липоевой кислоты должно носить курсовой режим, и отменять препарат возможно только при полном восстановлении половой функции и устранении причин окислительного стресса (ликвидация ожирения, метаболического синдрома, токсических факторов).
