количество статей
6593
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
VI съезд ревматологов России. Остеоартроз: от патогенеза к реальной практике
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Ревматология, травматология и ортопедия" № 2 (26)
- Аннотация
- Статья
- Ссылки
Остеоартроз – распространенное гетерогенное заболевание, с наибольшей частотой встречающееся у пожилых людей и характеризующееся выраженным болевым синдромом, нарушением функции суставов и наличием признаков воспалительного процесса. Лечение остеоартроза заключается прежде всего в купировании болевого синдрома с помощью нефармакологических и фармакологических средств. На сегодняшний день в мировой клинической практике существует множество препаратов для терапии остеоартроза, направленных не только на лечение его симптомов, но и на коррекцию катаболических и анаболических процессов, связанных с повреждением хряща. Пиаскледин, содержащий биологически активные компоненты, является эффективным препаратом для лечения остеоартроза различных локализаций. В ходе сателлитного симпозиума «Остеоартроз: от патогенеза к реальной практике» (Москва, 21 мая 2014 г.) ведущие специалисты в области ревматологии обсудили проблемы современной ревматологии и терапевтические подходы к купированию болевого синдрома при остеоартрозе.

Д.м.н. А.Е. Каратеев
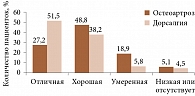
Рис. 1. Субъективная оценка эффективности терапии кетопрофеном

Профессор Л.И. Алексеева

Рис. 2. Количество больных, получающих лечение

Профессор Н.В. Чичасова
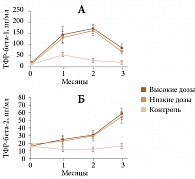
Рис. 3. Уровни ТФР-бета-1 (А) и ТФР-бета-2 (Б) в синовиальной жидкости
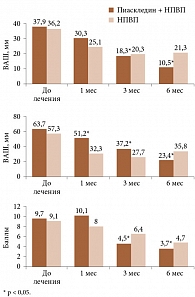
Рис. 4. Динамика боли в покое (А), при движении (Б) и динамика индекса Леккена (В) у больных остеоартрозом на фоне приема пиаскледина и НПВП

Таблица. Результаты анализа изменения суставной щели на рентгенограммах таза или тазобедренных суставов с использованием мануальной радиохондрометрии и числа прогрессирующих за три года больных
Фармакотерапия остеоартроза: оценка соотношения пользы и риска
Симпозиум открыл д.м.н. Андрей Евгеньевич КАРАТЕЕВ (Научно-исследовательский институт ревматологии им. В.А. Насоновой РАМН). Он рассмотрел вопросы фармакотерапии остеоартроза с позиции эффективности и безопасности.
Болевой синдром – основное проявление хронических заболеваний суставов и позвоночника, которое определяет функциональные нарушения и ухудшение качества жизни пациента. Нестероидные противовоспалительные препараты (НПВП) традиционно используются для лечения заболеваний суставно-мышечного аппарата и относятся к симптоматической терапии, направленной на временное улучшение состояния и качества жизни пациентов. Применение анальгетической терапии для купирования боли по-прежнему распространено среди больных остеоартрозом, несмотря на высокий риск осложнений со стороны сердечно-сосудистой системы и желудочно-кишечного тракта (ЖКТ). Однако, чтобы выбрать метод терапии остеоартроза, необходимо выяснить, насколько высок риск развития осложнений со стороны сердечно-сосудистой системы и ЖКТ на фоне приема обезболивающих препаратов и можно ли его снизить.
В НИИ ревматологии проведено исследование КОРОНА (количественная оценка риска осложнений у нуждающихся в анальгетиках). Целью исследования стала оценка распространенности заболеваний костно-мышечной системы в общей популяции пациентов, обращающихся за амбулаторной помощью к врачам разных специальностей в России и СНГ, а также рисков сердечно-сосудистых и желудочно-кишечных осложнений у данной группы пациентов. Критериями отбора пациентов для участия в исследовании были наличие диагноза ревматического заболевания и потребность в НПВП (боль > 4 баллов по десятибалльной шкале). В исследовании участвовало 21 185 больных, из них с диагнозом «остеоартроз» 4978 (23,5%) пациентов (59,1% женщин и 40,9% мужчин). Средний возраст составил 58,53 ± 12,06 года.
Установлены следующие факторы риска со стороны ЖКТ: каждый третий больной получал низкие дозы аспирина, 30,4% имели диспепсию, 12,7%–язвенный анамнез, 2% пережили желудочно-кишечные кровотечения и 31,8% были в возрасте старше 75 лет. Анализ факторов риска развития осложнений со стороны сердечно-сосудистой системы показал, что 56,6% пациентов имели артериальную гипертензию, 30,3% – ишемическую болезнь сердца, 10,5% перенесли острые сердечно-сосудистые заболевания (инфаркт миокарда, инсульт), 14% имели сахарный диабет 2-го типа.
Докладчик отметил, что, к сожалению, факторы риска сердечно-сосудистых и желудочно-кишечных осложнений очень часто присутствуют у пожилых больных остеоартрозом, нуждающихся в активной обезболивающей терапии. В лечении пожилых пациентов с коморбидными заболеваниями на первый план выходят вопросы безопасности терапии.
А.Е. Каратеев подробно рассмотрел препараты, широко применяемые в лечении остеоартроза, с позиции безопасности. Как известно, НПВП могут вызывать серьезные побочные эффекты со стороны верхних отделов ЖКТ, характеризующиеся появлением эрозий, язв, гастроинтестинальных катастроф – кровотечения и перфорации (0,5 ± 1 на 100 пациенто-лет). Риск сердечно-сосудистых осложнений у лиц, регулярно принимающих НПВП, составляет 1–2 на 100 пациенто-лет. Однако не только применение НПВП при лечении остеоартроза может способствовать развитию осложнений. Например, опиодные препараты, такие как трамадол, широко применяемые в США и Западной Европе, не могут считаться безопасной альтернативой НПВП. Их эффективность при длительном использовании у больных остеоартрозом вполне сопоставима с эффективностью НПВП, но они могут вызывать серьезные побочные эффекты.
В американском исследовании (1999–2005 гг.) с участием 12 840 больных остеоартрозом, получавших НПВП или опиоиды, частота госпитализаций у пациентов, принимавших опиоиды, была существенно выше, чем у пациентов, получавших НПВП. Сердечно-сосудистые осложнения отмечались чаще у больных, принимавших опиоиды, по сравнению с теми, кто получал традиционные НПВП. Применение опиоидов при остеоартрозе повышает риск падений и переломов в 4,5 раза по сравнению с больными, принимающими НПВП1.
Распространенным методом симптоматического лечения остеоартроза является внутрисуставное введение препаратов, как правило глюкокортикостероидов (ГКС), для эффективного подавления локального воспаления и уменьшения суставной боли. Однако серьезной проблемой при внутрисуставном введении препаратов является риск развития инфекционных осложнений – гнойного артрита. В Великобритании и Ирландии при опросе 759 врачей выявили 68 случаев за год гнойного артрита после внутрисуставных инъекций ГКС. Частота этого осложнения составила от 1 до 10 на 10 000 инъекций. Гнойные осложнения внутрисуставных инъекций – редкая, но серьезная проблема в клинической ревматологической практике. Докладчик подчеркнул, что гнойные осложнения могут стать следствием ошибки специалиста – введения инъекций без одноразовых перчаток. Поэтому необходимо помнить о соблюдении правил асептики во время процедуры.
При внутрисуставном введении препаратов гиалуроновой кислоты также существует риск возникновения осложнений. В одном из самых крупных исследований эффективности и безопасности гиалуроновой кислоты при лечении остеоартроза с участием 4253 пациентов 840 врачами проведено суммарно 12 699 инъекций препарата гиалуроновой кислоты гилана G-F. Частота осложнений после пункции и внутрисуставного введения препарата составила 4,2%. В 2,4% случаев отмечен суставной выпот, в 1,3% – отек сустава, в 1,2% – артралгия, в 0,3% – стойкая эритема. По данным исследований, препараты гиалуроновой кислоты с низким молекулярным весом обладают более высоким уровнем безопасности2.
Докладчик обратил внимание слушателей на то, что в последние годы в западных странах отмечается тенденция к негативному отношению к лечению остеоартроза медленно действующими симптоматическими средствами – хондропротекторами.
Европейским медицинским агентством были изданы рекомендации по ограничению использования стронция ранелата, а также предложения остановить продажу препарата, содержащего диацереин, из-за побочных эффектов. Однако результаты датского исследования, в котором 1798 больных остеоартрозом получали стронция ранелат, а группа контроля (65 636 пациентов) – алендронат/ризендронат, показали, что четко очерченный коронарный синдром развивался реже при терапии стронция ранелатом3.
В масштабном британском исследовании с участием 112 445 женщин, принимавших различные антиостеопоретические препараты, доказано отсутствие повышенного риска сердечно-сосудистых осложнений на фоне их приема4.
В настоящее время результаты исследований эффективности и безопасности диацереина достаточно противоречивы. Так, в кокрановском обзоре, включавшем результаты десяти рандомизированных клинических исследований, отмечена низкая приверженность лечению из-за побочных эффектов в виде диареи и небольшого терапевтического эффекта5. В трехлетнем исследовании эффективности диацереина по сравнению с плацебо у 507 больных коксартрозом показан положительный терапевтический эффект после приема препарата. Однако отмечен высокий процент случаев отмены терапии (25 против 12% в группе плацебо), связанный с нежелательными явлениями6.
Другая работа была посвящена оценке сравнительной эффективности препарата неомыляемого соединения авокадо и сои Пиаскледина (300 мг один раз в день) и хондроитина сульфата (400 мг три раза в день) при остеоартрозе коленных суставов. Активная терапия продолжалась шесть месяцев. В течение последующих двух месяцев за состоянием пациентов наблюдали. Результаты исследования показали, что Пиаскледин и хондроитина сульфат одинаково эффективны, хотя, по мнению пациентов и врачей, однократный прием первого препарата удобнее.
А.Е. Каратеев отметил, что в мире не ослабевает интерес к неселективным НПВП, используемым для лечения острой и хронической боли при остеоартрозе. Кетопрофен – НПВП с доказанным терапевтическим действием и относительной безопасностью несколько десятков лет используется в клинической практике. Проведенное в конце 1980-х гг. европейское наблюдательное исследование, в котором участвовало свыше 19 880 пациентов с остеоартрозом, продемонстрировало хорошую переносимость препарата. Побочные эффекты были зарегистрированы в 13,5% случаев, причем частота осложнений со стороны ЖКТ составила 0,03%.
Ряд исследований оценки риска развития инфаркта миокарда у больных, принимавших НПВП, показал низкий риск развития сердечно-сосудистых осложнений у пациентов с остеоартрозом при приеме кетопрофена по сравнению с другими НПВП.
В ходе отечественного исследования КУЛОН (Кетопрофен: удовлетворенность лечением и оценка нежелательных явлений) в реальной клинической практике оценивали эффективность и переносимость кетопрофена (препарат Артрозилен) у амбулаторных пациентов с заболеваниями или травмами опорно-двигательного аппарата и выраженной болью.
Период наблюдения составил две недели. Анализу были подвергнуты данные о применении препарата у 4609 амбулаторных больных. Среди пациентов преобладали женщины среднего и пожилого возраста с дорсалгией и остеоартрозом крупных суставов. Эффективность терапии определяли по динамике выраженности боли и удовлетворенности лечением.
Прием Артрозилена способствовал значительному уменьшению боли и улучшению самочувствия у большинства пациентов (51,5%) (рис. 1).
Из нежелательных явлений чаще отмечали осложнения со стороны ЖКТ. Побочные эффекты были зарегистрированы у 61 (1,3%) больного, в частности у 40 пациентов – диспепсия, у одного – язва желудка, у 16 – дестабилизация артериальной гипертонии, у двух – множественные эрозии слизистой оболочки органов ЖКТ, у двух – кожная реакция, у двух – локальная боль.
Таким образом, кетопрофен является препаратом выбора для кратковременной симптоматической терапии остеоартроза, особенно при повышенном риске сердечно-сосудистых осложнений. Риск осложнений со стороны ЖКТ может быть существенно снижен при тщательном наблюдении за пациентами и своевременном назначении гастропротективных препаратов.
Завершая выступление, А.Е. Каратеев подчеркнул, что большинство больных остеоартрозом имеют серьезную коморбидную патологию, которая является фактором риска развития лекарственных осложнений. Многие средства для лечения остеоартроза потенциально небезопасны. Все лекарственные препараты имеют побочные эффекты, поэтому проводить индивидуализированную терапию при остеоартрозе следует только с учетом баланса эффективности, безопасности и стоимости лечения.
Стратегии лечения остеоартроза с позиций этиопатогенеза и доказательной медицины. Обзор международных и российских исследований
Доктор медицинских наук, профессор Людмила Ивановна АЛЕКСЕЕВА (Научно-исследовательский институт ревматологии им. В.А. Насоновой РАМН) в своем выступлении рассмотрела проблему лечения остеоартроза с точки зрения доказательной медицины.
Первые рекомендации по лечению остеоартроза были опубликованы в 1995 г. и в процессе накопления новых исследовательских данных дополнялись и изменялись. Рекомендации включают различные фармакологические, нефармакологические и хирургические методы. Поскольку выбор метода терапии при остеоартрозе основан на доказательной базе, рекомендации по лечению заболевания базируются на данных метаанализов, систематических обзоров практически одних и тех же исследовательских работ. Однако выраженная гетерогенность пациентов, включенных в исследования, влияет на оценку исходов заболевания. Именно поэтому метаанализы часто дают неоднозначные результаты.
В патогенезе остеоартроза задействованы различные механизмы. Остеоартроз – гетерогенная группа заболеваний суставов различной этиологии, но со сходными биологическими, морфологическими и клиническими исходами. Поэтому на оценку и эффективность проводимой терапии остеоартроза влияют такие факторы, как фенотип заболевания, стадия (структурная или симптоматическая), наличие коморбидных заболеваний, индивидуальные особенности (пол, возраст, психосоциальный компонент).
Профессор Л.И. Алексеева отметила, что, несмотря на избыток рекомендаций, в мире не все больные получают лечение по поводу остеоартроза, что приводит к ранней инвалидизации и снижению качества жизни (рис. 2).
Оценка выполнения рекомендаций Международной ассоциации по изучению остеоартрита – OARSI (Osteoarthritis Research Society International) в общей клинической практике по нефармакологическим и фармакологическим методам лечения пациентов с остеоартрозом коленных и тазобедренных суставов, подвергшихся артропластике, показала, что большинство больных эти рекомендации в полном объеме не выполняли. Только 43% пациентов получили рекомендации по снижению избыточной массы тела, 23–67% – рекомендации по выполнению комплекса упражнений, 64% – по применению неселективных НПВП, из них 43% без гастропротекции, 5% – селективных НПВП, 19% – ГКС внутрисуставно. Таким образом, большинство пациентов, которые подверглись тотальному эндопротезированию суставов, рекомендации OARSI в полном объеме не выполняли7.
В этом году опубликован систематический обзор рекомендаций по ведению больных остеоартрозом, в котором проанализированы различные подходы к лечению заболевания. По данным обзора, целесообразно назначение НПВП из группы селективных ингибиторов и при необходимости неселективных НПВП в сочетании с гастропротективными средствами при наличии факторов риска развития нежелательных явлений со стороны ЖКТ. Имеются данные об эффективности применения локальных НПВП при остеоартрозе. Успешность обезболивания пациентов с остеоартрозом зависит от ряда индивидуальных факторов, таких как история заболевания, механизм формирования боли, коморбидные состояния, побочные эффекты. Таким образом, выбор препарата определяется не селективностью НПВП, а селекцией больных.
Внутрисуставное введение ГКС в настоящее время рассматривается как метод систематического лечения остеоартроза. Внутрисуставное введение ГКС значительно снижает выраженность симптомов остеоартроза, однако при применении ГКС следует учитывать индивидуальные особенности пациента, наличие синовита.
Группа препаратов замедленного действия, обладающих симптоматическим и структурно-модифицирующим эффектами (глюкозамина сульфат, хондроитина сульфат, диацереин, неомыляемые соединения сои и авокадо, препараты гиалуроновой кислоты), появилась в рекомендациях Европейской антиревматической лиги (European League Against Rheumatism, EULAR) в 2003 г. Европейские рекомендации по ведению больных с гонартрозом отмечают симптом-модифицирующий эффект препаратов замедленного действия и наличие у препаратов этой группы структурно-модифицирующего действия, а в рекомендациях EULAR по ведению больных с коксартрозом отмечено, что эти средства имеют симптоматический эффект и низкую токсичность, но структурно-модифицирующий эффект достоверно не установлен.
В данных обзора применения гиалуроновой кислоты для лечения пациентов с остеоартрозом наблюдаются расхождения во мнениях экспертов, что скорее всего обусловлено затруднениями в проведении рандомизированных исследований в связи с физическими свойствами гиалуроновой кислоты. Одни авторы говорят о низкой эффективности гиалуроновой кислоты в отношении симптомов остеоартроза, другие утверждают, что повторный курс препарата может отсрочить операцию по эндопротезированию. Препараты гиалуроновой кислоты эффективно уменьшают симптомы при остеоартрозе коленных суставов, в частности боль, припухлость и скованность. Задача врачей-ревматологов – замедлить прогрессирование заболевания, предотвратить необходимость хирургических вмешательств. Однако, по словам Л.И. Алексеевой, количество операций по эндопротезированию в нашей стране и за рубежом растет в геометрической прогрессии.
Несмотря на то что эффективность и безопасность моно- и комбинированных препаратов глюкозамина сульфата и хондроитина сульфата при лечении остеоартроза доказаны в многочисленных исследованиях, в международных рекомендациях имеется некоторое разночтение. В европейских рекомендациях, например, отмечается наличие у хондроитина сульфата симптоматического и структурно-модифицирующего действия, хотя его эффект считают невыраженным.
Неомыляемые соединения авокадо и сои (НСАС) также рекомендуются для лечения остеоартроза. Они уменьшают боль и улучшают функцию суставов. В последнее время интерес к этим препаратам постоянно растет. Одним из препаратов, имеющих доказанную эффективность, является Пиаскледин – неомыляемые соединения бобов сои и авокадо, полученные из экстрактов этих продуктов после гидролиза. Пиаскледин ингибирует интерлейкин 1, стимулирует синтез коллагена и протеогликанов. В хондроцитах человека также угнетает синтез коллагеназы, стромелизина, интерлейкинов 6 и 8, простагландина Е2.
При выборе оптимальной терапии больным остеоартрозом современные международные рекомендации предписывают учитывать особенности заболевания.
В связи с гетерогенностью остеоартроза эксперты OARSI предлагают подразделять заболевание на четыре группы в зависимости от фенотипа (остеоартроз коленных суставов с коморбидностью и без нее, генерализованный остеоартроз с коморбидностью и без нее). На сегодняшний день OARSI рекомендует в первую очередь в рамках нехирургического лечения пациентов с остеоартрозом применять основные обязательные лечебные методы, подходящие для всех больных, – лечебную физкультуру, в том числе в воде, снижение веса, самоконтроль и самообразование.
Профессор Л.И. Алексеева подчеркнула важность снижения массы тела у пациентов с остеоартрозом и отметила, что уменьшить его симптомы можно только при снижении массы тела более чем на 10% от исходной. Исследования показали, что снижение веса приводит к уменьшению боли и улучшению функционального состояния суставов.
Среди медикаментозных средств терапии остеоартроза в данных рекомендациях указан дулоксетин, не только являющийся антидепрессантом, но и обладающий в низких дозах анальгетическим эффектом. Как известно, боль в суставе при остеоартрозе обусловлена структурными изменениями и механизмами периферической и центральной боли. Поэтому рекомендации по лечению остеоартроза включают применение препаратов, воздействующих на эти механизмы.
При остеоартрозе коленных суставов у пациентов с коморбидностью рекомендации OARSI предлагают такие способы лечения, как использование биомеханики, трости для облегчения нагрузки на воспаленные суставы, локальных НПВП, внутрисуставных стероидов. При генерализованном остеоартрозе с коморбидностью пациентам рекомендованы бальнеотерапия, биомеханика, внутрисуставные инъекции стероидов, селективные НПВП, дулоксетин. Однако, несмотря на четкие рекомендации, при разработке терапевтической стратегии для лечения больных остеоартрозом необходимо учитывать индивидуальные особенности каждого пациента.
Подводя итог, профессор Л.И. Алексеева подчеркнула необходимость персонифицированного подхода к ведению пациентов. Диагностика остеоартроза должна быть предельно точной и учитывать предикторы прогрессирования заболевания. Для достижения эффективности терапии больных остеоартрозом надо правильно оценивать прогноз, мониторировать активность и прогрессирование болезни, подбирать препараты с оптимальной терапевтической доступностью, минимизируя нежелательные явления и экономические затраты. Создание препаратов, действие которых направлено на определенные патогенетические механизмы остеоартроза, расширяет перспективы терапии заболевания.
Хроническая боль в суставах и позвоночнике: опыт лечения при различных локализациях
Доктор медицинских наук, профессор кафедры ревматологии Первого МГМУ им. И.М. Сеченова Наталья Владимировна ЧИЧАСОВА посвятила свой доклад лечению остеоартроза препаратом Пиаскледин и привела данные нескольких исследований, подтверждающих его эффективность.
Экстракты масла авокадо и бобов сои (НСАС) содержит биологически активные компоненты. Они представляют собой комплекс активных фитостиролов, способных ингибировать всасывание холестерола. Исследования терапевтического действия НСАС были начаты в 1950 г. Результаты показали эффективность соединения при лечении заболеваний кожи и хряща. В 1971 г. НСАС были определены как вещества, способные активировать физиологические процессы, в частности, в эпидермисе. В 1972–1978 гг. результаты исследований продемонстрировали анальгетические свойства препарата при остеоартрозе тазобедренных и коленных суставов, а также возможное влияние на замедление прогрессирования заболевания.
Препарат НСАС Пиаскледин выпускается по европейскому стандарту качества и позиционируется как препарат, назначаемый при остеоартрозе и остеоартрите. Он применяется в Европе с 1978 г. как безопасное средство защиты и лечения суставов и позвоночника.
Пиаскледин продемонстрировал способность влиять на патологические процессы, приводящие к деградации хряща. Препарат вызывает достоверное снижение активности стромелизина, экспрессии интерлейкинов 6 и 8 и активности коллагеназы. Антикатаболическое действие Пиаскледина приводит к стимуляции продукции коллагена и протеогликана за счет увеличения синтеза трансформирующего фактора роста (ТФР) бета, а также ингибитора активатора плазминогена 1, участвующего в процессе повреждения хряща. Пиаскледин снижает катаболизм хряща за счет уникального состава сложной молекулы с возможностью влиять на провоспалительные медиаторы8.
Анаболические эффекты НСАС реализуются вследствие повышения экспрессии ТФР-бета-1 и -бета-2 в виде торможения деградации хряща, регуляции синтеза макромолекул межклеточного вещества. По данным исследований, Пиаскледин вызывает значительное повышение уровня ТФР в синовиальной жидкости коленного сустава при разных дозировках. Причем ТФР-бета-2 прогрессивно нарастает к третьему месяцу, ТФР-бета-1 начинает снижаться после второго месяца, но его концентрация остается значимой для предотвращения деградации хряща (рис. 3)9.
В нашей стране и за рубежом проведен ряд исследований, посвященных эффективности Пиаскледина в лечении остеоартроза крупных суставов.
В рандомизированном клиническом плацебоконтролируемом исследовании оценивали динамику количественных показателей, отражавших боль при остеоартрозе за шесть месяцев терапии у 164 больных остеоартрозом коленных (114) и тазобедренных (50) суставов, принимавших Пиаскледин 300 мг/сут, по сравнению с плацебо. Сохранение эффекта фиксировали в течение двух месяцев наблюдения по окончании приема препаратов. Пиаскледин показал по сравнению с плацебо достоверное уменьшение боли. Действие препарата нарастало в течение шести месяцев. Наблюдалось уменьшение потребности в НПВП в течение двух месяцев после отмены лечения, подтверждавшее наличие у Пиаскледина длительного и выраженного последействия10.
Аналогичные результаты были получены в ходе отечественного открытого исследования, в котором 92 пациента с остеоартрозом коленных и тазобедренных суставов были разделены на две равные группы. В первую группу вошли пациенты, принимавшие Пиаскледин, во вторую – те, кто получал НПВП. Длительность терапии составила шесть месяцев. На фоне приема Пиаскледина через три месяца терапии интенсивность боли значительно уменьшалась. В большей степени при приеме НПВП снижалась интенсивность утренней скованности. Показано, что анальгетический эффект Пиаскледина определяется не только противовоспалительным действием, но и многогранным влиянием на опосредованные цитокинами патологические процессы при остеоартрозе (рис. 4)11.
В ходе недавнего отечественного восьминедельного исследования терапевтических свойств Пиаскледина с контролем НПВП у больных с хронической дорсалгией отмечены значимое снижение выраженного мышечного синдрома на 4 балла, отчетливый эффект улучшения показателей жизнедеятельности по оценке Освестровского индекса (минимальное нарушение)12.
Профессор Н.А. Шостак и соавт. провели открытое рандомизированное исследование эффективности и безопасности Пиаскледина в комбинации с НПВП по сравнению с монотерапией НПВП у 30 больных старше 40 лет с умеренными и выраженными болями в нижней части спины, вызванными спондилоартрозом. Пациенты основной группы получали Пиаскледин (одна капсула 300 мг/сут) в комбинации с нимесулидом в дозе 200 мг/сут в течение 24 недель. Обследования проводили до лечения, спустя один, три и шесть месяцев от начала терапии. На фоне комбинированной терапии с использованием Пиаскледина у пациентов достоверно уменьшались боли (на 74,2%), расширялась функциональная активность позвоночника, появлялась возможность значительно больше двигаться. По оценкам пациентов, применение Пиаскледина существенно улучшило их качество жизни13.
Значительное снижение показателей болевого синдрома в спине, улучшение функционального состояния позвоночника после терапии Пиаскледином позволяет рекомендовать его для лечения синдрома болей в спине.
Было отмечено положительное влияние терапии Пиаскледином на больных узелковым артрозом, у которых уменьшалось число болезненных узелков и выраженность болевого синдрома.
Оценка влияния Пиаскледина на выраженность симптомов остеоартроза с локализацией в мелких суставах ранее не проводилась, поэтому на базе НИИ ревматологии и кафедры ревматологии Первого МГМУ им. И.М. Сеченова проведено исследование эффективности и безопасности НСАС (Пиаскледина) при остеоартрозе суставов кистей при длительном наблюдении. В исследовании участвовало 40 пациентов с остеоартрозом суставов кистей. Длительность наблюдения составила четыре месяца. У части больных терапия Пиаскледином продолжалась еще восемь месяцев (всего 12 месяцев).
Основная группа (20 больных) получала Пиаскледин 300 мг/сут и ибупрофен 1200 мг/сут, группа сравнения (20 больных) – ибупрофен 1200 мг/сут. Достоверные показатели уменьшения боли были зарегистрированы у всех больных через два месяца терапии и сохранялись до конца лечебного периода. Через четыре месяца терапии улучшение отмечалось у всех больных, получавших Пиаскледин и ибупрофен, по сравнению с 65% пациентов из группы ибупрофена. Выраженное влияние Пиаскледина на боль и восстановление функциональной активности суставов наблюдались через шесть – восемь месяцев терапии в основной группе больных. В конце продленной фазы исследования (через год) 100% больных оценили свое состояние как улучшение. Достоверные показатели уменьшения боли сохранялись у всех больных через 12 месяцев терапии. Таким образом, Пиаскледин продемонстрировал симптом-модифицирующий эффект при лечении остеоартроза.
Основная группа (20 больных) получала Пиаскледин 300 мг/сут и ибупрофен 1200 мг/сут, группа сравнения (20 больных) – ибупрофен 1200 мг/сут. Достоверные показатели уменьшения боли были зарегистрированы у всех больных через два месяца терапии и сохранялись до конца лечебного периода. Через четыре месяца терапии улучшение отмечалось у всех больных, получавших Пиаскледин и ибупрофен, по сравнению с 65% пациентов из группы ибупрофена. Выраженное влияние Пиаскледина на боль и восстановление функциональной активности суставов наблюдались через шесть – восемь месяцев терапии в основной группе больных. В конце продленной фазы исследования (через год) 100% больных оценили свое состояние как улучшение. Достоверные показатели уменьшения боли сохранялись у всех больных через 12 месяцев терапии. Таким образом, Пиаскледин продемонстрировал симптом-модифицирующий эффект при лечении остеоартроза.
Структурно-модифицирующий эффект Пиаскледина также оценивали в многоцентровых плацебоконтролируемых исследованиях. В исследовании с участием 163 пациентов с коксартрозом обязательным критерием включения было рентгенологически регистрируемое сужение щели тазобедренного сустава. Постоянную боль в пораженных суставах продолжительностью не менее шести месяцев отмечали все пациенты. Они были разделены на две группы: 85 больных весь срок исследования получали 300 мг/сут Пиаскледина, 78 больных – плацебо. В целом в обеих группах отмечалась сходная динамика изменения ширины суставной щели. Но среди больных, имевших ширину суставной щели в начале исследования, равную или менее 2,45 мм, прием Пиаскледина снизил отрицательную динамику по сравнению с плацебо практически в два раза: при приеме Пиаскледина уменьшение ширины суставной щели в год составило 0,24 мм, на фоне плацебо – 0,47 мм (p < 0,05)14.
В другом трехлетнем исследовании участвовало 399 больных коксартрозом с постоянной или рецидивирующей болью. Оценка изменения ширины суставной щели тазобедренного сустава была первичной конечной точкой и проводилась независимым экспертом в соответствии с последними рекомендациями. В исследование включались пациенты с передне-латеральным или передне-медиальным поражением. Величина суставной щели должна была варьировать от 1 до 4 мм. Поскольку международный консенсуc не рекомендовал использовать изменение ширины суставной щели в качестве первичной конечной точки в связи с трудностью трактовки такого изменения, дополнительно в группах больных, получавших Пиаскледин или плацебо, оценивали число больных с рентгенологическим прогрессированием. Прогрессирование деструкции регистрировалось, если уменьшение суставной щели было ≥ 0,5 мм за три года. Среди пациентов, закончивших исследование (по 170 пациентов в каждой группе), уменьшение суставной щели за три года составило -0,67 мм в группе плацебо и -0,64 мм в группе больных, получавших активный препарат (разница 0,034 мм, 95% доверительный интервал [-0,156 до 0,225]), различия недостоверны (р = 0,72). При этом, как видно из таблицы, достоверно меньше было больных с рентгенологическим прогрессированием сужения суставной щели при лечении Пиаскледином (40,4%), чем в группе плацебо (50,3%) (р = 0,040)15.
Во всех клинических исследованиях отмечен высокий уровень безопасности препарата Пиаскледин. Не зарегистрировано значимого числа побочных эффектов при длительном применении, препарат хорошо переносится пациентами, в том числе с коморбидными заболеваниями.
В заключение профессор Н.В. Чичасова отметила, что Пиаскледин является эффективным препаратом для лечения остеоартроза и предназначен для широкого применения в клинической ревматологической практике.
Заключение
1. Solomon D., Rassen J., Glynn R. et al. The comparative safety of analgesics in older adults with arthritis // Arch. Intern. Med. 2010. Vol. 170. № 22. P. 1968–1976.
2. Kemper F., Gebhardt U., Meng T. et al. Tolerability and short-term effectiveness of hylan G-F 20 in 4253 patients with osteoarthritis of the knee in clinical practice // Curr. Med. Res. Opin. Vol. 21. № 8. P. 1261–1269.
3. Svanström H., Pasternak B., Hviid A. Use of strontium ranelate and risk of acute coronary syndrome: cohort study // Ann. Rheum. Dis. 2014. Vol. 73. № 6. P. 1037–1043.
4. Cooper C., Fox K.M., Borer J.S. Ischaemic cardiac events and use of strontium ranelate in postmenopausal osteoporosis: a nested case-control study in the CPRD // Osteoporos. Int. 2014. Vol. 25. № 2. P. 737–745.
5. Fidelix T.S.A., Macedo C.R., Maxwell L.J. et al. Diacerhein for osteoarthritis // Cochrane Database Syst. Rev. 2014.
6. Dougados M., Nguyen M., Berdah L. et al. Evaluation of the structure-modifying effects of diacerein in hip osteoarthritis: ECHODIAH, a three-year, placebo-controlled trial. Evaluation of the Chondromodulating Effect of Diacerein in OA of the Hip // Arthritis Rheum. 2001. Vol. 44. № 11. P. 2539–2547.
7. Beadle C., Howie C.R., Nuki G. et al. OARSI Recommendations for the management of hip and knee osteoarthritis: which treatments are being used? Audit of patients coming to arthroplasty in Scotland // Osteoarthritis Cartilage. 2010. Vol. 18. № 2. P. S45–S256. Аbstr. 343.
8. Henrotin Y.E., Sanchez C., Deberg M.A. et al. Avocado/soybean unsaponifiables increase aggrecan synthesis and reduce catabolic and proinflammatory mediator production by human osteoarthritis chondrocytes // J. Rhematol. 2003. Vol. 30. Р. 1825–1834.
9. Altinel L., Saritas Z.K., Kose K.C. et al. Treatment with unsaponifiable extracts of avocado and soybean increases TGF-beta1 and TGF-beta2 levels in canine joint fluid // Tohoku J. Exp. Med. 2007. Vol. 211. № 2. P. 181–186.
10. Maheu E., Mazieres B., Valat J.-P. et al. Symptomatic efficacy of avocado/soybean unsaponifiables in the treatment of osteoarthritis of the knee and hip // Arthritis Rheum. 1998. Vol. 41. Р. 81–91.
11. Бадокин В.В. Пиаскледин – хондропротективный препарат с антицитокиновой активностью // Consilium medicum. 2007. Т. 9. № 8. С. 147–152.
12. Меркулова Д.М., Онсин А.А., Меркулов Ю.А. Пиаскледин в терапии хронической дорсалгии // Журнал неврологии и психиатрии им. С.С. Корсакова. 2013. № 9. С. 18—22.
13. Шостак Н.А., Правдюк Н.Г. Дегенеративное поражение позвоночника: представления о болезни, подходы к терапии (собственные данные) // Современная ревматология. 2008. № 3. С. 30–36.
14. Lequesne M., Maheu E., Cadet C. et al. Structural effect of avocado/soybean unsaponifiables on joint space loss in osteoarthritis of hip // Arthritis Care Research. 2002. Vol. 47. Р. 50–58.
15. Maheu E., Cadet C., Marty M. et. al. Randomised, controlled trial of avocado-soybean unsaponifiables (Piaskledine) effect on structure modification in hip osteoarthritis: the ERADIAS study // Ann. Rheum. Dis. 2013.
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
