XIX Российский национальный конгресс «Человек и лекарство»: Креон в алгоритмах ведения больных хроническим панкреатитом
- Аннотация
- Статья
- Ссылки

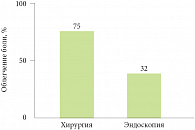


«Таким образом, мы можем дифференцированно подходить к хирургическому лечению, выделяя две формы – хронический панкреатит с широким протоком и хронический панкреатит с преимущественным поражением паренхимы поджелудочной железы, где в 50% случаев преобладают изменения в головке», – уточнил Р.В. Петров. По его словам, эндоскопическое вмешательство является менее эффективным методом, чем хирургическая операция, и в большей степени показано для лечения осложнений хронического панкреатита. Так, по данным рандомизированного клинического исследования D.L. Cahen и соавт. (2007), при хирургическом вмешательстве облегчение болевого синдрома у пациентов с ХП наблюдалось более чем в два раза чаще, чем при эндоскопическом вмешательстве (рис. 1). Выделяют два класса оперативных вмешательств:
- дренирующие операции, направленные на улучшение оттока секрета ПЖ (продольное вскрытие ПЖ вдоль ее поверхности на протяжении не менее 7 см);
- резекционные операции (дистальная резекция, проксимальная резекция).
Как показывают отдаленные результаты лечения, дренирующие операции, основным достоинством которых является малая травматичность, малоэффективны в купировании хронической боли – с течением времени более половины пациентов чувствовали возвращение болевого синдрома с прежней силой6, 7. На современном этапе целесообразным считается применение органосохраняющих операций в виде изолированных резекций головки ПЖ и сочетания резекций головки ПЖ с дренирующими операциями, улучшающими непосредственные и отдаленные результаты лечения. Анализ осложнений, купирования боли, качества жизни показывает, что такие органосохраняющие операции, как, например, резекция головки ПЖ с сохранением двенадцатиперстной кишки, являются надежным и безопасным методом устранения основных симптомов и осложнений ХП8.
По мнению докладчика, панкреатодуоденальная резекция (ПДР) при хроническом панкреатите считается «хирургической передозировкой», единственным показанием для ее проведения является подозрение на рак ПЖ. В целом использование резекций головки ПЖ в настоящее время относится к стандартным хирургическим вмешательствам, которые позволяют при минимальном риске послеоперационных осложнений и летального исхода эффективно купировать боль и улучшать качество жизни пациентов. Послеоперационное ведение больного предполагает компенсацию экзокринной и эндокринной недостаточности, а также длительное наблюдение за состоянием пациента с целью предупредить возможность развития рака ПЖ. Адекватная коррекция экзокринной недостаточности возможна при правильном назначении ферментной терапии, в которой препаратом выбора является Креон®.
Возможности эндоскопических методов в диагностике и лечении хронического панкреатита и его осложнений
По словам старшего научного сотрудника кафедры госпитальной хирургии № 2 Российского национального исследовательского медицинского университета им. Н.И. Пирогова, к.м.н. С.А. БУДЗИНСКОГО, существует четыре основных типа хирургических осложнений ХП, которые предполагают применение эндоскопических методик:
- осложнения, возникающие вследствие нарушения целостности протоковой системы ПЖ (кисты ПЖ, наружные и внутренние панкреатические свищи);
- осложнения, возникающие вследствие обструкции разрастающейся фиброзной тканью образований панкреатодуоденальной области (компрессия желчных протоков, дуоденальная непроходимость, портальная гипертензия);
- стриктуры или окклюзия камнями панкреатического протока (протоковая гипертензия, атрофия паренхимы ПЖ);
- рак ПЖ.
Диагностика заболевания включает анамнез и физикальное обследование, а также лабораторную и инструментальную диагностику. Алгоритм выбора метода с учетом оценки паренхимы ПЖ и протоков предполагает, чтобы предпочтение отдавалось инструментальной диагностике, которая включает классическое ультразвуковое исследование (УЗИ), эндосонографию (эндоскопическая ультрасонография, эндоскопический ультразвук), компьютерную томографию (КТ), эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ), магнитно-резонансную томографию (МРТ) и магнитно-резонансную холангиопанкреатографию (МРХПГ), ангиографию, радионуклидную холецистографию, манометрию сфинктера Одди, гистологическое исследование. Докладчик, дав краткую характеристику каждому методу, более детально остановился на возможностях эндосонографии и ЭРХПГ в диагностике хронического панкреатита.
Эндоскопическая ультрасонография (ЭУС) является высокоинформативным методом ультразвуковой диагностики заболеваний ПЖ; при этом исследовании сканирование проводится через стенку желудка и двенадцатиперстной кишки. Такое приближение датчика к ПЖ позволяет детально изучить структуру ткани органа, состояние протоковой системы, провести дифференциальную диагностику панкреатита с раком ПЖ и пр. Диагностическая точность эндосонографии в диагностике хронического панкреатита достаточно высока – чувствительность и специфичность метода составляют 86–98%10, 11.
ЭРХПГ является одним из важнейших методов исследования, позволяющим выявить стеноз главного панкреатического протока и определить локализацию обструкции, обнаружить структурные изменения мелких протоков, а также изменения общего желчного протока. Чувствительность и специфичность эндоскопической ретроградной холангиопанкреатографии в диагностике ХП варьируют в пределах 70–90% и 80–100% соответственно12, 13. ЭУС и ЭХПГ обеспечивают 100-процентную визуализацию головки ПЖ и ее протоков, в отличие от УЗИ и КТ, а эндоскопическая ультрасонография – еще и 100-процентную визуализацию тела ПЖ14, 15. По мнению С.А. Будзинского, эндосонографию можно считать «золотым стандартом» диагностики ХП. Основными целями эндоскопических лечебных вмешательств при ХП и его осложнениях являются:
- декомпрессия главного панкреатического протока (ГПП) ПЖ (стеноз устья ГПП, стриктуры вирсунгова протока, вирсунголитиаз);
- лечение осложнений ХП (наружные и внутренние панкреатические свищи, псевдокисты ПЖ);
- декомпрессия холедоха при наличии механической желтухи.
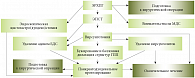
С.А. Будзинский дал краткую оценку ряду эндоскопических методов лечения, входящих в алгоритм выполнения эндоскопических вмешательств по поводу ХП (рис. 2). По его словам, эндоскопическая папиллосфинктеротомия (ЭПСТ) в большинстве случаев является подготовительным этапом перед последующими эндоскопическими манипуляциями на протоковых системах ПЖ, и только при некоторых вариантах папиллостеноза данный метод можно рассматривать как окончательное лечение. Эндоскопическое бужирование и баллонная дилатация стриктур ГПП на современном этапе также рассматриваются как подготовительное вмешательство для дальнейшего выполнения панкреатодуоденального стентирования стриктур ГПП и/или извлечения супрастенотических вирсунголитов. Эндоскопическое удаление вирсунголитов в ряде случаев может являться методом окончательного эндоскопического лечения при изолированном вирсунголитиазе, а наряду с панкреатодуоденальным стентированием стриктур ГПП может рассматриваться как способ окончательного эндоскопического лечения ХП.
Этот метод может быть этапом подготовки к хирургическому лечению ХП и его осложнений. Согласно результатам исследования T. Rosch (2002), эффективность данного метода составляет 85%16. Методом окончательного эндоскопического лечения при изолированных стриктурах ГПП, а также наружных и внутренних панкреатических свищах считается эндоскопическое панкреатодуоденальное стентирование. У этого метода есть и недостатки. Одним из осложнений стентирования является рецидив болевого синдрома, который может возникать у 50% больных через 12 месяцев после удаления стента17. Однако, как показывают результаты других исследований, при стентировании на срок 23 месяца рецидив болевого синдрома возникал у 30% больных18, а при стентировании на срок 12 месяцев, но с использованием нескольких стентов – у 16% пациентов19 .
Для эндоскопического лечения ряда кист ПЖ, связанных с ГПП, используется эндоскопическая цистогастростомия – цистогастродуоденостомия под контролем ЭУС. Данный метод может рассматриваться как этап диагностики и подготовки к дальнейшему хирургическому лечению. По данным исследования, при эндоскопическом лечении кист ПЖ риск возможных осложнений легкой степени составлял 14%, тяжелой степени – 6%, летальные исходы отсутствовали. К методам окончательного лечения можно отнести эндоскопическое удаление доброкачественных образований большого дуоденального сосочка (БДС) и эндоскопические вмешательства на малом дуоденальном сосочке (МДС) при ХП, связанном с аномальным строением протоковой системы ПЖ. Медикаментозная поддержка пациентов после эндоскопических лечебных вмешательств по поводу ХП предусматривает консервативное ведение больных в ближайшем и отдаленном послеоперационном периоде.
Консервативное лечение в отдаленном послеоперационном периоде включает диету и коррекцию ферментно-ингибиторного дисбаланса (создание функционального покоя ПЖ, подавление функции ацинарных клеток). В создании функционального покоя ПЖ значимая роль принадлежит ферментной терапии, препаратом выбора в которой выступает Креон®. Завершая выступление, С.А. Будзинский сделал следующие выводы:
- эндоскопические методики являются наиболее информативными (наряду с МРХПГ) методами диагностики протоковой патологии;
- ЭУС является одним из важнейших методов обследования паренхимы ПЖ;
- эндоскопические вмешательства на ранних стадиях развития ХП при преимущественных изменениях протоковой системы ПЖ являются предпочтительными по сравнению с хирургическим лечением в связи с сопоставимой эффективностью и низким уровнем осложнений и летальности;
- на поздних стадиях развития ХП, при верифицированных изменениях паренхимы органа, а также при наличии нескольких осложнений основного заболевания эндоскопические операции служат лишь подготовительным этапом для последующей хирургической коррекции.
Современные подходы в лекарственной терапии хронического панкреатита и профилактике осложнений
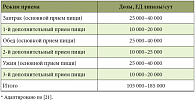
Заместительная ферментная терапия является одним из основных способов профилактики прогрессирования фиброзно-дегенеративных изменений в паренхиме ПЖ, уменьшения болевого синдрома и расстройств пищеварения. Поэтому назначение заместительной ферментной терапии, правильный выбор препарата и его дозы имеют огромное значение для успеха консервативного лечения. Однако, по мнению доцента кафедры пропедевтики внутренних болезней и гастроэнтерологии лечебного факультета МГМСУ, к.м.н. Ю.А. КУЧЕРЯВОГО, назначение низких доз ферментного препарата является одной из наиболее важных причин неэффективности заместительной терапии. Между тем разработаны и внедрены в практическое здравоохранение во всем мире дозы микрокапсулированного панкреатина для коррекции экзокринной панкреатической недостаточности (табл.)21.
Для уточнения вопроса, почему необходимо назначать высокие дозы препарата, докладчик кратко остановился на патофизиологических основах ферментной терапии. Известно, что в норме за сутки выделяется 2 л панкреатического секрета с содержанием ферментов в 10 раз большим, чем необходимо для адекватного пищеварения, что говорит о колоссальных резервных возможностях ПЖ. Постпрандиальная экскреция липазы составляет порядка 140 000 ЕД/час, в течение 6 часов ПЖ выделяет около 840 000 ЕД липазы. Мальабсорбция не развивается при поступлении в двенадцатиперстную кишку более 5% от физиологически секретируемой липазы. «Следовательно, чтобы предупредить мальабсорбцию, необходимы 42 тысячи единиц липазы на один прием пищи. Мы назначаем пациенту на прием пищи одну капсулу современного препарата Креон® в дозе 40 000 и предупреждаем таким образом развитие мальабсорбции. Препарат имеет форму минимикросфер, что позволяет достичь максимального контакта с химусом и оптимального ферментного взаимодействия», – пояснил Ю.А. Кучерявый.
Прием ферментных препаратов при ХП может продолжаться годами, причем уменьшение диспепсического синдрома и определенная стабилизация массы тела не являются показаниями для прекращения ферментотерапии, поскольку у большинства пациентов с нормальным индексом массы тела отмечается расстройство нутритивного статуса и дефицит микронутриентов. На сегодняшний день существует ряд клинических исследований, в которых оценивали безопасность длительной терапии панкреатическими ферментами. С результатами одного из них докладчик познакомил участников симпозиума. В двойном слепом плацебоконтролируемом рандомизированном исследовании22 оценивали безопасность терапии высокими дозами Креона (360 000 ЕД липазы в сутки) в течение 4 недель. В исследовании приняли участие 12 здоровых мужчин (средний возраст – 27 лет), которые были рандомизированы в 2 группы: в 1-й группе пациенты получали Креон®, во 2-й группе – плацебо. На основании анализа результатов данных исследования были сделаны следующие выводы:
- за период наблюдения не отмечено достоверных признаков нарушения эндокринной и экзокринной функций ПЖ, а также морфологических изменений ПЖ;
- в здоровой ПЖ не происходят функциональные приспособительные реакции на фоне ферментной терапии панкреатином в высоких дозах.
Осложнениями ХП являются кисты и псевдокисты, желчная и дуоденальная непроходимость, холангит, абсцессы железы, парапанкреатит, портальная гипертензия. К исходам ХП относятся фиброз, панкреатическая недостаточность, сахарный диабет и рак ПЖ. Независимыми факторами риска развития ХП и его осложнений являются курение и алкоголь, поэтому больным ХП необходимо рекомендовать отказаться от курения и приема алкоголя. В период манифестации панкреатита доминирует болевой абдоминальный синдром, со временем интенсивность боли снижается и увеличивается частота осложненных форм, что связано с прогрессирующим фиброзом. Говоря о роли цитокинов в развитии фибротического процесса, докладчик остановился на значении основного трансформирующего фактора роста TGF-бета в патогенезе хронического панкреатита. Согласно данным исследования, у больных ХП обнаружены высокие концентрации TGF-бета в панкреатическом соке; через 12 недель от начала обострения отмечалось пиковое повышение TGF-бета, сопровождавшееся морфологическими изменениями в ПЖ с максимально выраженным фибротическим процессом к 16-й неделе от начала обострения; при ХП отмечалось увеличение экспрессии рецепторов TGF-бета в 5–38 раз и увеличение количества коллагена 1-го типа в 24 раза; уровень гиперэкспрессии TGF-бета при ХП коррелировал с выраженностью инкреторной недостаточности ПЖ23.
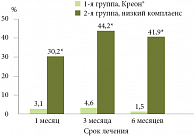
Однако, по словам Ю.А. Кучерявого, на сегодняшний день у врачей есть инструмент управления развитием фиброза ПЖ – это эффективная заместительная ферментная терапия в адекватных дозах. Подтверждение тому – результаты исследования динамики TFG-бета у больных ХП после уменьшения клинико-инструментальных проявлений обострения на фоне поддерживающей терапии Креоном24. В зависимости от степени экзокринной недостаточности у пациентов, входивших в подгруппы А и Б (1-я группа (n = 39) – с сохранной экзокринной функцией ПЖ; 2-я группа (n = 53) – с умеренной экзокринной недостаточностью; 3-я группа (n = 25) – с тяжелой экзокринной недостаточностью), пациенты подгруппы А получали заместительную ферментную терапию Креоном в дозе 50 000–150 000 ЕД липазы в сутки в течение 6 месяцев, пациентам подгруппы Б ферментотерапия не назначалась. Данные исследования показали, что уровень экспрессии TGF-бета был достоверно более низким во всех подгруппах А по сравнению с соответствующими подгруппами Б начиная с 3-го месяца и далее в течение всего периода исследования. Рецидив болевого синдрома у пациентов, принимавших Креон®, через 3–6 месяцев наблюдался почти в три раза реже, чем у пациентов, не получавших ферментной терапии (рис. 3).
Установлено, что при угнетении эндокринной функции ПЖ угнетается и ее экзокринная функция25. Поэтому сахарный диабет, даже в отсутствие панкреатита, может рассматриваться как фактор риска его развития. У больных ХП отмечен высокий риск развития рака ПЖ26. Результаты многоцентрового исследования A.B. Lowenfels и соавт. (1993) подтвердили наличие такой взаимосвязи: приблизительно у 4% пациентов с ХП развивается рак ПЖ в течение 20 лет от начала заболевания; длительный анамнез ХП в 15–16 раз превышает риск развития рака ПЖ по сравнению с риском в общей популяции27. Безусловно, адекватное и своевременное лечение ХП является залогом профилактики прогрессирования заболевания и развития осложнений, в том числе и рака ПЖ. В заключение Ю.А. Кучерявый подчеркнул, что данное заболевание полиэтиологично и имеет междисциплинарный характер, поскольку им занимаются не только гастроэнтерологи, но и терапевты, эндоскописты, хирурги. Поэтому выработка оптимального мультидисциплинарного подхода к диагностике и лечению ХП позволит существенно снизить заболеваемость и развитие его осложнений.
Заключение
Алгоритмы ведения больных ХП как при консервативном лечении, так и в послеоперационном периоде предусматривают использование заместительной ферментной терапии. По мнению докладчиков, среди широкого спектра современных ферментных средств именно Креон® является препаратом выбора. Креон® содержит липазу, амилазу и протеазы в оптимальном соотношении, кроме того, он выпускается в форме минимикросфер, обеспечивающей быстрое наступление клинического эффекта: уменьшение интенсивности болевого синдрома и проявлений расстройств пищеварения и мальабсорбции. Данные опубликованных исследований доказывают не только высокую эффективность, но и хороший профиль безопасности препарата Креон®. Все это в значительной степени определяет целесообразность использования Креона для купирования двух важнейших синдромов ХП – экзокринной недостаточности и болевого абдоминального синдрома.
