количество статей
7415
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Адъювантная гормональная терапия после радикальной простатэктомии
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №5
- Аннотация
- Статья
- Ссылки
Радикальная простатэктомия на протяжении последних двух десятилетий остается одним из наиболее популярных методов лечения локализованного и местнораспространенного рака предстательной железы. В то же время оперативное вмешательство не во всех случаях приводит к полному излечению от заболевания.
Причинами возникновения рецидива заболевания могут быть нерадикальное выполнение хирургического вмешательства, приводящее к наличию остаточной опухолевой ткани, или скрытая диссеминация опухолевого процесса, не выявленная на момент радикальной простатэктомии.
Достаточно высокая частота прогрессирования рака после радикальной простатэктомии обусловливает актуальность разработки методов комбинированного лечения, снижающих вероятность развития рецидива заболевания.
Эффективным методом профилактики развития прогрессирования заболевания является адъювантная гормональная терапия, немедленное назначение которой после радикальной простатэктомии позволяет увеличить безрецидивную и общую выживаемость больных.
Радикальная простатэктомия на протяжении последних двух десятилетий остается одним из наиболее популярных методов лечения локализованного и местнораспространенного рака предстательной железы. В то же время оперативное вмешательство не во всех случаях приводит к полному излечению от заболевания.
Причинами возникновения рецидива заболевания могут быть нерадикальное выполнение хирургического вмешательства, приводящее к наличию остаточной опухолевой ткани, или скрытая диссеминация опухолевого процесса, не выявленная на момент радикальной простатэктомии.
Достаточно высокая частота прогрессирования рака после радикальной простатэктомии обусловливает актуальность разработки методов комбинированного лечения, снижающих вероятность развития рецидива заболевания.
Эффективным методом профилактики развития прогрессирования заболевания является адъювантная гормональная терапия, немедленное назначение которой после радикальной простатэктомии позволяет увеличить безрецидивную и общую выживаемость больных.
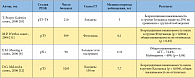
Таблица 1. Изменения уровня ПСА, среднее время выживания до развития рецидива и уменьшение болевого синдрома у больных с ГР РПЖ в рандомизированных исследованиях III фазы с применением химиотерапии

Таблица 2. Результаты химиотерапии доцетакселом
Рак предстательной железы (РПЖ) является в настоящее время одним из наиболее распространенных злокачественных новообразований в России. По темпам прироста заболеваемости РПЖ занимает 1-е место среди всех солидных опухолей, за десятилетие с 1999 по 2009 г. показатель заболеваемости увеличился на 153,27% [1]. В то же время ежегодно наблюдается и увеличение доли больных, у которых выявляют локализованный опухолевый процесс: в 2009 г. РПЖ I?II стадии диагностировали у 44,8% больных, еще у 34,9% первично зарегистрирован местнораспространенный процесс. Увеличение числа больных с неметастатическим РПЖ приводит к существенному росту числа выполняемых радикальных простатэктомий (РПЭ). В то же время частота развития биохимического прогрессирования после РПЭ у больных локализованным и местнораспространенным РПЖ, по некоторым данным, составляет 15–46% [2]. Причинами возникновения рецидива заболевания могут быть нерадикальное выполнение хирургического вмешательства, приводящее к наличию остаточной опухолевой ткани, или скрытая диссеминация опухолевого процесса, не выявленная на момент РПЭ. Достаточно высокая частота прогрессирования РПЖ после РПЭ обусловливает актуальность разработки методов комбинированного лечения, снижающих вероятность развития рецидива заболевания. Адъювантная, или послеоперационная, гормональная терапия (ГТ) подразумевает немедленное назначение эндокринной терапии больным РПЖ после выполнения РПЭ. Целью проведения адъювантной ГТ является предотвращение развития биохимического прогрессирования опухолевого процесса, а следовательно, увеличение безрецидивной и общей выживаемости больных.
Адъювантная ГТ после РПЭ у больных с метастазами в лимфатических узлах
Одними из первых опубликованных работ, посвященных изучению роли адъювантной ГТ после РПЭ, были исследования H. Zincke и соавт. из клиники Мэйо (США) [3–5]. Авторы провели ретроспективный анализ лечения больных РПЖ с метастазами в лимфатических узлах, получавших и не получавших адъювантную андроген-депривационную ГТ (хирургическая или медикаментозная кастрация) после РПЭ. При среднем периоде наблюдения 6,5 лет выявлено, что в группе, составляющей 790 больных со стадией РПЖ pN+, адъювантная ГТ не влияла на показатели опухолево-специфической выживаемости у пациентов с недиплоидными (анеуплоидными и тетраплоидными) опухолями. Выживаемость больных с диплоидными опухолями, получавших адъювантную ГТ менее 10 лет и не получавших ее, также достоверно не отличалась. В то же время смертность от РПЖ в подгруппе больных с диплоидными опухолями, получавших немедленную ГТ более 10 лет, достоверно снижалась по сравнению с пациентами, получавшими отсроченную терапию (р < 0,002).
В более поздней публикации R.P. Myers и соавт. при ретроспективном анализе также показали преимущество адъювантной ГТ перед хирургическим лечением [6]. В исследование были включены 289 больных, у которых при патоморфологическом исследовании после позадилонной РПЭ и тазовой лимфаденэктомии выявлены лимфогенные метастазы. 231 больному в послеоперационном периоде начинали ГТ, 58 пациентов не получали дополнительного лечения до прогрессирования. Средний период наблюдения за больными составил 15,3 года, за этот период умерли 164 пациента. Следует отметить, что у больных в группе комбинированного лечения достоверно чаще наблюдались такие прогностически неблагоприятные данные морфологического исследования, как экстракапсулярная инвазия (р = 0,015), положительный хирургический край (р < 0,001) и низкая степень дифференцировки опухоли (р = 0,006). Показатели выживаемости без признаков клинического прогрессирования (местного рецидива и метастазов) у больных, получавших адъювантную ГТ, оказались достоверно выше, чем у пациентов, которым выполняли только РПЭ (р < 0,001). 15-летняя и 20-летняя опухолево-специфическая выживаемость составила соответственно 75% и 72% в группе комбинированного лечения и 58% и 51% в группе хирургического лечения (р = 0,015). Относительный риск смерти от РПЖ при проведении адъювантной ГТ, по сравнению с хирургическим лечением, составил 0,54 (95% ДИ – 0,33?0,89). При анализе отношения рисков с учетом степени дифференцировки опухоли, стадии, возраста, плоидности ДНК, состояния хирургического края, наличия экстракапсулярной инвазии и числа метастатически измененных лимфатических узлов также выявлено достоверное преимущество адъювантной ГТ: относительный риск – 0,38 (95% ДИ – 0,21–0,69).
Единственным рандомизированным исследованием, посвященным оценке эффективности адъювантной ГТ после РПЭ у больных с метастазами в лимфатических узлах, является протокол ECOG EST 3886 [7, 8]. Исследование проведено на базе 36 клиник США, оно включило 98 больных лимфогенно-диссеминированным РПЖ, которым была выполнена РПЭ по поводу клинически локализован-ного процесса. В группе комбинированного лечения больным (n = 47) проводили немедленную ГТ (70% больных получали Золадекс 3,6 мг каждые 4 недели, 30% пациентов выполнена билатеральная орхидэктомия), в контрольной группе (n = 51) за пациентами проводили тщательное динамическое наблюдение и назначали ГТ только после возникновения биохимического или клинического прогрессирования. Группы больных были сопоставимы по основным предоперационным прогностическим факторам (дифференцировке опухоли по шкале Глисона, уровню ПСА и стадии процесса). На протяжении первого года проводилось динамическое наблюдение всех больных каждые 3 месяца, затем – каждые 6 месяцев. Медиана наблюдения составила 11,9 года (9,7–14,5 года). Общая (ОР = 1,84; 95% ДИ – 1,01–3,35; p = 0,04), опухолевоспецифическая (ОР = 4,09; 95% ДИ – 1,76?9,49; p = 0,0004), а также безрецидивная (ОР = 3,42; 95% ДИ – 1,96?5,98; p < 0,0001) выживаемость больных в группе немедленной ГТ была достоверно выше, чем в контрольной группе. Так, в группе адъювантной ГТ общая выживаемость больных составила 72,4%, а в группе отсроченного лечения – только 49%, опухолево-специфическая выживаемость – 87,2% и 56,9% соответственно. Таким образом, исследование показало явные преимущества немедленной ГТ у больных лимфогенно-диссеминированным РПЖ после РПЭ по сравнению с отсроченным лечением.
Адъювантная ГТ после РПЭ у больных местнораспространенным РПЖ
Одной из первых публикаций, посвященных оценке роли адъювантной ГТ у больных с инвазией опухоли в семенные пузырьки (pT3b), является работа также из клиники Мэйо [9]. Из 707 больных, у которых по данным патоморфологического исследования после РПЭ выявлена инвазия опухоли в семенные пузырьки, 157 пациентам в течение 90 дней после операции начинали ГТ, остальных больных наблюдали до прогрессирования опухолевого процесса. Результаты лечения в группе адъювантной ГТ оказались достоверно лучше, чем при хирургическом лечении: 10-летняя безрецидивная (ПСА ? 0,2 нг/мл) выживаемость составила 67% в группе комбинированного лечения и 23% в группе только РПЭ (р < 0,001), безметастатическая выживаемость – 95% и 87% (р < 0,001), опухолево-специфическая выживаемость – 95% и 78% соответственно (р < 0,001).
В 2000 г. были опубликованы предварительные результаты итальянского рандомизированного многоцентрового исследования по сравнению комбинированного лечения с применением адъювантной ГТ после РПЭ и только хирургического лечения, включающего 210 больных местнораспространенным РПЖ (рТ3?Т4) [10]. После выполнения РПЭ больных рандомизировали в группу адъювантной ГТ Золадексом или в группу наблюдения. При 5-летнем наблюдении отмечено существенное преимущество (25%) в безрецидивной (ПСА < 0,5 нг/мл, отсутствие местного рецидива и отдаленных метастазов) выживаемости больных, которым проводили немедленную ГТ, по сравнению с только хирургическим лечением. В то же время дальнейшие публикации об отдаленных результатах данного исследования отсутствуют, что не позволяет судить о том, привело ли назначение адъювантной ГТ к преимуществу в опухолевоспецифической и общей выживаемости.
M.P. Wirth и соавт. опубликовали в 2004 г. результаты протокола по применению флутамида у больных после РПЭ с экстракапсулярной инвазией опухоли (рТ3) без лимфогенных метастазов [11]. 152 больным, включенным в рандомизированное исследование, проводили адъювантную ГТ, 157 пациентов после операции наблюдали до прогрессирования. Средний период наблюдения составил 6,1 года. Безрецидивная выживаемость в группе комбинированного лечения была лучше, чем в группе хирургического лечения (р = 0,0041), но различий в общей выживаемости не выявлено (р = 0,92). Следует отметить, что 12% больных были исключены из исследования, в том числе 43% – по причине токсичности флутамида. Самым крупным рандомизированным исследованием, посвященным изучению роли адъювантной ГТ в лечении больных РПЖ, является протокол ЕРС (Early Prostate Cancer) [12]. Программа ЕРС состояла из 3 многоцентровых плацебоконтролируемых исследований [13–15], в которые включали больных локализованным и местнораспространенным РПЖ. Целью протокола являлось изучение эффективности и переносимости терапии Касодексом в дозе 150 мг, которую назначали в дополнение к стандартным методам лечения (РПЭ, ДЛТ, тщательное наблюдение). Адъювантную терапию Касодексом 150 мг после хирургического лечения применяли в исследовании C. Catton и соавт., которое проводилось в Северной Америке и включало 3293 больных [16]. Касодекс 150 мг или плацебо назначали сразу после операции, длительность лечения составила 2 года.
Средний период наблюдения за больными составил 7,7 года. У пациентов с местнораспространенными опухолями терапия Касодексом достоверно увеличивала выживаемость без признаков клинического прогрессирования (местного рецидива и генерализации). Отношение рисков безрецидивного течения в группах адъювантной терапии Касодексом 150 мг и плацебо составило 0,75 (95% ДИ – 0,61–0,91; р < 0,004). Следует отметить, что в исследование включали пациентов с относительно хорошим прогнозом, больные с лимфогенными метастазами составили всего 2% от общей популяции пациентов. Отсроченную терапию начинали при незначительном росте уровня ПСА. В связи с этим в данном исследовании только у 5% больных выявлено объективное прогрессирование, поэтому более выраженных различий в показателях безрецидивной выживаемости не выявлено. Напротив, при более позднем анализе результатов данного исследования различия в безрецидивной выживаемости больных местнораспространенным РПЖ после РПЭ в группах плацебо и бикалутамида 150 мг стали менее выраженными (ОР = 0,85; 95% ДИ – 0,71?1,01; р = 0,065).
Общая и опухолевоспецифическая выживаемость больных, получавших бикалутамид 150 мг и плацебо, достоверно не отличалась. Лечение Касодексом 150 мг хорошо переносилось пациентами, из побочных реакций превалировали гинекомастия и боли в грудных железах, которые редко приводили к отмене ГТ. Частота развития импотенции и снижения либидо существенно не отличалась в группе бикалутамида 150 мг и плацебо. Таким образом, адъювантная ГТ после РПЭ у больных местнораспространенным РПЖ приводит к увеличению безрецидивной выживаемости, но не влияет на общую и опухолево-специфическую выживаемость пациентов.
Адъювантная ГТ после РПЭ у больных локализованным РПЖ
Результаты применения послеоперационной ГТ у больных локализованным РПЖ также изучали в рамках мультицентрового рандомизированного исследования ЕРС [17]. При среднем периоде наблюдения 9,7 лет достоверных различий в безрецидивной (ОР = 0,94; 95% ДИ – 0,79–1,12; р = 0,516) и общей выживаемости (ОР = 1,03; 95% ДИ – 0,85?1,25; р = 0,759) в группах бикалутамида 150 мг и плацебо не выявлено. Таким образом, проведение адъювантной ГТ после РПЭ у больных локализованным РПЖ не показано.
В 2009 г. опубликован метаанализ исследований, изучавших эффективность адъювантной ГТ после РПЭ и ДЛТ [18]. При анализе безрецидивной выживаемости отмечено достоверное преимущество немедленной послеоперационной ГТ перед отсроченным лечением (ОР = 3,73; 95% ДИ – 2,30?6,03; р < 0,00001). В то же время влияния адъювантной ГТ на общую выживаемость больных в течение 5 и 10 лет выявлено не было. Наиболее частыми побочными эффектами адъювантной ГТ являлись гинекомастия, импотенция, желудочно-кишечные и гематологические проявления. Результаты рандомизированных исследований по изучению эффективности адъювантной ГТ после РПЭ представлены в таблице 1.
Исследование SWOG S9921
Исследование SWOG, инициированное Юго-Западной онкологической группой, посвящено изучению эффективности адъювантной ГТ и гормонохимиотерапии (ГХТ) у больных с неблагоприятными патоморфологическими находками после радикальной простатэктомии (РПЭ) [19]. Хирургическое лечение является одним из наиболее эффективных методов у больных РПЖ с высоким риском прогрессирования, в то же время частота развития рецидива заболевания после РПЭ у пациентов с патологически местнораспространенным (рТ3–Т4) и лимфогеннодиссеминированным опухолевым процессом (рN+), а также у больных с низкой дифференцировкой опухоли (8?10 баллов по шкале Глисона) достигает 70%. Адъювантная ГТ показала эффективность при ее проведении после лучевой терапии (исследования RTOG 8531 и EORTC 22863), которая выразилась в увеличении общей выживаемости больных с местнораспространенным и низкодифференцированным РПЖ (8?10 баллов). При проведении адъювантной ГТ после РПЭ у больных с метастазами в лимфатических узлах в рандомизированном исследовании ECOG также отмечено увеличение выживаемости больных по сравнению с группой отсроченного лечения. В связи с этим проведение большого исследования по изучению эффективности адъювантной ГТ после РПЭ у больных с высоким риском прогрессирования, по мнению инициаторов исследования, является актуальной задачей. Кроме того, одной из задач протокола являлось изучение роли химиотерапии в комбинации с ГТ в адъювантном режиме.
Критериями включения в исследование были следующие неблагоприятные факторы прогноза: сумма Глисона 8 баллов и более, стадия рТ3b, рТ4 или рN1, предоперационный уровень ПСА ? 15 нг/мл или сумма Глисона 7 баллов в сочетании с позитивным хирургическим краем или уровнем ПСА > 10 нг/мл. Больных рандомизировали в 2 группы: в одной группе пациенты получали адъювантную ГТ в режиме максимальной андрогенной блокады Золадексом и Касодексом, в другой – помимо аналогичной антиандрогенной терапии больным назначали митоксантрон. Длительность ГТ в обеих группах составила 2 года. Митоксантрон вводили 6 раз в дозе 12 мг/м? с интервалом в 21 день. В течение первых 5 лет после РПЭ уровень ПСА определяли каждые 3 мес., затем каждые 6 мес. в течение 10 лет после окончания терапии. Прогрессированием считали повышение уровня ПСА выше 0,2 нг/мл в трех последовательных измерениях или проведение лучевой терапии. В период с 2000 по 2007 г. в протокол включены 983 больных, из них 487 рандомизированы в группу «ГТ + митоксантрон», а 496 – в группу только ГТ. Набор в исследование был прекращен после сообщения о развитии 3 случаев острого миелолейкоза в группе пациентов, получавших митоксантрон. К настоящему времени опубликованы результаты лечения больных, получавших только ГТ.
После окончания 2-летнего периода ГТ восстановление уровня тестостерона выше посткастрационных значений наблюдалось в среднем через 11,7 мес., возвращение концентрации гормона к исходным показателям через 6 мес. наблюдалось только у 16%, через 1,5 года – у 89% больных. ГТ в целом переносилась пациентами хорошо, зарегистрировано 135 побочных явлений 3-й степени токсичности, при этом неожиданных токсических проявлений, не характерных для антиандрогенной терапии, не отмечено. Только 30 больных из 481 прекратили лечение в связи с развитием побочных реакций.
Средний период наблюдения за больными составил 4,4 года. За это время умерли только 27 пациентов, из них 13 – от РПЖ. 5-летняя общая выживаемость составила 96%, 8-летняя – 88%. 5-летняя безрецидивная выживаемость составила 92,5%. Показатели выживаемости различались в подгруппах больных с различными патоморфологическими и клиническими характеристиками (табл. 2).
T.B. Dorff и соавт. отмечали, что при планировании исследования предполагаемая 5-летняя выживаемость, на основании анализа данных предыдущих публикаций, составляла 71%, а 8-летняя – 57%. Полученные результаты оказались намного лучше ожидаемых, что может быть обусловлено несколькими причинами. Так, одним из объяснений может являться уменьшение вероятности включения в исследование больных с клинически не выявленной генерализацией РПЖ, что связано с широким распространением ПСА-скрининга. Кроме того, возможно, на видимое улучшение показателей выживаемости повлияло изменение оценки дифференцировки опухоли по шкале Глисона: например, степень злокачественности опухоли, классифицированная ранее как 6 баллов, в настоящее время оценивается как 7 баллов. Еще одной возможной причиной хорошей выживаемости больных в исследовании SWOG S9921 может являться расширение спектра эффективной спасительной терапии при развитии прогрессирования (широкое применение доцетаксела, абиратерона, сипулеуцила-Т). В то же время основной причиной улучшения результатов лечения авторы считают назначение адъювантной ГТ в течение 2 лет после РПЭ. При анализе частоты развития сердечнососудистых осложнений, которая, по данным популяционных исследований, увеличивается при проведении длительной андрогендепривационной терапии, отмечено развитие только одного ишемического осложнения, тогда как в группе больных, получавших помимо ГТ митоксантрон, выявлено 5 таких осложнений. Зарегистрировано 2 смертельных исхода, связанных с сердечно-сосудистыми проблемами, в группе только ГТ и 3 – в группе ГХТ.
Таким образом, по мнению авторов исследования, адъювантная ГТ в течение 2 лет после РПЭ у больных с высоким риском прогрессирования позволяет достигать высоких показателей безрецидивной и общей выживаемости, в связи с чем вариант комбинированного лечения – РПЭ в сочетании с адъювантной ГТ – должен приниматься во внимание при планировании лечебной тактики у данной категории пациентов.
Заключение
Адъювантная ГТ после РПЭ у больных РПЖ является эффективным методом профилактики развития прогрессирования заболевания. При выявлении после операции метастазов в лимфатических узлах длительная адъювантная ГТ является стандартным методом лечения, позволяющим увеличить общую выживаемость пациентов. У больных РПЖ с высоким риском прогрессирования (местнораспространенный опухолевый процесс, низкая степень дифференцировки опухоли, высокий предоперационный уровень ПСА) немедленное назначение ГТ после РПЭ приводит к увеличению безрецидивной выживаемости и также может рассматриваться как вариант лечебной тактики, который следует обсуждать с больным.
1. Злокачественные новообразования в России в 2009 году (заболеваемость и смертность) / под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. М.: ФГУ «МНИОИ им. П.А. Герцена Минздравсоцразвития России», 2011. 260 с.
2. Moul J.W. Prostate specific antigen only progression of prostate cancer // J. Urol. 2000. Vol. 163. № 6. P. 1632–1642.
3. Zincke H., Bergstralh E.J., Larson-Keller J.J. et al. Stage D1 prostate cancer treated by radical prostatectomy and adjuvant hormonal treatment. Evidence for favorable survival in patients with DNA diploid tumors // Cancer. 1992. Vol. 70. № 1. Suppl. P. 311–323.
4. Myers R.P., Larson-Keller J.J., Bergstralh E.J. et al. Hormonal treatment at time of radical retropubic prostatectomy for stage D1 prostate cancer: results of long-term followup // J. Urol. 1992. Vol. 147. № 3. Pt. 2. Р. 910–915.
5. Seay T.M., Blute M.L., Zincke H. Long-term outcome in patients with pTxN+ adenocarcinoma of prostate treated with radical prostatectomy and early androgen ablation // J. Urol. 1998. Vol. 159. № 2. Р. 357–364.
6. Myers R.B., Slezak E.J., Farrow J.M. et al. Use of adjuvant hormonal therapy with radical prostatectomy in lymph node-positive disease: rationale and contribution to outcome // Prostate and renal cancer, benign prostatic hyperplasia, erectile dysfunction and basic research: an update / C.H. Bangma, D.W.W. Newling (eds). Boca Ration, Fl: Parthenon Publishing Group, 2003. Р. 390–399.
7. Messing E.M., Manola J., Sarosdy M. et al. Immediate hormonal therapy compared with observation after radical prostatectomy and pelvic lymphadenectomy in men with node-positive prostate cancer // N. Engl. J. Med. 1999. Vol. 341. № 24. P. 1781–1788.
8. Messing E.M., Manola J., Yao J. et al. Immediate versus deferred androgen deprivation treatment in patients with node-positive prostate cancer after radical prostatectomy and pelvic lymphadenectomy // Lancet Oncol. 2006. Vol. 7. № 6. Р. 472–479.
9. Zincke H., Lau W., Bergstralh E., Blute M.L. Role of early adjuvant hormonal therapy after radical prostatectomy for prostate cancer // J. Urol. 2001. Vol. 166. № 6. Р. 2208–2215.
10. Prayer-Galetti T., Zattoni F., Capizzi A. et al. Disease free survival in patients with pathological «C stage» prostate cancer at radical retropubic prostatectomy submitted to adjuvant hormonal treatment // Eur. Urol. 2000. Vol. 38. Р. 504.
11. Wirth M.P., Weissbach L., Marx F.J. et al. Prospective randomized trial comparing flutamide as adjuvant treatment versus observation after radical prostatectomy for locally advanced, lymph node-negative prostate cancer // Eur. Urol. 2004. Vol. 45. № 3. Р. 267–270.
12. McLeod D.G., Iversen P., See W.A. et al. Bicalutamide 150 mg plus standard care vs standard care alone for early prostate cancer // BJU Int. 2006. Vol. 97. № 2. Р. 247–254.
13. Catton C., Gospodarowicz M., Warde P. et al. Adjuvant and salvage radiation therapy after radical prostatectomy for adenocarcinoma of the prostate // Radiother. Oncol. 2001. Vol. 59. № 1. P. 51–60.
14. Do L.V., Do T.M., Smith R., Parker R.G. Postoperative radiotherapy for carcinoma of the prostate: impact on both local control and distant disease-free survival // Am. J. Clin. Oncol. 2002. Vol. 25. № 1. P. 1–8.
15. Petrovich Z., Lieskovsky G., Langholz B. et al. Postoperative radiotherapy in 423 patients with pT3N0 prostate cancer // Int. J. Radiat. Oncol. Biol. Phys. 2002. Vol. 53. № 3. P. 600–609.
16. McLeod D.G., See W.A., Klimberg I. et al. The bicalutamide 150 mg early prostate cancer program: findings of the North American trial at 7.7-year median followup // J. Urol. 2006. Vol. 176. № 1. Р. 75–80.
17. Iversen P., McLeod D.G., See W.A. et al. Antiandrogen monotherapy in patients with localized and locally advanced prostate cancer: final results from bicalutamide Early Prostate Cancer programme at median followup at 9,7 years // BJU Int. 2010. Vol. 105. № 8. P. 1074–1081.
18. Shelley M.D., Kumar S., Coles B. et al. Adjuvant hormone therapy for localised and locally advanced prostate carcinoma: a systematic review and meta-analysis of randomised trials // Cancer Treat Rev. 2009. Vol. 35. № 7. Р. 540–546.
19. Dorff T.B., Flaig T.W., Tangen C.M. Adjuvant androgen deprivation for high-risk prostate cancer after radical prostatectomy: SWOG S9921 study // J. Clin. Oncol. 2011. Vol. 29. № 15. P. 2040–2045.
Новости на тему
Отправить статью по электронной почте
Ваш адрес электронной почты:
Радикальная простатэктомия на протяжении последних двух десятилетий остается одним из наиболее популярных методов лечения локализованного и местнораспространенного рака предстательной железы.
В то же время оперативное вмешательство не во всех случаях приводит к полному излечению от заболевания. Причинами возникновения рецидива заболевания могут быть нерадикальное выполнение хирургического вмешательства, приводящее к наличию остаточной опухолевой ткани, или скрытая диссеминация опухолевого процесса, не выявленная на момент радикальной простатэктомии.
Достаточно высокая частота прогрессирования рака после радикальной простатэктомии обусловливает актуальность разработки методов комбинированного лечения, снижающих вероятность развития рецидива заболевания.
Эффективным методом профилактики развития прогрессирования заболевания является адъювантная гормональная терапия, немедленное назначение которой после радикальной простатэктомии позволяет увеличить безрецидивную и общую выживаемость больных.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
